單次大分割放療在體外對樹突狀細胞激活T細胞的影響
鄭聲琴,范璟,鄭勤,童金龍,田小強
(南京中醫藥大學附屬南京醫院/南京市第二醫院 1.腫瘤科, 2.中心實驗室, 江蘇 南京 210003)
肝細胞性肝癌(hepatocellular carcinoma,HCC)是我國最常見的惡性腫瘤之一,在全球惡性腫瘤發病率中排名第5位,而其死亡率位于惡性腫瘤死亡率的第4位,且有逐年上升趨勢[1]。放射治療在肝癌局部治療中受到越來越多的重視,相繼被列入各國肝癌的治療指南當中,成為近年來腫瘤放療學者關注的最新熱點,在肝癌、早期非小細胞肺癌、椎體轉移癌的治療中發揮顯著的局部控制療效[2]。
腫瘤的免疫治療是近年來最矚目的治療手段。腫瘤免疫治療的研究方向主要是兩個方面:一是在體外對T細胞進行基因修飾再回輸到體內;二是通過抗體刺激免疫細胞使其發揮抗腫瘤作用[3]。本研究將從后者角度出發,以單次大分割放療后肝癌細胞釋放的蛋白為抗原負載樹突狀細胞(dendritic cell,DC),探究其對DC表型、細胞因子分泌、功能的影響,旨為肝癌的臨床治療提供數據支撐。
1 資料與方法
1.1 一般資料
選取2017年8月至2018年8月南京中醫藥大學附屬南京醫院收治的5例肝癌患者。納入標準:通過病理學、CT和MRI檢測,確診為原發性肝癌的患者;患者無其他重要臟器重大疾病;患者簽訂本研究的知情同意書。采集患者外周血5 ml,用于后續研究。
1.2 主要試劑
RPMI- 1640和DMEM培養基均購自Gibco公司;淋巴細胞分離液購自南京三生生物技術有限公司;磁珠分選試劑盒購自美天旎公司;細胞因子IL- 4、GM- CSF和TNF- α購自PeproTech公司;流式抗體均購自eBioscience公司;ELISA試劑盒購和MTT試劑盒購自杭州聯科生物技術股份有限公司;胞內染色試劑盒購自BD公司。
1.3 DC的體外培養
利用Ficoll密度梯度離心法分離經肝素抗凝的肝癌患者外周血單核細胞(PBMC)。經PBS洗滌后,利用磁珠分選法分選PBMC獲得CD14+單核細胞,CD14+細胞>95%。將獲得的單核細胞以2×106ml-1的濃度接種到RPMI- 1640培養基中,在37 ℃體積分數5% CO2的細胞培養箱中進行孵育,并加入細胞因子GM- CSF(500 U·ml-1)和IL- 4(200 U·ml-1)。每隔3 d對細胞進行半量換液并補充上述細胞因子。在培養到第5天時,加入促進DC成熟因子LPS(100 ng·ml-1)。再經48 h培養,即可獲得成熟DC細胞。
1.4 DC表面表型的流式細胞儀測定
分別收集上述培養到第5天和第7天的非成熟和成熟DC,經PBS洗滌后,轉入流式管中,分別加入PerCP、PE、FITC或APC標記的抗人HLA- DR、CD40、CD80、CD83、CD86抗體,置4 ℃避光孵育30 min后,用PBS洗滌2次,加入250 μl PBS懸浮細胞,最后利用流式細胞儀檢測分析DC表型。
1.5 肝癌腫瘤相關抗原的制備
用含5%胎牛血清的DMEM培養基對肝癌細胞HepG2進行培養,將HepG2細胞懸液濃度調整為1×106ml-1,接種到25 cm2培養瓶中,在37 ℃體積分數5% CO2的培養箱中培養24~48 h。待HepG2細胞鋪滿瓶底時,進行放療照射。將培養的HepG2細胞分為兩組,即一組照射劑量為15Gy/1f,另一組照射劑量為5Gy/3f。照射完成后,細胞繼續培養48 h,收集細胞上清,以1 600 r·min-1離心5 min后,繼續收集上清,重復上述步驟1次。將獲得的上清以10 000 r·min-1離心20 min,取獲得的沉淀作為HepG2細胞釋放的腫瘤相關抗原(tumor- associated antigen, TAA),用PBS溶解后存貯于-80 ℃備用。
1.6 ELISA
將上述培養的成熟DC分為3組:一組加入25 μg·ml-115 Gy/1f TAA進行刺激(以下稱為15 Gy/1f組);一組加入25 μg·ml-15 Gy/3f TAA(以下稱為5 Gy/3f組);一組作為陰性對照。在37 ℃體積分數5% CO2條件下繼續培養48 h,以1 600 r·min-1離心5 min,取細胞培養上清。利用ELISA試劑盒檢測DC分泌細胞因子IL- 12p70、IL- 1β、IL- 6、IL- 18的情況。
1.7 免疫磁珠法(MACS)分離純化T淋巴細胞
取上述提取的肝癌患者外周血PBMC,用PBS洗滌細胞,以1 600 r·min-1離心5 min,取沉淀的細胞,加入80 μl PBS重懸細胞,加入20 μl CD3磁珠,置4 ℃ 孵育30 min;用PBS洗滌細胞,以1 600 r·min-1離心5 min,取500 μl PBS重懸細胞。將LS分離柱放置在MACS分離器磁場中,用1 ml PBS沖洗分離柱,重復操作3次。收集流出液,流出液中含有T淋巴細胞。
1.8 DC與T細胞的共培養
根據上述方法將DC分為3組,分別為15 Gy/1f TAA+DC組、5 Gy/3f TAA+DC組和僅DC組。將DC細胞濃度調整到1×104ml-1,接種到24孔板中,DC∶T細胞以1∶10的比例接種上述分選的T淋巴細胞,并以僅加入T細胞組作為陰性對照。在37 ℃體積分數5% CO2的培養箱中繼續培養7 d。通過胞內染色法,利用流式細胞儀分別檢測CD4+T細胞和CD8+T細胞分泌IFN- γ情況。
1.9 MTT法測定活化T細胞的殺傷活性
取上述DC和T細胞共培養7 d后的細胞,制備成5×105ml-1的單細胞懸液,加入含有HepG2細胞的96孔細胞培養板(20∶1),作為實驗組。另外單獨加入未經DC激活的T細胞作為對照組,每孔均設3個復孔。放置在37 ℃體積分數5% CO2的培養箱中繼續培養48 h,以1 600 r·min-1離心5 min,棄去上清,每孔加入10 μl MTT溶液(5 mg·ml-1),繼續孵育4 h,離心去上清,每孔加入100 μl二甲亞砜,振蕩后溶解15 min。利用酶標儀在570 nm處測定OD值。T細胞殺傷活性(%)=(實驗組OD570 nm-對照組OD570 nm)/HepG2 OD570 nm×100%。
1.10 統計學處理
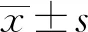
2 結 果
2.1 肝癌患者外周血體外DC的培養及鑒定
利用細胞因子IL- 4和GM- CSF刺激肝癌患者PBMC,在培養第5天收獲非成熟DC。在15Gy條件下對肝癌細胞HepG2進行照射,通過反復離心法獲得15Gy/1f TAA。利用流式細胞儀檢測非成熟DC和負載了15Gy/1f TAA的DC細胞表面HLA- DR、CD40、CD80、CD83、CD86分子的表達情況。由圖1和圖2結果可知,負載TAA的DC[15Gy/1f TAA +非成熟DC(iDC)]細胞表面HLA- DR、CD40、CD80、CD83、CD86分子表達的百分比和平均熒光強度(mean fluorescence intensity,MFI)均高于iDC:(1) HLA- DR百分比,(90.48±3.09)%vs(68.08±6.29)%,P=0.009 5;CD40百分比,(50.23 ±8.81)%vs(8.43±1.29)%,P=0.017 9;CD80百分比,(36.38±8.06)%vs(2.44±0.99)%,P=0.026 9;CD83百分比,(45.50±13.55)%vs(2.48±0.95)%,P=0.045 4;CD86百分比,(56.75±10.8)%vs(21.43±3.55)%,P=0.029 2。(2) HLA- DR的MFI,3 478 ±494.3vs682.5±97.45,P=0.007 5;CD40的MFI,876.3±53.38vs280±17.76,P<0.001;CD80的MFI,331±44.27vs130±11.02,P=0.016;CD83的MFI,265.8 ±39.42vs87.33±12.03,P=0.033 7;CD86的MFI,18 189±428.7vs3 020±477.1,P=0.044 3。
2.2 單次大分割放療后HepG2細胞釋放的TAA對DC細胞因子分泌的影響
在成熟DC中分別加入15Gy/1f和5Gy/3f條件下的TAA。通過ELISA法檢測細胞培養上清中DC分泌的細胞因子濃度。負載了TAA的DC分泌細胞因子IL- 12p70、IL- 1β、IL- 6、TNF- α的濃度均高于未加TAA的DC組。其中15Gy/1f組(15Gy/1f TAA+DC)的DC分泌細胞因子IL- 12p70和IL- 18的濃度高于5Gy/3f組(5Gy/3f TAA+DC)。15Gy/1f TAA+DC組、5Gy/3f TAA+DC組和DC組各細胞因子分泌比較:IL- 12p70的質量濃度,(996.6±118.0)pg·ml-1vs(564.4±54.04)pg·mlvs(327.2±30.63) pg·ml-1,P=0.000 2;IL- 1β的質量濃度,(196.2±31.32)pg·ml-1vs(187.4±22.14)pg·ml-1vs(86.40±8.19)pg·ml-1,P=0.008 6;IL- 6的質量濃度,(2 215±192.8) pg·ml-1vs(1 395±122.9)pg·ml-1vs(887±51.12) pg·ml-1,P=0.000 1;TNF- α的質量濃度,(1 099±109.4)pg·ml-1vs(1 023±81.06)pg·ml-1vs(571.2±66.68)pg·ml-1,P=0.002 2。見圖3。
灰色曲線代表同型對照,深灰色曲線代表DC,黑色曲線代表15Gy/1f TAA+iDC
2.3 負載TAA的DC刺激特異性T細胞分泌IFN- γ情況
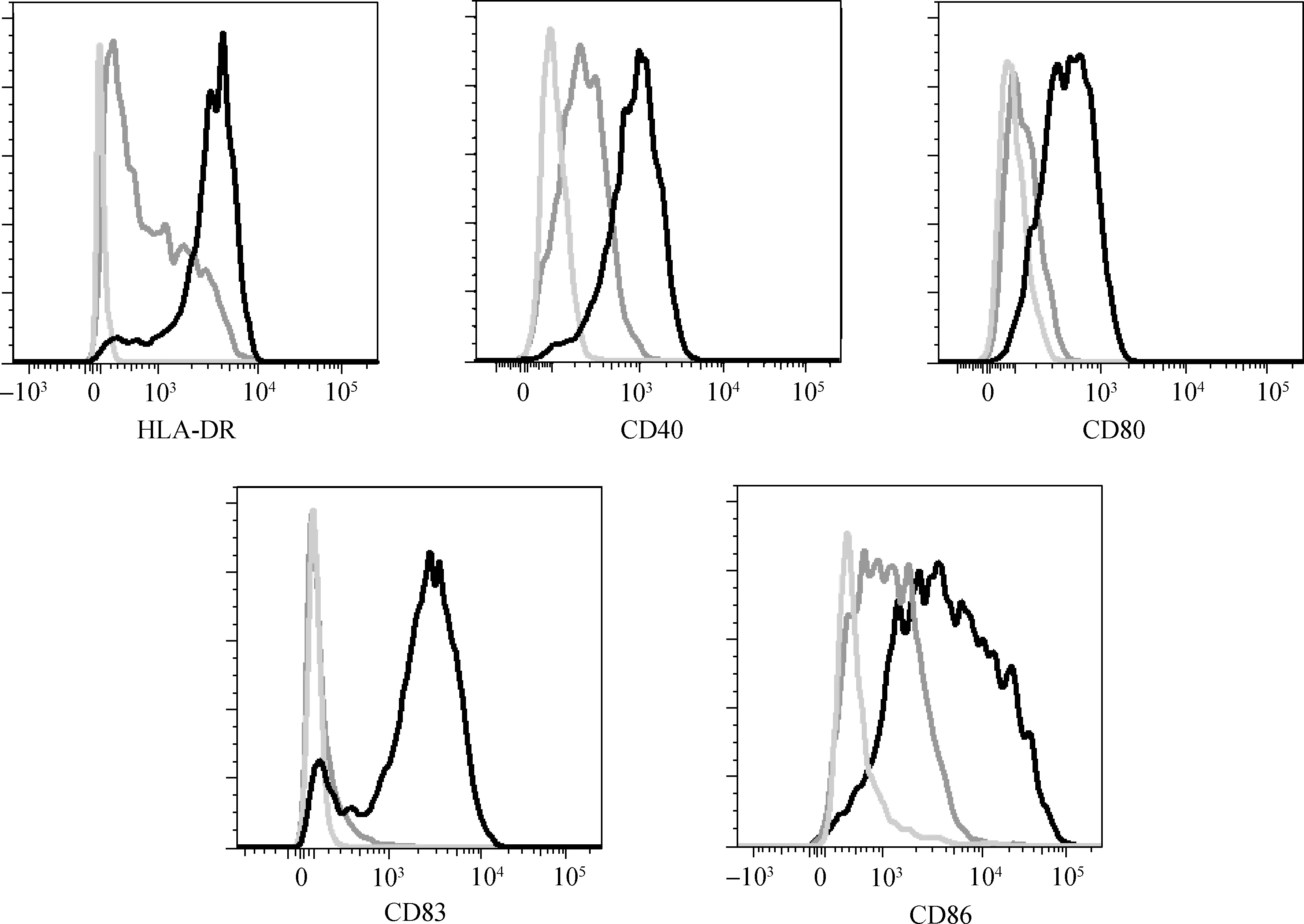
分別用15Gy/1f組和5Gy/3f組的TAA負載DC,然后與自體T細胞共培養,利用流式細胞儀分別檢測特異性CD4+T細胞和CD8+T細胞分泌IFN- γ的情況。負載15Gy/1f TAA的DC刺激特異性CD4+T細胞和CD8+T細胞分泌IFN- γ均高于5Gy/3f組 (P<0.05),見表1。
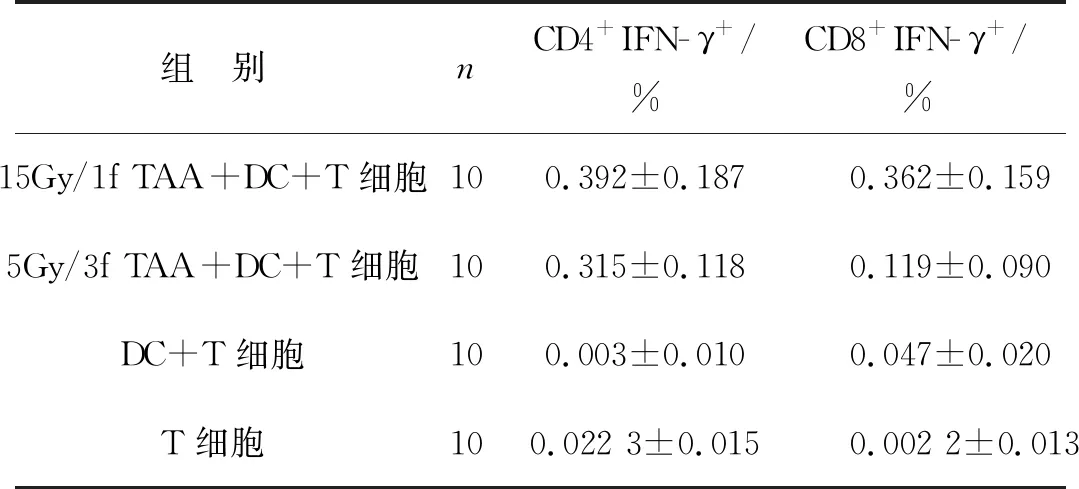
表1 不同抗原負載DC刺激特異性T細胞分泌IFN- γ情況
2.4 活化后T細胞的殺傷活性
15Gy/1f組刺激的T細胞殺傷活性最高,達到(38.33±1.76)%,顯著高于5Gy/3f組的(29.33±2.19)%(P<0.05),見圖4。
3 討 論
原發性肝癌是起源于肝細胞或肝內膽管上皮細胞的惡性腫瘤。2018年我國肝癌發病率、死亡率和1年患病率分別為18.3/10萬、17.1/10萬和10.8/10萬[4]。原發性肝癌具有發病迅速、致死率高、生存期短等特點,這嚴重影響了我們人民的生命健康,因此尋求切實有效的臨床治療方法迫在眉睫。
放療在肝癌的局部治療中越來越受重視,特別是單次大分割放療也有應用到臨床的實例[5- 6]。放療一方面可以提高腫瘤細胞上主要組織相容性復合物- I(MHC- 1)的表達,這有利于提高細胞毒性T細胞對腫瘤細胞的識別[7];另一方面也可以提高腫瘤死亡受體(如Fas等)的表達,這有利于免疫細胞通過Fas配體與腫瘤細胞Fas受體的結合傳遞信號,引起靶細胞凋亡[8]。但單次大分割放療對免疫細胞功能影響的研究較少。DC是人體內最強的抗原提呈細胞(antigen- presenting cells, APC),能攝取、加工、處理抗原從而啟動激活T細胞,在腫瘤免疫中發揮重要作用。因此,本研究將在體外模擬體內環境,探討單次大分割放療對DC細胞表型、細胞因子分泌及T細胞功能的影響。
圖2 體外培養DC細胞表面分子表達的百分比和MFI值(n=4)
首先,本研究利用單次大分割放療(15Gy)照射肝癌細胞HepG2。利用反復離心法獲得TAA,通過流式細胞儀檢測負載了15Gy/1f TAA的DC細胞表面分子的表達。本研究結果顯示,通過15Gy照射腫瘤細胞釋放的抗原可以促進DC細胞表面分子HLA- DR、CD40、CD80、CD83和CD86表達的提高。HLA- DR是DC激活CD4+T細胞的關鍵分子,CD40、CD80和CD86與DC刺激T細胞抗原提呈能力有關,而CD83是DC成熟的標志[9]。這些分子的表達都有利于DC發揮免疫刺激作用,說明經過單次大分割放療后肝癌細胞釋放的TAA有利于DC的成熟,這一功能與促進DC成熟的細胞因子TNF- α、LPS及CD40L等類似[10- 11]。為了進一步驗證這一結果,通過ELISA法檢測了15Gy/1f TAA對DC細胞因子分泌的影響。結果提示,經過抗原刺激后,DC分泌細胞因子IL- 12p70、IL- 1β、IL- 6、IL- 18均高于未刺激組。同時,以5Gy/3f TAA為對照組,實驗結果顯示高劑量放療組更能刺激DC分泌細胞因子。因此,單次大分割放療更有利于DC對免疫細胞的激活。這一結果與Kulzer等[12]的研究結果一致。
TAA負載DC15Gy/1f組相比5Gy/3f組更能刺激CD4+和CD8+T細胞分泌IFN- γ。這一研究結果在小鼠體內也有一致的實驗結果。Gupta等[13]在小鼠中發現,單次大分割放療(10 Gy)可以通過DC激活腫瘤特異性CD8+T細胞發揮抗腫瘤免疫作用。最后,被激活的T細胞對肝癌細胞HepG2具有殺傷作用,而且相比5Gy/3f組,15Gy/1f組對腫瘤細胞的殺傷作用更強。
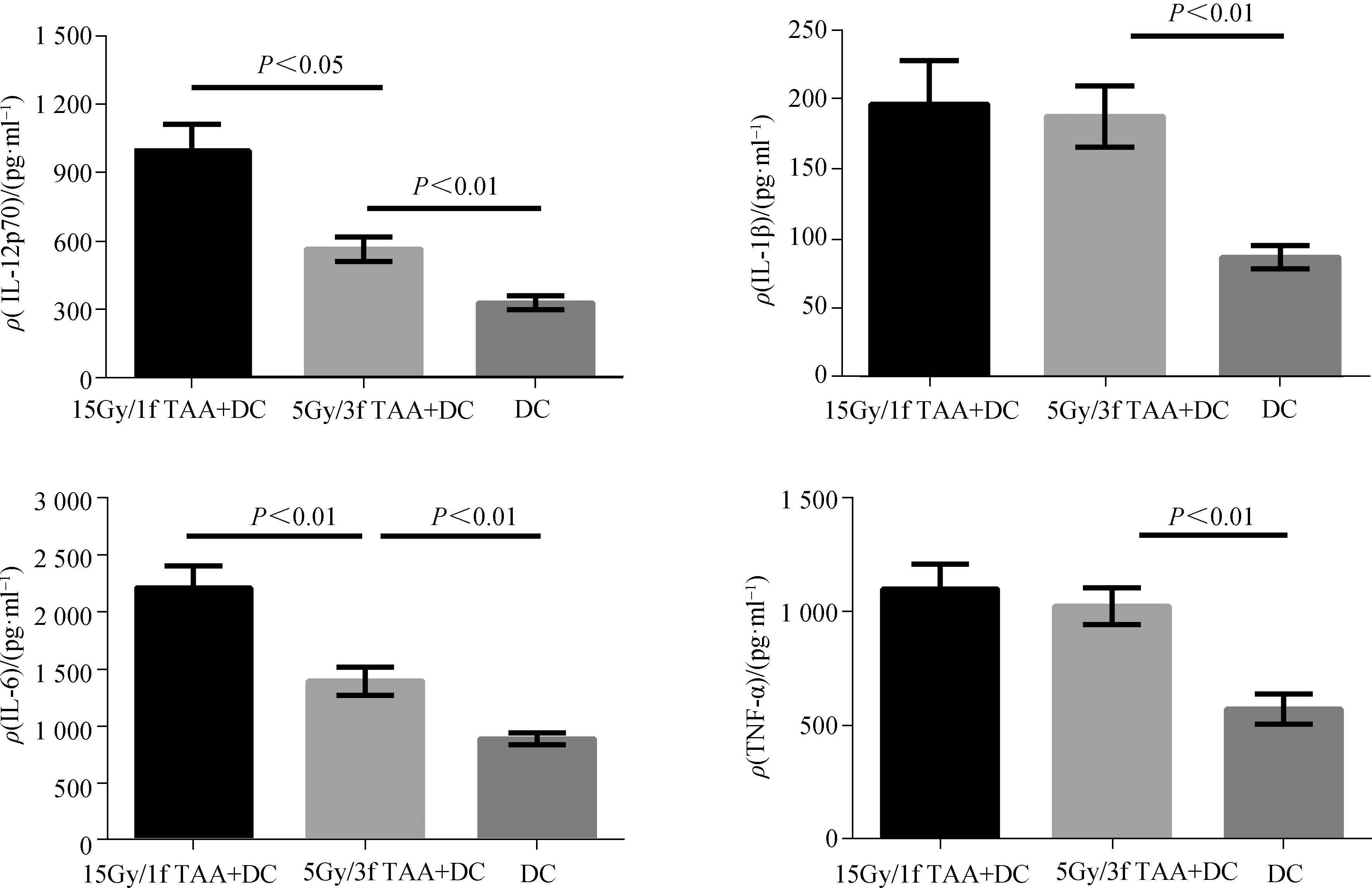
圖3 負載TAA的DC分泌細胞因子情況
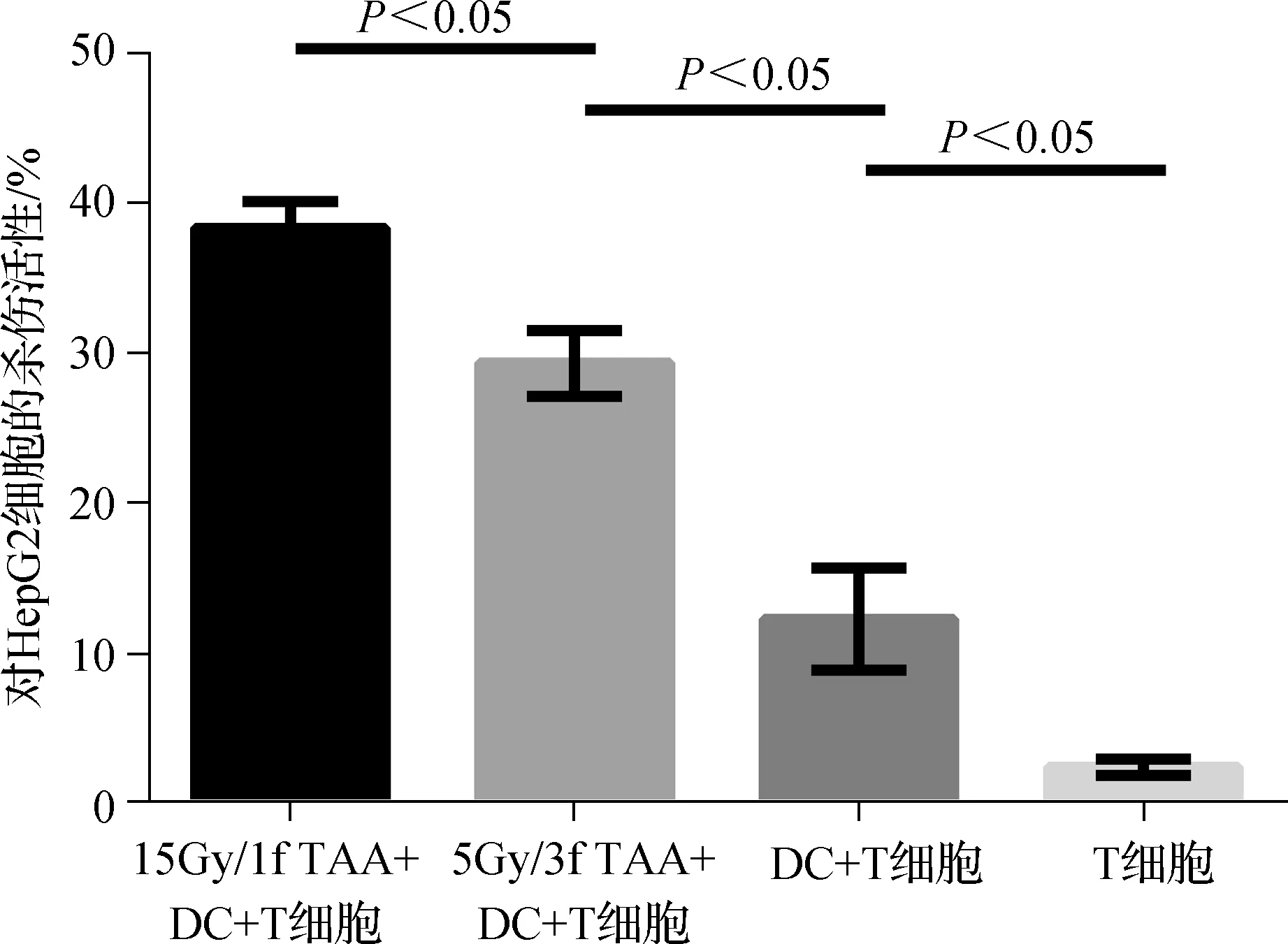
圖4 不同抗原負載DC激活的T細胞對HepG2細胞的殺傷活性
綜上所述,單次大分割放療更能刺激DC發揮免疫激活作用,可促進DC的成熟、細胞因子分泌及激活T細胞特異性殺傷腫瘤細胞。

