CO2(g)-NH3(aq)-CaSO4·2H2O(s)三相體系中碳酸鈣結晶工藝研究
范曉宇,葛 敬,朱家驊,夏素蘭
(四川大學 化學工程學院,四川 成都 610065)
0 引言
目前,CO2減排與廢棄磷石膏多重利用已經成為熱門研究課題。四川大學在國內外率先提出低濃度尾氣CO2直接礦化磷石膏聯產硫基復肥與碳酸鈣的一步法新工藝。該工藝充分體現了“以廢治廢”理念,符合國家發展戰略,極大地提高了CO2和磷石膏資源化利用的經濟性。
CO2和磷石膏在氨介質體系中進行碳酸化反應生成碳酸鈣[1]。磷石膏作為反應原料,因其雜質含量較高,不僅導致反應轉化率低[2],而者造成碳酸鈣產品的純度與白度較低,產品只能作為附加值較低的水泥生產原料或煙氣脫硫劑使用[3]。因此,CO2直接礦化磷石膏只是在“以廢治廢”理念的基礎上得到一定的經濟效益,而要獲得更高的經濟效益,則有必要提高碳酸鈣產品的品質和附加值[4]。磷石膏的主要成分為二水硫酸鈣,為了避免雜質對碳酸鈣產品的影響,選取二水硫酸鈣作為反應原料進行碳酸鈣產品優化的工藝研究。
筆者在CO2(g)-NH3(aq)-CaSO4·2H2O(s)三相反應體系下,在一水合氨與二水硫酸鈣物質的量之比為1.85時,分別考察反應溫度、CaSO4·2H2O加料量、攪拌轉速、CO2流量對CaCO3粒徑分布的影響,以平均粒徑及其分布函數的變異系數為評價指標確定了實驗的優化工藝條件,為工業應用提供參考。
1 反應推動力分析
CO2(g)-NH3(aq)-CaSO4·2H2O(s)三相反應體系下制取CaCO3的反應方程式如下:
當反應溫度為298.15 K時,反應物CaSO4·2H2O與生成物CaCO3在水中的溶度積常數分別為9.1×10-6、2.8×10-9,兩者相差3 250倍。該反應過程中,主要涉及CaSO4·2H2O 在水中溶解與CaCO3在溶液中結晶兩個過程。CaSO4· 2H2O 在水中溶解并電離出Ca2+,CO2溶解在水中形成CO32-,CO32-和Ca2+結合形成更加難溶的CaCO3,使得溶液中的Ca2+濃度不斷降低,從而促進了CaSO4·2H2O的溶解,該推動力使反應能夠順利進行[5-6]。
2 工藝評價指標
2.1 平均粒徑D50
顆粒的平均粒徑D50是指顆粒的累計粒度分布百分數達到50%時所對應的粒徑,它是評價粒度分布函數的一個重要指標[7],反映顆粒群總體粒度分布情況。
2.2 顆粒分布函數的變異系數
顆粒的體積密度分布函數與粒數密度分布函數主要服從于對數正態分布函數,但二者的累積分布函數則一般服從于正態分布函數。變異系數(CV)[8]表示粒度分布的寬窄程度,CV值越大,表示粒度分布越寬,反之則越窄。評價指標重點考察顆粒分布的變異系數,該量是一個統計量,與正態分布函數的偏差σ有關,計算式如下:
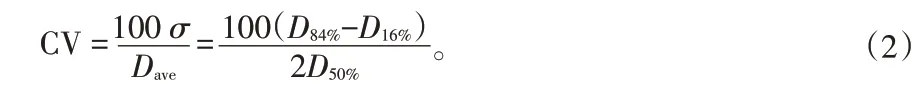
式中 Dave——顆粒的平均粒徑,μm;
Dx%——顆粒的累積粒度分布百分數為x%時對應的粒徑,μm;
σ——正態分布函數的標準差。
不同粒徑的顆粒分別具有不同的應用價值。顆粒分布越均勻,其利用價值越高,變異系數恰好能夠評價這一指標的優劣。
3 實驗部分
CO2(g)-NH3(aq)-CaSO4·2H2O(s)三相結晶反應體系中,鈣源選用固體二水硫酸鈣(分析純),NH3(aq)選用氨水(w(NH3)28%,分析純)。反應裝置如圖1所示。
首先,向玻璃夾套結晶反應器中加入去離子水1.40 L、氨水100 mL、二水硫酸鈣0.36 mol;初始反應溫度保持在(296.15 ± 0.50)K,CO2體積流量為245 mL/min,攪拌轉速為600 r/min。待反應器中溶液溫度維持在目標溫度3 min 不變后,打開氣路閘閥,向反應體系中通入CO2氣體并開始計時。一定時間后,開始取樣(每次取樣50 mL),立即使用馬爾文激光粒度分析儀(Spratec)對樣品粒徑分布進行測量,當分布圖像穩定不變時,結束反應。重復上述實驗步驟,完成不同反應溫度、加料量、攪拌轉速、CO2體積流量下的實驗。
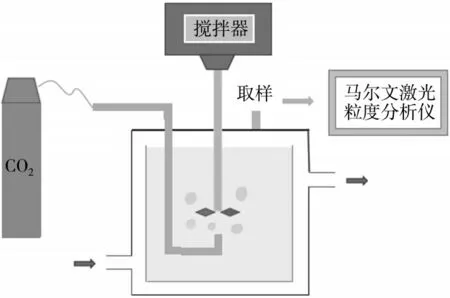
圖1 實驗裝置
4 結果與討論
4.1 反應溫度對碳酸鈣晶體粒度分布的影響
反應溫度是工業結晶中極其重要的操作參數,不同的操作溫度可以影響CaCO3顆粒形成過程中晶種的形成、晶習的改變、晶體的長大等,所以對于反應溫度的控制極其重要。基于已有動力學研究成果中反應的初始條件,在二水硫酸鈣加料量0.36 mol,氨、鈣物質的量之比1.85,攪拌轉速600 r/min,CO2體積流量245 mL/min 條件下改變反應溫度,考察反應溫度為296.15、303.15、313.15、323.15、333.15、343.15 K時對粒度分布的影響。
以反應溫度為橫坐標,分別以平均粒徑與顆粒分布的變異系數為縱坐標作圖,見圖2。
由圖2a.可知,CaCO3平均粒徑隨反應溫度的升高,呈現先減小后增大的趨勢。通過文獻調研可以發現,溫度升高時CaCO3晶體的成核速率與生長速率都在增加。孫艷紅所在課題組開發了磷石膏制取CaCO3的低溫工藝[9],其實驗結果表明,反應溫度越低,形成的CaCO3平均粒徑越大,與本實驗結果相吻合。由圖2b.可知,CaCO3顆粒分布的變異系數隨著溫度的升高呈現先減小后增大的趨勢。當反應溫度為333.15 K時,顆粒分布的變異系數達到最小值42.57%;當反應溫度為323.15 K時,顆粒分布的變異系數為43.72%,二者相差1.15個百分點,相較于其他溫度的差值最小。考慮到工業上節能減排等因素,選擇323.15 K為下一步實驗的優化溫度。
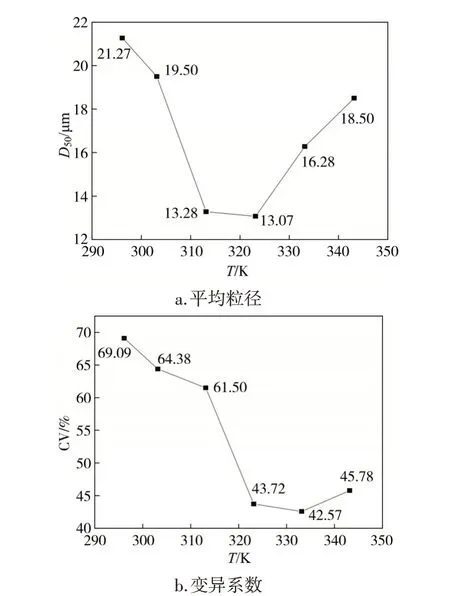
圖2 平均粒徑與顆粒分布的變異系數隨溫度的變化
4.2 二水硫酸鈣加料量對碳酸鈣晶體粒度分布的影響
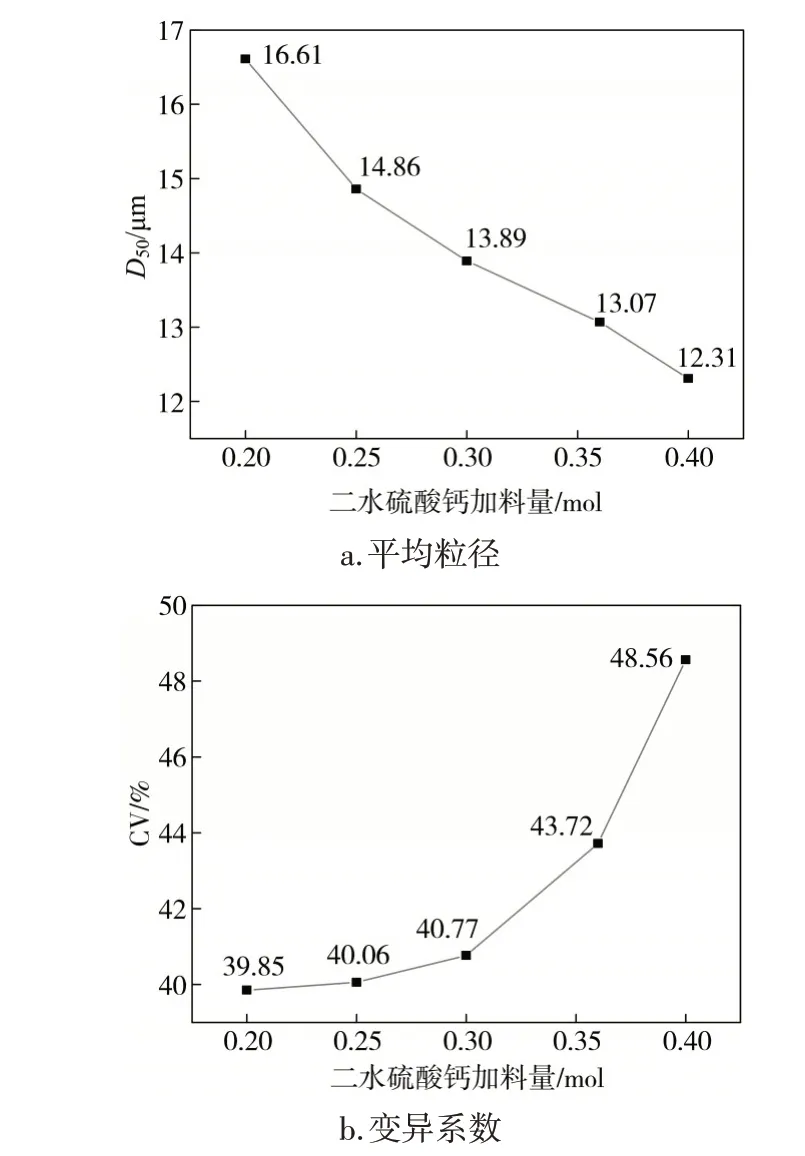
圖3 平均粒徑與顆粒分布的變異系數隨二水硫酸鈣加料量的變化
在反應溫度323.15 K,攪拌轉速600 r/min,CO2體積流量245 mL/min,氨、鈣物質的量之比1.85時,分別加入二水硫酸鈣0.20、0.25、0.30、0.36、0.40 mol進行反應,考察其對碳酸鈣晶體粒度分布的影響。以二水硫酸鈣加料量為橫坐標,分別以平均粒徑與顆粒分布的變異系數為縱坐標作圖,結果見圖3。
由圖3a.可知,CaCO3顆粒平均粒徑隨二水硫酸鈣加料量的增加而減小。分析產生這一現象的原因:增加二水硫酸鈣的加料量,可持續為CaCO3結晶反應提供鈣源,導致晶體的成核速率大于生長速率,產生大量微小晶核,使總體粒子的平均粒徑減小。進一步可以發現,隨著二水硫酸鈣加料量的增大,晶體平均粒徑的整個變化趨勢接近于線性過程,擬合可得y=-20.33x+20.29,R2=0.95,以此作為其他加料量操作參數的參考標準。由圖3b.可知,CaCO3顆粒分布的變異系數隨二水硫酸鈣加料量的增加而增大。分析產生這一現象的原因:二水硫酸鈣加料量增大時,形成許多細小的晶核,導致體系混亂度增加,從而使顆粒的均勻性下降,導致變異系數升高。綜上所述,選取0.20 mol作為優化實驗二水硫酸鈣的加料量。
4.3 攪拌轉速對碳酸鈣晶體粒度分布的影響
在反應溫度323.15 K,二水硫酸鈣加料量0.20 mol,氨、鈣物質的量之比1.85,CO2體積流量245 mL/min條件下,分別采用300、400、500、600、700 r/min 5個攪拌轉速進行操作,考察攪拌轉速對碳酸鈣晶體粒度分布的影響。
以攪拌轉速為橫坐標,分別以平均粒徑與顆粒分布的變異系數為縱坐標作圖,結果見圖4。
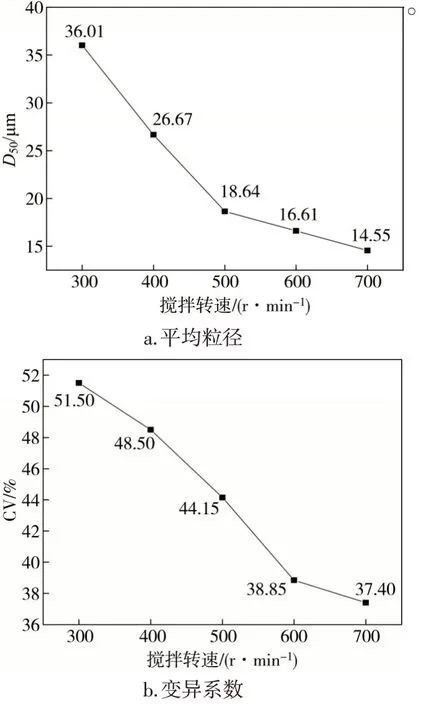
圖4 平均粒徑與顆粒分布的變異系數隨攪拌轉速的變化
由圖4a.可知,CaCO3顆粒平均粒徑隨攪拌轉速的增大而減小,分析其原因:并聚方式被認為是晶粒長大的途徑之一,具體指CaCO3晶體之間受靜電吸引作用或某種外部推動力的影響結合長大,但此種方式并不牢靠,會隨著外部條件的改變而改變,攪拌轉速的增大正是破壞這種結合力的一個主要因素。由圖4b.可知,CaCO3顆粒分布的變異系數隨攪拌轉速的增大而減小。分析其原因:攪拌轉速增大,破壞長大的晶體,使其形成大小均勻的顆粒,以適應逐漸增大的轉速;而微小顆粒晶體則不受影響,繼續長大到適應攪拌轉速的尺寸范圍內。所以CaCO3顆粒總體粒徑分布隨攪拌轉速增大而逐漸均勻,變異系數逐漸減小。進一步發現,隨著攪拌轉速的增大,顆粒分布的變異系數接近于線性變化,擬合得y=-0.03x+62.7,R2=0.98,以此作為其他攪拌轉速操作參數的參考標準。綜上所述,選取600 r/min作為優化實驗的攪拌轉速。
4.4 CO2體積流量對碳酸鈣晶體粒度分布的影響
在反應溫度323.15 K,二水硫酸鈣加料量0.20 mol,氨、鈣物質的量之比1.85,攪拌轉速600 r/min條件下,分別采用100、165、245、330、400 mL/min 5個CO2體積流量進行操作,考察CO2體積流量對碳酸鈣晶體粒度分布的影響。
以CO2體積流量為橫坐標,分別以平均粒徑與顆粒分布的變異系數為縱坐標作圖,結果見圖5。
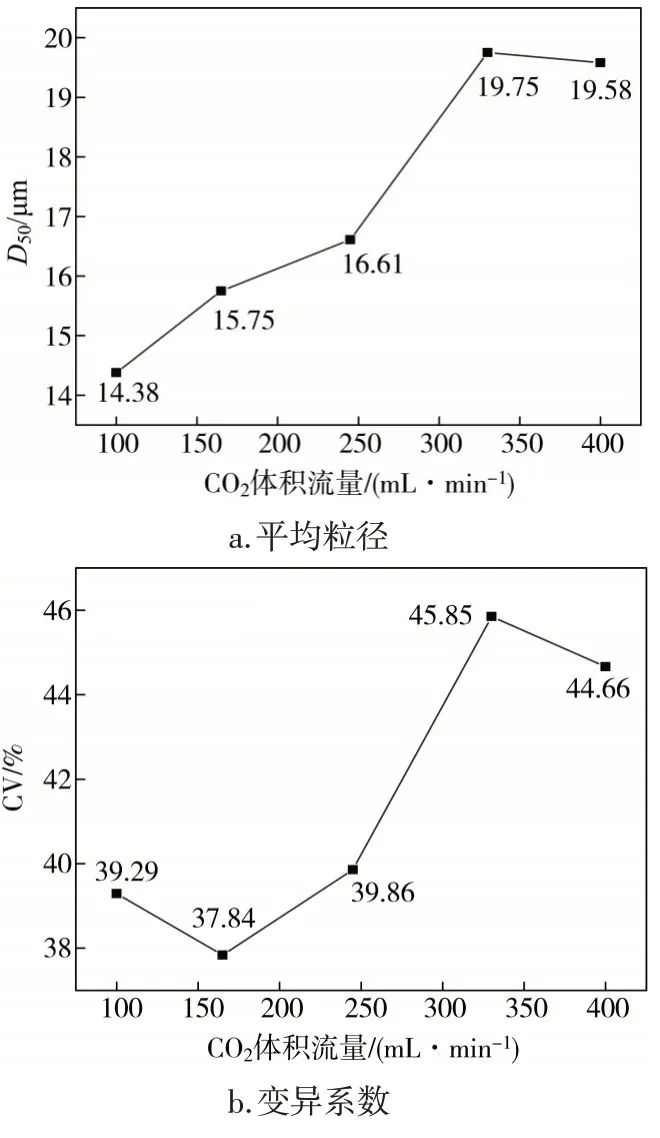
圖5 平均粒徑與顆粒分布的變異系數隨CO2體積流量的變化
由圖5a.可知,CaCO3顆粒平均粒徑隨CO2體積流量的增加呈先增大后減小的趨勢。分析產生這一現象的原因:隨著CO2進氣量的增加,溶液中溶解的CO2不斷增加,為CaCO3晶體的形成提供了豐富的碳源及足夠的推動力,表現為平均粒徑增大。當CO2體積流量達到330 mL/min時,晶體平均粒徑達到最大值19.75 μm,之后隨流量的增加又呈減小的趨勢,產生這個現象的原因可能是由于CO2的不斷通入導致體系逐漸趨于酸性,一部分碳酸鈣晶體又發生溶解反應,表現為平均粒徑減小。
由圖5b.可知,CaCO3顆粒分布的變異系數隨CO2體積流量的增加呈現先減小后增大再減小的三段變化趨勢。分析其原因:當CO2體積流量為100 ~165 mL/min時,推動力主要作用于晶體的成核,總體分布趨于均勻,使變異系數逐漸減小;當CO2體積流量為165 ~330 mL/min 時,推動力一部分作用于晶體的成核,另一部分作用于生長,體系分布逐漸混亂,使得變異系數增大;當CO2體積流量大于330 mL/min時,推動力主要作用于晶體的生長,分布趨于均勻,變異系數減小。綜上所述,CO2體積流量為165 mL/min 時,整個分布的變異系數最小,為37.84%。
5 結論
在CO2(g)-NH3(aq)-CaSO4·2H2O(s)三相反應體系中制備CaCO3晶體的優化工藝條件為:一水合氨與二水硫酸鈣物質的量之比1.85、溫度323.15 K、二水硫酸鈣加料量0.20 mol、攪拌轉速600 r/min、CO2體積流量165 mL/min。在此工藝條件下可以制得平均粒徑為15.75 μm、粒徑分布函數變異系數為37.84%的CaCO3顆粒,為工業應用操作條件提供參考。

