前列地爾聯合諾和銳30及瑞舒伐他汀對糖尿病下肢血管病變患者糖脂代謝及ANGPTL4、hs-CRP水平的影響
代紅沙 王新莉 趙春云
下肢血管病變屬于糖尿病患者較為常見的一種并發癥,主要臨床癥狀表現包括下肢疼痛以及感覺異常等,如不予以及時有效的治療,隨著病情的進展可能并發心腦血管疾病,甚至截肢[1]。臨床上針對該病患者的治療主要以控制血糖水平為主,其中前列地爾、諾和銳30及瑞舒伐他汀均是應用較為廣泛的控制血糖藥物,其聯合應用可能發揮更為明顯的治療效果[2]。此外,動脈粥樣硬化斑塊的形成是糖尿病下肢血管病變的重要病理改變,和糖脂代謝存在密切相關。而脂肪因子血管生成素樣蛋白4(adipokine angiogenin-like protein 4,ANGPTL4)屬于血管生成樣蛋白家族成員之一,廣泛分布在人體的肝臟、脂肪組織以及腎臟,且外周血ANGPTL4可通過與血液循環的HDL微粒結合,從而介導糖脂代謝[3]。超敏C-反應蛋白(hypersensitive c-reactive protein,hs-CRP)屬于炎癥急性時相蛋白最為敏感的非特異性驗證標志物,可有效反映炎癥以及動脈粥樣硬化嚴重程度[4]。鑒于此,本文通過研究前列地爾聯合諾和銳30及瑞舒伐他汀對糖尿病下肢血管病變患者糖脂代謝及ANGPTL4、hs-CRP水平的影響,旨在明確上述治療方案的治療效果及可能作用機制,報道如下。
1 資料與方法
1.1 一般資料 將我院2017年2月至2019年12月收治的82例糖尿病下肢血管病變患者納入研究。隨機數字表法將其等分成試驗組和對照組,每組41例。試驗組男23例,女18例;年齡38~89歲,平均年齡(66.42±10.32)歲;糖尿病病程3~16年,平均病程(8.91±1.33)年。對照組男24例,女17例;年齡39~89歲,平均年齡(66.47±10.35)歲;糖尿病病程3~17年,平均病程(8.96±1.34)年。2組上述指標比較,差異無統計學意義(P>0.05),具有可比性。所有受試者在知情同意書上簽字,并獲批于醫院倫理委員會。
1.2 納入與排除標準 納入標準:(1)受試者均符合中華醫學會糖尿病學分會《中國2型糖尿病防治指南(基層版)》[5]中所制定的相關診斷標準;(2)入院前尚未接受相關治療;(3)年齡>20歲。排除標準:(1)凝血功能障礙或伴有出血性疾病者;(2)心、肝、腎等重要臟器發生嚴重病變者;(3)入院前3個月內接受過抗炎或(和)抗血小板藥物治療者;(4)意識障礙或合并精神疾病者;(5)正參與其他研究者。
1.3 方法 (1)治療方式:對照組實施常規治療:即為患者制定糖尿病飲食,叮囑其餐后進行適量的運動。每日三餐前15 min注射4~26 U諾和銳30(諾和諾德),同時予以阿卡波糖嚼服,嚼服劑量為50 mg/次,連續治療2個月。試驗組在對照組的基礎上增用前列地爾(前列地爾制藥)及瑞舒伐他汀(浙江京新藥業)治療:前列地爾靜脈滴注10 μg/次,1次/d,連續注射15 d為1個療程,每個療程間隔2周。瑞舒伐他汀口服劑量為20 mg/次,1次/d。連續治療2個月。(2)標本采集:分別于治療前1 d以及治療2個月后,采集所有受試者的清晨空腹靜脈血5 ml,以6 cm為離心半徑,進行時長為10 min的3 000 r/min離心處理,獲取血清保存在-80℃冰箱中待檢。
1.4 評價指標 比較2組治療前后糖脂代謝及血清ANGPTL4、hs-CRP水平變化情況,行走距離以及疼痛變化。其中糖脂代謝指標包括空腹血糖(fasting plasma glucose,FPG)、糖化血紅蛋白(HbA1c)、總膽固醇(Total cholesterol,TC)、三酰甘油(triacylglycerol,TG)、低密度脂蛋白膽固醇(low density lipoprotein cholesterin,LDL-C)、高密度脂蛋白膽固醇(high density lipoprotein cholesterol,HDL-C)。分別于治療前后采用全自動生化分析儀檢測。血清ANGPTL4、hs-CRP水平均以酶聯免疫吸附法完成檢測,具體操作遵循試劑盒說明書完成,相關試劑盒購自上海酶聯生物科技有限公司。行走距離以歐姆龍計步器完成計數。疼痛情況采用視覺模擬評分法(visual analogue scoring,VAS)進行評估,總分0~10分,得分越高,反映疼痛越劇烈[6]。
2 結果
2.1 2組治療前后糖脂代謝指標比較 治療后試驗組FPG、HbA1c水平均低于對照組(P<0.05)。見表1。

表1 2組治療前后糖脂代謝指標比較
2.2 2組治療前后ANGPTL4、hs-CRP水平比較 治療后試驗組ANGPTL4水平高于對照組,而hs-CRP水平低于對照組(P<0.05)。見表2。

表2 2組治療前后ANGPTL4、hs-CRP水平比較
2.3 治療前后2組行走距離比較 治療后試驗組最大行走距離以及無疼痛行走距離均多于對照組(P<0.05)。見表3。

表3 治療前后2組行走距離比較
2.4 治療前后2組VAS評分比較 治療后試驗組及對照組VAS評分均低于治療前,且試驗組低于對照組(均P<0.05)。見表4。
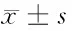
表4 治療前后2組VAS評分比較 n=41,分,
3 討論
當前,關于糖尿病下肢血管病變的具體發病機制尚未完全明確,但普遍認為可能和血小板聚集、血糖波動以及炎性反應等可能介導該病的發生、發展過程[7,8]。其中血糖波動可導致細胞形態以及功能受損,從而引起人臍靜脈內皮細胞內蛋白激酶激活,細胞間黏附因子-1水平提高,進一步加重氧化應激反應,從而導致炎癥級聯反應的發生,對血管內皮功能造成不同程度的損傷[9-11]。同時,高血糖水平會促使機體血液處于高凝狀態,從而為動脈粥樣硬化形成創造有利條件,增加了心血管事件發生的風險。由此可見,治療糖尿病下肢血管病變應以抗血糖、抗血小板凝聚以及抗炎等為主要目標[12-14]。
本文結果發現,治療后試驗組及對照組的FPG、HbA1c水平均有所改善,且試驗組改善程度更高。這在張敘填等[15]的研究報道中得以佐證,提示了前列地爾、諾和銳30以及他汀類藥物治療糖尿病下肢血管病變,可有效控制患者血糖水平。分析原因,前列地爾可發揮較佳的抗血小板聚集作用,有助于血液黏度以及紅細胞聚集性下降,促使紅細胞變性能力以及血液流變學得以改善,為血管內皮功能的修復創造了有利條件。瑞舒伐他汀則可有效減輕炎性反應,具有明顯的降脂效果。諾和銳30是一種雙時相胰島素類似物,具有控制血糖水平的作用,且經皮下注射具有起效快、作用時間持久的特點。諸藥聯合應用具有一定的協同互補作用,繼而為患者的糖脂代謝改善提供了重要基礎。然而,鄧舒妮等[16]的研究結果發現:他汀類藥物與血糖控制藥物聯合治療糖尿病下肢血管病變患者,可顯著改善其LDL-C以及HDL-C水平。這和本研究結果存在一定差異,而導致兩項研究結果出現差異的主要原因可能是研究藥物存在一定的差異以及研究對象的年齡跨度不同有關。治療后試驗組ANGPTL4水平高于對照組,而hs-CRP水平低于對照組。其中ANGPTL4屬于一種分泌型糖蛋白,介導了血管生成以及轉移調控過程,和糖尿病的發生、發展密切相關。且有相關研究報道表明,機體外周血循環內的中ANGPTL4可與血液中HDL微粒向結合,進一步介導脂質代謝,在糖尿病患者的脂代謝紊亂中起著至關重要的作用[17,18]。同時,動脈粥樣硬化作為糖尿病下肢血管病變的病理基礎,往往伴有一定程度的炎癥,長期的炎癥刺激會促進血管活性因子、細胞因子以及生長因子的產生,繼而促進肝臟合成CRP。另有相關研究報道指出:胰島素會阻斷肝臟合成CRP,而胰島素抵抗則會引起胰島素生理作用降低,進一步促進CRP的合成增加[19,20]。由此,可推測試驗組治療方式的可能機制為提高ANGPTL4水平以及降低hs-CRP水平。本文還發現,治療后試驗組最大行走距離以及無疼痛行走距離均多于對照組,且治療后試驗組及對照組VAS評分均低于治療前,而試驗組又低于對照組。這表明了試驗組治療方式可有效增加患者行走距離,減輕軀體疼痛。究其原因,前列地爾聯合諾和銳30及瑞舒伐他汀三聯療法可發揮較佳的穩定血糖水平作用,同時有助于患者臨床癥狀的改善,繼而減輕靜息痛、麻木感以及冷感,從而使得患者可堅持步行,進一步促進行走距離的增加。
綜上所述,前列地爾聯合諾和銳30及瑞舒伐他汀三聯療法在改善糖尿病下肢血管病變患者糖脂代謝以及ANGPTL4、hs-CRP水平方面效果明顯,且有助于患者行走距離的增加,減輕疼痛。

