重型新型冠狀病毒肺炎118例臨床特征分析
謝丹,陳俊春,邱婷,趙川
(1.南京中醫藥大學附屬昆山市中醫醫院急診科,江蘇 昆山 215300; 2.華中科技大學同濟醫學院附屬同濟醫院綜合醫療科,湖北 武漢 430030)
2019冠狀病毒病(coronavirus disease 2019, COVID-19)仍在全球蔓延,可引起呼吸衰竭等嚴重呼吸道癥狀[1]。已證實COVID-19由一種新型冠狀病毒引起,現稱為重癥急性呼吸綜合征冠狀病毒2(severe acute respiratory syndrome coronavirus 2, SARS-CoV-2),最有可能來源于人畜共患病冠狀病毒,如2002年出現的SARS-CoV。在第一次報告后的幾個月內,SARS-CoV-2在我國和世界范圍內蔓延,達到了大流行水平[2]。本科室相關醫務人員在2020年2月至3月前往武漢參與救治新型COVID-19患者,在重癥監護室搶救重型COVID-19患者時發現,同樣是重型患者部分最終死亡,部分經治愈出院。因此,本研究擬通過回顧性分析死亡和非死亡COVID-19患者在臨床特點和檢驗指標等方面的差異,為今后收治同樣患者提供預判的可能。
1 對象與方法
1.1 研究對象
選擇2020年2月至3月武漢同濟醫院光谷院區重癥監護室COVID-19 確診死亡患者51例作為死亡組;同時,選擇同期重癥監護室出院未死亡患者67例作為未死亡組。確診病例依據國家衛健委印發《新型冠狀病毒肺炎診療方案(試行第七版)》診斷標準執行: ① 通過采集咽拭子或痰液等分泌物標本進行SARS-CoV-2 核酸檢測;② 胸部CT提示早期肺外帶多發小斑片影,進行性發展為多發磨玻璃影或肺實變。本回顧性研究分析遵照赫爾辛基宣言原則進行并通過醫院倫理委員會審查(批件號:KZY2020-41)。
1.2 納入標準
1.2.1 入選標準 符合《新型冠狀病毒肺炎診療方案(試行第七版)》臨床分型為重型標準中的任何一條的成人患者,具體標準:靜息狀態下指氧飽和度≤93%;氧合指數PaO2/FiO2≤300 mmHg;呼吸急促(>30次/min);肺部影像顯示24~48 h病灶明顯進展>50%。
1.2.2 排除標準 非重型COVID-19;合并惡性腫瘤、肺結核等慢性消耗性疾病;合并新近心肌梗死和腦卒中;合并血液病或肝功能、腎功能等重要臟器功能衰竭病史;年齡<18歲;因藥物過敏等原因出現意外死亡。
1.3 數據收集
1.3.1 臨床基本特征 記錄患者年齡、性別、吸煙史、高血壓、心功能不全、糖尿病和慢性阻塞性肺疾病(COPD)等。
1.3.2 臨床結局 記錄患者是否發生呼吸衰竭、心力衰竭、膿毒血癥、腎功能衰竭、多器官功能衰竭(MODS)、50%以上肺受累破壞等。
1.3.3 實驗室檢查 記錄兩組患者進重癥監護室第1天外周血白細胞計數、中性粒細胞計數、谷草轉氨酶(AST)、尿素氮、乳酸脫氫酶(LDH)、估算腎小球濾過率(eGFR)、心衰標志物N-末端B型利鈉肽原(NT-proBNP)等。
1.4 統計學方法
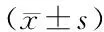
2 結果
2.1 COVID-19重癥死亡患者的臨床特征
死亡組和非死亡組年齡、吸煙史(>10年)和合并COPD比較差異有統計學意義(P均<0.05);性別,合并癥(高血壓、心功能不全、糖尿病)比較,差異無統計學意義(P均>0.05)。見表1。
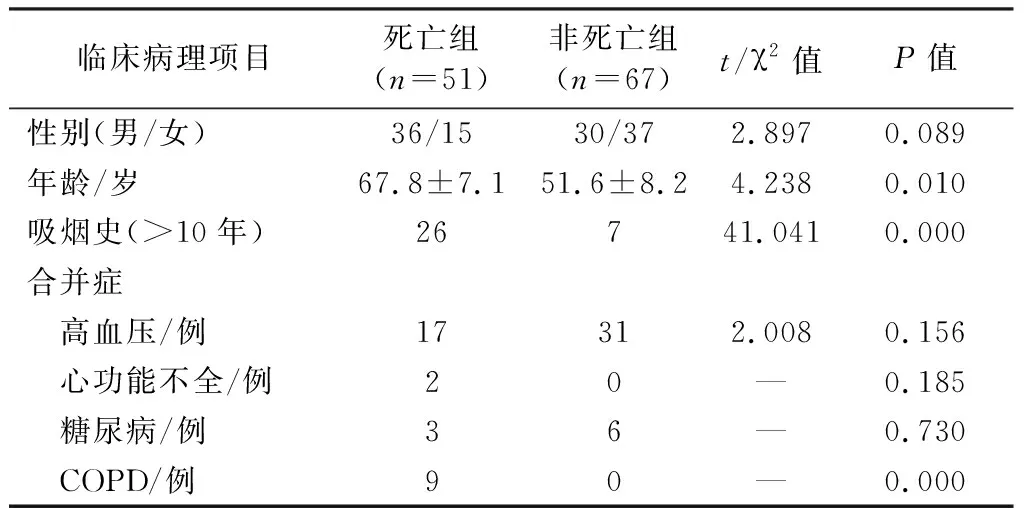
表1 COVID-19死亡組和非死亡組臨床病理特征差異
2.2 兩組患者臨床結局差異
死亡組呼吸衰竭、心力衰竭、腎功能衰竭和MODS合并癥發生率明顯高于非死亡組(P均<0.05);而兩組患者合并膿毒血癥無顯著差異(P>0.05)。影像學提示,死亡組50%以上肺受累破壞(胸部CT)患者數明顯高于非死亡組(P<0.05)。見表2。
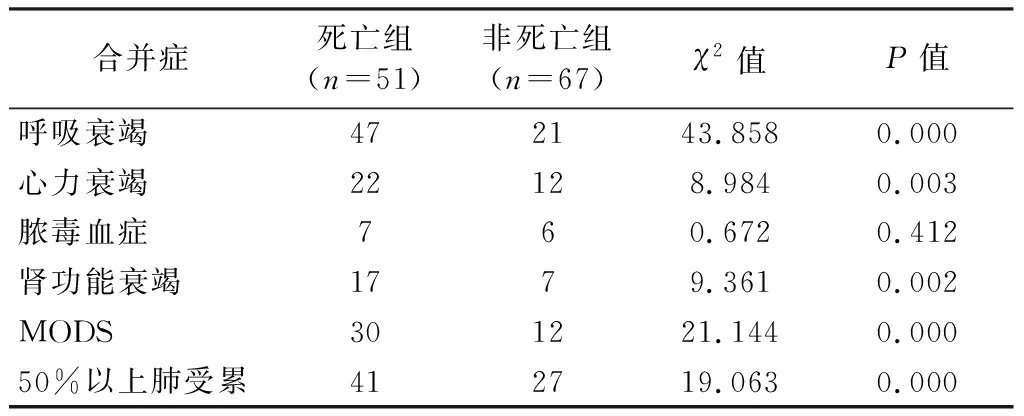
表2 COVID-19重癥患者的疾病進程差異
2.3 兩組患者外周血指標的差異
如表3,死亡組和非死亡組患者進重癥監護室第1天外周血白細胞計數、中性粒細胞計數、AST、尿素氮、LDH、eGFR、NT-proBNP水平均存在顯著差異(P<0.05)
2.4 多因素logistic回歸分析
進一步采用多因素logistic回歸分析顯示,年齡、吸煙史>10年、呼吸衰竭、MODS、尿素氮和eGFR可作為COVID-19患者死亡預后的獨立因素(P<0.05)。見表4。
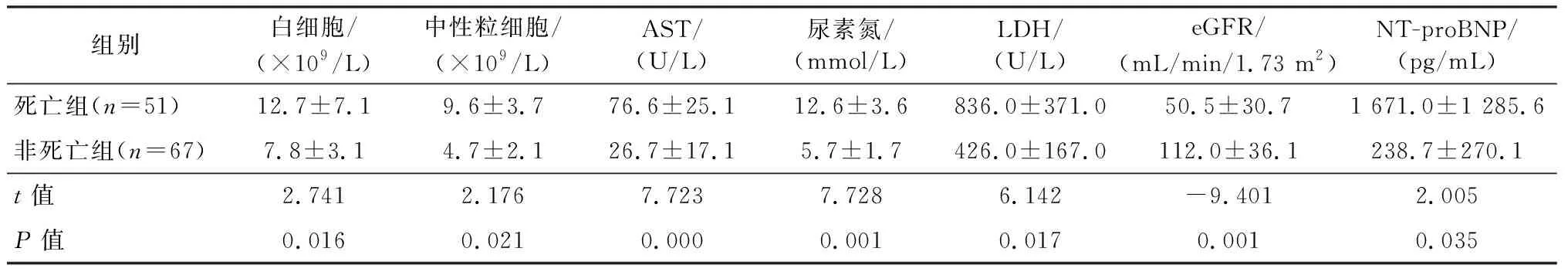
表3 兩組患者外周血指標差異
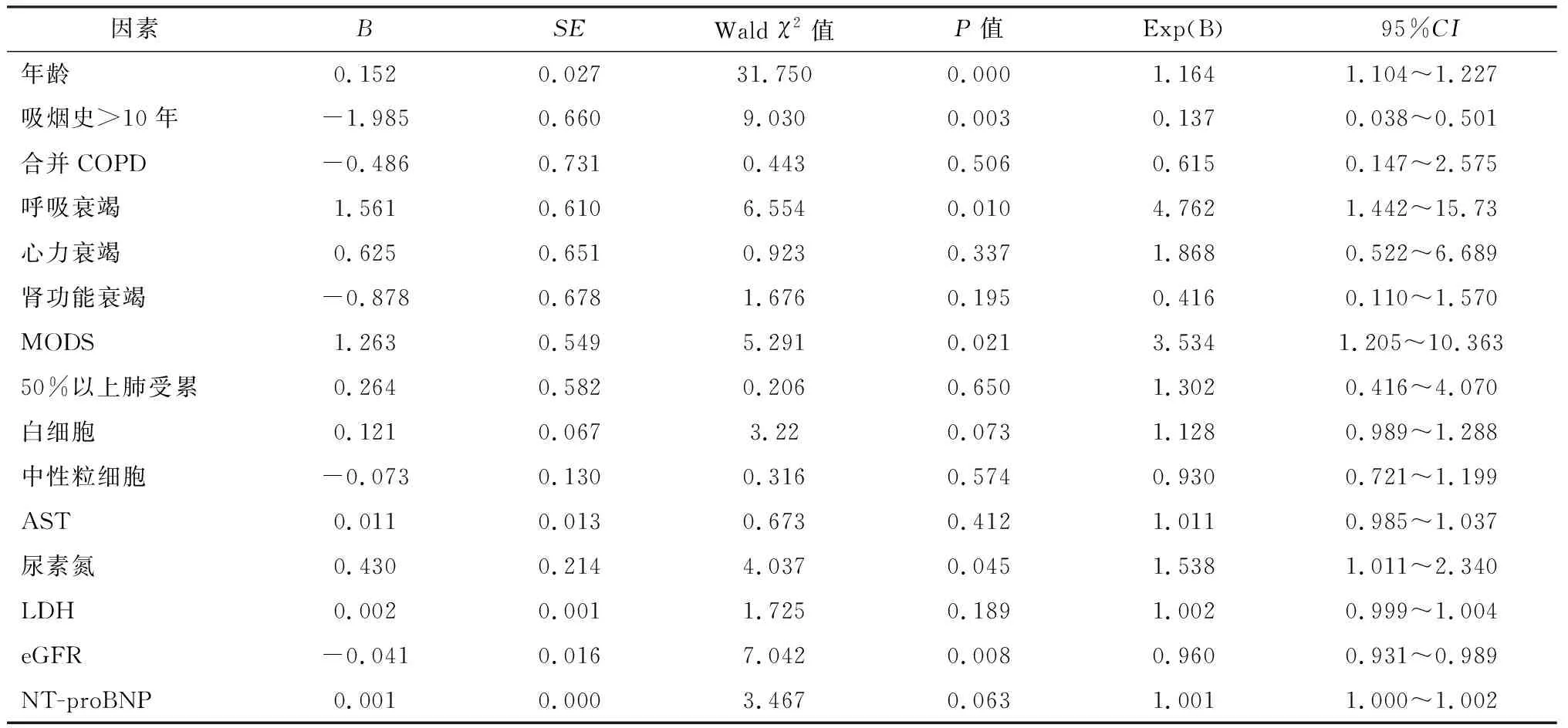
表4 多因素logistic回歸分析結果
3 討論
據報道,大多數SARS-CoV-2感染患者出現輕度癥狀,如干咳、喉嚨痛和發燒,且大多數情況都可自行緩解[3-4]。然而,有部分患者出現各種致命的并發癥,如器官衰竭、敗血性休克、肺水腫、嚴重的肺炎和急性呼吸窘迫綜合征,需要進一步的重癥監護支持[5-7]。重癥監護支持的重型COVID-19患者中相當一部分病情持續惡化后死亡,目前并沒有明確的指標和參數能支持早期預警重癥患者出現死亡的風險[8]。多項報道提示,年齡>80歲患者易出現病情加重而發展成重型COVID-19[9-10]。本研究發現,>67歲患者死亡風險增加,且與性別無關,其往往合并吸煙史、高血壓、心功能不全、糖尿病和COPD;最終分析提示,合并有吸煙史>10年和COPD的重型COVID-19患者更易發生死亡。
死亡組外周血白細胞和中性粒細胞計數明顯高于非死亡組,這提示外周血白細胞和中性粒細胞計數增高預示患者病情惡化,有死亡風險。同時,兩組外周血AST、尿素氮、LDH、eGFR和NT-proBNP含量存在統計學差異。AST主要存在心肌、肝臟、骨骼肌和腎臟等,其上升往往提示心肌受損,或多器官功能受損;尿素氮是判斷腎小球濾過功能的指標,其增高提示腎功能不全;LDH主要存在心肌、腎臟和骨骼肌中,其升高也提示相關臟器細胞受損;eGFR是用來評價腎小球濾過率的一個指標,下降提示腎功能不全;NT-proBNP是目前心衰診療中應用最廣泛的生物標志物,其升高提示心力衰竭[11-13]。上述指標主要圍繞心臟和腎兩大器官,表明COVID-19死亡患者除肺部嚴重損害外,往往伴隨顯著的心、腎損害,同時,預警患者有死亡風險。
此外,并發呼吸衰竭、心功能衰竭、腎功能衰竭和MODS患者死亡風險增加,而病程中合并膿毒血癥則無顯著差異,推測這可能與敏感抗生素應用有關。并且,發生死亡的患者往往伴隨雙肺的嚴重損害。進一步發現,僅年齡、吸煙史>10年、呼吸衰竭、MODS、尿素氮和eGFR可作為COVID-19患者預后的獨立因素。
綜上所述,對重型COVID-19患者入住重癥監護病房后應及時進行死亡風險評估,對于67歲以上合并有吸煙史>10年患者更要密切關注。同時,動態監測尿素氮和eGFR等指標,及時發現患者出現呼吸衰竭和MODS,對預測COVID-19死亡風險有預警意義。

