磷酸鐵鋰電池老化后的產熱規律研究*
錢柯宇,黃 瑞,俞小莉,陳芬放,吳啟超
(浙江大學 能源工程學院,浙江 杭州 310027)
0 引言
隨著世界各國對節能減排要求的不斷提高,傳統燃油汽車的生產和銷售將逐步受到法律法規的限制,新能源汽車受到社會各界越來越多的重視。鋰離子電池作為電動汽車的主流儲能系統也在近幾年得到快速的發展[1]。電池內部產熱對鋰離子性能和安全均有重要影響,因此電池的內部產熱是鋰離子電池的研究熱點。
由于鋰離子電池是一個封閉的系統,用實驗的方法研究電池的熱特性相對復雜。因此通過數值模擬的方法建立電池熱模型,得到電池內部各項熱參數,在電池熱特性研究中起著重要作用。電池的產熱模型可分為電-熱模型[2-3]、電化學-熱模型[4-6]以及熱濫用[7-8]模型。宋文吉等人[2]建立分層結構的電-熱耦合模型研究電池的內部溫度分布。Jiang等人[3]建立了一種低溫電-熱耦合模型用于研究低溫下電池放電和產熱特性。Liang等人[4]通過建立電化學-熱模型計算不同放電倍率下電池的可逆熱與不可逆熱。Karthik等人[5]建立電化學-熱模型探究電池的熱行為以及PCM熱管理方法。上海交通大學的賴彭飛等人[7]建立電池的熱濫用模型,研究了鋰離子電池的放電產熱行為,并提出了判別電池安全性能的方法。
但是,上述模型在預測充電或放電過程中電池的熱特性時均忽略了電池老化的影響。隨著工作時間的增加,電池內部發生副反應,導致鋰離子損失和內部阻抗增加,電池發生老化,電池的熱特性也相應的發生變化,現階段很少有研究關注到了這一現象。因此本文基于COMSOL軟件,建立了電化學-熱-老化耦合模型,探究考慮電池老化后的產熱規律,并在此基礎上進一步研究了不同充電倍率和環境溫度對電池老化后內阻、容量、產熱特性的影響,可為后續基于產熱的動力電池熱管理研究提供理論參考。
1 模型建立
1.1 電化學模型
本研究采用Doyle和Newman建立的準二維電化學模型預測電池內部產熱[9]。電池準二維模型描述了電池內部固相、液相兩相以及正極、隔膜、負極三區域的電化學反應過程。其中在電池的兩極中是固相電極活性粒子和液相電解液的均勻混合,而電池的隔膜中只有液相的電解液。該模型在計算時只考慮電池的電極厚度方向以及電池的活性粒子半徑方向。模型中包括五項化學反應:鋰離子固相擴散,鋰離子液相擴散,固相歐姆定律,液相歐姆定律和電化學反應動力學。
1)固相擴散
鋰離子的固相擴散符合菲克第二定律:
(1)
其中,cs(t,r)為活性材料的內部r位置處的固相鋰離子濃度;Ds為鋰離子的固相擴散系數;r為固相的活性粒子的徑向位置,由于固相活性粒子的半徑為R,因此當r=R時,cs表示的是活性粒子表面的鋰離子的濃度,當r=0時,cs表示的是活性粒子球心處的鋰離子濃度。
固相擴散有兩個邊界條件,在活性粒子的內部的顆粒中心,鋰離子的濃度梯度始終為0。
(2)
在活性粒子表面的固相鋰離子濃度梯度與局部反應的電流密度滿足以下關系式:
(3)
其中,R為正負極活性粒子的半徑,ji為局部反應電流密度:
(4)
式中,F為法利第常數,as為活性粒子比表面積,計算公式如下:
(5)
式中,εs為固相體積分數。
2)液相擴散
液相擴散同樣遵循菲克第二定律:
(6)
式中,εe為液相體積分數,De為鋰離子液相擴散系數,t+為鋰離子遷移數。在電池的兩極與集流體的交界面處,鋰離子濃度梯度為0。
3)固相歐姆定律
在正負電極處的固相電勢分布遵循歐姆定律:
(7)
其中,φs為固相電勢,is為固相電流密度,σeff為有效電導率,計算公式如下:
(8)
式中,σ為固相電導率。
在電池的正負極與集流體的交界面處的固相電流等于電池的充放電電流,在電池的隔膜處不存在固相電流,因此,固相電勢分布的兩個邊界條件如下所示:
(9)
4)液相歐姆定律
電池液相的電勢分布遵循歐姆定律:
(10)
其中,R為摩爾氣體常數,T為電池溫度,t+為鋰離子液相轉移系數,電池正負電極和集流體交界面處的液相電勢梯度為0,與隔膜交界面處的電勢梯度連續。κeff為液相有效電導率,計算公式如下:
(11)
5)Bulter-Volmer電化學反應方程
鋰離子電池在固相活性離子和電解液溶液臨界面處的電化學反應遵循巴特勒-伏爾默(Butler-Volmer)動力學方程:
(12)
(13)
式中,αa以及αc分別為陰陽極的電化學反應傳遞系數,一般取值為0.5。ki為反應速率常數,cs,surf為電極活性顆粒表面的固相鋰離子濃度,cs,max為活性材料可嵌入的最大鋰離子濃度。
電池的表面過電勢計算方式如下:
(14)
其中,φs為固相電勢,φe為液相電勢,Uref為參考開路電壓,為正負電極自身性質相關的SOC函數。
本文研究對象為圓柱形石墨-磷酸鐵鋰26650電池,型號ANR26650M1A,標稱容量2.3Ah,電池具體的參數見表1。
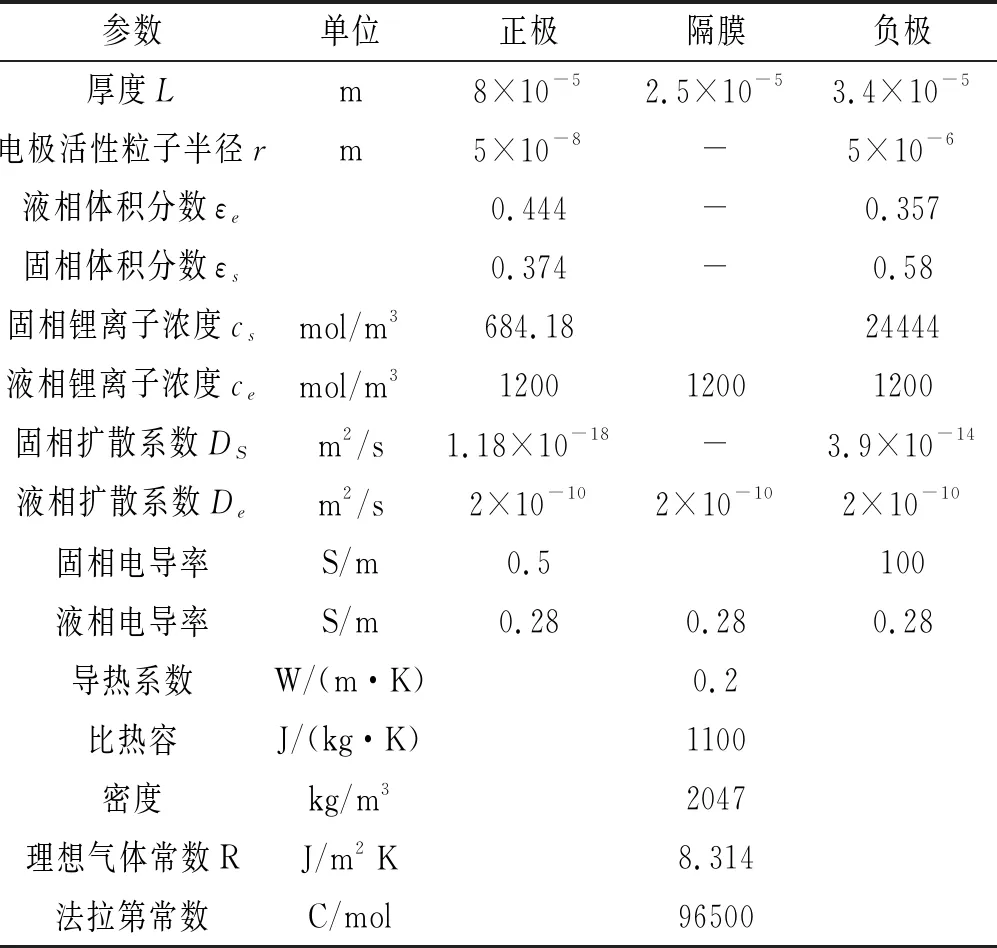
表1 ANR26650M1A磷酸鐵鋰電池的主要參數[10]
1.2 電池老化模型
電池老化包括SEI膜增長、負極析鋰、顆粒破裂等,正常循環工況下電池老化主要發生的是SEI膜生長增厚的副反應,因此本研究在傳統的電化學準二維模型中引入SEI膜增長的老化方程[11]。
電池內部的電流可以分為主反應電流密度ji和副反應電流密度jsei,即:
j=ji+jsei
(15)
和主反應類似,SEI膜的增長可用Tafel方程代替,具體方程為:
(16)
j0,sei=nFkseics
(17)
其中,ksei為反應速率常數,cs為活性粒子表面電解液濃度。SEI生成的副反應不僅僅只受反應動力學限制,同時還受到擴散的限制,因此在電池SEI生長的副反應公式中引入擴散的限制,具體方程如下:
(18)
其中δ為電池副反應的SEI膜厚度。
(19)
式中,M為SEI層的分子質量,ρ為SEI的密度。SEI膜的阻值計算如下:
(20)
電池老化的SEI膜參數具體見表2。

表2 電池SEI膜的主要參數[11]
1.3 電池傳熱模型
為簡化模型,在模型中不考慮電池的熱輻射,因此電池內部導熱過程的控制方程如下:
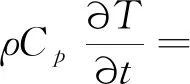
(21)
其中,qbatt為一維電化學模型中的總產熱,Cp為電池的比熱容,λ為電池的導熱系數。
電池表面與空氣接觸,在電池表面,溫度和熱流密度是連續的,因此電池/空氣表面的能量守恒方程如下:
(22)
其中,n表示電池表面法向,h為對流換熱系數。
1.4 模型驗證
在COMSOL軟件中建立上述電化學-老化-熱耦合模型,并與參考文獻[10]中的實驗結果進行對比。仿真采用與實驗相同的邊界條件,圖1顯示電化學-熱模型的仿真結果和實驗結果吻合較好。基于此將電化學-熱模型與老化模型耦合,進行1C多次充放電循環仿真。將計算得到的電池容量衰退曲線的橫坐標單位轉化為月份后,與參考文獻[11]中的老化實驗結果進行對比,發現也能較好吻合,說明該模型滿足本文的研究所需。
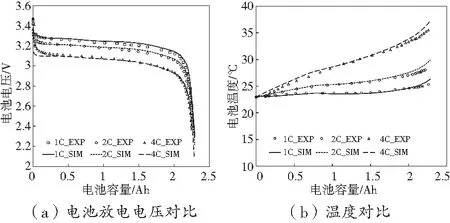
圖1 實驗數據和仿真數據對比
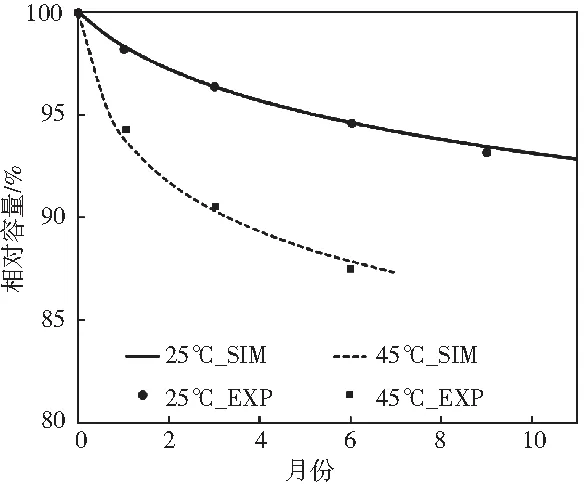
圖2 電池老化模型驗證
2 充電電流對電池老化以及產熱的影響研究
2.1 不同充電電流下電池的老化規律
鋰離子的消耗導致的電池老化和充電電流大小密切相關[12]。因此設計不同的充電電流工況,探究電池在不同的充電倍率下老化的規律及其對產熱的影響。令電池放電電流為1 C,充電倍率分別為0.5 C、1 C、2 C、3 C,充放電循環4000次,環境溫度恒定為25 ℃,得到在不同充電倍率下電池的SEI內阻和膜厚的變化規律。如圖3所示,充電倍率越低,電池副反應生成的SEI膜越厚,相應的內阻也越大[13]。并且隨著充放電循環的增加,SEI內阻增長的速率減慢。
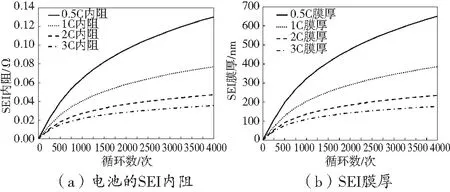
圖3 不同充電倍率下電池的內阻、膜厚

圖4 不同充電倍率下電池的相對容量變化
電池容量是衡量電池老化的主要指標之一,如圖4所示是不同充電倍率循環下,電池的相對容量變化情況,由圖可知,電池的放電容量隨著循環數的增加逐漸降低,并且充電倍率越低,電池的容量衰退越嚴重,在電池以0.5 C充電1 C放電4000個循環后電池的相對容量衰退達到了85%。
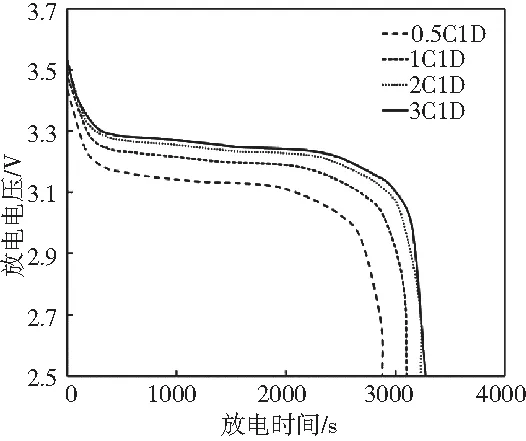
圖5 不同充電倍率老化后電池的放電特性曲線對比
電池老化也會導致電池的放電特性衰退,分別取不同充電倍率下循環4000次后的電池進行1 C放電仿真,由圖5可知,低充電倍率老化的電池放電電壓最低,放電時間最短,電池的放電量減少,電池老化越嚴重。
由于SEI膜存在阻值,導致放電電壓下降,因此電池老化后,放電的起始電壓降低。如圖6所示為電池不同循環數下SEI膜上的壓降,充電倍率越小,SEI膜上的壓降越大,這和圖5所示的放電起始電壓的規律保持一致。
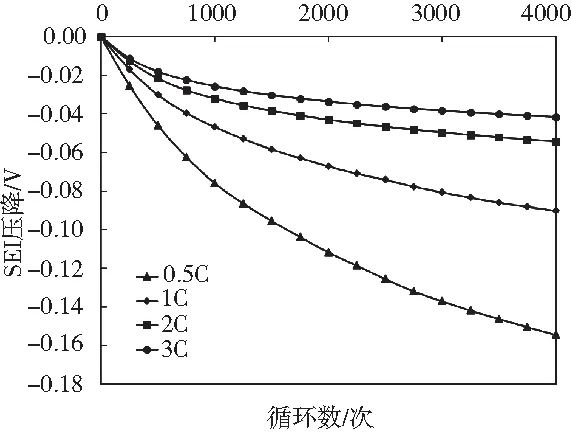
圖6 不同老化工況下的SEI壓降
2.2 電池老化前后產熱特性研究
2.2.1 電池未老化時放電過程中的產熱特性
鋰離子電池的放電過程將化學能轉變為電能,鋰離子從負極活性粒子中脫出,嵌入到正極活性物質中,在放電過程中產生的熱包括電化學反應熱、極化熱和歐姆熱。
如圖7至圖9所示是新電池在1 C放電時負極、正極和隔膜的產熱功率曲線,圖10為電池的總產熱曲線。電池的負極產熱主要由極化熱和反應熱組成,歐姆熱的占比較小。極化熱在放電過程中恒為正值,而反應熱呈現先負后正的趨勢,疊加后得到電池負極在放電過程中的總產熱曲線,在整個放電過程中負極存在吸熱過程和放熱過程。
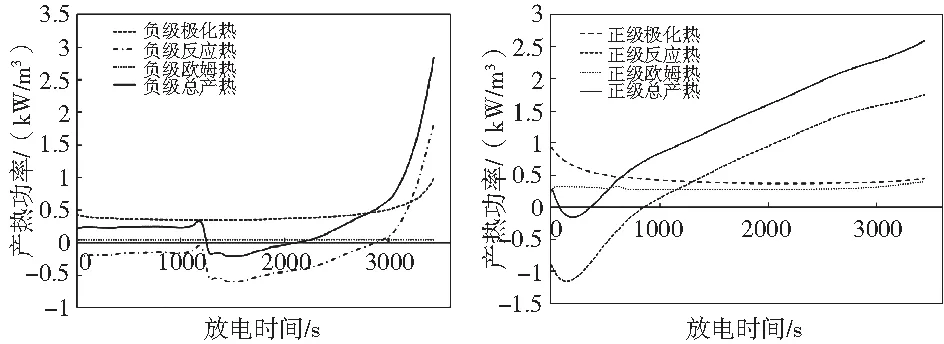
圖7 電池負極產熱功率 圖8 電池正極產熱功率
電池的正極產熱功率如圖8所示,正極的產熱同樣由極化熱、反應熱和歐姆熱三部分組成,正極產熱功率低于負極。由于在電池隔膜處不發生電化學反應,產熱只包括歐姆熱,并且與多孔電極相比,電池隔膜的產熱功率較小,因此可以忽略不計。電池的總產熱曲線見圖10,是電池正極、負極以及隔膜產熱功率的總和,恒為正值。
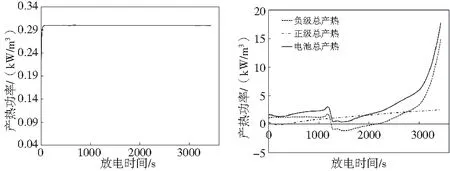
圖9 電池隔膜產熱功率 圖10 電池總產熱功率曲線
2.2.2 電池老化后的產熱特性變化規律
伴隨著電池的多次充放電循環,電池副反應導致內部活性物質的損失以及電池內阻的增加,這都會引起電池在放電過程中的放熱特性變化。如圖11所示分別為電池在未老化,2000次和4000次充放電循環后,負極和正極的總產熱功率變化。負極總產熱功率顯著上升, 由于老化后電池的容量衰退,導致電池的放電時間逐漸縮短,在4000次充放電循環后,放電時間縮短至未老化時間的86.3%。由于副反應生成的SEI膜在負極生長,因此,電池正極產熱功率幾乎不發生變化。電池的總產熱功率隨著充放電循環數增加也逐漸增加。
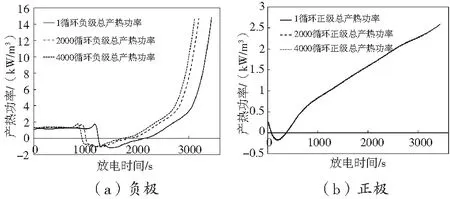
圖11 電池不同循環數下正負極的產熱功率變化
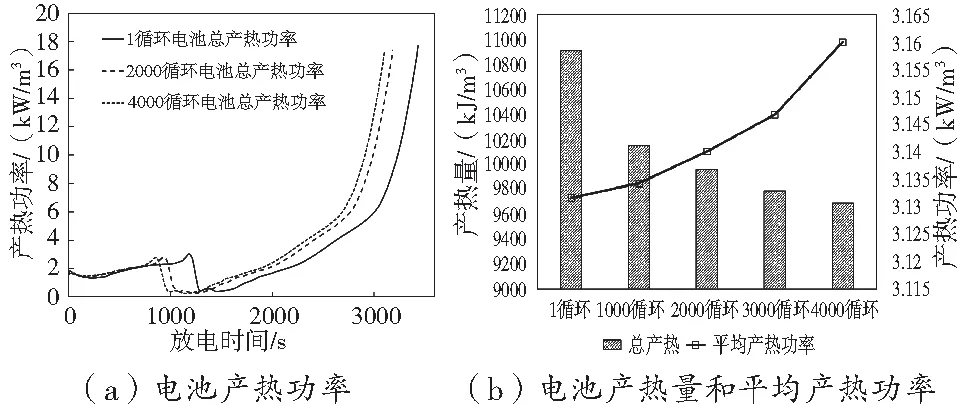
圖12 不同循環下電池產熱功率、產熱量和平均產熱功率變化
由于電池的副反應導致電池內部活性物質和鋰離子的減少,使得電池放電更快到達截止電壓,放電時間縮短,電池的產熱曲線整體左移,相應的在整個放電過程中電池的放電總量減少。當循環數從1到2000和到4000,電池的產熱量分別降低8.7%和11.7%,而電池的平均產熱功率上升1.5%和2.1%。
2.2.3 不同充電工況老化后電池的產熱特性
電池在不同的充電工況下進行充放電循環后,電池的老化狀態不同,從而會進一步影響電池的產熱特性。因此對電池分別在0.5 C、1 C、2 C、3 C充電,1 C放電條件下(以下簡稱0.5C1D、1C1D、2C1D、3C1D),進行4000次循環,得到電池正負極的產熱對比如圖13所示,由圖可知,充電倍率越低,電池老化越嚴重,放電時間越短,電池正負極的產熱曲線越靠左。由于SEI膜在負極生長,因此負極的產熱功率顯著上升。
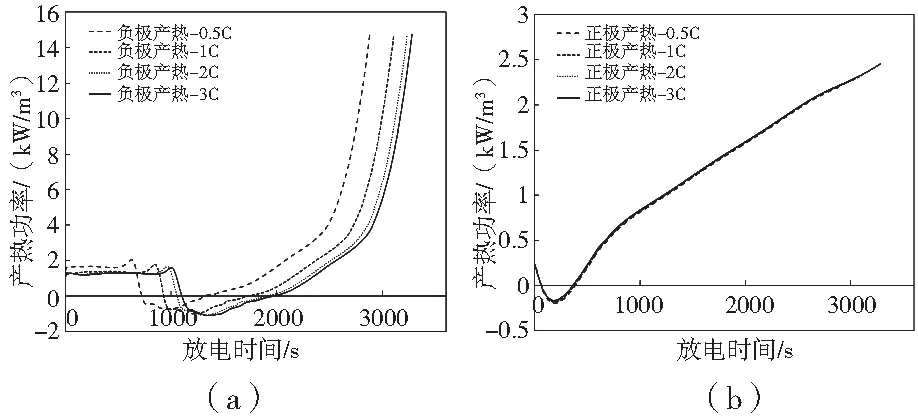
圖13 不同充電工況下電池老化后正負極產熱功率對比
如圖14(a),電池總產熱功率也隨著充電倍率的減小而上升。圖14(b)中,電池在以0.5C1D條件下老化后,放電產熱總量最小,比3C1D工況時產熱量少10.3%,但是平均產熱功率高5.3%。由此可見,充電倍率越小,電池老化越嚴重,電池老化會進一步影響電池的產熱,導致產熱功率上升。
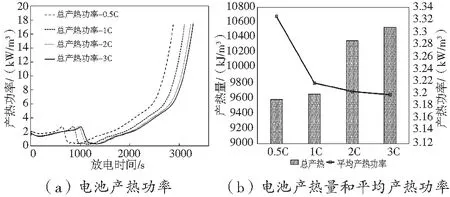
圖14 不同充電工況下電池產熱功率、產熱量和平均產熱功率
3 環境溫度對電池老化以及產熱的影響規律研究
3.1 環境溫度對電池老化的影響
環境溫度會影響電池內部的反應速率和擴散速率,因此選取不同環境溫度,探究電池在不同的溫度條件下老化以及產熱的變化規律。在1 C充放電條件下,保持自然對流冷卻方式,改變環境溫度為283 K、298 K、313 K,電池SEI膜增長以及容量衰退如圖15所示。環境溫度越高,SEI膜增長越快,電池的容量衰退越劇烈,在溫度為313 K時,電池4000次循環后的容量衰退已經達到13%。
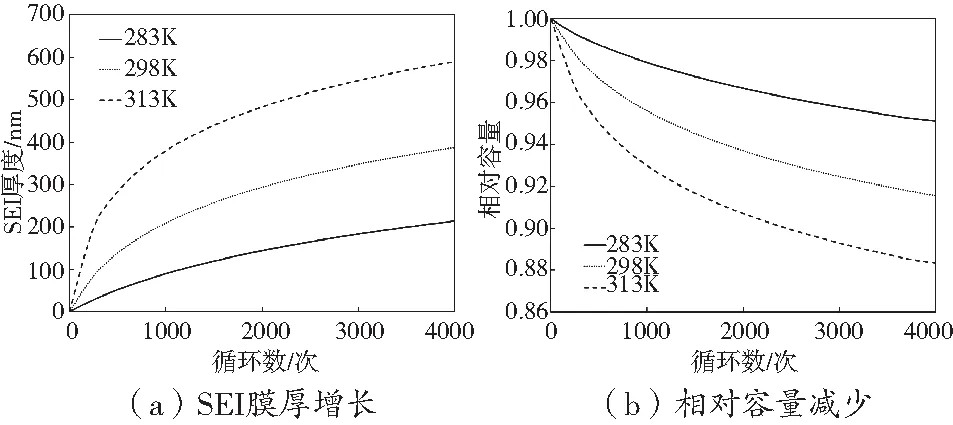
圖15 不同溫度下電池SEI膜厚和相對容量變化
3.2 環境溫度對電池老化后產熱的影響
在不同的環境溫度下進行4000次充放電循環后,電池的老化特性不同。如圖16所示,環境溫度從283 K、298 K,再到313 K的上升過程中,電池的產熱功率依次上升3.4%和8.5%,產熱量減少2.6%和3.7%。
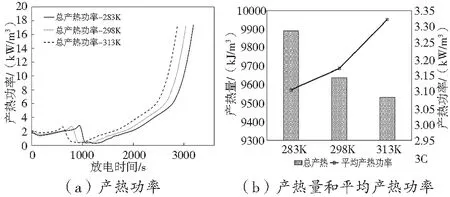
圖16 不同環境溫度下電池產熱功率、產熱量和平均產熱功率
4 結論
本文以型號為ANR26650的圓柱形LiFePO4電池為研究對象,建立鋰離子電池電化學-老化-熱耦合模型,研究了不同充放電倍率和環境溫度對電池老化和產熱的影響,主要結論如下:
1)隨著充放電循環的增加,電池老化,容量衰退,SEI膜厚以及內阻增大。電池老化后,放電產熱功率上升,放電容量衰減,導致放電時間縮短,因此電池放電總產熱量減小。
2)充電倍率越小,老化越劇烈,產熱功率變大。由于放電容量衰退,放電時間縮短,因此產熱量略有減小。電池在0.5C1D狀態老化下的電池放電產熱平均功率,比在3C1D工況老化下的產熱功率高約5.3%,產熱量減小約10.3%。
3)環境溫度越高,老化越劇烈,放電產熱功率越大,產熱量減小。在313 K條件下老化的電池比在283 K下老化的電池,平均產熱功率高約8.5%,產熱量低約3.7%。

