FeCl3活化的麥秸活性炭對水中硝酸根的去除
李際會,魏 萍,李寶強,國金義,李 靜,楊寶山,宋吉青
(1.臨沂市農業科學院,山東 臨沂 276012;2.東營市墾利區永安鎮農技站,山東 東營 257503;3.中國農業科學院農業環境與可持續發展研究所,北京 100081)
水體中大量營養元素的富集會導致水體富營養化,藻類等浮游生物大量繁殖,水體溶解氧量降低,水質惡化,增加水處理成本并危害人體健康[1-3]。氮和磷是導致水體富營養化的關鍵營養元素[4]。去除水體中的硝酸根對改善水質及保護生態環境具有重要意義[5]。傳統方法主要是通過化學、物理、生物等過程去除水體中的硝酸根[4]。經濟簡便的吸附法被大量應用于各類污水的凈化處理中[2-4]。有研究表明,鐵氧化物對水體中含氧陰離子具有高親和力和吸附選擇性[6-8],但水體中粉末狀的鐵氧化物分離較困難,限制了其在去除污染物方面的應用[9]。利用FeCl3作為活化劑制得的負載鐵氧化物活性炭對水體中有機物和砷酸根有較強的吸附能力[8-11]。麥秸生物炭通過鐵鹽溶液改性負載鐵氧化物后對水體中硝酸根和磷酸根的吸附能力大于原狀生物炭[10],但吸附硝酸根能力(純氮計2.47 mg·g-1)低于吸附磷酸根能力(純磷計16.58 mg·g-1)。這是因為鐵氧化物對磷酸鹽具有更高的親和力和選擇吸附性[7],且生物炭負載鐵氧化物的過程對提高硝酸根吸附能力作用較小[10]。
該研究通過制備吸附硝酸根能力高的麥秸活性炭,并應用響應面回歸分析方法(response surface methodology, RSM)確定吸附能力最佳時的制備條件(炭化溫度和FeCl3添加比)[12-14],麥秸活性炭的相關性質通過掃描電鏡分析、比表面積儀、紅外光譜分析、X射線衍射儀、X射線光電子能譜儀、磁學測量系統等來表征分析,研究可為農業廢棄物秸稈的綜合利用和水體硝酸根的去除提供理論基礎。
1 材料與方法
1.1 麥秸活性炭的制備
1.1.1制備方法
小麥秸稈和活性炭的物理和化學性質如表1所示,將干燥的小麥秸稈剪成長度為1 cm左右小段備用,使用FeCl3·6H2O試劑(分析純)配制FeCl3溶液。
小段秸稈加到10 mL的FeCl3溶液中,充分攪拌后浸漬20 min(混合物無溶液流出且麥秸保持濕潤);將此秸稈混合物轉入瓷坩堝內,加蓋后放入電阻爐中,升溫(50 ℃·min-1)到設定溫度并維持100 min;冷卻后用蒸餾水沖洗至濾液pH值恒定,烘箱中75 ℃干燥,即得麥秸活性炭,將其粉碎過1 mm孔徑篩備用。
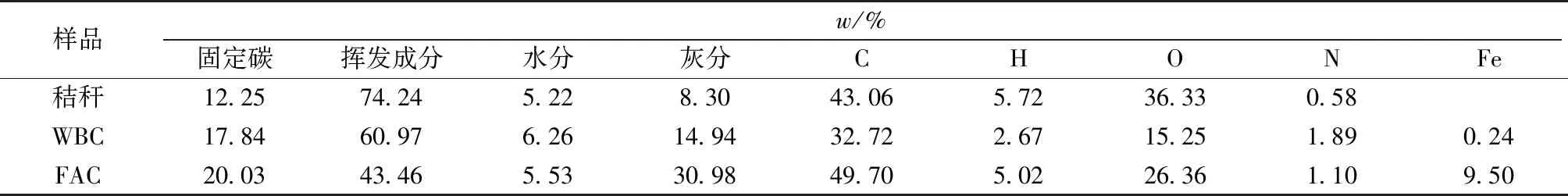
表1 秸稈和秸稈碳的物理與化學元素分析Table 1 Proximate analysis and elemental analysis of wheat straw, WBC and FAC
1.1.2麥秸活性炭吸附性能優化
采用Small Composite: Hartley Method響應面分析方法,設置炭化溫度(X1)和FeCl3添加比(X2)2個因素,制定2因素5水平實驗設計,共9個實驗,6個析因實驗,3個中心點實驗估計實驗誤差和再現性[14],以麥秸活性炭的吸附量為響應值(Y)。
通過單因素實驗,即炭化溫度和FeCl3添加比對吸附量的影響來確定中心點實驗的水平值。FeCl3添加比為72.0%時,炭化溫度為300、400、500、600和700 ℃;炭化溫度為400 ℃時FeCl3添加比為0、44.1%、72.0%、144.0%和232.3%。選擇吸附量最大的活性炭制備條件為中心點實驗水平值,吸附量通過下式計算。
qe=(C0-Ce)V/m。
(1)
式(1)中,qe為吸附平衡時的吸附量,mg·g-1;C0為初始濃度,mg·L-1;Ce為吸附平衡時的濃度,mg·L-1;V為溶液體積,L;m為炭用量,g。
最終可得麥秸活性炭的最佳制備條件,此麥秸活性炭記為FAC,相同炭化溫度下未添加FeCl3的麥秸生物炭記為WBC。
1.2 FAC和WBC的性質表征
采用元素分析儀(elementar analysen systeme GmbH, Hanau, Germany)測定FAC和WBC的C、H、O、N含量;采用鄰菲羅啉比色法測定Fe含量,波長為530 nm;采用Hitachi S-4800(Hitachi, Japan)掃描電子顯微鏡(SEM)觀察表面形態;采用全自動物理化學吸附儀(ASAP2000, Micromeritics, USA)測定FAC和WBC的比表面積和孔徑分布,孔徑分布通過Barrett-Joyner-Halenda (BJH)法測定,平均孔徑直徑由4VT/SBET計算得出;采用傅里葉變換紅外光譜儀(VERTEX 70 Bruker, Germany)掃描定性紅外光譜圖;采用AXS D8 Focus型X射線衍射儀(Bruker AXS Inc., Madison, USA)分析FAC和WBC的晶型結構;采用Escalab 250Xi型X射線光電子能譜儀(Thermo Scientific Co., USA)測定FAC和WBC的XPS譜圖;常溫下采用MPMS-3型磁學測量系統(Quantum Design, USA)測定FAC和WBC的磁滯回線;水溶液中通過Zetasizer Nano ZS90型電位儀(Malvern, England)測定FAC和WBC表面Zeta電位。
1.3 麥秸活性炭吸附實驗
1.3.1吸附量的計算
活性炭樣品0.1 g加入30 mL KNO3溶液中,pH值為7,室溫下振蕩3 h后過濾,采用酚二磺酸比色法測定過濾液氮濃度,波長420 nm,根據式(1)計算吸附量(以純氮計)。
1.3.2溶液濃度、炭用量、pH值和吸附時間對FAC吸附能力的影響
把FAC樣品0.1 g加到KNO3溶液中,使得ρ(N)分別為20、30、40、50、80、100、150和200 mg·L-1,計算不同溶液濃度下FAC吸附量;在ρ(N)為40 mg·L-1的KNO3溶液中添加0.03~1.00 g FAC,計算不同FAC添加量下的吸附量;在ρ(N)為30 mg·L-1的KNO3溶液中利用HCl或NaOH調節溶液初始pH值為2~12,隨后加入FAC樣品0.1 g,計算不同pH值條件下FAC吸附量;加入FAC樣品0.1 g到KNO3溶液中,使ρ(N)為30和50 mg·L-1,混合振蕩1、5、10、30、60、120 和180 min后過濾,計算不同吸附時間下FAC吸附量。
根據下式計算NO3-去除率。
(2)
式(2)中,R為NO3-去除率,%;C0為溶液初始濃度值,mg·L-1;Ce為吸附平衡時溶液濃度值,mg·L-1。
應用Langmuir和Freundlich吸附模型方程研究濃度對FAC吸附能力的影響及吸附行為,方程的直線形式[3]為
(3)
(4)
式(3)~(4)中,b為Langmuir吸附平衡常數,L·mg-1;Q0為Langmuir理論最大吸附量,mg·g-1;Kf和n為Freundlich常數,代表吸附劑的吸附能力和吸附強度。
利用準一級動力學(Pseudo First-Order)和準二級動力學(Pseudo Second-Order)方程擬合不同時間時的吸附量數據以明確吸附過程的控制機制,方程直線形式[3]為
(5)
(6)
式(5)~(6)中,qt為t時刻的吸附量,mg·g-1;k1為準一級模型的吸附平衡速率常數,min-1;t為反應時間,min;k2為準二級模型的吸附平衡速率常數,g·mg-1·min-1。
2 結果與討論
2.1 麥秸活性炭吸附性能優化
2.1.1溫度和FeCl3對吸附性能的影響
隨炭化溫度的升高,麥秸活性炭吸附能力先快速增加后逐漸減小,500 ℃時的麥秸活性炭吸附能力顯著大于其他溫度(P<0.05)(圖1)。溫度300 ℃時的吸附能力非常小,僅為0.27 mg·g-1。半纖維素、纖維素和木質素的初始分解溫度為300~400 ℃[15],所以300 ℃時的麥秸僅有部分炭化,孔隙發育不完全,吸附位點較少,導致吸附量小。當溫度為500 ℃時,麥秸活性炭結構穩定,孔隙結構發育完全,此時的麥秸活性炭吸附量顯著大于300和400 ℃時的吸附量(P<0.05)。但隨溫度的繼續升高,麥秸活性炭吸附能力卻顯著減小(P<0.05),可能由于活性炭發生收縮及碳結構的重排而引起孔體積和比表面積減少[16],導致吸附量減小;也可能由于FeCl3隨溫度的升高對麥秸的活化、侵蝕程度增加,部分微孔被腐蝕,破壞了孔結構[17],導致吸附能力下降。
FeCl3添加比為72.0%和144.0%時的麥秸活性炭吸附能力顯著大于其他添加比(P<0.05),隨添加比的增大吸附能力顯著減小(P<0.05),過多添加FeCl3破壞了麥秸活性炭的微孔[16],部分微孔擴張變大,導致吸附能力下降。
2.1.2最佳制備條件的確定
如圖1所示,炭化溫度和FeCl3添加比顯著影響麥秸活性炭的吸附性能,炭化溫度500 ℃及FeCl3添加比72.0%和144.0%時吸附量最大。選擇炭化溫度500 ℃和FeCl3添加比72.0%為RSM方法的中心點實驗水平值(表2)。不同麥秸活性炭的氮吸附量在0.21到5.10 mg·g-1之間(ρ為30 mg·L-1),產率在29.6%到55.7%之間。
運用SAS 9.2軟件的響應面回歸過程建立二次響應面回歸模型,該模型充分考慮炭化溫度、FeCl3添加比及其交互作用對吸附量的影響[18],擬合的二元二次方程為
Y=4.97+0.37X1+1.30X2-0.80X12-2.00X22+0.61X1X2。
(7)
該回歸模型方差分析結果如表3所示,擬合麥秸活性炭的實際制備條件較好,可用于制備條件的分析和預測。
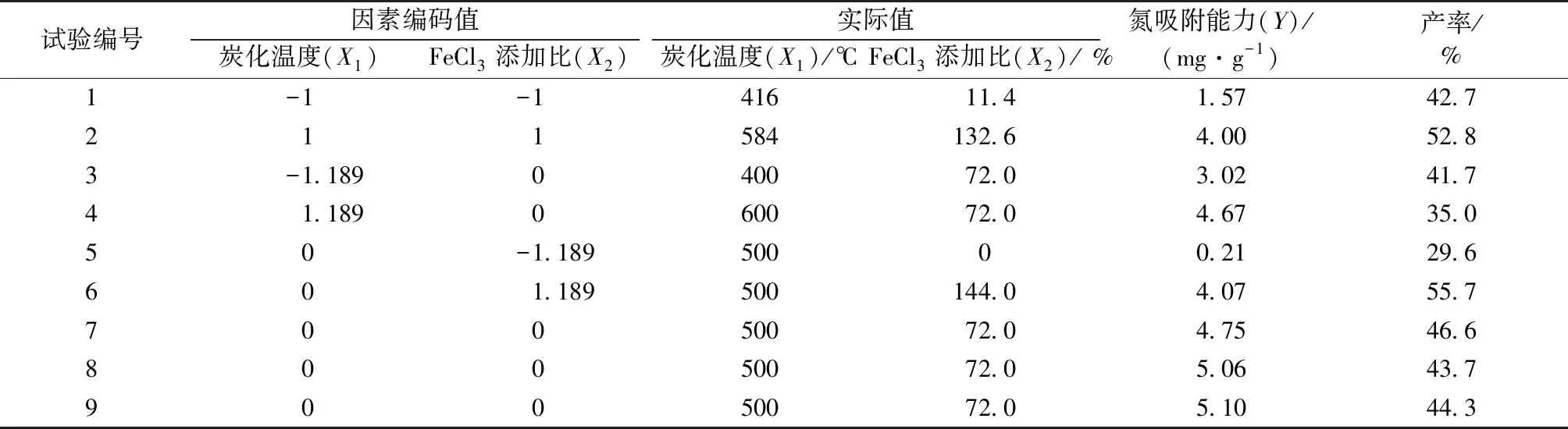
表2 實驗設計和結果Table 2 The design and results of the experiment
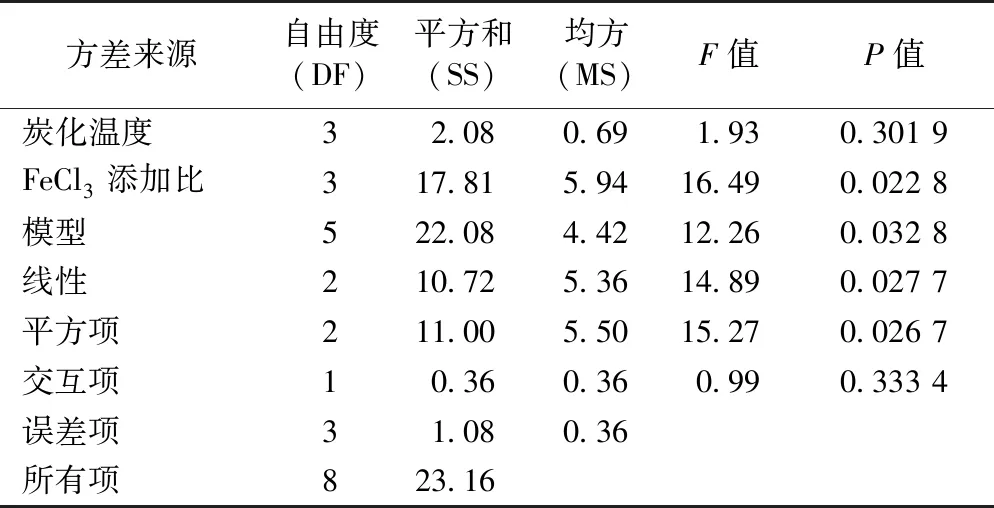
表3 回歸模型方差分析結果Table 3 Analysis of variance for regression model
由圖2可以看出,基于炭化溫度和FeCl3添加比的交互影響,圖中存在極大值點,即最佳制備條件及預測吸附量。根據回歸分析得出該點的編碼值:X1為0.319 678,X2為0.321 389,預測值為5.29,即炭化溫度527 ℃和FeCl3添加比92.5%為最佳制備條件,預測氮吸附量為5.29 mg·g-1。
2.1.3響應面分析方法預測吸附量的驗證
FAC的氮吸附量為(5.09±0.17) mg·g-1,大于WBC,與預測值僅相差3.8%,其產率也高于WBC,說明該方法設計合理,具有較好的應用性。
2.2 FAC和WBC的性質表征
2.2.1FAC和WBC的元素含量和表面形態分析
FAC中鐵和氧元素含量(9.50%)高于WBC(0.24%)(表1),說明有鐵氧化物負載到FAC的表面或孔隙中。FAC也含有更多的碳和氫元素。相應地,FAC中固定碳、揮發分和灰分含量更多。圖3為WBC和FAC掃描電鏡圖。WBC表面光滑,而FAC表面粗糙,有大量孔隙及附著物,說明由于FeCl3的活化作用,FAC形成大量孔隙,其比表面積可能大于WBC。
2.2.2FAC和WBC的結構特性和表面基團分析
FAC和WBC的吸附等溫線類型介于Ⅱ型與Ⅳ型之間(圖4)[19]。相對壓力在0~0.8之間時,吸附曲線先快速后平緩上升。相對壓力大于0.9至接近飽和時,FAC的吸附曲線上升幅度大于WBC,這主要由于FAC中VBJH大而發生更多的中孔及大孔吸附。相對壓力大于0.4時FAC解吸等溫線存在屬于B類回線的脫附滯后,反映其含有大量狹窄縫形孔[19]、大量中孔(2~50 nm)和一定量的大孔[20]。FAC和WBC的孔隙結構大部分為微孔和中孔(小于10 nm),FAC含有更大的BET比表面積和孔體積(表4)。

表4 FAC和WBC的結構特性Table 4 Textural characteristics of FAC and WBC
FAC和WBC 的紅外光譜如圖5所示。在波數為3 437和3 454 cm-1附近的吸收峰為羥基—OH基團[21],也可能是FAC樣品中針鐵礦(a-FeOOH)成分的羥基—OH基團[22]。波數為1 110和880 cm-1附近的吸收峰分別為C—OH基團的伸縮振動和羥基—OH基團的彎曲振動,880 cm-1附近的吸收峰也是FAC樣品中針鐵礦(a-FeOOH)成分羥基—OH基團的彎曲振動[22-23]。波數為460 cm-1附近的吸收峰為Si—O基團的彎曲振動[24],也是磁赤鐵礦(g-Fe2O3)及赤鐵礦(a-Fe2O3)成分Fe—O基團的伸縮振動[22]。FAC樣品中波數為557 cm-1的吸收峰是其磁鐵礦(Fe3O4)及磁赤鐵礦(g-Fe2O3)成分Fe—O基團的伸縮振動[22-23]。
FAC和WBC樣品的XRD衍射圖在2θ為20°附近都有一個弱寬衍射峰(圖6),這是樣品中所含無定形碳的衍射峰[25-26]。FAC樣品的XRD衍射圖在33.3°、35.5°、62.7°處出現了3個明顯的衍射峰,33.3°和62.7°處為赤鐵礦(a-Fe2O3)成分的晶格面,在35.5°附近的衍射峰說明FAC樣品中存在磁鐵礦(Fe3O4)(35.45°)和磁赤鐵礦(γ-Fe2O3)(35.68°)成分[27]。
FAC和WBC樣品在285和532 eV附近都出現強峰(圖7),FAC在711.3和724.5 eV處出現了弱峰,而WBC則沒有,這說明FAC和WBC表面C元素(分別為95.06%和97.63%)含量最高,FAC含有Fe元素(2.68%)。
從圖8的FAC中Fe 2p的XP5譜圖可以得出,Fe 2p3/2的峰位在711.14和713.68 eV處,711.14 eV處峰位的衛星峰在719.71 eV處;Fe 2p1/2的峰位在724.51和727.11 eV處,724.51 eV處峰位的衛星峰在733.10 eV處。有研究表明,Fe2O3中Fe 2p3/2的峰位在710.6至711.2 eV之間,而且衛星峰大約位于超過Fe 2p3/2的峰位8 eV處;Fe2SiO4中Fe2+的Fe 2p1/2的峰位在722.6 eV附近,其衛星峰大約位于超過Fe 2p1/2的峰位6 eV處;Fe3O4中Fe 2p1/2和Fe 2p3/2的峰位分別在724.07和710.56 eV處,Fe 2p3/2不存在衛星峰;針鐵礦(a-FeOOH)中Fe 2p1/2和Fe 2p3/2的峰位分別在724.98和710.48 eV處[28-29]。因此,FAC中Fe元素存在2價和3價2種價態,包含多種鐵氧化物(a-FeOOH、Fe2O3、Fe3O4)成分。
2.2.3FAC和WBC的磁性分析
FAC的磁化強度(M)隨外加磁場強度的增大而趨于飽和,反向施加也趨于飽和(圖9)。FAC的磁滯回線近似為“S”型回線,而WBC的磁滯回線接近為一條直線,這說明FAC具有良好的超順磁性[30],矯頑力低,移除外加磁場后,其磁化強度趨于0[31](圖9),而WBC不帶磁性。根據FAC的磁滯回線,其飽和磁化強度為4.12 emu·g-1。被外加磁場作用10 s后,分散在水溶液中的FAC被吸附在另一側,說明其具有良好的磁響應性,可利用磁選方式分離。
2.3 FAC的吸附實驗
2.3.1溶液初始濃度的影響
隨溶液初始氮濃度的增大,FAC的吸附量快速增加(圖10),當初始氮濃度(C0)為200 mg·L-1時,吸附后溶液氮濃度(Ce)為152 mg·L-1,氮吸附量為13.32 mg·g-1。由式(3)和(4)擬合數據,R2為0.961和0.948,b為0.036,Q0為14.68 mg·g-1(以NO3-計為65.01 mg·g-1);Kf為2.43,n為3.11,說明該吸附過程是易于進行的[3]。
2.3.2FAC添加量的影響
隨FAC添加量從1.53增加到14.00 g·L-1,硝酸根去除率從28%增加到89%,說明吸附位點和面積隨FAC量的增加而增加[4],導致去除率增加,但吸附量從7.27下降到2.55 mg·g-1。當添加量大于14.00 g·L-1時,FAC的增多造成顆粒的聚集和吸附位點的重疊[32],有效吸附面積沒有顯著增加,去除率保持在90%左右。
2.3.3溶液pH值的影響
在低pH值條件下FAC容易形成質子化表面,其帶正電荷的表面吸附位點多于高pH值條件[4]。FAC吸附量隨pH值為2.84時的5.34 mg·g-1快速下降至pH值為12.01時的0.74 mg·g-1。FAC表面帶正電荷的吸附位點數量并沒有因初始pH值的升高而快速下降,仍有吸附發生。吸附平衡后溶液pH值較初始值有所下降,當初始pH值升高至11.6和12.01時,平衡后pH值降為7.75和10.58,此時FAC表面負電荷數量多于正電荷數量,吸附量快速減少。
2.3.4吸附時間的影響
在吸附開始時段吸附量迅速增加,而后隨吸附過程的進行趨向穩定,120 min時達到吸附平衡,此時吸附量分別為4.40和5.30 mg·g-1(初始濃度為30和50 mg·L-1)。利用式(5)和(6)擬合數據(表5),初始吸附速率h01=k1qe,h02=k2qe2[21]。FAC吸附的準二級動力學模型的R2為0.999,大于準一級動力學方程,且h02大于h01,因此準二級動力學模型更真實、全面地反映該吸附過程[33]。
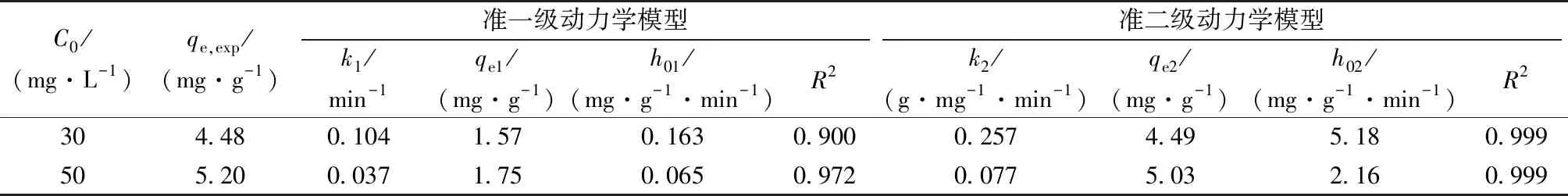
表5 FAC吸附氮的準一級動力學模型和準二級動力學模型參數Table 5 Constants of the pseudo first- and second-order models for nitrate adsorption onto FAC
2.4 FAC吸附作用討論
FAC所含的多種鐵氧化物成分的形成可用下式來描述[34]:Fe3++3H2O→Fe(OH)3+3H+,炭化溫度≤350 ℃;Fe(OH)3→FeOOH→Fe2O3, 炭化溫度≤400 ℃;3Fe2O3+C(CO)→2Fe3O4+CO(CO2),500 ℃≤炭化溫度≤700 ℃。
而FAC吸附過程又符合準二級動力學模型,說明該吸附過程也存在化學吸附過程,且為主要控速步驟[35],形成內層配合物[6]。水溶液中Fe3+具有明顯的水解性,易發生逐級水解。
因此,溶液中FAC表面也發生類似水解[12]。所以,隨溶液pH值的升高,FAC所含[C—Fe(OH2)5](s)3+轉變為[C—Fe(OH2)4(OH)](s)2+、[C—Fe(OH2)3(OH)2](s)+和H3O+,這將導致其吸附能力逐漸下降和吸附平衡后溶液pH值下降。
LIU等[9]也應用FeCl3溶液為活化劑制備了負載Fe3O4松木鋸末活性炭,其對砷酸鹽的吸附能力(204.2 mg·g-1)遠高于未負載Fe3O4活性炭(43.7 mg·g-1)。OLIVEIRA等[11]應用FeCl3溶液為活化劑在較低溫度下(280 ℃)制備了咖啡殼活性炭,其具有高比表面積(965 m2·g-1)、更小孔徑和高染料及苯酚吸附能力。WANG[36]應用含Fe3+的鹽酸酸洗廢液制備了具有高比表面積和高亞甲藍吸附能力的花生殼活性炭。可見,利用各類生物質原材料經FeCl3活化制備的活性炭都有較好的吸附能力,適用于水體中污染物的去除。
WBC表面含有大量負電荷,水溶液中與硝酸根離子產生靜電互斥,導致其吸附能力遠低于FAC。FAC含有多種鐵氧化物成分、更大比表面積和孔體積,吸附能力也高于改性麥秸生物炭[12]和改性水生植物生物炭[37],是一種高效的、原材料來源廣泛的陰離子吸附劑。
3 結論
(1)利用FeCl3的活化作用,制得負載鐵氧化物麥秸活性炭,并應用響應面回歸分析方法明確了吸附硝酸根能力最佳時的制備條件,即炭化溫度527 ℃和FeCl3添加比92.5%(FeCl3/麥秸量)。
(2)最佳制備條件下的麥秸活性炭中鐵元素含量(9.50%)、比表面積(243.50 m2·g-1)和孔隙體積(0.174 cm3·g-1)都大于同溫度下未加FeCl3制備的麥秸生物炭;其對N2的吸附等溫線類型介于Ⅱ型與Ⅳ型之間,有屬于B類回線的脫附滯后,含有大量狹窄的縫形孔;負載多種鐵氧化物(針鐵礦、赤鐵礦、磁赤鐵礦、磁鐵礦)成分。
(3)最佳麥秸活性炭的Langmuir理論最大氮吸附量為14.68 mg·g-1(以NO3-計為65.01 mg·g-1);當炭用量大于14.00 g·L-1時,溶液中硝酸根去除率保持在90%左右;吸附量隨溶液pH值的升高而降低;吸附硝酸根過程符合準二級動力學模型。
(4)最佳麥秸活性炭的飽和磁化強度為4.12 emu·g-1,具有良好磁響應性,水體中應用磁選方式能方便快捷地分離該吸附劑(包含硝酸根),為改善生態環境(廢棄物利用和水體污染物去除)提供方法。

