妊娠期牙周臨床指標和齦溝液生物標記物與早產相關性的巢式病例對照研究
葉嬋娟 吳敏 陳少武 楊秀巧 李蕙君 朱素君 周方明 郝穎
1.南方醫科大學附屬深圳婦幼保健院口腔病防治中心,深圳518048;2.南方醫科大學附屬深圳婦幼保健院婦產科,深圳518048;3.南方醫科大學附屬深圳婦幼保健院檢驗科,深圳518048
牙周病是以牙菌斑為始動因素的牙周組織慢性炎癥性疾病,局部免疫反應產生大量的炎癥介質是主要的致病機制[1]。近20 年來,牙周炎癥作為早產(preterm birth,PTB)的一種可能的危險因素受到學者的關注[2]。早產指妊娠滿28 周至不足37 周的分娩,占分娩總數的5%~18%,是新生兒死亡和發病的首要原因[3],其機制可能是胎兒胎盤系統炎癥介質升高,提前達到子宮激活的閾值,從而觸發過早分娩。但目前預測方法不確定。
體內氧壓力升高與牙周疾病以及早產等妊娠不良結局相關。8-羥基-2-脫氧鳥苷(8-hydroxy-2-deoxyguanosine,8-OHdG)是一種新型的氧壓力生物標志物[4]。
本研究采用巢式病例對照研究(nested casecontrol study,NCCS),檢測妊娠婦女的牙周臨床指標和齦溝液(gingival crevicular fliud,GCF)生物標記物,包括白細胞介素(interleukin,IL)-1β、IL-6、腫瘤壞死因子α (tumor necrosis factor-α,TNF-α)、前列腺素E2(prostaglandin E2,PGE2)和8-OHdG,并隨訪妊娠結局,探討妊娠各期牙周臨床指標和GCF生物標記物水平與早產的相關性,評價何種指標有預測早產的可能。
1 材料和方法
1.1 研究對象
選取2017 年1 月—2018 年5 月期間于深圳市婦幼保健院產檢的405例孕婦為研究對象。納入標準:年齡20~40 歲,妊娠36 周以內,無系統性疾病史。排除標準:1)早產史、家族史、多胎妊娠、病理妊娠、妊娠合并癥或妊娠并發癥;2)精神壓力和工作壓力過大等[5];3)吸煙、酗酒等不良嗜好;4)3 個月內服用過抗菌素;5)6 個月內做過牙周治療;6)拒絕隨訪者。參加本研究的婦女簽署書面知情同意書。
1.2 分組
1.2.1 孕周分期 根據納入時孕周分成4 期,分別為孕早期(9~12周)、孕中早期(13~23周)、孕中后期(24~28周)、孕后期(29~36周)。
1.2.2 分娩結局分組 早產組:分娩周數滿28周至不足37 周;足月(full term birth,FTB)組:分娩周數超過37周。
1.2.3 巢式對照組 為了控制混雜因素的影響,使早產組和足月組的年齡、身體質量指數(body mass index,BMI)、職業狀況等基線資料均衡可比,每組中按1∶4 匹配選擇足月產者組成巢式對照組。
1.3 研究方法
1.3.1 問卷調查 包括人口學構成特征(年齡、文化程度、職業等)、口腔衛生習慣(每天刷牙次數、刷牙方式、牙線使用)及自評牙周炎癥癥狀,并進行口腔衛生指導。
1.3.2 牙周檢查 每個牙檢查頰(唇)和舌面遠中、中央、近中6 個位點。記錄牙齦指數(gingival index,GI)、牙周探診深度(probing depth,PD)和出血指數(bleeding index,BI)。
1.3.3 GCF 的采集和洗提 采用袋內法在牙周檢查前采集。采集前囑孕婦漱口,每位孕婦取口內雙側上頜第一和第二前磨牙的近頰位點[6]。收集前先用無菌棉球拭干牙面和牙齦,隔濕,將消毒紙尖插入齦緣下直至有輕微阻力,留置30 s 后取出,有血則棄之,重新選牙。將4個紙尖集中放在一個EP 管中密封,置于-80 ℃低溫冰箱中凍存待查[6]。然后從冰箱中取出裝有紙尖的EP管,加入1%PBS,靜置1 h后,4 ℃下10 000 r·min-1離心10 min,取上清液待測[6]。采用酶聯免疫吸附測定法(enzyme linked immunosorbent assay,ELISA)檢測,使用人PGE2、IL-1β、IL-6、TNF-α 和8-OHDG 試 劑盒,嚴格按照說明書的步驟進行操作,在酶標儀上讀取450 nm 波長下的光密度(optical density,OD)值,繪制標準曲線,得出相應濃度。
1.3.4 隨訪并記錄妊娠結局 滿28 周至不足37 周為早產,滿37周以后為足月。
1.4 統計學處理
采用SPSS 20.0 統計軟件進行分析,計量資料以均數±標準差表示,計數資料以頻數(百分比)表示。連續變量2 組間比較采用t檢驗;分類變量組間比較采用卡方檢驗;對于單因素分析P<0.05的指標采取Logistic 回歸分析早產的危險因素;繪制接受者操作特性曲線(receiver operating characteristic curve,ROC),計算ROC 曲線下面積評估指標的診斷準確性;Pearson 相關分析評估牙周指標與GCF 生物標記物水平的相關性;P<0.05 表示差異有統計學意義。
2 結果
2.1 一般情況
本研究初始納入405例孕婦,排除早產史、精神緊張、妊娠并發癥等已知的早產危險因素,最終納入300 例孕婦。其中足月組281 人,早產組19人,早產占6.3%。2組間分娩周數有顯著差異(P<0.01)。在2 組研究人群的人口學特征、口腔衛生習慣及自評牙周炎癥狀比較中,早產組無業者偏多(P<0.01),其他項目均未見明顯差異(P>0.05)(表1)。
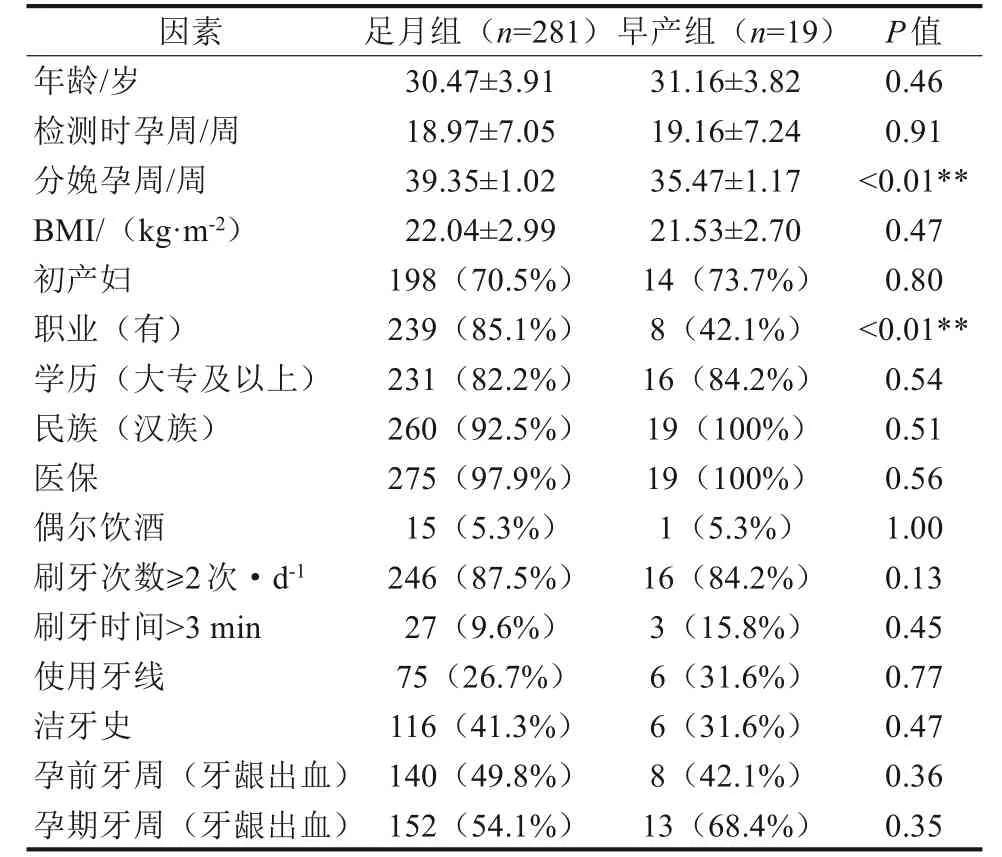
表1 早產組與足月組一般情況的比較Tab 1 Comparison of general conditions of PTB and FTB
2.2 不同孕期婦女牙周指標和GCF 生物標記物水平的比較
孕9~12 周(77 人,早產5 人,足月產72 人)、13~23周(128人,早產6人,足月產122人)、24~28 周(64 人,早產7 人,足月產57 人)、29~36 周(31 人,早產1 人,足月產30 人)。按年齡、BMI、職業狀況等基線資料,每組早產人數按1∶4 匹配巢式對照組。僅在孕24~28 周中,早產組的GI、BI 和8-OHdG 顯著高于巢式對照組(P<0.05)(表2~4)。
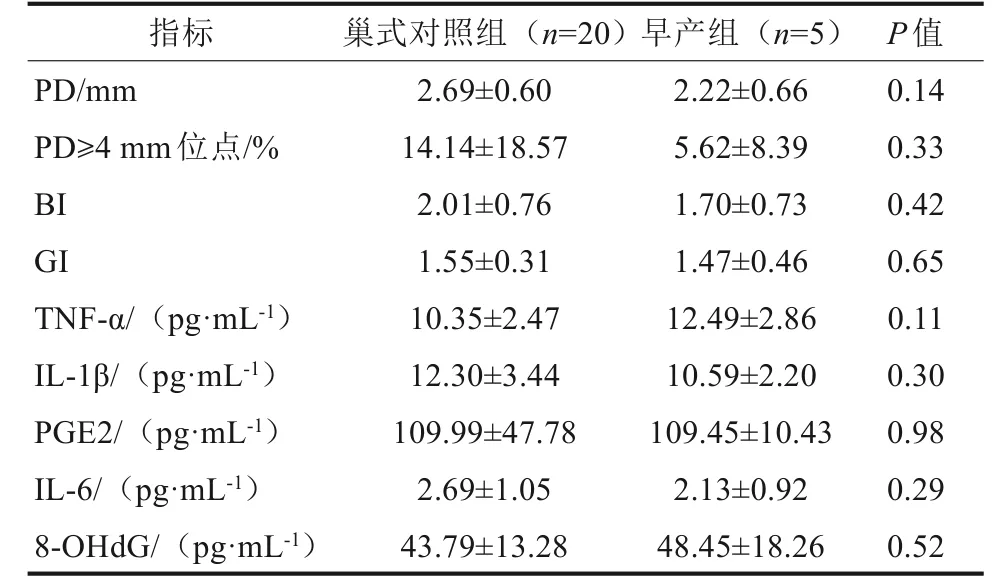
表2 孕9~12 周早產組與足月組牙周指標和GCF 生物標記物水平的比較Tab 2 Comparison of periodontal indexes and biomarkers in GCF of PTB and FTB at 9-12 gestational weeks

表3 孕13~23 周早產組和足月組牙周指標和GCF 生物標記物水平的比較Tab 3 Comparison of periodontal indexes and biomarkers in GCF of PTB and FTB at 13-23 gestational weeks
2.3 早產的危險因素Logistic回歸分析
將妊娠24~28 周GI、BI、8-OHdG(單因素分析P<0.05的指標)納入逐步Logistic回歸模型,以妊娠結局為因變量,BI和8-OHdG是早產的危險因素(OR=5.90,P=0.034,95%可信區間:1.139~30.554;OR=1.18,P=0.045,95%可信區間:1.003~1.384)。

表4 孕24~28 周早產組和足月組牙周指標和GCF 生物標記物水平的比較Tab 4 Comparison of periodontal indexes and biomarkers in GCF of PTB and FTB at 24-28 gestational weeks
2.4 孕9~36 周牙周指標與GCF 生物標記物水平的相關性分析
PD與PD≥4 mm 位點、BI、GI 呈正相關(r>0.6,P<0.05);在牙周指標與GCF 生物標記物水平之間,未見明顯相關性(P>0.05)(表5)。

表5 孕9~36 周牙周指標與GCF 生物標記物的相關性分析Tab 5 Correlation analysis of periodontal indexes and biomarkers in GCF on pregnant women at 9-36 gestational weeks
2.5 BI 和8-OHdG 水平聯合檢測的ROC 曲線分析結果
以妊娠結局為金標準,將妊娠24~28周早產組7 例及巢式對照組28 例BI、8-OHdG 水平的結果,繪制成ROC 曲線。BI 在ROC 曲線下面積為0.80,95%可信區間為0.435~0.948,8-OHdG水平在ROC曲線下面積為0.69,95%可信區間為0.647~0.950。以BI、8-OHdG 水平為自變量,建立Logistic 回歸模型,通過模型中的概率值來擬合聯合檢測的ROC 曲線。聯合檢測的ROC 曲線下面積為0.82,95%可信區間為0.592~1.000,聯合檢測的ROC 曲線下面積均大于BI、8-OHdG單項檢測,但差異無統計學意義(P>0.05)。聯合檢測BI 閾值為1.86,8-OHdG 的閾值為33.87 pg·mL-1。根據臨界值得出聯合預測時的敏感度、特異性、準確度分別為85.7%、64.3%、68.6%(表6、圖1)。

表6 BI 和8-OHdG 水平聯合檢測的ROC 曲線分析結果Tab 6 ROC curve of combined detection of BI and 8-OHdG levels
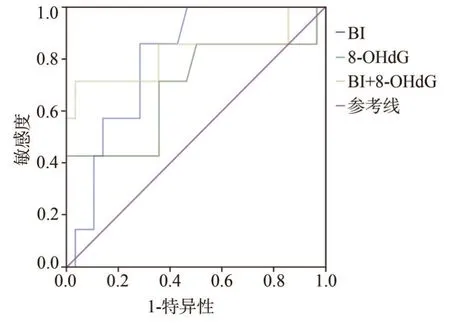
圖1 BI和8-OHdG水平單獨和聯合檢測的ROC曲線Fig 1 ROC curve of alone and combined detection of BI and 8-OHdG levels
3 討論
NCCS是指收集某一隊列成員的基線資料和生物學標本后,隨訪一定時間,把發生疾病的全部人群作為病例組,按一定匹配條件和比例隨機抽取該隊列中未發病人群組成巢式對照組,按照病例—對照研究方法進行統計分析[7]。
考慮孕期性激素水平可能對牙周臨床指標和炎癥介質的影響,將納入的300名孕婦根據孕周進行分組并比較。結果顯示,僅在孕24~28周時,早產組的GI、BI和8-OHdG顯著高于巢式對照組(P<0.05),同時BI和8-OHdG升高是早產的危險因素。根據NCCS 的特點,牙周炎癥和GCF 生物標記物水平升高在早產發生之前,提示與早產的發生相關。通過ROC 曲線,發現BI 和8-OHdG 聯合檢測的ROC 曲線下面積大于單項檢測,盡管差異無顯著性,但提示二者聯合檢測可能對早產的預測有一定價值。聯合檢測時BI的閾值為1.86,8-OHdG的閾值為33.87 pg·mL-1,其陽性預測值和準確度都比單獨檢測8-OHdG 水平高,但低于單獨檢測BI。因此8-OHdG對早產的預測作用,今后將擴大樣本量或增加其他指標來探討。
BI 能比較客觀地反映牙齦和牙周袋內壁的炎癥情況,有較高的特異性,是牙周炎癥處于活動期的敏感標志[8]。Bieri等[9]的縱向研究中也發現在未得到任何牙周治療的情況下,即使PD、GCF炎癥因子水平無顯著性改變,探診出血(bleeding on probing,BOP)在產后4~6周顯著下降。
Tarannum等[10]在隊列研究中,納入了22 名妊娠28~32 周患有中度牙周炎的孕婦,發現早產組GCF-PGE2 比足月組略高,但差異無統計學意義,因此并未得出GCF-PGE2 是早產預測因子的結論。與本研究結果不同,可能和納入對象牙周炎癥狀況和納入時間不同有關。
評估妊娠期牙周炎癥狀況的困難主要是缺乏X線片的依據[9],本研究采用GI、BI 和PD 來判斷牙周炎癥狀況。而沒有記錄菌斑指數(plaque index,PLI) 和臨床附著喪失(clinical attachment loss,CAL)。未記錄PLI 的原因為:早在20 世紀60 年代,有學者提出妊娠期牙齦炎的嚴重程度會增加,但和菌斑聚集量不成比例[11],后來大部分研究也支持這個觀點[12];筆者[13]前期研究也發現即使PLI 控制在較低水平時,GI、BI 仍隨著孕期發展顯著升高。而未記錄CAL 的原因是:孕婦檢查時未潔治可能影響CAL 的檢測[14]。CAL 反映既往牙周破壞程度,不代表當前的牙周炎癥程度[15]。研究[16]表明在缺少CAL 時,PD 的增加是牙周炎的早期體征。另外,本研究樣本量大,調查對象為孕婦,為了研究的順利進行,縮短檢查時間也是必要的[17]。
本研究沒有發現9~12 周、13~23 周就診孕婦在早產與足月組之間檢測指標的明顯差異,可能與孕期的激素水平有關。Abuelghar等[18]發現24~28周唾液孕酮水平對早產有一定的預測意義,認為16~20周唾液中孕激素水平并不能代表生產發生前的變化,因為后期在早產發生前激素水平的變化會更大。有研究[19]發現與孕早期(8~12 周)和產后6~8 周相比,孕中期(24~28 周)炎癥因子與孕早期持平,可較好維持胎兒的生長,該時期的炎癥感染和任何持續的促炎信號將引起流產或早產。提示孕中期(24~28 周)炎癥因子處于穩定狀態,對炎癥反應的增加更敏感。因此,24~28周可能是生物標記物變化的敏感時期。
在整個孕期牙周指標與GCF 生物標記物的相關性分析中,沒有發現明顯的相關性。Bieri等[9]也發現孕期BOP 與GCF 中IL-1β、TNF-α 等細胞因子沒有相關性,妊娠時期的GCF 炎癥介質水平,除了受細菌引起的局部炎癥和宿主免疫反應影響外[10],妊娠時期的激素水平和免疫抑制也起了作用[20]。此外,還與研究中納入對象的牙周炎癥狀況較好有關[9-10],本研究早產組與足月組孕婦PD平均值均小于3 mm。
綜上所述,本研究探討了不同妊娠階段牙周指標和GCF 中炎癥介質水平與早產的關系。妊娠24~28 周BI 和8-OHdG 水平升高是早產的危險因素,二者聯合檢測可能對早產的預測有一定的價值,但需要進一步擴大樣本的研究來探討,從而建立牙周病患者早產預警體系。
利益沖突聲明:作者聲明本文無利益沖突。

