鉀改性CuZnAl催化仲丁醇脫氫制甲乙酮
李 鵬,戴詠川,苑興洲,王彥娟,張 健
(遼寧石油化工大學 石油化工學院,遼寧 撫順 113001)
甲乙酮(MEK)因溶解性好、穩定性高、低毒等優點,常被應用于洗滌劑、黏合劑、煉油和制藥等領域[1],是一種應用廣泛的工業溶劑。目前,MEK生產工藝主要有仲丁醇(SBA)氣相脫氫法、正丁烷液相氧化法和正丁烷直接氧化法[2]。其中,SBA脫氫法因具有SBA轉化率高、MEK選擇性好、產物分離方便等優點而備受關注[3]。
銅系催化劑作為醇脫氫催化劑被較多地應用于工業領域[4],其中,Cu/SiO2和CuZnAl催化劑因具有脫氫反應溫度低、活性好等優點被廣泛用于醇脫氫反應中[5]。Zhu等[6]采用浸漬法和離子交換法制備了Cu/SiO2催化劑,催化劑上的CuO可被還原,且SBA脫氫活性穩定。Liu等[7]采用共沉淀法制備了不同摩爾比的CuZnAl催化劑,并應用于環己醇脫氫反應中,催化劑的最佳配比為n(Cu)∶n(Zn)∶n(Al)=1.34∶0.66∶1.0。Jiang等[8]考察了Cu/Zn摩爾比為1時CuZnAl催化劑對SBA脫氫反應的影響,實驗結果表明,在常壓、240 ℃、空速為17.5 h-1條件下,SBA轉化率為80.54%、MEK收率為76.04%。程淑艷等[9]研究發現,堿金屬或堿土金屬(Li,K,Na,Cs,Rb)作為CuZnAl催化劑的助劑可以提高Cu組分的分散度,從而提高催化劑的性能。
本工作采用共沉淀法制備了CuZnAl催化劑,并通過浸漬法引入K,制備了不同K含量的改性CuZnAl(K-CuZnAl)催化劑,將該系列催化劑應用于SBA脫氫制MEK反應中,研究了K含量對催化劑結構和性能的影響,并對SBA脫氫反應條件進行考察。
1 實驗部分
1.1 催化劑的制備
采用共沉淀法制備CuZnAl催化劑:以硝酸銅、硝酸鋅和硝酸鋁為原料,按一定配比混合成鹽溶液,以碳酸鈉水溶液作為沉淀劑,先采用并流法在80℃中性條件下進行沉淀;然后將沉淀后的母液陳化6 h,經過濾、洗滌后,在100 ℃下干燥8 h;最后在500 ℃下焙燒4 h,即得CuZnAl催化劑,其中,CuO,ZnO,Al2O3的質量分數分別為45%,45%,10%。
采用浸漬法制備K-CuZnAl催化劑:配制一定濃度硝酸鉀溶液,滴加到CuZnAl催化劑上,在室溫下攪拌12 h后于100 ℃下干燥8 h。干燥結束后在500 ℃下焙燒4 h,即制得K-CuZnAl催化劑,記作x%K-CuZnAl(x%為催化劑中K2O的質量分數)。
1.2 催化劑的表征
采用美國康塔儀器公司TPD/TDR-Pulsar型全自動動態化學吸附分析儀對催化劑進行H2-TPR的表征。首先在高純He氣流中以10 ℃/min的升溫速率由50 ℃升至150 ℃,并保持30 min進行預處理,溫度降為50 ℃后,切換成H2(5%(φ))/N2(95%(φ))混合氣并以10 ℃/min的升溫速率升溫至800 ℃。
采用日本島津公司XRD-7000型X射線衍射儀對催化劑進行晶相結構分析。CuKα輻射源,管電流30 mA,管電壓40 kV,掃描速率8( °)/min。
采用日本日立公司SU8010型場發射掃描電子顯微鏡對催化劑進行SEM表征,加速電壓20 kV。
采用美國儀器公司Microscales ASAP 2010型物理吸附儀對催化劑進行N2吸附-脫附表征,測試前先在200 ℃下脫氣5 h,然后采用低溫(-196℃)N2吸附法測定,采用BET方法計算試樣的比表面積,采用BJH方法計算平均孔徑。
采用日本UlVAC-PHI公司PHI 5000 VersaProbe型電子能譜儀進行XPS表征。
1.3 催化劑性能評價
在威瑞科教儀器有限公司MY-DTT型固定床反應器中考察了催化劑對SBA脫氫反應的性能,反應在內徑為10 mm的不銹鋼微型反應器中進行。稱取1 g待評價催化劑(20~40目)和2 g石英砂(20~40目)于反應器的恒溫區中;催化劑床層上、下兩段均由石英砂填充。在活性評價前需對催化劑進行還原,以5 ℃/min的升溫速率將反應管溫度由室溫升至260 ℃,在氫氣(10%(φ))和氮氣(90%(φ))混合氣氛下對催化劑進行4 h的還原,之后持續通入氮氣冷卻至反應溫度。以恒流泵將原料SBA注入到反應器中,在常壓、反應溫度為220 ~260 ℃、液態空速(LHSV)為2.5 ~4.5 h-1的反應條件下,通過考察SBA轉化率、MEK選擇性和MEK收率評價催化劑的性能。每個溫度點穩定3 h,放空后進行取樣,利用北京北風三譜公司3420A型氣相色譜對催化劑進行分析,毛細管色譜柱為KB-INNOWax色譜柱,柱長為30 m,柱徑為320 μm,FID檢測,升溫程序:60 ℃保持6 min,然后以10 ℃/min的升溫速率升至220 ℃,保持10 min。
2 結果與討論
2.1 催化劑的表征結果
2.1.1 H2-TPR表征結果
圖1為K改性前后CuZnAl催化劑的H2-TPR譜圖。從圖1可看出,催化劑在250~350 ℃處均出現明顯的還原峰,為高分散的CuO和Cu2O還原峰[10],且所有還原峰均表現出不對稱的拖尾狀態,這說明可還原物是多價態的。與CuZnAl催化劑比較發現,K改性后,CuO還原峰的中心位置向高溫方向偏移,這是由于焙燒過程中形成的K2O覆蓋在催化劑表面,阻礙了催化劑表面CuO與H2的接觸,使CuO需要得到較高的溫度才能夠被還原[9]。此外,相比于CuZnAl催化劑的還原峰面積,K改性后的K-CuZnAl催化劑的還原峰面積有所提高。這說明K的引入提高了催化劑的氫耗量,即經過還原后可以得到更多的活性組分Cu0[11],同時K的供電子作用也增加了催化劑表面的電荷密度,促進了CuO的還原[12]。不同K含量的KCuZnAl催化劑耗氫量大小順序為:2%K-CuZnAl(4.13 mmol/g)>4%K-CuZnAl(3.92 mmol/g)>8%K-CuZnAl(3.88 mmol/g)>1%K-CuZnAl(2.60 mmol/g)>CuZnAl(2.03 mmol/g),這 說 明K2O含量為2%(w)的CuZnAl催化劑經過還原后得到的Cu0含量最多,適量K的引入可以提高CuZnAl催化劑的還原溫度,增加還原氫耗量,從而提高催化劑的催化活性。

圖1 K改性前后CuZnAl催化劑的H2-TPR譜圖Fig.1 H2-TPR patterns of CuZnAl catalyst before and after K modification.
2.1.2 XRD表征結果
圖2為K改性前后CuZnAl催化劑的XRD譜圖。從圖2可看出,催化劑在2θ=35.5°,38.7°,48.8°處出現了CuO的特征衍射峰;在2θ=36.52°,61.46°處出現了Cu2O的特征衍射峰;在2θ=32.8°,34.3°處出現了ZnO的特征衍射峰。譜圖中沒有出現Al2O3和K2O的特征衍射峰,說明二者是以非晶態形式或高度分散形式存在于催化劑表面[13]。ZnO的存在可以使Cu物種很好地分散在催化劑表面,且可以與Cu物種形成特殊的固溶體[14],從而提高了活性組分的分散度。相比于CuZnAl催化劑,K-CuZnAl催化劑特征峰的半峰寬明顯減小,說明K改性增大了CuO、Cu2O和ZnO的晶體尺寸。從圖2還可發現,K-CuZnAl催化劑在2θ=67°附近出現了尖晶石型CuAl2O4納米晶的特征衍射峰,該物質的存在可以提高CuZnAl催化劑的耐熱穩定性[15],從而有效降低催化劑在高溫條件下的失活機率。
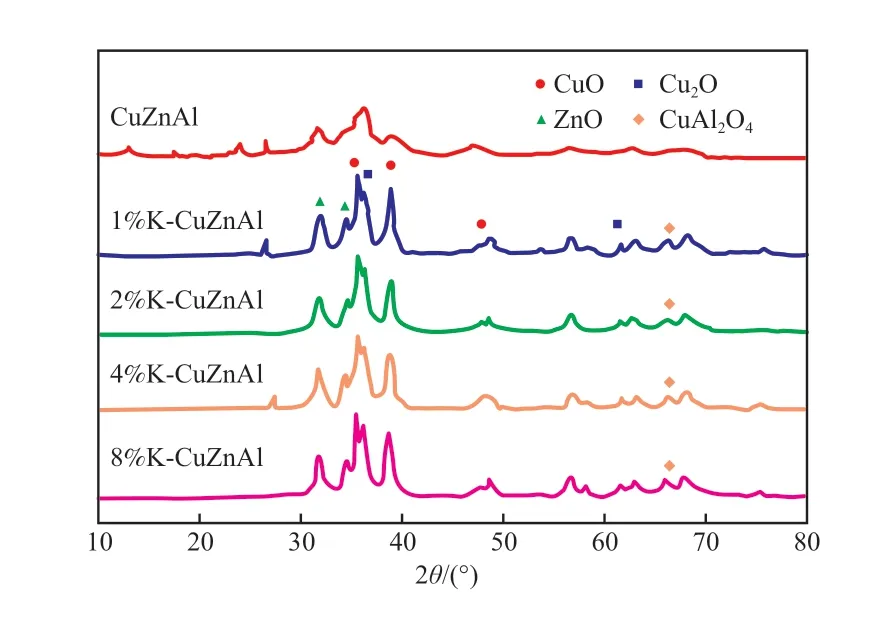
圖2 K改性前后CuZnAl催化劑的XRD譜圖Fig.2 XRD patterns of CuZnAl catalyst before and after K modification.
2.1.3 SEM表征結果
圖3為CuZnAl催化劑和2%K-CuZnAl催化劑的SEM照片。從圖3可看出,CuZnAl催化劑表面呈現出塊狀結構并存在一定的團聚,聚集現象明顯。2%K-CuZnAl催化劑表面存在大量尖晶狀結構,結合XRD表征結果可以判斷為類尖晶石型CuAl2O4納米晶,生成原因可能是由于CuZnAl焙燒時分解析出一定量的納米Cu,該結構的存在極大地改善了催化劑的耐熱性。從圖3還可看出,引入K元素后,催化劑的結構更加蓬松,提高了活性組分的分散程度,增大了催化劑與反應物料的接觸面積[16]。
2.1.4 N2吸附-脫附表征結果
圖4為CuZnAl催化劑和2%K-CuZnAl催化劑的N2吸附-脫附等溫線。從圖4可看出,K改性前后CuZnAl催化劑的吸附-脫附等溫線為具有H3滯后環特征的Ⅳ型等溫線,表明催化劑表面孔結構類型主要是由粒子堆積產生的狹縫孔。
表1為K改性前后CuZnAl催化劑的結構參數。從表1可知,K的引入提高了催化劑的比表面積,且對CuZnAl催化劑的孔道也進行了修飾,增加了催化劑的孔體積和平均孔徑。較大的孔體積和孔徑有利于反應物在活性中心表面上的擴散,從而有效提高催化劑的活性。
2.1.5 XPS表征結果
圖5為CuZnAl催化劑和2%K-CuZnAl催化劑的Cu 2p的XPS譜圖。

A,B CuZnAl;C,D 2%K-CuZnAl
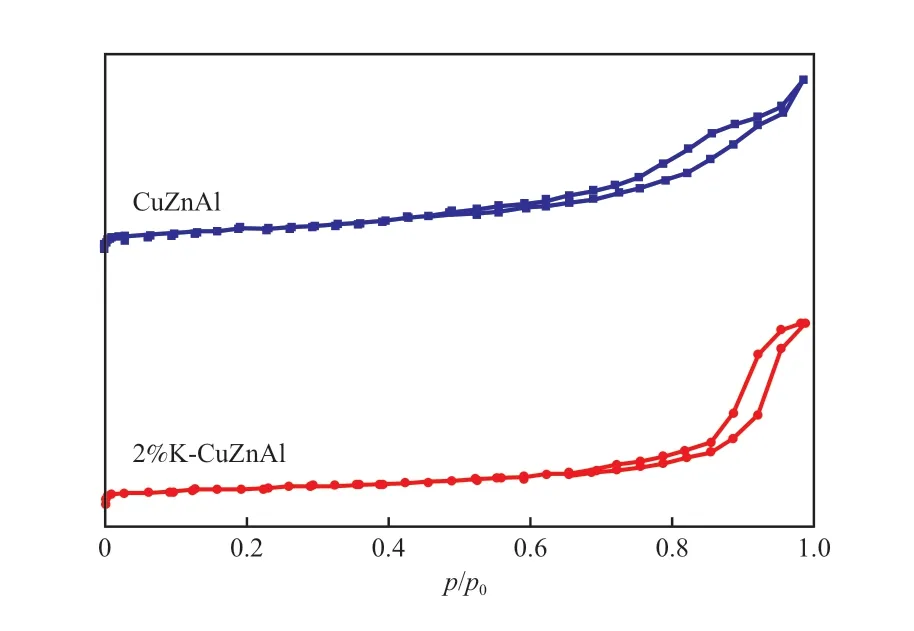
圖4 CuZnAl和2%K-CuZnAl催化劑的N2吸附-脫附等溫線Fig.4 N2 adsorption-desorption isotherms of CuZnAl and 2%K-CuZnAl catalysts.

表1 CuZnAl和2%K-CuZnAl催化劑的結構參數Table 1 Texture parameters of CuZnAl and 2%K-CuZnAl catalysts
從圖5可看出,CuZnAl催化劑表面的Cu物種有兩種價態,其中,高結合能934.0 eV對應Cu2+,可將其歸屬于CuO;而低結合能931.5 eV對應低價態的Cu+,可將其歸屬于Cu2O[17]。譜圖中940~945 eV之間出現的衛星峰說明催化劑表面存在的可還原物質是多態的[18],這與H2-TPR和XRD表征結果相一致。根據XPS表征數據可知,相比于CuZnAl催化劑,2%K-CuZnAl催化劑表面的Cu+與Cu2+的摩爾比增加(從1.2增至1.5)。Cu2O不同于CuO,由于吉布斯自由能較低,Cu2O難以和氧化鋁發生反應,與載體的相互作用也比較弱,所以在高溫下狀態比較穩定,因此進入氧化鋁晶體結構中的銅物種較少,進而銅的分散度得以提升[10]。結合H2-TPR表征結果可知,表面Cu2O量和耗氫量的增加可以提高可還原Cu物種的含量,即K的引入有助于催化劑的還原,促使還原后活性組分含量增加。

圖5 CuZnAl和2%K-CuZnAl催化劑的XPS譜圖Fig.5 XPS patterns of CuZnAl and 2%K-CuZnAl catalysts.
2.2 催化劑的性能評價結果
2.2.1 K含量的影響
圖6為不同K含量CuZnAl催化劑在SBA脫氫生成MEK反應中的催化性能。從圖6可看出,當K2O含量為2%(w)時,催化劑對SBA脫氫生成MEK的催化性能最佳,SBA脫氫轉化率和MEK收率分別為83.5%和78.1%,此時MEK選擇性為93.5%。當K2O含量大于2%(w)時,SBA轉化率和MEK收率降低。結合H2-TPR和XRD表征結果可知,當K2O含量為2%(w)時,K-CuZnAl催化劑通過還原得到的活性組分Cu0含量最多、分散度最好,因此選擇2%K-CuZnAl催化劑用于進一步考察其他反應條件對SBA脫氫生成MEK的影響。

圖6 不同K含量的CuZnAl催化劑的催化性能Fig.6 Catalytic performance of CuZnAl catalysts with different K contents.
2.2.2 反應溫度的影響
SBA脫氫反應是吸熱可逆反應,因此提高反應溫度可以提高脫氫反應的速率,有利于反應向正反應方向移動[19]。但反應的溫度過高,發生副反應的概率會增加,也會降低MEK的收率。 圖7為不同的溫度下CuZnAl和2%K-CuZnAl催化劑催化SBA脫氫生成MEK的性能。從圖7可看出,SBA轉化率隨溫度的升高而升高,在反應溫度為260 ℃時,CuZnAl和2%K-CuZnAl催化劑的SBA轉化率分別為83%和85.2%。MEK在CuZnAl催化劑上的選擇性隨溫度的升高而升高,在260 ℃時,MEK的選擇性為91.1%。MEK在2%K-CuZnAl催化劑上的選擇性隨溫度的升高先升高后降低,在240 ℃ 時選擇性最高,為93.5%,MEK收率也表現出同樣的趨勢,最高收率為78.1%。綜合考慮,2%K-CuZnAl催化劑在反應溫度為240 ℃時活性最佳,此時SBA轉化率為83.5%、MEK選擇性為93.5%、MEK收率為78.1%。

圖7 溫度對SBA脫氫反應的影響Fig.7 Effect of temperature on the dehydrogenation of SBA.Reaction conditions:atmospheric,LHSV=3.5 h-1.
2.2.3 LHSV的影響
圖8為LHSV對2%K-CuZnAl催化SBA脫氫反應的影響。從圖8可看出,SBA的轉化率和MEK的選擇性隨著LHSV的增大呈現出先增加后降低的趨勢。當LHSV=3.0 h-1時,MEK選擇性最佳,為94.0%;當LHSV=3.5 h-1時,SBA轉化率最佳,為83.5%,同時MEK的收率也達到最佳,為78.1%。綜合考慮,選取LHSV=3.5 h-1。

圖8 LHSV對SBA脫氫反應的影響Fig.8 Effect of LHSV on the dehydrogenation of SBA.Reaction conditions:atmospheric,240 ℃.
2.2.4 催化劑的穩定性
工業上大多數化學反應是在高溫下進行的,不僅要求催化劑具有高活性、耐熱性,并且還需要催化劑在長時間的反應過程中保持穩定。為了考察K的引入對CuZnAl催化劑耐熱性的影響,在常壓、240 ℃、LHSV=3.5 h-1的條件下,首先測定2%K-CuZnAl催化劑與CuZnAl催化劑對SBA脫氫反應的初始活性,然后升溫至400 ℃,恒定2 h,再將溫度降到240 ℃,考察催化劑的穩定性,實驗結果見圖9。

圖9 催化劑的穩定性Fig.9 The stability of catalyst.
從圖9可看出,在反應進行100 h時間內,SBA轉化率保持在83%左右,MEK選擇性保持在93%左右,MEK收率保持在78%左右。上述結果說明,2%K-CuZnAl催化劑具有良好的耐熱穩定性,在長時間SBA脫氫過程中沒有發生失活現象。
3 結論
1)采用共沉淀法和浸漬法制備了K-CuZnAl催化劑,K改性有利于催化劑表面Cu物種的還原,提高了催化劑還原后的活性組分Cu0的含量。且K改性使催化劑的比表面積增大,增加了催化劑的孔體積和平均孔徑,改性后的催化劑具有尖晶石CuAl2O4晶型特征,該晶型的存在提高了催化劑的耐熱穩定性。
2)2% K-CuZnAl催化劑在常壓、240 ℃、LHSV=3.5 h-1的反應條件下,SBA轉化率為83.5%、MEK選擇性為93.5%、MEK收率為78.1%。且催化劑具有良好的穩定性,可連續使用100 h。

