對比全身成像三維量化超聲心動圖與MRI定量評估主動脈瓣反流
唐海霞,林 凌,鐘文津,劉麗莉
(海南省人民醫院 海南醫學院附屬海南醫院超聲科,海南 海口 570311)
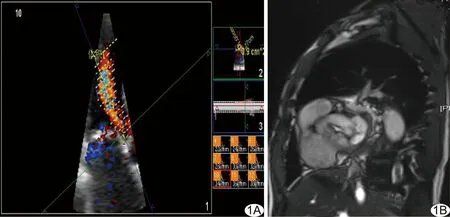
圖1 2種方法評估AR-Vol A.GI3DQ評估AR-Vol; B.MRI評估AR-Vol
主動脈瓣反流(aortic regurgitation, AR)是常見瓣膜病變,及時診斷和準確評價AR對于臨床治療決策甚為重要。外科手術中只能通過灌注后觀察左心室是否飽漲和主動脈根部壓力對AR進行半定量評價,而主動脈根部造影有創且費用高,不宜作為常規檢查。目前主要采用超聲心動圖定量分析 AR程度,AR容積(AR volume, AR-Vol)是其重要指標。隨著超聲新技術的發展和軟件的不斷更新,全身成像三維量化法(general imaging three-dimensional quantification, GI3DQ)已成為直接測量和評估AR的新方法;而MR多序列綜合掃描可對心臟瓣膜病進行準確定性及定量評價。本研究對比觀察GI3DQ超聲心動圖與MRI定量評估AR的效果。
1 資料與方法
1.1 一般資料 回顧性分析2018年1月—2019年9月海南省人民醫院收治的45例AR患者,男29例,女16例,年齡31~71歲,平均(52.4±11.6)歲;其中9例主動脈瓣環或升主動脈擴張,8例瓣葉對合不良或脫垂,5例二葉畸形,23例主動脈瓣鈣化。納入標準:年齡>18歲,根據文獻[1]標準診斷AR。排除標準:頻發房性或室性期前收縮,房室傳導阻滯(Ⅱ度以上),主動脈瓣狹窄及極重度AR[1],心房纖維顫動、先天性心臟病及嚴重肺部疾病患者,或超聲檢查中不能較好控制呼吸及存在MR禁忌證。
1.2 儀器與方法 于入院后同日先行超聲心動圖檢查,再行MR檢查。
1.2.1 GI3DQ評估AR 采用Philips iE33超聲診斷儀,二維相控陣探頭S5-1(頻率2~4 MHz),實時三維矩陣探頭X5-1(頻率1~3 MHz);三維彩色多普勒血流成像系統;QLab 9.0及GI3DQ圖像處理工作站。行常規超聲心動圖檢查,連接心電圖肢體導連,取心尖五腔心切面,采用X5-1探頭經胸獲取AR血流圖,囑患者吸氣后屏氣,于AR血流匯聚區域連續采集4個心動周期彩色全容積圖像。將圖像導出,采用Philips QLab 9.0軟件GI3DQ插件載入導出數據,連接反流束起點和終點,軟件自動切割為15層;于每層手動勾畫AR輪廓邊緣,軟件自動計算得出AR-Vol(圖1A);同時采集4個心動周期的心尖四腔心切面三維全容積圖像,以QLAB 3DQ Adv軟件測量左心室舒張末期容積(left ventricular end-diastolic volume, LVEDV)和左心室收縮末期容積(left ventricular end-systolic volume, LVESV),獲得每搏量(stroke volume, SV),計算反流分數(reflux fraction, RF)。RF%=AR-Vol/SV×100%。
1.2.2 MRI評估AR 囑患者仰臥,行心臟及主動脈軸位、矢狀位成像。以TrueFISP電影序列采集左心室短軸電影,對相應瓣膜切面依次采用TrueFISP快速小角度激發成像電影序列掃描及相位流速編碼電影成像。采用Siemens血流分析軟件對AR相位圖進行手工描記和分析,獲得LVEDV、LVESV及SV。AR束為舒張期左心室內出現的來自主動脈瓣的低信號區,選取有低信號區的層面,沿低信號區邊緣勾畫,得到每層反流面積,以相鄰兩層的面積均值為層面間隔面積,獲得反流束容積(即AR-Vol),計算RF%,見圖1B。
1.3 統計學分析 采用SPSS 18.0統計分析軟件。符合正態分布的計量資料以±s表示,組間比較采用配對t檢驗;2種方法評估數據的相關性采用Pearson相關分析法,一致性分析采用Bland-Altman分析法。P<0.05為差異有統計學意義。
2 結果
GI3DQ與MRI所測AR-Vol、RF%差異均無統計學意義(P均>0.05),見表1;2種方法所測AR-Vol(r=0.93,P<0.001)、RF%均呈正相關(r=0.94,P<0.001),見圖2。2種方法評價AR-Vol的平均差為-4.25 ml,95%一致性界限(-20.65,-12.16),評價AR-Vol差異無統計學意義(P>0.05);2種方法評價RF%的平均差為6.56%,95%一致性界限(-5.85%,-18.97%),差異無統計學意義(P>0.05)。見圖3。

圖2 GI3DQ與MRI評價AR-Vol、RF%的相關性散點圖 A.AR-Vol; B.RF%

圖3 GI3DQ與MRI評價AR-Vol、RF%的Bland-Altman一致性分析散點圖 A.AR-Vol; B.RF%
3 討論
急性AR主要見于細菌性心內膜炎、主動脈夾層、創傷及人工血管轉換術急性功能障礙等,慢性AR最常見原因為風濕熱、主動脈瓣退行性改變、先天性主動脈瓣畸形(發病率為0.5%~2.0%)[2]、結締組織病引起的主動脈瓣環擴張及嚴重高血壓(舒張壓≥110 mmHg)致升主動脈增寬或主動脈瓣相對關閉不全[3]等。AR對人體的危害主要取決于反流量。隨著AR加重,患者從勞力性呼吸困難、夜間陣發性呼吸困難發展至端坐呼吸,部分急性患者可突發左心衰竭甚至死亡。
表1 GI3DQ與MRI測量AR-Vol、RF%比較(±s,n=45)

表1 GI3DQ與MRI測量AR-Vol、RF%比較(±s,n=45)
方法AR-Vol(ml)RF%GI3DQ29.26±19.8448.56±22.57MRI32.10±19.0155.31±29.78t值-2.483-1.900P值0.0570.064
無論何種病因所致主動脈瓣病變,手術均為AR的主要治療方式,而選擇手術時機對預后具有決定性意義,故術前準確判斷反流程度極為重要。術前經超聲心動圖診斷結果對于手術與否及手術方案具有關鍵性作用。臨床發現部分病例經超聲心動圖檢測結果與手術結果不相符,二維超聲心動圖對于瓣膜反流程度可能低估,如超聲心動圖示主動脈瓣未見明顯增厚、回聲增強,瓣膜反流程度為輕度,而術中經注水發現左心室明顯飽漲、主動脈根部壓力較大,瓣膜對合度欠佳,診斷為中度以上反流,需手術更換瓣膜。
AR-Vol和RF%是定量評估瓣膜反流程度的常用指標。本研究以GI3DQ評估AR,并與MRI相對照,結果顯示GI3DQ與MRI所測AR-Vol差異無統計學意義,但MRI測值略高于GI3DQ,提示GI3DQ可能低估AR-Vol。分析可能原因:①實時三維超聲心動圖采集圖像時對患者呼吸、心率有一定要求,患者如不能很好地配合,則測量誤差相對較大;②實時三維超聲心動圖顯像幀頻較低,且其觸發采集模式可能產生時間偽差,造成血流信號部分丟失而被低估;③AR在部分患者為呈偏心性,GI3DQ以疊式輪廓進行分析時,較難辨別其邊緣輪廓。本研究中GI3DQ與MRI所測量RF%差異亦無統計學意義,提示輕微低估AR-Vol并不影響對于RF%的評估結果;且本研究中2種方法所測AR-Vol、RF%均呈正相關,一致性較好,提示GI3DQ可用于評估AR。
目前評價AR-Vol的方法主要有心導管造影、雙源CT、超聲心動圖和MRI。心導管檢查有創,操作復雜,且有輻射[4]。雙源CT可用于評估AR[5],其結果與超聲心動圖相關性良好,但存在對比劑過敏風險,且其判斷AR程度并不精確,原因在于CT只能測量解剖結構而不能評價血流動力學情況。超聲心動圖診斷心臟瓣膜病和評估其嚴重程度的準確性較高[6-7]。二維彩色血流成像法是目前最常用于評價AR的方法,但其僅依據反流束長度對反流程度進行分級評估,受反流束速度和心腔順應性等諸多因素影響而精確性較差。實時三維超聲心動圖可從三維空間對AR進行定量評價,操作簡便,結果可靠[8],但實際上超聲心動圖測得的AR-Vol是立體彩色多普勒信號的集合,并不等同于真實的反流容積,且需通過多普勒計算,相對耗時。MRI對于診斷和評價瓣膜性疾病具有舉足輕重的作用,可通過瓣膜形態、開放和關閉狀態、瓣口流速和壓差及反流容積等對心臟瓣膜病進行定性、定量評價,異常高速湍流信號反映瓣膜活動異常,同時提示受累心腔及大血管發現相應繼發性改變,其定量評價反流嚴重程度的精確性優于超聲心動圖[9-11]。MRI評估AR的方法較多,本研究對反流束進行分層,計算各層、間隔反流面積、層厚、間隔厚度等參數得到反流束容積,即AR-Vol。GI3DQ在對反流束容積進行三維重建的基礎上將其分割成數個層面進行疊加分析,兼顧反流容積的不規則性,與MRI疊加分析法原理最相近,便于比較,且更加簡便、準確,耗時短且費用低[12-13]。
綜上所述,GI3DQ可對AR進行定量評估,其與MRI測值的相關性和一致性均較好,可作為AR術前常規檢測手段。但本研究樣本量偏少,且未納入極重度AR患者,尚待進一步完善。

