氫氧直接合成的過氧化氫原位氧化反應研究進展
鞏笑笑,張曉昕,宗保寧
(中國石化石油化工科學研究院石油化工催化材料與反應工程國家重點實驗室,北京 100083)
過氧化氫(H2O2)作為一種重要的無機化工原料和綠色基礎化學品,已被列為世界上最重要的100種化學品之一[1]。其活性氧含量高(質量分數為47%)且降解副產物只有水,省去了反應后的分離和純化過程,成為工業常用的氧化劑t-BuOOH、HNO3、N2O和高錳酸鹽等的替代物。與分子氧相比,H2O2可以在溫和的液相環境、酸性或堿性條件下進行氧化反應,是一種高效的多功能強氧化劑[2-3]。現今已有大量的研究工作以H2O2為氧化劑應用于烯烴的環氧化[4-7]、芳烴的羥基化[8-10]、酮的氨氧化[11-14]及烷烴的氧化[15-17]等反應中,因選擇性高、反應條件溫和、綠色環保等優勢而具有良好的工業應用前景。
目前,工業上生產H2O2的方法主要為蒽醌法。此方法工業技術成熟,但存在設備投入量大、工藝流程復雜、環境污染等問題。受工藝成本限制,H2O2生產廠常建于偏遠地區,工業應用中需經儲存和運輸至使用點稀釋,而高濃度H2O2不穩定,極易分解,儲運成本高,且存在安全隱患。由H2和O2直接合成H2O2的技術因具有原子經濟性高、環境效益好等優勢而成為研究熱點,其適合于低成本、小規模生產H2O2。該反應的機理為H2解離吸附形成H·,與O2非解離吸附形成的O—O·作用,經·OOH中間體生成H2O2。反應過程存在大量的氫過氧化物和活性氧物種,均為H2O2作用于氧化反應的活性物種。近些年的許多研究指出,將 H2和O2直接合成H2O2反應與丙烯環氧化、污水處理等化工過程或其他氧化反應耦合,不僅可以省去H2O2的生產、儲存和運輸過程,大大降低成本,簡化生產工藝,甚至可以合成指定濃度的H2O2以滿足不同的氧化反應需求,因而此工藝路線具有廣闊的研究意義和工業應用前景。以下以國內外廣泛研究的幾個特征反應為例,綜述H2O2的合成用于原位氧化反應的研究進展及關鍵問題,以期為今后的研究工作提供思路。
1 H2和O2直接合成H2O2的反應
H2和O2直接合成H2O2的過程涉及氣、液、固3相,其反應路徑如圖1所示。將H2和O2混合氣體通入分散有催化劑的懸浮液中,反應物進入溶劑介質與固體催化劑表面的Pd物種接觸,除生成H2O2外,還存在H2和O2直接反應生成 H2O、產物H2O2的分解和H2O2加氫3個副反應。由熱力學數據可知,H2與O2反應極易生成H2O,導致H2O2的濃度較低。
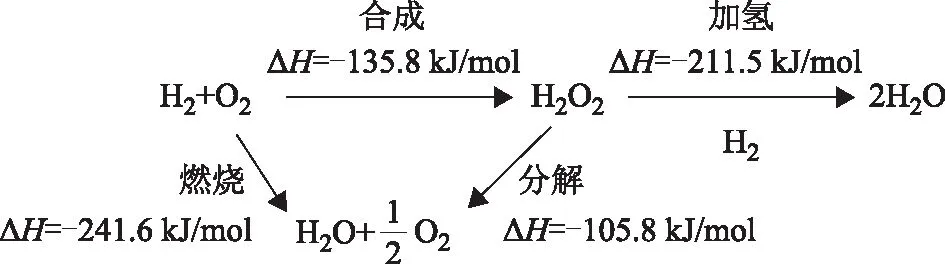
圖1 H2和O2直接合成H2O2的反應路徑
Lunsford等[18-19]研究發現,以上反應的微觀過程存在大量的活性H,O,OH,OOH物種的生成和轉化。用*表示金屬催化劑上的表面物種,反應微觀過程解釋如下:首先,H2被吸附在催化劑活性位點上,解離為活性H原子:H2→H2*→2H*;接著,O2非解離吸附并與活性H原子生成反應中間體OOH物種:O2→O2*,O2*+H*→OOH*;然后,OOH物種氫化為產物H2O2:OOH*+H*→H2O2。吸附和加氫步驟是合成H2O2的主要反應步驟。如果O2,OOH,H2O2在催化劑表面強吸附,發生O—O鍵的斷裂或氫化,則生成OH*和H2O,即為副反應的主要路徑:O2*→2O*,O*+H*→OH*;OOH*→O*+OH*;OOH*+H*→H2O*+O*;OOH*+H*→2OH*;H2O2*→2OH*;H2O2*+H*→H2O*+OH*。
因此,H2和O2直接合成H2O2的本質反應為活性H,O,OH,OOH物種的生成和轉化。這些物種在H2O2的原位氧化反應中發揮重要作用。
2 H2O2原位氧化反應
2.1 丙烯環氧化制環氧丙烷
環氧丙烷(PO)是一種高價值含氧有機物和基本有機化工原料,主要用于生產聚醚多元醇、丙二醇和各類非離子表面活性劑等重要化學品,其生產和應用在石油、化工、農藥、紡織、日化等行業具有重要意義。目前工業生產PO的方法主要為氯醇法和共氧化法,但氯醇法對環境污染嚴重,受環保要求限制;共氧化法雖沒有污染,但會副產市場需求低于PO的叔丁醇和苯乙烯,設備投資較大,工藝流程復雜。H2O2直接氧化法(HPPO)具有操作簡單,原子經濟性高,反應條件溫和,環境友好等優點[20],成為當今研究開發的重點。
工業上HPPO工藝以 H2O2溶液和丙烯氣體為原料,H2O甲醇為反應溶劑,選用合適的鈦硅催化劑在相對溫和的條件下進行直接氧化[21],需就近建立H2O2工廠作為配套,以降低高濃度H2O2溶液的儲運成本[22]。探索以H2、O2和丙烯為原料,用H2和O2直接生成的H2O2原位氧化丙烯,可以去除預先制備H2O2的工藝,在經濟、環保及未來發展等各方面均具有優勢。文獻報道中,以Au,Pd,Pt貴金屬或其組合形式作為催化劑活性組分,TS-1[23-28]、Ti-MCM-41[29-31]及其氧化物[32-34]等鈦材料為載體,組成雙功能催化劑;生成的H2O2在溫和條件下由載體內孤立的Ti4+位點活化,此為反應的速控步驟。其反應機理如圖2所示:H2與O2在金屬表面產生·OOH自由基或H2O2;丙烯吸附在鈦材料載體上,生成雙配位丙氧基化合物;·OOH自由基與雙配位丙氧化合物相互作用并于催化劑表面脫附生成PO和H2O[35-36]。載體本身較大的孔結構有利于反應物和產物的擴散。
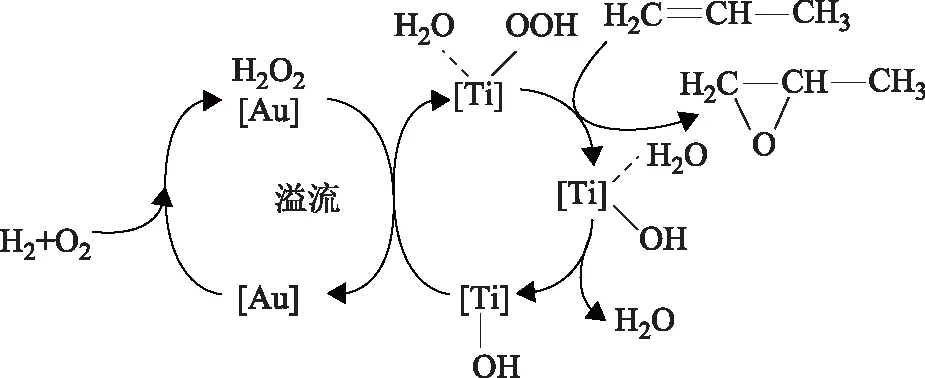
圖2 鈦硅分子篩負載的Au基催化劑上H2O2原位氧化合成環氧丙烷機理
反應體系中加入Cs2CO3[37],CsNO3[38],CsCl[29]等無機鹽,可抑制丙烯加氫、PO水解及PO與甲醇反應等諸多副反應的發生,提高PO產率。Chen Qi等[39]發現,當使用0.2%PdTS-1+0.02%PtTS-1催化劑并以醋酸銨為抑制劑時,在壓縮的 CO2介質中可以得到28.7%的丙烯轉化率和81.8%的PO選擇性。Qi Caixia等[40]認為副反應丙烯加氫與Au納米團簇的大小及是否存在堿性促進劑有關,2~5 nm的Au顆粒及堿性促進劑均可促進環氧化反應。Lu Jiqing等[41]研究了第二組分對AuTS-1催化劑的影響,發現加入堿金屬(K,Cs)對金屬負載無影響但可提高催化活性,堿土金屬(Mg,Ca,Sr,Ba)對Au負載量和催化活性均存在促進作用,其中以Mg為最優。此外,Ge的添加對AuTS-1催化劑活性中心產生配體效應,可以降低環氧反應的活化能,從而影響丙烯的轉化率和PO選擇性[42]。
HPPO是當前發展較快且工藝成熟的工業化生產技術,開發以H2、O2和丙烯為初始原料的綠色新技術,可從根本上解決H2O2的供應來源問題。國內對這方面的研究還相對薄弱,因而需開發高活性、高穩定性的催化劑,加大力度研發具有自主知識產權的綠色PO生產新工藝。
2.2 Fenton反應
含酚廢水是指主要含有苯酚、甲酚、硝基甲酚等高毒性、難降解有機物的工業廢水,來源于石化、制藥、塑料及樹脂等生產過程,對人體、水生生物和自然環境存在巨大危害,已被許多國家列入重點污染物的黑名單。工業上根據廢水中酚類物質組成、濃度及酸堿度不同,采用物化、化學、生化等不同方式處理[43-45]。Fenton反應是指將有機污染物通過H2O2與Fe2+的混合溶液,H2O2經歧化反應生成具有強氧化能力的·OH自由基及其他活性氧物種,在溫和條件下采用化學方法氧化分解有機物以達到去除目的,適用于中低濃度廢水有機污染物的降解,是一種非常具有潛力的高級催化氧化技術[46-51]。
Esplugas等[52]對比了O3、紫外光、H2O2、Fe2+及光催化等不同催化體系氧化降解苯酚的效果,Fenton試劑對苯酚的降解速率最大,而選用H2O2為氧化劑時,其氧化產物只有H2O和O2等環境友好物種,且此過程具有操作簡單(在室溫和常壓下操作)和無毒、反應快、降解完全等優點。商業上多為蒽醌法生產的高濃度H2O2,其運輸、稀釋成本較高,因此探究原位生成H2O2的技術直接用于Fenton廢水處理具有重要意義和巨大優勢。先前的研究者考察了兩種不同的催化體系:負載型Pd基催化劑與均相Fe2+催化劑組成的半均相體系,Pd-Fe負載于不同載體上的非均相體系。Triki等[53]認為Pd-Fe合金雖可產生較多的H2O2但并不利于苯酚降解,但Pd與Fe2O3的協同作用可以有效地促進Fenton反應。
Yalfani等[54-57]為解決H2O2合成過程中H2和O2直接接觸的安全性問題,采用甲酸、肼和羥胺等替代H2作氫源,研究結果表明,O2甲酸混合物在有機物的氧化階段可控制H2O2的生成量,O2肼更適用于中性及弱堿性廢水的處理。Yuan Songhu等[58]研究采用PdC催化劑和分段電解技術,先電解水生成H2和O2再生成H2O2,并探究與Fenton反應聯合降解羅丹明 B的效果,結果表明,在pH為2和100 mA電流作用下,H2O2可在120 min內達到最高質量濃度53.1 mgL,與Fe2+形成Fenton試劑,30 min內完全降解羅丹明B(準一級速率常數為0.109 min-1±0.009 min-1),反應過程和結果見圖3。Osegueda等[59]將Pd負載于過渡金屬氧化物上制備膜催化反應器作用于H2和O2直接生成H2O2,發現Fe2+加入后反應體系表現出良好的苯酚氧化活性,此研究證明了H2O2原位生成與Fenton反應結合用于廢水處理的可行性。
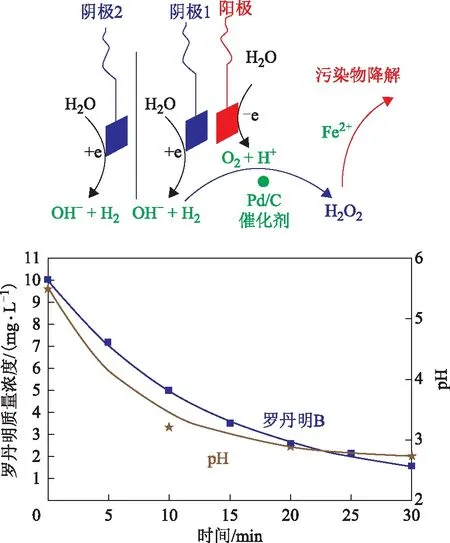
圖3 H2O2原位生成與Fenton反應結合用于廢水處理
Underhill等[60]在負載型Pd-Fe雙金屬催化劑上進行了原位生成的H2O2與后添加的商用H2O2的苯酚降解性能對比,發現前者具有更好的作用效果和活性,可能是商業H2O2在反應前一次性大量加入,導致了自由基物種的自終止。此外,苯酚氧化的中間產物導致催化劑中活性組分Fe析出,影響了催化劑的穩定性和使用壽命。在以后的研究中可以通過對催化劑的優化或反應體系的改進,提高催化劑的壽命和穩定性,保持苯酚的高降解活性。上述研究結果表明,原位生成的H2O2在Fenton處理有機物氧化反應中具有巨大潛力,工藝上具有操作過程簡單、反應易得、運行成本低廉、設備投資少且環境友好等優點,可有效規避氧化劑H2O2生產成本高的問題。
2.3 甲烷氧化制甲醇
甲烷是天然氣、油田氣及頁巖氣的主要成分,在自然界中分布極廣且儲量豐富,實現甲烷分子活化或選擇性轉化為甲醇等液體燃料和其他化工產品可以實現天然氣的有效利用,對調整能源結構及綠色化工生產意義重大。甲烷直接部分氧化合成甲醇被稱為“夢幻工藝”,一直以來都是科研領域具有挑戰性的研究課題。甲烷分子中包含4個相同的C—H鍵,形成高度對稱的四面體構型,C—H鍵非常穩定且活化能很高(440 kJmol),因此,甲烷氧化需要強酸、高溫等較為苛刻的反應條件。但甲醇、甲醛等甲烷氧化產物反應活性高,更易深度氧化為CO、CO2等副產物,因而難以在實現高轉化率的同時得到較好的選擇性。
在現代石化工業中,甲烷轉化常采用間接轉化方式,即在高溫條件下將甲烷C—H鍵完全斷裂轉化為合成氣(CO+H2),再通過費-托合成得到甲醇等基礎化學品,如圖4所示[61]。此工藝需要兩個獨立的工藝步驟,反應條件苛刻,對工藝設備要求高。研究發現,沸石負載的Cu或Fe基催化劑在高溫高壓下以O2N2O作氧化劑,進行循環氧化可以得到甲醇和甲醛,此氣相氧化法要求反應條件苛刻(>400 ℃)且易過度氧化,反應進程難以控制,產品總收率低[62]。甲烷液相氧化反應可顯著降低反應溫度,以一系列Hg,Pt,Pd,Au,Ru,Rh,V的配合物為均相催化劑,在較為溫和的條件下(室溫~200 ℃)可以將甲烷選擇性氧化為甲醇。反應需以硫酸、三氟乙酸、鹽酸或氫溴酸等強酸作為反應介質,先生成中間產物硫酸甲酯,再經水解得到甲醇。該反應中強酸物質的使用對設備提出更高的要求,并產生廢酸等污染物[63-69]。
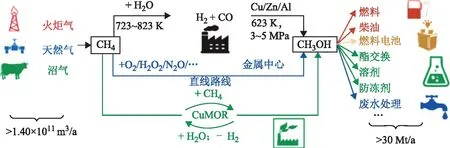
圖4 當前工業甲烷轉化制甲醇涉及的化工過程
探索新型友好的綠色氧化劑(如H2O2)替代濃硫酸或O2等常用氧化劑,實現甲烷在較溫和的反應條件下選擇性氧化生產甲醇,在經濟和環境方面均具有重要意義[70-71]。Yuan Qiang等[70]考察了不同過渡金屬氯化物在水介質中以H2O2為氧化劑,選擇性氧化甲烷和乙烷的結果,證實H2O2的分解和甲烷的氧化均為自由基反應,H2O2在過渡金屬表面上生成活性氧物種HOO·和HO·,活性氧物種活化C—H鍵生成甲基自由基CH3·,可以測得中間產物CH3OOH的存在,最后得到產物CH3OH和HCHO。但是商用H2O2價格較高且在反應過程中大量分解,成本損耗較大。相比外部添加H2O2的方式,以O2CH4H2為反應原料,實現H2O2的原位合成與氧化反應的一步耦合更具經濟效益。早期的研究工作集中在O2COH2O反應體系[71],首先發生水煤氣變換反應生成H2,H2與O2作用直接合成H2O2,H2O2再對甲烷、乙烷和丁烷進行選擇性氧化,反應過程見圖5。Lin Minren等[72-73]采用RhCl3或PdC和CuCl2K2PdCl4催化體系,鹵素離子穩定催化劑的活性組分Pd,Pd及其氧化物負責H2O2的原位生成、甲烷的活化及甲酸的生成,Cu基催化劑負責C—H鍵的活化并促使其轉化為相應的醇。Fan Yafang等[74]發現在PdC催化體系中加入四氯苯醌(TCQ)可對甲烷氧化產物HCOOH或CF3COOCH3進行調節。
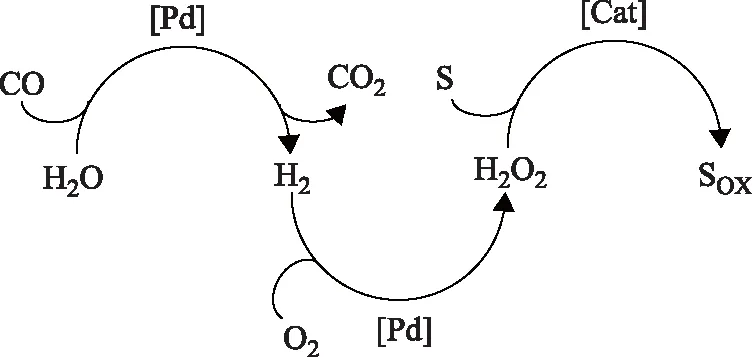
圖5 O2COH2O反應體系中H2O2的合成與低鏈烷烴的氧化反應集成S—基底; SOX—氧化態基底; Cat—Pd或其他
與O2COH2O反應體系相比,直接使用H2O2作為反應原料氣能夠省去水煤氣變換反應步驟,反應過程更簡單,低溫活性更高。Park等[75-76]通過考察PdC和Cu(CH3COO)2催化劑或V化合物用于H2O2體系甲烷氧化反應的催化效果,證明了CuV化合物對甲烷活化的重要作用。Min等[77]探究了一系列雜多酸化合物的催化效果,其中Pd0.08Cs2.5H0.34PVMo11O40效果最好,其酸性中心Pd促進了活性氧物種的生成,而活性氧與甲烷相互作用為反應的決速步驟,羥基化則發生在雜多化合物結構內部。
Hutchings等[78-79]最早提出負載的Au-PdTiO2雙金屬催化劑在無酸或鹵素離子作穩定劑的情況下仍具有較好的H2和O2直接合成H2O2催化性能,后將此催化劑用于H2O2原位生成與甲烷氧化反應。該過程與添加商用H2O2時相比,雖然產率相同,但H2O2原位合成更有利于O2的捕獲和液相中活性氧物種的生成,因此原位合成具有更好的氧化效率和甲醇選擇性。采用ZSM-5替代最初的載體TiO2,可以調變載體的硅鋁比和酸堿度,從而影響反應活性,效果優于其他氧化物載體上的同類催化劑[80]。后續研究發現,無需載體的AuPd納米粒子經聚乙烯吡咯烷酮(PVP)保護后可形成穩定的膠體狀態,此催化劑不存在金屬-載體的相互作用,可以有效減少生成的H2O2在催化劑表面進一步地加氫和分解,使得甲醇選擇性高達92%。采用同位素標記法追蹤O原子,推斷反應以H2O2與O2共同作為氧化劑,H2O2存在兩種活化路徑,機理如圖6所示[81]。第一種路徑是:H2O2在催化劑表面生成HO·,HO·與CH4作用奪取H·生成CH3·,CH3·與O2反應生成關鍵的中間產物CH3OOH,最后分解產生CH3OH。第二條路徑為:H2O2分解生成O2和HOO·,與CH3·生成CH3OOH。
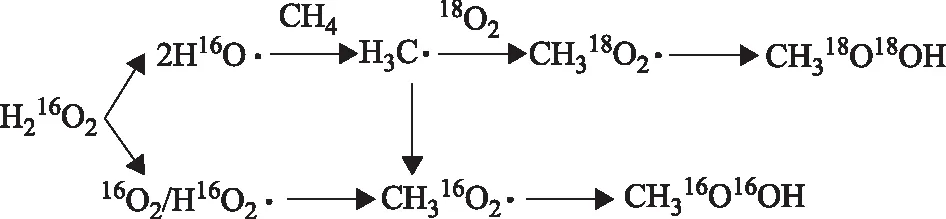
圖6 H2和O2直接合成H2O2的原位氧化甲烷反應機理
Zhu Jin等[82]認為影響甲醇產率的關鍵在于H2O2濃度,因而以提高H2和O2的合成效率,降低甚至抑制生成的H2O2分解和進一步加氫為研究的重點。該課題組提出“分子圍欄”概念,設計了一種在溫和條件下(70 ℃)原位生成H2O2高效氧化甲烷的催化劑,如圖7所示。其將Au-Pd合金納米顆粒封裝在硅酸鹽分子篩內部,通過有機硅烷改性對載體進行疏水處理,制備了一系列AuPd@ZSM-5-C3,AuPd@ZSM-5-C6,AuPd@ZSM-5-C16催化劑。H2和O2通過傳質進入沸石晶體中生成H2O2,沸石外層的疏水基團可以有效阻礙親水的H2O2擴散,H2O2局部濃度得以提高。甲烷分子通過疏水層進入沸石內部與H2O2發生反應。改性后的疏水沸石不影響H2、O2和甲烷的擴散,通過提高氧化劑H2O2的局部濃度,顯著提高了反應效率,得到目前報道的最高甲醇收率91.6 mmol(h·g)。
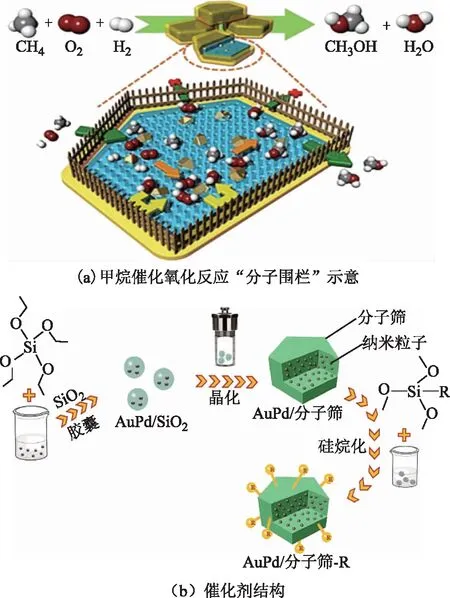
圖7 甲烷催化氧化反應“分子圍欄”示意與催化劑的結構[82]
先前的研究已經證明了原位生成的H2O2選擇性氧化短鏈烷烴的可行性,該工藝可以很好地控制反應進程,并在一定程度上規避了含氧產物過度氧化為CO2的問題,具有良好的開發前景和工藝優勢。但產品甲醇的收率仍然很低,與工業應用所需值相差甚遠。因此,通過設計、開發高活性催化劑或改進反應器及工藝路線等方式提高甲醇收率,仍然是未來研究的重大挑戰。
2.4 其他氧化反應
Remias等[83]報道了釩和鐵氧化物負載的Pd催化劑在H2和O2中原位生成H2O2并用于苯和環己烷羥基化反應的機理研究,采用原位生成H2O2時的產物選擇性優于添加H2O2時的選擇性。膜反應器被大量應用于H2、O2和苯羥基化體系,但苯酚產率仍較低。對于鈦硅分子篩催化劑與H2O2氧化劑聯合應用于化學品合成的研究已經有大量報道。如在TS-1[84],HTS[85],KIT-6負載的磷酸礬[86]等催化劑上進行環己烷氧化制環己酮和環己醇試驗,反應活性均較低。活性較高的反應體系一般采用均相催化劑,但存在催化劑與反應物難以分離的問題。Kuznetsova等[87-88]以H2、O2和環己烷為原料,通過原位生成的H2O2實現環己烷的氧化,發現少量離子液體添加劑可以顯著改善PtC-H3PMo12O40催化劑在O2和H2混合液中原位生成H2O2氧化環己烷的催化性能。離子液體中的Br-和陰離子可穩定活性過氧化物和抑制環己醇的二次氧化,降低H2O2的降解速率,提高環己醇環己酮(KA油)產率。Shetti等[89]認為H2O2與鈦硅分子篩作用會生成Ti—O—O-·和HO—Ti—OO-·兩種不同的含Ti過氧基團,第一種對環氧化反應有良好的選擇性。大連理工大學Li Gang等[90-92]采用AuTS-1、AuTi-HMS等催化劑,探究H2、O2共存時H2O2原位合成并用于液相氧化脫除燃油中的硫化物。其反應機理與H2、O2、丙烯環氧化反應類似:Au主要用于催化合成H2O2過程,H2O2物種遷移至骨架鈦活性位上,Ti與·OOH物種形成過渡態,此過程為硫化物氧化反應的速控步驟;大分子硫化物的底物先被氧化為具有一個O的亞砜化合物,進而氧化為砜。催化劑在連續使用5次后仍可保持幾乎100%的硫去除率。Karmee等[93]在超臨界CO2H2O雙相體系中采用PdTiO2催化劑催化H2和O2直接生成H2O2,再在TiO2上將硫茴香醚選擇性氧化制備甲基亞砜。H2O2作為綠色氧化劑用于工業過程的研究較多,因而原位生成與氧化反應的集成研究也較廣泛,但現階段的研究因受到產品產率限制而仍處于實驗室研究階段。
3 總結與展望
由H2和O2原位生成的H2O2進行選擇性氧化是一種具有潛力的替代當前工藝的方法;與現代工業常用的工藝相比,該反應條件溫和,綠色環保,可以很好地控制反應進程,避免高溫自氧化產生副產物;與添加市售的H2O2相比,采用來源豐富的分子氧作為原料,無需在氧化現場儲存大量H2O2,可有效降低生產和設備成本,避免了商用H2O2的分解造成的成本損耗。但是,此方法目前僅停留在實驗室研究階段,這是由于直接生成的H2O2在無穩定劑情況下產率較低,酸與鹵素等穩定劑存在時又會降低催化劑和反應器的使用壽命,這些均是合成反應中亟需解決的科學問題。此外,此工藝包括H2O2的合成及目標底物氧化兩個反應的串聯過程,這一系列過程微觀機理復雜,涉及各組分在活性位點的吸附、脫附及擴散,同時還需考慮生成的H2O2分解,因而,對于未來催化劑的設計側重同時可進行兩種反應的活性位,避免生成的H2O2受到擴散限制。經證實集成系統原位生成了大量的氫過氧化物和活性氧物種,促進非活性 C—H 鍵氧化為相應的含氧化合物,效果優于直接添加的H2O2。可根據類似策略進行推廣與設計,加深對反應機理的認識,制定進一步的策略,通過催化劑設計、工藝參數、系統控制等手段提高整體產品收率,實現工藝路線的經濟可行性。此外,提高催化劑在選擇性氧化過程中的穩定性,防止金屬組分流失或毒化,以及考慮到反應系統的安全問題,控制系統中H2O2混合物比例,都是影響未來工業應用的關鍵。
在過去的幾十年中,國外許多研究機構開展了H2和O2直接合成H2O2及原位氧化反應的研究,包括一些傳統 H2O2制造商:Evonik,Solvay,Mitsubishi等,已取得階段性成果,直接合成技術和HPPO技術聯產,使人們看到產業化的希望。在我國,H2O2綠色合成技術的報道較多,但與氧化反應的集成研究相對薄弱。通過開發高效、高活性的多功能催化劑以及工藝、設備的優化與設計,探索以H2、O2和有機物為原料的原位氧化體系,無論是從化學品市場角度還是安全生產來看,都具有重要的開發和研究意義。

