2019年上海地區H9N2禽流感病毒分子特征及演化分析
葛杰,徐志遠,李鑫,劉健,楊德全,鞠厚斌,葛菲菲*
(1. 上海市動物疫病預防控制中心,上海 201103;2. 揚州大學生物科學與技術學院,江蘇 揚州 225009)
禽流感病毒(avian influenza virus,AIV)H9亞型在全球野生鳥類中傳播,并且在亞洲、中東和非洲國家的許多家禽中呈地方流行[1-2]。盡管它們是低致病性禽流感病毒(LPAIV),受感染的雞會有輕微的呼吸道疾病,死亡率一般低于20%[3-4],但仍然令農業和衛生部門擔憂。H9亞型流感會影響肉雞體重、蛋雞的產蛋量和育種雞的質量[5-6]。另外,受感染的家禽更容易繼發感染[7],群體死亡率最高能達到65%[8]。
家禽中的H9禽流感病毒會對人類構成人畜共患病風險。自從1998年第1次正式報告人感染H9N2,孟加拉國、中國、埃及、巴基斯坦和阿曼共有59例人的病例[9]。人感染一般無癥狀或表現為輕度呼吸道疾病,只有1例相關死亡報告,可能是由于共感染導致[10]。在人群中檢測到的所有H9N2病毒與同期的家禽病毒基因上是相似的[9]。H9禽流感病毒通常通過重組,將內部基因組片段供應給非H9病毒,產生可能對畜牧業和人類健康構成威脅的禽流感基因型[11]。2013年以來在中國發現的最普遍的AIV是H9基因型[1,11]。本研究對上海市某活禽市場2019年11月分離到的4株H9N2亞型AIV進行全基因進化分析,以期為了解上海地區H9N2 AIV 流行情況及其防控和疫苗選擇提供依據和參考。
1 材料與方法
1.1 病毒株
4株H9N2亞型AIV毒株由本實驗室參照文獻[12]分離保存,其詳細背景見表1。

表1 4株H9N2禽流感病毒毒株的信息
1.2 SPF雞胚及主要試劑
SPF雞胚購自北京梅里亞維通實驗動物技術有限公司。H9熒光RT-PCR試劑盒由深圳匹基提供。新城疫陽性血清、禽流感血凝素分型血清(H5、H9)由哈爾濱獸醫研究所提供。AMV反轉錄酶等試劑均購自寶生物(大連)工程公司;特異引物由寶生物(大連)工程公司合成。
1.3 8個基因的擴增及序列分析
按照文獻[13]的方法進行病毒RNA的提取和8個基因的全長擴增,測序由上海桑尼生物科技有限公司完成。參照GenBank中相關參考毒株, 用 MEGA3.1構建鄰近樹,自展值設為1 000次,自展值≥60%顯示在主要的節點上,本研究中的4株病毒用實心三角標記。
1.4 序列分析比較
采用DNAStar軟件包(Madison, WI, USA)的EditSeq和MegAlign,對增加病毒適應性的分子特征進行分析以及抗原位點相關的氨基酸變化進行比較。
2 結果
2.1 全基因組同源性分析
4株病毒全基因節段的NCBI登錄號為MN918119~918150。分離株HA基因ORF全長為1 683 bp,編碼560個氨基酸,核苷酸同源性為91.8%~99.9%,氨基酸序列同源性為93.6%~99.8%。分離株的HA基因與A/Duck/Y280/1997的HA基因核苷酸同源性為88.5%~89.0%,氨基酸同源性為89.3%~92.0%。分離株NA基因ORF全長為1 401 bp,編碼466個氨基酸,核苷酸同源性為97.4%~98.9%,氨基酸序列同源性為97.2%~98.9%。4株病毒內部基因M、NP、NS、PA、PB1和PB2核苷酸同源性分別為98.7%~99.5%, 93.1%~94.1%, 98.8%~99.8%,95.7%~96.2%,97.8%~98.4%和96.7%~96.8%。
2.2 8個基因遺傳演化分析
利用Mega3.1軟件對分離毒株和參考毒株8個基因的遺傳演化關系進行分析,繪制遺傳演化樹(圖1至圖8)。結果顯示,所有分離株均為Y280系。根據繪制的8個基因節段的遺傳演化樹進行分析,4株分離株重組模式完全相同,均為四重重組體,由Y280亞系、Unknown、G1以及F98重組而成,根據已發表的文獻[14],這4株病毒均屬于G57基因型。

圖1 4株H9N2亞型禽流感病毒HA基因節段的基因進化樹

圖2 4株H9N2亞型禽流感病毒NA基因節段的基因進化樹
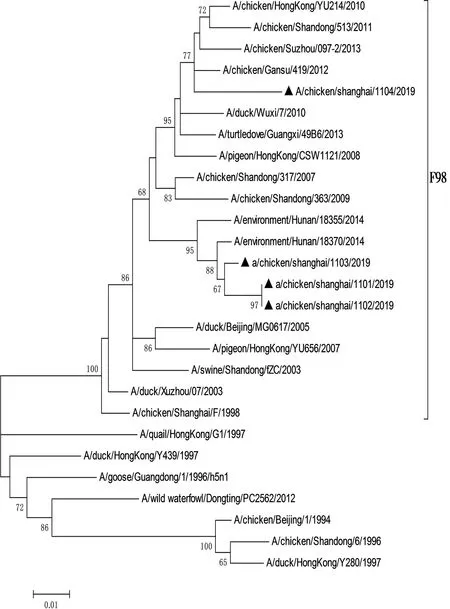
圖3 4株H9N2亞型禽流感病毒NP基因節段的基因進化樹

圖4 4株H9N2亞型禽流感病毒PA基因節段的基因進化樹

圖5 4株H9N2亞型禽流感病毒M基因節段的基因進化樹

圖6 4株H9N2亞型禽流感病毒NS基因節段的基因進化樹

圖7 4株H9N2亞型禽流感病毒PB1基因節段的基因進化樹
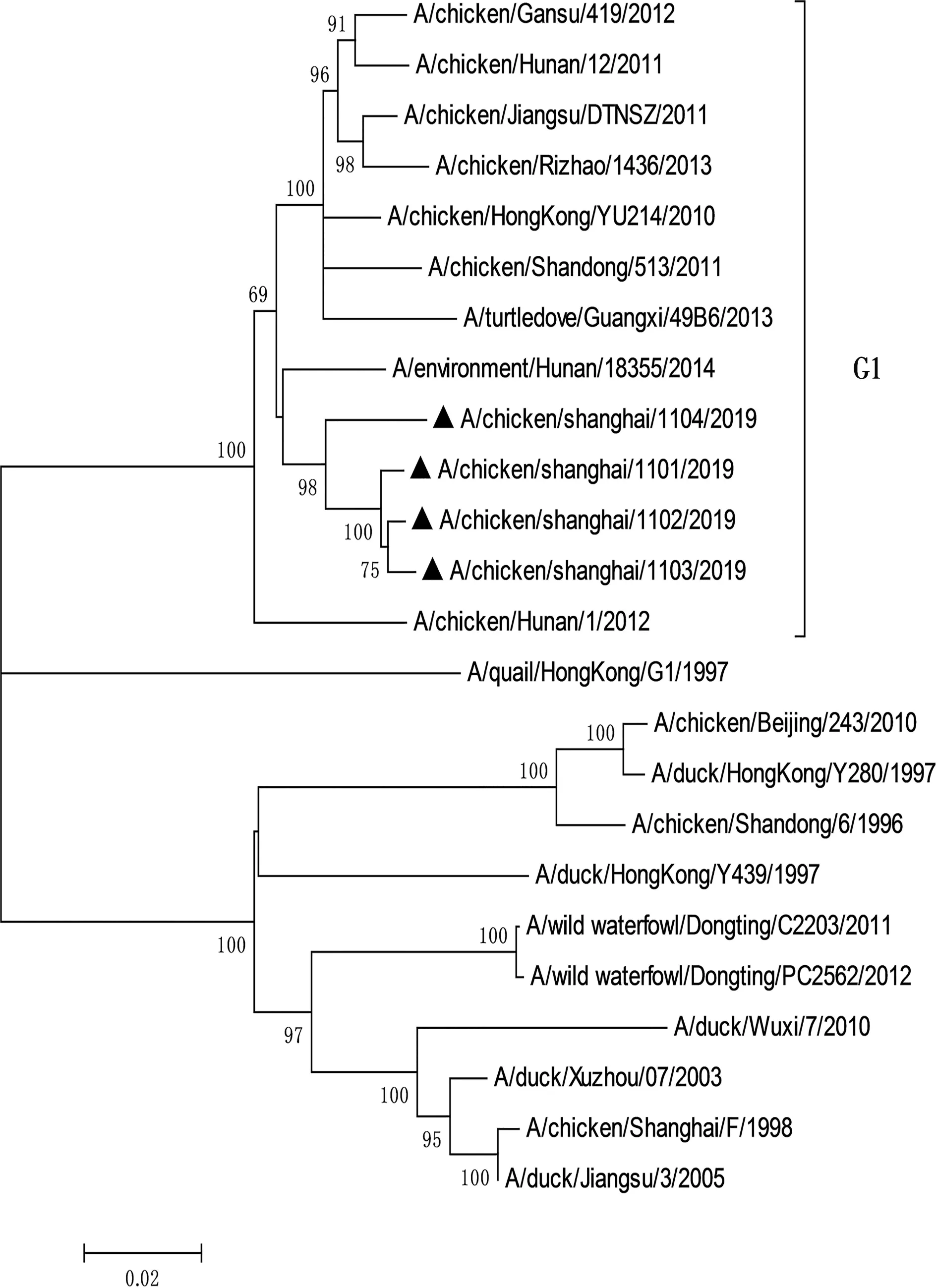
圖8 4株H9N2亞型禽流感病毒PB2基因節段的基因進化樹
2.3 4株H9N2禽流感病毒適應性增強的分子特征分析
表2顯示了已知的影響禽流感病毒致病性的氨基酸突變,這4個毒株的HA裂解位點均為PSRSSR/GLF。這4株HA基因含有3個共同的氨基酸突變和1個只有A/Chicken/ Shanghai/1103/2019發生的突變,3個共同的突變分別為:155位為T,248位為D以及226位為L,A/Chicken/ Shanghai/1103/2019毒株在158位突變為N;這4株病毒分別為 PB2基因上588位為V,在PB1-F2縮短為90 aa以及622位突變為G;PA基因的63位和356位突變為I和R,均為全長PA-X;NP基因上105位氨基酸突變為V;M1基因上43位氨基酸突變為M;M2的31位突變為N;在NS1的42位突變為S,在NS1的149位突變為A。
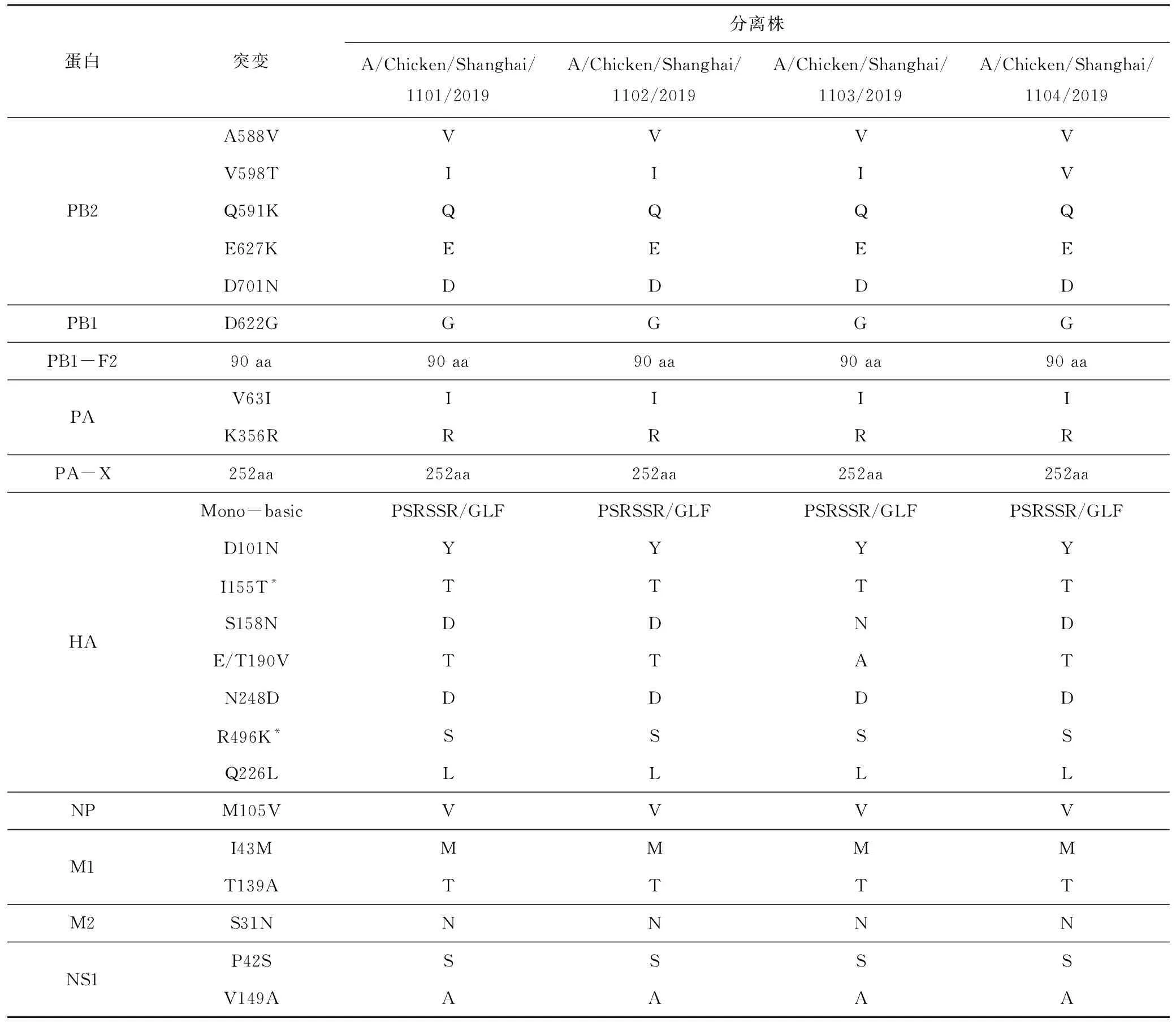
表2 4株H9N2流感病毒基因上與增強病毒適應性相關的氨基酸突變
2.4 H9N2流感病毒與目前使用的疫苗株同源性比較
根據已報道的33個抗原位點[15],這4株病毒與2株疫苗株(A/Chicken/Shandong/6/96和A/Chicken/Shanghai/F/98)最多有18個抗原位點的差異(表3)。這4株病毒和目前國內使用的疫苗A/chicken/Shandong/6/96 (6/96)和A/chicken/Shanghai/F/98 (F/98)核苷酸和氨基酸同源性分別為88.4%~89.1%和88.9%~92.0%。
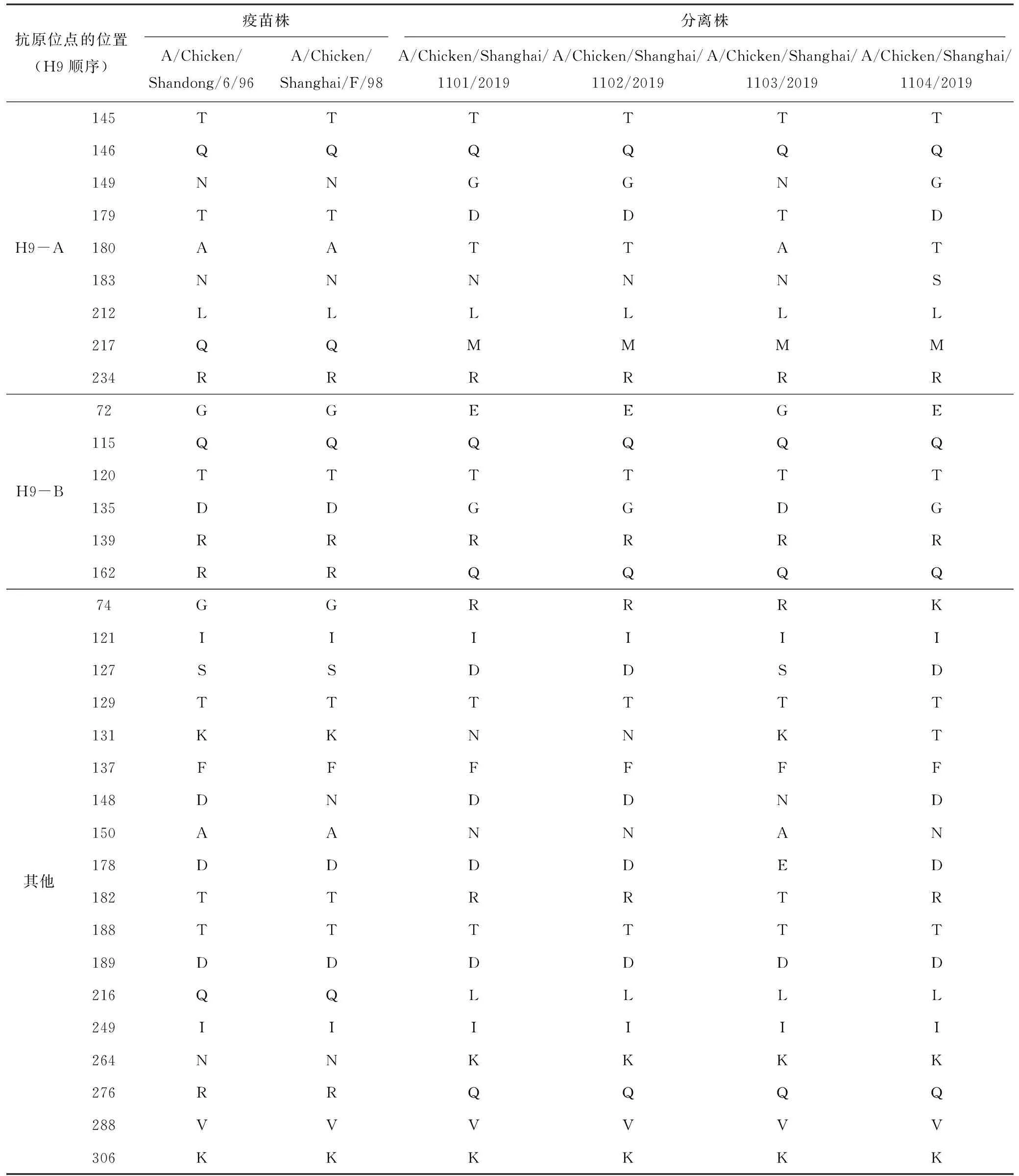
表3 4株H9N2流感病毒與2株疫苗株HA上抗原位點比較
3 討論
近年來發現,H9N2亞型AIV是可以感染人的新型H7N9亞型AIV內部基因的供體,這一發現使得H9N2亞型AIV 成為公共安全的潛在威脅。因此,探究病毒演化過程中基因的變化對掌握病毒流行規律具有重要意義。目前國內流行的H9N2亞型AIV的HA、NA雖然以CK/Bei-like分支基因型為主,但其內部基因經常被其他分支的基因節段所取代,出現越來越多的重組基因型。Pu等[11]研究表明,G57在2007年出現,其流行率在2009年劇增,并自2010年后在中國占主導地位。本研究分離的4株H9N2亞型AIV均屬于G57。G57在雞群中適應性增強部分是由于獲得了G1系的M和PB2基因,這些基因增加了禽流感病毒的聚合酶活性、復制能力以及毒力[15]。分子分析表明這4株病毒含有多個適應哺乳動物的氨基酸位點,這4株病毒均含有Q226L的突變,從而明顯增加H9流感病毒與人Sia-α-2,6-唾液酸受體的結合,增強禽流感病毒在豚鼠間的傳播[15]。H9N2流感病毒的6個內部基因也存在一些突變,導致在哺乳動物中復制能力和毒力增強,雖然PB2基因上并未發現流感病毒適應哺乳動物的2個位點E627K和D701N,但是4個毒株均含有A588V,該位點能增強哺乳動物和禽細胞系上H7N9和H9N2聚合酶活性和復制能力,從而增強AIV在哺乳動物上的毒力。自從2013年以來,全球范圍內攜有A588V的H9N2以及H7N9病毒已經明顯增加[15]。禽群的免疫以及生物安全程序能有效減少AIV的傳播,從而減少了人群暴露感染的風險。目前我國使用的2種疫苗株A/chicken/Shandong/6/96(6/96)和A/chicken/Shanghai/F/98(F/98)均為90年代的毒株,由于抗原漂移,H9亞型禽流感疫苗的有效性持續降低。本試驗中的4株病毒與上述2種疫苗株最多有18個抗原位點差異,這種變異與疫苗有效性的降低是否有關還需進一步評估。總之,H9N2流感病毒在上海市活禽市場的持續流行提示,應進一步加強流感病毒的監測和預警。

