多組分超分子藥物水凝膠的構建及其用于滅血吸蟲尾蚴藥物緩釋研究
胡小濤 李海龍 譚 悅
(1.贛南師范大學化學化工學院,江西 贛州 341000;2.江西潤澤藥業有限公司,江西 贛州 341000)
血吸蟲病廣泛存在于熱帶、亞熱帶地區,感染該病后死亡人數已超過2.8萬人,是一種嚴重危害人類健康的傳染病。現今,世界衛生組織(WHO)已將該傳染病列為易復發傳染病[1],尾蚴期是血吸蟲生命周期中唯一的感染期。目前,已報道了一些可用于預防控制和殺死水面尾蚴的藥物,例如氯硝柳胺,吡喹酮等[2]。但是,這些藥物在水中的溶解性差、價格昂貴、滅尾蚴時間短,難以大面積使用。因此,提高載藥量和藥時特性對防治血吸蟲病具有重要意義。
1 水凝膠簡介
水凝膠具有優異的物理化學性能,其三維空間結構可作為細胞、藥物吸收和釋放的基質材料,且具有良好的生物相容性[3-6]。因此,它在組織工程、藥物釋放和細胞三維培養等方面具有重要的應用前景[7-11]。水凝膠的主要驅動力為分子間氫鍵、范德華力、π-π堆積作用、積作用、金屬配位作用、主客體相互作用和離子相互作用。它具有分子間相互作用能力強、合成工作量相對較小等優點。
水凝膠分為單組分凝膠和多組分凝膠,單組分凝膠是由溶液中的凝膠因子通過非共價鍵相互作用驅動產生的凝膠化物質,多組分凝膠是由兩個或兩個以上凝膠因子之間通過非共價鍵相互作用自組裝形成的具有三維網絡結構的穩定組分。
低分子凝膠是在溶液中通過各種非共價鍵作用力自組裝形成三維網絡結構的半固態材料。其經常表現出對外界環境如溫度、光照、pH等的響應,在分子水平上構造和修飾低分子凝膠的化學結構以及在納米尺度上調控低分子凝膠的自組裝結構并不復雜。它還具有良好的高響應性和可修飾性,在藥物釋放、組織工程和細胞培養等領域顯示出巨大的潛力。此外,低分子凝膠的發展還受到機械強度的限制。
2 凝膠因子介紹
氨基酸是一種生物相容性好、易修飾的化合物。通過對其羥基、羧基和酰胺基的官能團進行修飾,引入結構片段,進一步獲得反應位點。氨基酸衍生物作為一種低分子凝膠劑,是利用C=O和N-H氫鍵自組裝而成的穩定水凝膠優良材料,是最具特色的生化材料之一,在細胞培養、藥物釋放和生物醫學成像等方面有著廣泛的應用。NAAPD是由天冬氨酸與3,4,9,10-花四羧酸酐在一定條件下反應生成的,NAAPD的結構表明,它由兩部分組成:具有顯著的π-π堆積能力的苝和在凝膠化過程中作為氫鍵供體和受體的末端羧基。
石墨烯(GO)是一種新型的碳族單層二維納米材料(其結構如圖1)。大量的研究者對其深感興趣,故掀起了一股GO的研究熱潮[12]。石墨烯是一種由碳正環己烷構成的二維納米材料,GO表面含有許多可修飾的含氧官能團,具有良好的水溶性和生物相容性。目前,GO在基因轉移方面取得了優異的成果,具有載藥、生物成像和光熱療法等功能。近年來,由于GO具有較高的比表面積、多個含氧官能團以及良好的生物相容性等優點,關于GO的報道越來越多,GO在藥物傳遞中也得到了相當大的關注。在載藥和釋藥方面表現出來的機械性能也是極其重要的,多個含氧官能團導致碳正環已烷的排列不均勻,因此,設計分子來修飾GO使其作為藥物載體材料是提高GO力學性能的一種方法。Wan等人用小分子自組裝法制備了環氧石墨烯,結果表明材料的力學性能得到了顯著改善[13]。
因此,本研究設計了N,N-天冬氨酸-3,4,9,10四羧酸二亞胺(NAAPD)作為目標分子修飾石墨烯(GO),以獲得NAAPD/GO雙組分超分子水凝膠,得到其優異的力學性能。本文利用氨基酸衍生物通過自組裝行為構建水凝膠,分別探討其力學性能、藥物釋放過程和防治血吸蟲病的能力,通過光譜和顯微鏡技術測定或表征了水凝膠的化學組成和結構。
3 實驗細節
3.1 合成方法
NAAPD和GO的合成分別參考Li等人[14]和Hummers等人[15]的詳細方法,NMD的合成則使用本實驗室之前報道過的方法進行[16]。
3.2 傅里葉紅外光譜
在室溫下,在AVATAR 360 FT-IR分光光度計(美國威斯康星州麥迪遜市Nicolet)上使用KBr片進行FT-IR光譜分析。
3.3 凝膠的掃描特性
將水凝膠滴在圓柱形銅基片的平面上制備掃描電鏡樣品,通過掃描電子顯微鏡(FEI,QUANTA 450,Hillsboro,OR,USA)在加速電壓為20.0 kV的情況下觀察樣品的形態。
3.4 流變性質
通過冷凍干燥將新制的水凝膠干燥3小時,之后使用MSP-1S磁控濺射鍍膜機(日本東京)對樣品進行鍍金處理,再使用板直徑為35 mm 的HAAKE RheoStress 6000流變儀(德國奧芬堡)測量其流變特性。在25℃下,0.01~10hz范圍內對新形成的水凝膠進行頻率掃描測量。應變振幅設置為1%,時間掃描測量的頻率設置為6.28rads-1,應變為30%。
3.5 X射線衍射分析
在Bruker-D8聚焦衍射儀上,用CuKα射線衍射儀對干燥后的有機凝膠進行了小角X射線衍射(SA-XRD)分析。
3.6 核磁共振
在室溫下,在400 MHz的ULTRASHIELD 400(Bruker,Zürich,Switzerland)光譜儀上記錄了核磁共振譜(NMR)。
3.7 凝膠化研究
對NAAPD和GO在復合溶液(THF/H2O=1/1)中的凝膠化進行了研究。為了制備不同NAAPD/GO摩爾比的水凝膠體系,在玻璃管中稱取大量NAAPD和GO,加入0.5mL四氫呋喃(THF)后加入相當量的二次蒸餾水,在室溫下超聲振動6h。結果表明,在1/1摩爾比下,NAAPD/GO水凝膠體系能穩定形成,管內倒置時不流動;還發現該體系的最小凝膠濃度為4.0%(w/v)。以氯硝柳胺衍生物(NMD)為控釋劑,考察了該控釋體系的釋藥性能;為了考察載藥量,將不同質量的NMD以1/1的摩爾比加入1ml的NAAPD/GO水凝膠(THF/H2O=1:1)中。然后,在室溫下超聲處理6h。通過觀察水凝膠的形成,研究了這種超分子水凝膠材料的最大載藥量。通過體外釋放試驗,從96孔玻璃板中取出300μL的溶液,在不同的釋放時間(依次為1h、2h、5h、24h、200h)。在錐形瓶中從水面采集日本血吸蟲尾蚴,在強光照射下浸泡2h,在不同的釋放時間,將感染的日本血吸蟲尾蚴從孔中取出,每隔30min用生物顯微鏡觀察尾蚴活性。
4 結果與討論
4.1 NAAPD、GO和NMD的化學式
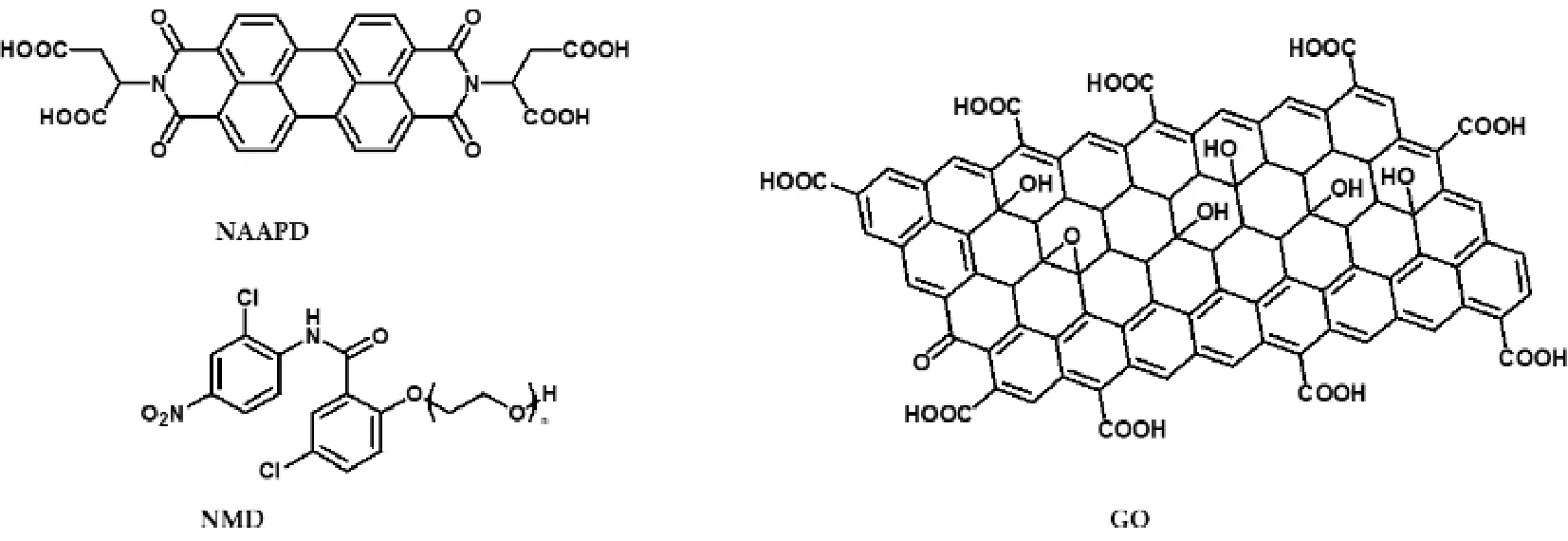
圖1 N,N-天冬氨酸-3,4,9,10-四羧酸二亞胺(NAAPD)、氧化石墨烯(GO)和氯硝柳胺衍生物(NMD)的化學結構
眾所周知,化學式是對化合物性質的初步認識。NAAPD、GO和NMD的化學式如圖1所示,NAAPD的結構中心是一個大的苝烯,左右兩個天冬氨酸殘基。由于石墨烯基部和邊緣含氧基團的存在,GO在水和極性有機溶劑中具有高度分散性。花烯被吸引到具有多個苯環結構和GO結構的m-m堆積鍵上,NAAPD具有良好的生物相容性和親水性,可以通過氫鍵參與凝膠化過程。通過試驗,利用普通試管,在復合溶液(THF/H2O=1/1)中測定了化合物NAAPD和GO的凝膠能力。
4.2 NAAPD/GO水凝膠的表征
水凝膠的照片如圖2a所示。為了深入研究水凝膠的性質,我們將水凝膠冷凍干燥,然后通過掃描電鏡觀察。發現該水凝膠具有三維網絡結構,并與層狀結構交聯,圖2b顯示了該水凝膠具有良好的載藥性能與空間結構,能夠承載添加的藥物。

圖2 (a)水凝膠的照片;(b)NAAPD/GO樣品的SEM圖像;(c)NAAPD/GO的AFM圖像及其厚度直方圖
原子力顯微鏡(AFM)是表面形貌領域的一種重要儀器,利用熱解石墨HOPG原子力顯微鏡研究了NAAPD/GO的顯微結構。NAAPD/GO的AFM圖像及其厚度直方圖如圖2c所示,NAAPD/GO呈層狀結構,平均表面粗糙度為0.9nm。其結構與凝膠的層狀結構SEM圖像一致,NAAPD強烈地被排列有序的GO表面所吸引,水凝膠作為藥物載體材料具有優良的力學性能。結果表明,GO和NAAPD在一定的厚度范圍內形成了穩定的結構。
紅外光譜是研究水凝膠分子間作用力的一種非常有效的方法。為了進一步了解水凝膠的性質,對凍干水凝膠進行了紅外分析。圖3a中的酰胺基形成氫鍵,其吸收峰從3458cm-1移動到3428cm-1。酰胺基形成氫鍵是NAAPD和GO自組裝水凝膠形成的主要驅動力,使NAAPD與GO交聯形成三維層狀結構。
X射線衍射(XRD)是利用X射線衍射分析粉末材料的衍射圖樣,獲得材料成分、材料內部原子或分子的結構或形態等信息的研究方法。圖3b中加入NAAPD后在10度之間有兩個較強的吸收峰,說明水凝膠排列有序。水凝膠是由有序排列的m-m堆積作用形成的,這說明水凝膠在藥物載體材料方面具有良好的性能。
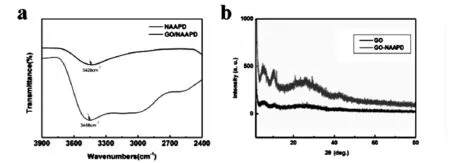

圖3 (a)2400-3900 cm-1之間的紅外吸收光譜,代表N-H拉伸帶的變化;(b)GO和NAAPD/GO干凝膠的X射線衍射圖譜;(c)濃度為4.0%(w/v)的NAAPD/GO水凝膠的應變掃描;(d)濃度為4.0%(w/v)的NAAPD/GO水凝膠的動態儲能模量(G′)和損耗模量(G″)的頻率依賴性濃度。
力學性能是衡量水凝膠性質的重要物理量,通常用流變儀測量,如水凝膠的線性粘彈性應變掃描響應所示(圖3c),在6.28 rad s-1下,在0.1Pa到100Pa的振幅下,儲能模量G′保持在大于損耗模量G″的狀態,這表明水凝膠是一種粘彈性材料,圖3d為水凝膠在4.0%(w/v)濃度下的動態儲能模量和損耗模量的頻率依賴關系。所有的G′都在G″以上,兩者之間的差異基本上沒有變化,這表明該水凝膠具有良好的穩定性。G′隨頻率的增加而略有下降,表明該水凝膠對外部剪切具有良好的耐受性。這些研究證實了NAAPD/GO形成的是穩定的水凝膠,并顯示出優良的力學性能,該水凝膠可作為藥物載體材料用于藥物釋放。
4.3 NAAPD/GO/NMD水凝膠的表征
作為一種新型載藥材料,水凝膠呈現出令人驚訝的三維網狀層狀結構。在此基礎上,自發地對水凝膠進行了載藥性能的測試。在不破壞凝膠形成的情況下,1mL NAAPD/GO水凝膠(4%w/v)在1/1摩爾比下可達到600mg最大載藥量,如圖4a所示。如圖4b所示,與未載藥水凝膠相比,載藥水凝膠具有更致密的三維網絡結構,是一種穩定的結構。結果表明,藥物在水凝膠材料表面有較強的吸附。

圖4 (a)NAAPD/GO水凝膠的照片;(b)樣品的掃描電鏡圖像;(c)NAAPD/GO水凝膠在4.0%(w/v)濃度下的應變掃描;(d)NAAPD/GO水凝膠在0.1%應變下的頻率掃描。
流變儀還測量了超分子載藥水凝膠的力學性能。儲能模量曲線高于損耗模量曲線,但隨著應力的增大而突然減弱,表明水凝膠的三維網絡結構已失去交聯(圖4c)。如圖4d所示,儲能模量大于損耗模量,兩條曲線始終保持直線趨勢,說明載藥水凝膠具有良好的彈性和穩定性。這意味著水凝膠在給藥后仍具有良好的力學性能,是一種優良的藥物載體。
4.4 藥物釋放研究
水凝膠在藥物傳遞領域取得了許多優異的成果。研究中,在NAAPD/GO水凝膠體系中,水凝膠的最大負載量達到了600mg。在500μL水和500μL四氫呋喃(THF)溶液中加入20mg NAAPD和20mg GO。這是NMD在326.5nm處紫外可見分光光度計的標準曲線匹配圖(圖5a)。用于藥物釋放實驗中NMD濃度的計算。在圖5b中,水凝膠的藥物釋放在前10天的破裂速率快速增加,表明載體水凝膠能夠在水中釋放藥物,達到治療血吸蟲病的效果。在Li等人的基礎上進行了抗藥性實驗,明確表明尾蚴在半小時內NMD釋放量達10%以上。藥物釋放率隨時間逐漸降低,64天后達到最大值。因此,該水凝膠的釋藥性能可維持60天,并在早期具有快速釋藥性能。
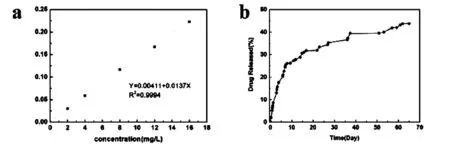
圖5 (a)氯硝柳胺衍生物在326.5nm處紫外吸收標準曲線;(b)載藥后NAAPD/GO水凝膠在25℃水中的累積釋放
所有實驗至少分三次進行。

圖6 NAAPD/GO/NMD水凝膠緩釋水溶液抗尾蚴實驗(25℃)的日本血吸蟲尾蚴死亡率
對該藥物緩釋系統體外抗尾蚴能力進行了實驗研究。從圖6可以看出,96孔玻璃板在1小時的死亡率為7.5%,3小時后死亡率達到92.5%,甚至2小時釋放水的死亡率也可以達到100%。可見,NAAPD/GO/NMD水凝膠體系對水體表面具有良好的抗尾蚴活性。
5 結論
低分子水凝膠具有良好的高響應性和可修飾性,在生物醫學領域有著廣泛的應用。同時,低分子水凝膠由于力學性能差而表現出不穩定性,這一問題成為低分子水凝膠發展的關鍵。
本文設計了一種力學性能優良的雙組分水凝膠(NAAPD/GO)用于在水溶液中的藥物釋放,水凝膠的主要驅動力是氫鍵和m-T堆積相互作用,NAAPD的-COOH與GO表面含氧官能團形成氫鍵。通過NAAPD與GO分子間交聯,水凝膠呈現出三維網狀結構和層狀結構。發現該水凝膠具有良好的機械強度和較大的抗血吸蟲病藥物載藥量,水凝膠流變數值達到104Pa,超過了我們所知的正常低分子水凝膠流變數值(103Pa)。在1ml水凝膠體系中(20mg NAAPD/20mg GO),水凝膠載藥量可達600mg。通過抗尾蚴試驗,NAAPD/GO/NMD水凝膠能持續快速殺滅水中尾蚴,釋放時間超過2個月。
這項工作為不同需求的尾蚴防治提供了更大的可能性,藥物分子設計有望成為材料領域的新方向。

