無創(chuàng)血糖檢測(cè)技術(shù)的發(fā)展
韋 哲 張秉璽 石恒兵 趙 剛 王能才
糖尿病是世界三大慢性病之一,國(guó)際糖尿病聯(lián)盟的最新數(shù)據(jù)顯示,截至2019年,全球約有4.63億成年人患有糖尿病,并且到2030年這一數(shù)據(jù)可能增長(zhǎng)為5.78億。我國(guó)是擁有糖尿病患者數(shù)量最多的國(guó)家,約有1.16億成年患者,極大危害了國(guó)民健康[1]。糖尿病初期患者并無明顯不適,但如血糖長(zhǎng)期處在較高值,人體器官及組織會(huì)受到不可逆的損傷,出現(xiàn)并發(fā)癥。據(jù)統(tǒng)計(jì),在高收入國(guó)家,糖尿病是導(dǎo)致心血管疾病、失明和下肢截至的主要原因。目前的醫(yī)療手段無法根治糖尿病,只能從一定程度上進(jìn)行控制和緩解。血糖監(jiān)測(cè)、飲食治療、運(yùn)動(dòng)治療、藥物治療及糖尿病宣傳教育是糖尿病現(xiàn)代治療手段的五架馬車,血糖監(jiān)測(cè)是其中的重中之重,能對(duì)患者病情判斷和治療方法的選擇提供重要依據(jù)。通過闡述血糖檢測(cè)發(fā)展過程,分析有創(chuàng)檢測(cè)、微創(chuàng)檢測(cè)及光學(xué)無創(chuàng)血糖檢測(cè)方法的基本原理、測(cè)量?jī)?yōu)勢(shì)及存在的問題等,證明光學(xué)法的應(yīng)用潛力,使無創(chuàng)血糖檢測(cè)在未來有可能實(shí)現(xiàn)臨床應(yīng)用,并指出未來需從提高測(cè)量系統(tǒng)信噪比及消除背景干擾等方面展開研究。
1 血糖有創(chuàng)檢測(cè)
個(gè)體監(jiān)護(hù)的血糖測(cè)量方法多種多樣,根據(jù)測(cè)量時(shí)對(duì)人體造成的損傷程度,可分為有創(chuàng)檢測(cè)、微創(chuàng)檢測(cè)及無創(chuàng)檢測(cè),血糖檢測(cè)技術(shù)分類架構(gòu)見圖1。
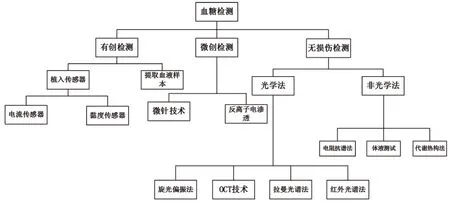
圖1 血糖檢測(cè)技術(shù)分類架構(gòu)圖
有創(chuàng)檢測(cè)是傳統(tǒng)的檢測(cè)方法,分為皮下植入傳感器法和靜脈血管采血法,可獲取精度較高的血糖濃度,但多次采血會(huì)對(duì)患者造成較大傷害,引發(fā)患者抵抗情緒。
1.1 第一代葡萄糖生物傳感器
Clark等[2]于1962年設(shè)計(jì)出第一代葡萄糖生物傳感器,其原理利用了葡萄糖氧化酶可使葡萄糖氧化為葡萄糖內(nèi)酯,并產(chǎn)生過氧化氫的化學(xué)反應(yīng)。根據(jù)氧氣濃度的下降量及過氧化氫的釋放量可間接計(jì)算出葡萄糖濃度。此過程中,氧氣為電子的受體,但由于其濃度遠(yuǎn)低于測(cè)量的葡萄糖濃度,會(huì)導(dǎo)致測(cè)量出現(xiàn)誤差。
1.2 第二代葡萄糖生物傳感器
針對(duì)上述缺陷,第二代傳感器的設(shè)計(jì)中,氧氣被鐵氰化鉀所取代。檢測(cè)裝置分為工作電極和參考電極,其中工作電極設(shè)計(jì)為網(wǎng)狀結(jié)構(gòu),先將碳電極壓在聚酰亞胺底板上,再將葡萄糖氧化酶、鐵氰化鉀、穩(wěn)定劑及連接劑以一定比例配成溶液涂在電極上并使其變干。葡萄糖氧化酶可氧化葡萄糖生成蛋白結(jié)合性載體,鐵氰化鉀起著酶與電極間的電子傳遞作用,穩(wěn)定劑和連接劑可使混合溶液化學(xué)平衡,防止其分解,參考電極則不含有葡萄糖氧化酶。工作電極與血液接觸一定時(shí)間后,在兩個(gè)電極間加上約300 mV的電位差,工作電極中產(chǎn)生的蛋白結(jié)合性載體可將鐵氰化物變成亞鐵氰化物,參考電極中鐵氰化物則會(huì)直接還原成亞鐵氰化物的反應(yīng),此時(shí)電極間的電流與血糖濃度成正比。
第二代葡萄糖傳感器的出現(xiàn)方便了血糖的自我監(jiān)測(cè),使用者刺破手指采集血液,通過測(cè)試試紙和血糖儀進(jìn)行體外分析,克服了第一代葡萄糖生物傳感器的響應(yīng)特性差和干擾大等缺點(diǎn),是目前市場(chǎng)上使用最廣泛的自我監(jiān)測(cè)方式[3]。
1.3 第三代葡萄糖生物傳感器
第三代葡萄糖生物傳感器為皮下植入式,該傳感器同樣利用葡萄糖氧化酶的基本原理。該植入式血糖監(jiān)測(cè)系統(tǒng)可提供定期的血糖水平讀數(shù),但由于傳感器漂移等,高達(dá)21%的監(jiān)測(cè)數(shù)據(jù)不準(zhǔn)確,需要通過手指刺穿的方法定期重新校準(zhǔn)設(shè)備[4]。如美國(guó)雅培公司生產(chǎn)的植入式血糖監(jiān)測(cè)儀,每1~5 min可提供一次實(shí)時(shí)測(cè)量,但每?jī)芍苄枰匦滦?zhǔn)一次。
2 血糖微創(chuàng)檢測(cè)
血液及周圍的血管組織易通過組織間液的擴(kuò)散交換生物分析物和小分子。因此,組織液中含有許多臨床標(biāo)志物,具有重要的醫(yī)學(xué)診斷潛力。微針法及反向離子電滲透法均利用組織液來測(cè)量血糖濃度。
2.1 微針法
Jina等[5]利用微針及微針列技術(shù)設(shè)計(jì)開發(fā)了一種葡萄糖傳感貼片,該裝置被設(shè)計(jì)為兩個(gè)隔間:第一個(gè)隔間包含微針陣列及葡萄糖生物傳感器,使提取的組織液在此發(fā)生反應(yīng)生成過氧化氫;第二個(gè)隔間的工作電極可測(cè)量過氧化氫濃度,從而獲得葡萄濃度。微針的長(zhǎng)度較短,無法到達(dá)真皮層,可減少對(duì)真皮層毛細(xì)血管和神經(jīng)末梢的損傷,也可避免汗液污染。實(shí)驗(yàn)表明,該裝置可成功運(yùn)行72 h,但其必須每天通過手指刺入的方法重新校準(zhǔn),同時(shí)由于血液中的成分被動(dòng)擴(kuò)散到組織間液中需要17 min左右,所以測(cè)定的血糖值也有一定延遲。
2.2 反向離子電滲透法
反向離子電滲透法利用被測(cè)皮膚區(qū)域所施加的一小束電流,使組織液中的氯離子和鈉離子在電勢(shì)差作用下分別向正負(fù)極移動(dòng),形成凈離子流,中性的葡萄糖分子在力下遷移透過水凝膠經(jīng)皮膚析出,可被傳感器測(cè)量到。該方法缺點(diǎn)為抗干擾能力差,極易受溫度及汗液等外界因素影響,并且較為刺激使用者,其原理見圖2。
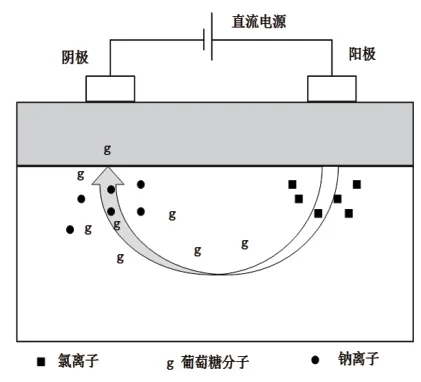
圖2 反向離子電滲透原理示圖
3 血糖無創(chuàng)檢測(cè)
無創(chuàng)血糖檢測(cè)根據(jù)所利用的信息載體的區(qū)別,可分為光學(xué)法和非光學(xué)法。
3.1 光學(xué)法
光作為檢測(cè)介質(zhì)不但可反映被測(cè)物質(zhì)的光學(xué)特性、濃度及組織結(jié)構(gòu)等信息,還具有快速便捷等特點(diǎn),因此光學(xué)法是目前無創(chuàng)血糖檢測(cè)的熱門研究方向[6]。常見的光學(xué)法有旋光偏振法、光學(xué)相干斷層成像法、拉曼光譜法、近紅外光譜法、中紅外光譜法、熒光法及光聲光譜法等。其中,熒光法和光聲光譜法在無創(chuàng)測(cè)量血糖中有一定可行性,但測(cè)量時(shí)無法消除環(huán)境及組織等背景干擾,局限性較大,故主要介紹其他5種可行性較強(qiáng)的光學(xué)法。
3.1.1 旋光偏振法
旋光偏振法即利用物質(zhì)旋光性質(zhì)推斷濃度的方法[7]。葡萄糖為手性分子,具有穩(wěn)定旋光特性。當(dāng)平面偏振光通過葡萄糖分子后,振動(dòng)平面會(huì)發(fā)生旋轉(zhuǎn),偏振角的大小與葡萄糖濃度呈線性關(guān)系[8]。旋光度(ψ)可計(jì)算為公式1:

式中aλ為波長(zhǎng)為λ下的旋光系數(shù),單位為dm-1(g/L);l為光程,單位為dm;c為溶液的濃度,單位為g/L。
旋光法的測(cè)量部位一般為眼前房,缺點(diǎn)明顯:①測(cè)量時(shí)移動(dòng)眼球?qū)⒃斐奢^大誤差;②在1 cm光程和1 mg/dL血糖濃度的變化情況下,偏振角的變化<0.00004弧度,測(cè)量難度大;③測(cè)量值反映眼房水的葡萄糖濃度,與真實(shí)血糖值相比存在滯后性。
3.1.2 光學(xué)相干斷層掃描法
光學(xué)相干斷層掃描(optical coherence tomography,OCT)法首先利用耦合器將光源分為兩路,入射到待測(cè)樣品和參考反射鏡上,并將其反射的光匯入耦合器中,相互干涉合成相干光,最后由探測(cè)器采集[9]。真皮組織的散射系數(shù)會(huì)因葡萄糖濃度的變化而改變,利用這一現(xiàn)象可檢測(cè)出微血管中的血糖值。光學(xué)相干斷層成像法原理見圖3。

圖3 光學(xué)相干斷層成像法原理示圖
OCT技術(shù)的優(yōu)點(diǎn)為可檢測(cè)到高信噪比的信號(hào),缺點(diǎn)為個(gè)體的移動(dòng)和體溫變化均會(huì)產(chǎn)生測(cè)量誤差,其他生理成分的變化也會(huì)引起散射系數(shù)改變,因此OCT技術(shù)還需進(jìn)一步研究以解決上述缺點(diǎn)[10]。
3.1.3 拉曼光譜法
1928年,印度物理學(xué)家C.V.拉曼首次提出拉曼光散射效應(yīng),入射光和被測(cè)分子碰撞時(shí)會(huì)產(chǎn)生拉曼散射和瑞利散射,兩者頻率之差即為拉曼位移。拉曼位移與被測(cè)分子的振動(dòng)頻率和所處的級(jí)能有關(guān),可用來分析分子的振動(dòng)信息,見圖4[11]。
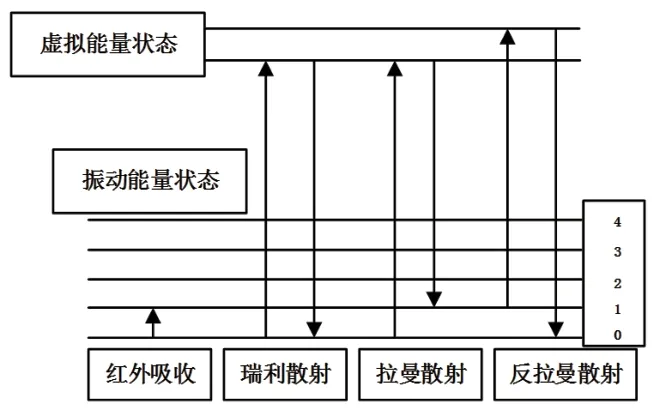
圖4 拉曼光譜法位能示圖
拉曼光譜譜峰清晰,受水的影響較少,Shao等[12]將血紅蛋白濃度作為參考值對(duì)血糖值進(jìn)行預(yù)測(cè),證實(shí)拉曼光譜法可用于血糖的無損傷檢測(cè)。拉曼光譜法缺點(diǎn)明顯,其信號(hào)微弱,易受干擾,并且一般選擇眼前房作為測(cè)量部位,因此光強(qiáng)需足夠小,不能對(duì)眼部造成傷害,降低了信噪比。
3.1.4 近紅外光譜法
紅外光譜法的理論基礎(chǔ)為朗伯比爾定律[13]。當(dāng)用波長(zhǎng)700~2500 nm的近紅外光照射人體時(shí),會(huì)發(fā)生散射和透射現(xiàn)象,用傳感器接收經(jīng)過人體的光譜,其中包含葡萄糖的C-H、N-H及O-H等含氫基團(tuán)振動(dòng)的合頻及倍頻吸收信息,利用化學(xué)計(jì)量分析技術(shù),可建立光譜數(shù)據(jù)及血糖值的數(shù)學(xué)模型,實(shí)現(xiàn)血糖的無創(chuàng)檢測(cè)[14]。
近紅外光譜法的測(cè)量方式可分為透射法和反射法[15]。透射法一般選擇組織較薄但微血管豐富的部位,如指尖和耳垂,檢測(cè)器和光源位于檢測(cè)部位兩側(cè),光程即為組織厚度;反射法的檢測(cè)部位一般為組織層較薄且血管分布較淺的部位,如小臂內(nèi)測(cè),檢測(cè)器和光源處在同側(cè),光程與徑向檢測(cè)距離有關(guān)。目前利用近紅外光譜法測(cè)量血糖濃度的研究取得許多突破性進(jìn)展。Maruo等[16]在一位糖尿病患者身上做實(shí)驗(yàn),通過反射法得到了真皮組織的血糖濃度,預(yù)測(cè)血糖值與真實(shí)血糖值間的相關(guān)系數(shù)達(dá)0.928;李剛等[17]提出的基于近紅外光譜的動(dòng)態(tài)光譜法,可有效減弱個(gè)體差異和測(cè)量環(huán)境對(duì)結(jié)果造成的干擾,提高了血糖預(yù)測(cè)精度;徐可欣等[18]利用近紅外雙光路系統(tǒng)搭建了無損傷血糖檢測(cè)模型,預(yù)測(cè)誤差在0.456 mmol/L以內(nèi)。近紅外光譜法檢測(cè)原理流程見圖5。
3.1.5 中紅外光譜法

圖5 近紅外光譜法檢測(cè)原理示圖
中紅外光譜法的檢測(cè)原理與近紅外光譜法相同,其波長(zhǎng)范圍2500~25000 nm。在此波長(zhǎng)范圍內(nèi),葡萄糖分子的吸收特性更集中,檢測(cè)時(shí)不易受到其他成分干擾,更易提取葡萄糖分子的吸光信息[19]。但中紅外光的穿透性差,且水分吸收強(qiáng)烈,僅能滲入最表層的皮膚,測(cè)量時(shí)僅能采用反射法,易受外界干擾,因此目前基于中紅外光譜法的無創(chuàng)血糖檢測(cè)的研究相對(duì)較少。
3.2 非光學(xué)法
非光學(xué)法包括人體體液法、電阻抗譜法和代謝熱重構(gòu)法。人體體液法即通過檢測(cè)易獲取的生物體液中葡萄糖濃度來近似估計(jì)血糖值[20]。電阻抗譜法是根據(jù)人體組織和器官生理狀況相關(guān)的電特性信息測(cè)定血糖值[21]。新陳代謝熱量重構(gòu)法為通過檢測(cè)人體消耗葡萄糖前后熱量的變化,實(shí)現(xiàn)血糖的無創(chuàng)檢測(cè)[13]。
4 展望
糖尿病檢測(cè)的方法可分為有創(chuàng)、微創(chuàng)及無創(chuàng)檢測(cè),由于患者需要頻繁測(cè)量血糖,有創(chuàng)及微創(chuàng)檢測(cè)會(huì)帶來身體和心理上的痛苦,故無創(chuàng)血糖檢測(cè)具有重要的應(yīng)用價(jià)值和市場(chǎng)前景。光學(xué)法是目前無創(chuàng)檢測(cè)血糖的熱門方向,具有測(cè)量精度低及可重復(fù)性差等缺點(diǎn),需從提高測(cè)量系統(tǒng)信噪比及消除背景干擾等方面入手。未來,隨著檢測(cè)精度的提升,無創(chuàng)血糖檢測(cè)技術(shù)有望真正普及。
- 中國(guó)醫(yī)學(xué)裝備的其它文章
- 飛利浦智能柵控微劑量診療系統(tǒng)R90讓新生兒科消化道造影不再兩難
- 神舟方艙CT、移動(dòng)CT助力醫(yī)院抗疫
- 個(gè)性化護(hù)理在重癥肺炎高熱驚厥小兒護(hù)理中的臨床意義研究
——評(píng)《新型冠狀病毒肺炎重癥護(hù)理手冊(cè)》 - 急性心肌梗死患者院前急救的護(hù)理價(jià)值
——評(píng)《解讀歐洲急性心肌梗死治療指南2018》 - 《中國(guó)醫(yī)學(xué)裝備》雜志社加入中國(guó)知網(wǎng)(CNKI)學(xué)術(shù)期刊優(yōu)先數(shù)字出版平臺(tái)
- 輸液泵的故障分析與風(fēng)險(xiǎn)控制

