鹽酸美金剛的合成改進
蘇 旭,閆 晗,谷成玉,吳茂江,闕日明
(1.張家港九力新材料科技有限公司,江蘇 蘇州 215625;2.山東凱威爾新材料有限公司,山東 淄博 255400;3.上海亞虹醫藥科技有限公司,上海 浦東 201206)
中國已經毫無懸念早早進入了老齡化社會。各種數據和預測顯示2020年中國老齡人口將達到2.55億,占比18%,超過聯合國關于老齡化社會的標準。困擾老年人最主要的問題是失能,約占老齡人口的20%,其中主要疾病為老年性癡呆或者阿爾茲海默(AD)疾病。到目前為止,科學家尚未找到有效根治該疾病的藥物,只能控制癥狀和疾病進展。在有限的對癥治療的藥物中,美金剛處于非常重要的地位,是首屈一指治療AD癥狀的藥物。
鹽酸美金剛是由德國Merz公司研制的癡呆癥治療藥物,是一種新型、低中度親和力、電壓依賴、非競爭性N-甲基-D-天冬氨酸(NMDA)受體拮抗藥,可非競爭性阻滯NMDA受體,降低谷氨酸引起的NMDA受體過度興奮,防止細胞凋亡,改善記憶,是新一代改善認知功能的藥物。2002年2月,歐洲專利藥品委員會(CPMP)批準其用于中、重度阿爾茨海默病患者的治療,同年8月在德國上市,2003年10月17日被美國食品與藥品監督管理局(FDA)批準用于治療中、重度阿爾茨海默病患者。進一步的研究表明,鹽酸美金剛對輕、中度阿爾茨海默病患者也有效。2015年FDA又批準了批準美金剛胺/多奈哌齊(Namzaric)復方膠囊,為AD患者又提供了一種選擇。
鹽酸美金剛胺( Memantine Hydrocloride) ,商品名為易倍申,化學名為1-氨基-3,5-二甲基金剛烷鹽酸鹽,關于鹽酸美金剛胺的制備方法,國內文獻報道的主要有以下幾種方法:
( 1) 溴代法[1-2]。即由起始原料1,3-二甲基金剛烷經溴素溴化得到1-溴-3,5-二甲基金剛烷中間體。此中間體通過濃硫酸作用下和乙腈或者尿素等制得中間體N-乙酰美金剛,進一步水解反應制得目標產物。
溴代法的主要問題就在于大量溴素的使用。溴素本身屬于劇毒品,揮發性液體,具有高腐蝕性,對操作者,實驗設備以及車間環境具有極大的損害,應盡量避免使用溴素。且溴化產物不穩定,不利于儲存。
(2)硝化法[3]。即1,3-二甲基金剛烷經通過硫酸硝酸進行硝化得到硝基中間體,然后再還原得到美金剛游離堿,鹽酸成鹽后得到目標產物。
硝化反應屬于危險反應,按照相關要求,需要額外增加安全設施設備,加大了投入和危險性。且硝基還原需要氫化,也是屬于安全隱患比較嚴重的反應。
(3)氯代法[4]。采用AlCl3和叔丁基氯對起始原料進行氯代。此法收率較好,按照文獻報道,總收率可達76%。其問題也不容忽視,AlCl3需要無水條件,且反應過程中釋放出HCl氣體,具有腐蝕性。另外叔丁基氯易于消去形成異丁烯,需要現場制備,增加了操作的難度。此法叔丁基氯本身易發生消去反應,需要不停添加無水三氯化鋁,并且1-氯-3,5-二甲基金剛烷的活性不高,反應轉化困難。整個反應對溫度要求較苛刻,增加了能耗。
(4)乙腈法[5]。文獻報道,乙腈法采用叔丁醇和乙腈通過濃硫酸發生Ritter反應,得到中間體乙酰美金剛胺,再水解制得游離美金剛。
此法避免了各種危險試劑和危險條件,但仍有較嚴重的缺點,需要使用叔丁醇。但是在濃硫酸作用下,會產生異丁烯,既浪費原材料,又有安全隱患。
(5)其他方法。比如甲酰胺法,此法也需要用到濃硝酸和濃硫酸。還有通過N-羥基鄰苯二甲酰亞胺( NHPI) 催化下[6],經濃硝酸硝化得到1-硝基-3,5-二甲基金剛烷。
基于以上分析,我們試圖找到一種既安全環保,又操作便利成本低廉的合成鹽酸美金剛的方法。以乙腈法為主要路線參考,進行反應改進和優化。根據筆者對反應的理解,叔丁醇并不參與反應,其作用可能是作為稀釋劑,控制濃度。
我們嘗試了不添加叔丁醇的情況下,嘗試了反應,發現結果不錯。因此我們確定了以下反應路線:1,3-二甲基金剛烷溶于濃硫酸,滴加乙腈,得到乙酰美金剛胺,高溫下NaOH水解酰胺鍵得到游離美金剛,再經酸化得到目標產品。操作簡便,安全可控,成本降低。總收率可達75%。
1 實驗部分
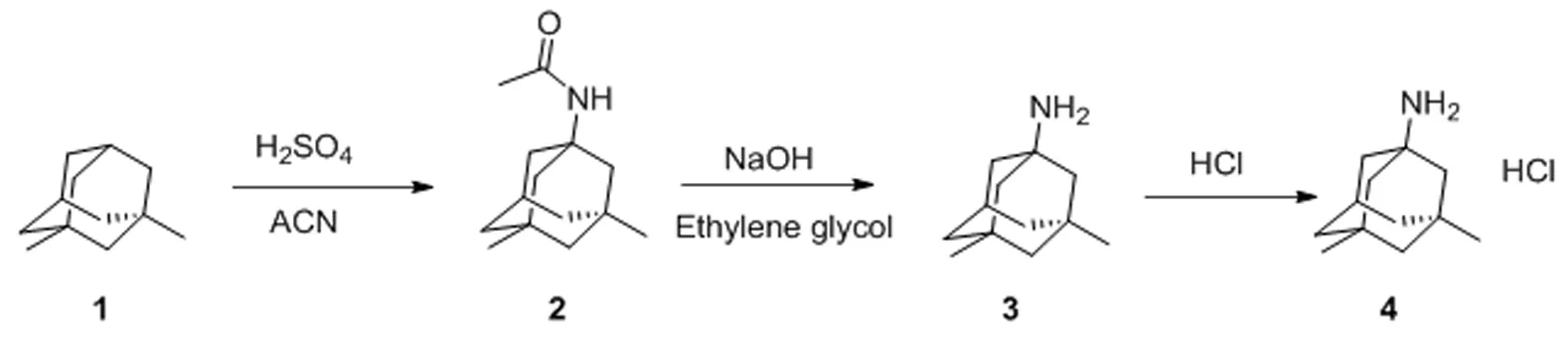
1.1 1-乙酰氨基-3,5-二甲基金剛烷(N-乙酰美金剛,2)的合成
在500 mL的三口燒瓶中,將1,3-二甲基金剛烷(1,國藥集團化學試劑有限公司, 99%, 40 g,0.244 mol )和濃硫酸(235 mL)混合,得到分層無色液體,冰水冷卻到30 ℃以下;攪拌下滴加乙腈(95 g),反應過程中由于放熱劇烈,控制乙腈滴加速度,以保證體系內部溫度不超過75 ℃。
滴加完畢后,形成均相淺黃色液體,控制溫度在60~65 ℃,繼續反應18 h。TLC顯示1已經轉化完畢,冷卻到室溫;將反應液倒入350 mL冰水中,攪拌;DCM萃取(100 mL×3),合并有機相,無水硫酸鈉干燥,濃縮,得白色固體粉末2(51 g,90%),GC純度99%;mp 112~115 ℃;1H NMR ( 400 MHz,DMSO-d6),δ:0.80( s,6H),1.08( s,2H),1.21~1.31 ( m,4H) ,1.51~1.55 ( m,4H) ,1.72 ( m,5H),2.04~2.06 ( m,1H),7.31( s,1H,NH)。
1.2 1-氨基-3,5-二甲基金剛烷鹽酸鹽,(鹽酸美金剛,4)的合成
水解反應:在3 L三口燒瓶內,將N-乙酰美金剛(150 g,0.679 mol )和乙二醇(1500 mL)混合,再依次加入NaOH(150 g,3.75 mol)和水(150 mL),加熱到160 ℃,攪拌反應18 h;冷卻至室溫,倒入到2000 g冰水中。正庚烷1000 mL萃取3次。合并有機相,500 mL水洗滌,無水硫酸鈉干燥,抽濾去除干燥劑得淺灰色溶液,直接用于下一步反應。
成鹽:攪拌下,往上一步反應得到的溶液中滴加濃鹽酸(80 g, 0.79 mol),滴加過程中析出白色固體,直至不再有固體析出;過濾,干燥,得白色固體4(132 g,)132g。兩步收率合并:90%,GC 純度99%;mp 292 ~ 295 ℃。1H NMR (400 MHz, CDCl3),δ: 0.85 ( s,6H),1.07~1.18 ( m,2H) ,1.29( m,4H),1.38~1.46 ( m,4H),1.62(s,2H) ,2.14~2.16(m,1H),7.98( br,3H)。
2 討論
第一步Ritter反應是合成鹽酸美金剛的關鍵步驟,我們考察了乙腈的使用量,反應溫度和時間的影響,優化得到合適的反應條件。
2.1 乙腈用量的考察
乙腈用量的考察見表1。
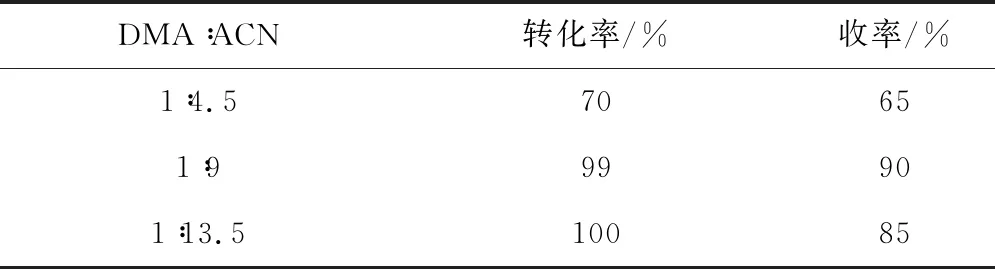
表1 乙腈用量(DMA:CAN)與轉化率及收率的關系
在4.5eq,收率偏低,大于13.5eq沒有明顯提高;純度均大于98%。
2.2 反應溫度的影響
反應溫度的影響見表2。
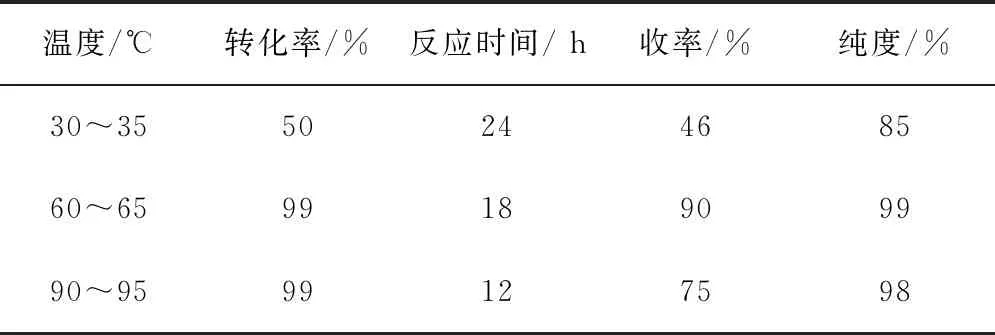
表2 反應溫度、反應時間與轉化率及收率的關系
當溫度較低時,即使反應超過24h,也仍然有大量DMA殘留,并且后處理得到的東西明顯不純,性狀不好。溫度在較高情況下,反應液變成褐色,盡管無原料DMA剩余,但是收率不高,且顏色較深。
2.3 反應時間的影響
反應時間的影響見表3。

表3 反應時間與轉化率及收率的關系
根據2.1和2.2考察優化后的條件,進一步對反應時間進行考察。反應時間在10h,明顯轉化不完全。超過24h,對反應沒有幫助。
第二步酰胺的水解反應需要較高的溫度,單純用水,難以完全轉化。所以我們選擇乙二醇來提高反應體系溫度。反應液經正庚烷萃取,替代甲苯,甲苯有可能造成苯的殘留給質量研究帶來不必要的麻煩。正庚烷溶液無需濃縮,得到的溶液直接進行成鹽反應,可簡化操作,且不影響產品質量。
2.4 可能的機理
通常,金剛烷的參與的Ritter反應,以碳正離子的形式和氰基的氮原子形成共價鍵,在水的作用下,形成酰胺[7]。所以碳正離子的形成,是反應的關鍵。
1,3-二甲基金剛烷和1-羥基-3,5-二甲基金剛烷或1-溴-3,5-二甲基金剛烷不同,并不容易形成碳正離子。我們發現1,3-二甲基金剛烷單獨與濃硫酸或者乙腈并不發生反應,而必須三者混合,且乙腈必須有較大的量,反應才能完全。我們猜測,乙腈除了參與Ritter反應形成酰胺,可能還存在其他作用,于是我們猜測以下機理:
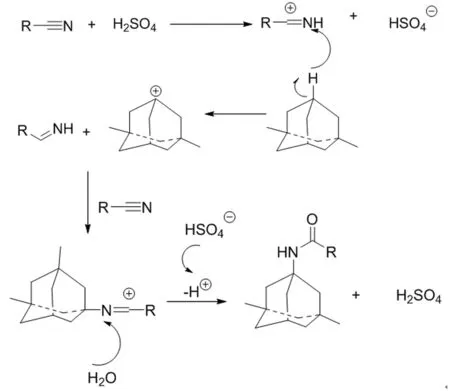
3 結論
本文以1,3-二甲基金剛烷為起始原料,在濃硫酸作用下和乙腈進行Ritter 反應、再通過高溫堿性水解得到游離堿溶液,最后成鹽得到高純度的鹽酸美金剛,產品總收率為82 %,GC 純度≥ 99.9%。對鹽酸美金剛合成工藝進行了系統研究和優化,使反應條件溫和,后處理操作簡便,工藝收率提高,生產成本降低,更易于工業化生產。此改進方法避免了如液溴、濃硝酸等毒劇試劑和易燃易爆等危險反應,具有較大的工業價值和潛在的社會經濟效益。

