外周血ACE基因I/D、AGT基因M235T多態性與妊娠期高血壓疾病的關系
高英,王情,郭紅,賀媛媛,張硯敏
1 寶雞市人民醫院,陜西寶雞721000;2 西京醫院;3 陜西省中醫醫院
妊娠期高血壓疾病(HDCP)是妊娠期常見的并發癥之一,其發病率為5.2%~8.2%[1]。HDCP不僅可導致妊娠期血管功能障礙,還可引起早產、胎兒宮內窘迫、胎兒生長發育受限等,嚴重威脅母嬰安全。迄今為止,HDCP的發病機制仍不完全清楚,可能是環境因素和遺傳因素共同作用的結果[2]。腎素—血管緊張素系統(RAS)是維持機體水電解質平衡、血壓穩定的內分泌系統。血管緊張素轉換酶(ACE)是RAS的關鍵酶,ACE基因第16內含子插入/缺失(I/D)多態性與原發性高血壓的發生密切相關[3-4]。血管緊張素原(AGT)是RAS的重要組成部分,具有血壓調節作用,該基因第2外顯子M235T多態性可影響血液AGT水平,與高血壓發病密切相關[5]。為了明確外周血ACE基因I/D、AGT基因M235T多態性與HDCP的關系,我們進行了如下研究。現報告如下。
1 資料與方法
1.1 臨床資料 選擇2015年2月—2019年12月寶雞市人民醫院收治的HDCP患者200例(觀察組),年齡(29.35±5.12)歲。所有患者符合《婦產科學》(第8版)中關于HDCP的診斷標準[6]。納入標準:①符合HDCP診斷標準;②漢族,本地長期居住;③單胎妊娠;④既往無高血壓、糖尿病病史。排除標準:①合并妊娠期糖尿病、腎炎、肝內膽汁淤積等并發癥者;②合并電解質紊亂者;③合并內分泌疾病、血液或免疫系統疾病者;④妊娠期服用ACE、AGT抑制劑或腎素抑制劑者。同期選擇在寶雞市人民醫院孕檢的健康孕婦200例(對照組),年齡(28.91±5.42)歲。兩組年齡具有可比性。本研究經寶雞市人民醫院醫學倫理委員會批準,所有研究對象知情同意。
1.2 外周血ACE基因I/D、AGT基因M235T多態性檢測 所有研究對象入組后,采集清晨空腹肘靜脈血3 mL,置于含2% EDTA的抗凝管中。取標本100 μL,加入紅細胞裂解液輕輕吹打混勻,冰浴裂解15 min,2 000 r/min離心3 min、離心半徑12 cm,棄上清,加入5% Chelez-100 200 μL充分混勻,56 ℃孵育20 min,2 000 r/min離心2 min、離心半徑12 cm,留取上清液,-20 ℃保存。取上清液60 μL,采用全自動核酸提取儀AU1001及其配套試劑提取DNA,經UV7500雙光束紫外可見分光光度計鑒定,提取的DNA純度、濃度和完整性合格,可用于后續實驗。通過GenBank數據庫查找ACE基因I/D、AGT基因M235T多態性,由上海天昊生物科技有限公司利用Premier5.0軟件設計引物。引物序列:ACE基因I/D上游引物5′-CCGATCTGGCAGAACCTC-3′,下游引物5′-GTGTTCCAGATCGTCTTC-3′;AGT基因M235T上游引物5′-GGTITGTGCAGGGCCTGGCTCT-3′,下游引物5′-AGGGTGCTGTCCACACCTGCTC-3′。按PCR擴增試劑盒說明配制反應體系。擴增條件:94 ℃預變性5 min,94 ℃變性30 s、55 ℃退火30 s、72 ℃延伸30 s共35個循環,最后72 ℃延伸5 min。取上述PCR擴增產物10 μL,用限制性內切酶MboII在37 ℃恒溫水浴鍋中酶切3 h,然后用2%瓊脂糖凝膠電泳分離30 min,溴化乙錠染色,SNaPshot基因分型技術分析ACE基因I/D、AGT基因M235T多態性。
1.3 血清ACE、AGT檢測 采集所有研究對象妊娠20~26周空腹肘靜脈血10 mL,4 ℃ 3 000 r/min離心15 min、離心半徑10 cm,取上層血清,-80 ℃保存。采用全自動酶標儀ELISA法檢測血清ACE、AGT。ELISA試劑盒均購自北京科美東雅生物技術有限公司。
1.4 資料收集與分析 所有研究對象入組后,收集其臨床資料,包括孕前體質量指數(BMI)、被動吸煙例數、高血壓家族史、收縮壓、舒張壓、孕次、產次、TC、TG、肌酐(Cr)等。比較兩組上述臨床資料,將有統計學差異的臨床資料以及外周血ACE基因I/D、AGT基因M235T多態性納入多因素Logistic回歸模型,分析影響HDCP發病的危險因素。
2 結果
2.1 兩組外周血ACE基因I/D、AGT基因M235T多態性分布比較 兩組ACE基因I/D、AGT基因M235T多態性分布均符合Hardy-Weinberg遺傳平衡定律,具有群體代表性。兩組ACE基因I/D基因型分布和等位基因頻率比較差異均有統計學意義(χ2分別為7.071、5.183,P均<0.05),AGT基因M235T基因型分布和等位基因頻率比較差異均有統計學意義(χ2分別為7.925、8.619,P均<0.05)。兩組外周血ACE基因I/D、AGT基因M235T基因型分布和等位基因頻率見表1、2。

表1 兩組ACE基因I/D基因型分布和等位基因頻率

表2 兩組AGT基因M235T基因型分布和等位基因頻率
2.2 HDCP患者外周血ACE基因I/D、AGT基因M235T不同基因型者血清ACE、AGT水平比較 見表3、4。
表3 HDCP患者外周血ACE基因I/D不同基因型者血清ACE、AGT水平比較
表4 HDCP患者外周血AGT基因M235T不同基因型者血清ACE、AGT水平比較
2.3 影響HDCP發病的危險因素分析 觀察組孕前BMI(24.35±4.15)kg/m2,被動吸煙例數45例,有高血壓家族史32例,收縮壓(139.15±8.09)mmHg、舒張壓(76.32±6.12)mmHg,孕次(3.25±1.52)次,產次(2.53±0.61)次,TC(3.95±0.42)mmol/L,TG(1.91±0.35)mmol/L,Cr(13.26±3.26)μmol/L;對照組孕前BMI(21.05±3.02)kg/m2,被動吸煙例數21例,有高血壓家族史10例,收縮壓(116.43±5.03)mmHg、舒張壓(64.83±4.08)mmHg,孕次(3.29±1.53)次,產次(2.03±0.36)次,TC(3.91±0.31)mmol/L,TG(1.88±0.33)mmol/L,Cr(9.65±2.15)μmol/L。觀察組孕前BMI、被動吸煙例數、有高血壓家族史例數、收縮壓、舒張壓、產次、Cr均高于對照組(P均<0.05),而兩組孕次、TC、TG比較差異均無統計學意義(P均>0.05)。
以是否患有HDCP為因變量,以孕前BMI、被動吸煙、高血壓家族史、收縮壓、舒張壓、產次、Cr及外周血ACE基因I/D、AGT基因M235T多態性為自變量,建立多因素Logistic回歸模型。結果顯示,孕前BMI、被動吸煙、產次、ACE基因I/D多態性、AGT基因M235T多態性是HDCP發病的危險因素(P均<0.01),見表5。其中,外周血ACE基因I/D多態性中攜帶DD基因型孕婦罹患HDCP的風險是攜帶II基因型孕婦的1.324倍(95%CI:1.023~2.062,P<0.05),外周血AGT基因M235T多態性中攜帶TT基因型孕婦罹患HDCP的風險是攜帶MM基因型孕婦的1.905倍(95%CI:1.705~2.398,P<0.05)。
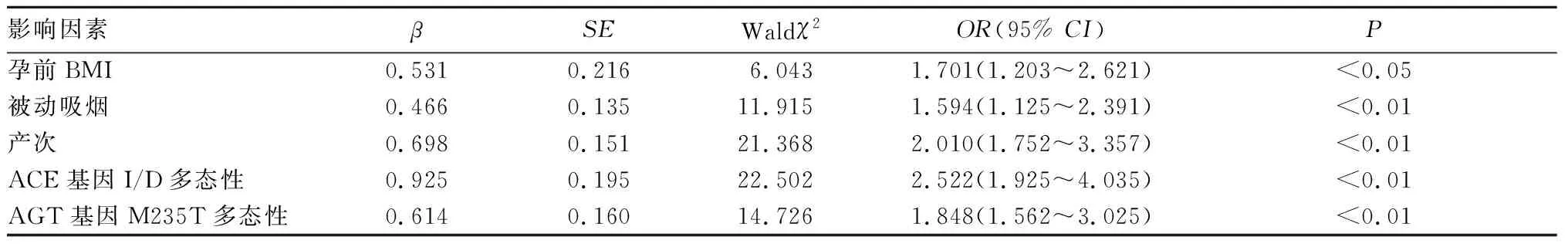
表5 影響HDCP發病的多因素Logistic回歸分析結果
3 討論
HDCP是妊娠期嚴重并發癥之一,以高血壓、蛋白尿、水腫為主要臨床表現。HDCP可導致胎兒宮內發育遲緩、胎兒宮內窘迫、早產等并發癥,還能導致母體腦血管意外、臟器功能衰竭、休克甚至死亡[7]。HDCP是一種遺傳異質性疾病,但其具體發病機制仍不完全清楚。因此,明確HDCP的候選基因對其防治具有重要意義。
RAS是人體內重要的體液調節系統之一,對心血管系統發育、心功能穩態、電解質平衡、血壓調控等均具有重要作用。有研究報道,RAS基因多態性與HDCP患者血壓、24 h壓力負荷動態變化有著密切聯系[8]。ACE、AGT作為RAS的重要組成部分,其基因多態性可能導致HDCP的發病風險升高。ACE是RAS的關鍵酶,可調節血管收縮和血管舒張,維持機體正常血壓。ACE作用產物血管緊張素Ⅱ(AngⅡ)受體是RAS作用于效應器的關鍵成分,可發揮介導血管收縮、水鹽代謝、血管平滑肌增生等生理作用[9,10]。ACE基因定位于人染色體17q23,包括26個外顯子和25個內含子,其第16內含子上有一個287 bp的I/D多態性位點,該位點多態性已被證實與原發性高血壓、頑固性高血壓發病以及運動訓練降壓效果等有關[11-12]。但ACE基因I/D多態性與HDCP關系的報道少見,且其結論存在一定爭議性。AGT是RAS的一種限速底物,經腎素酶催化轉變為血管緊張素Ⅰ(AngⅠ),AngⅠ再經ACE催化生成AngⅡ;AngⅡ通過調節血管收縮,增加醛固酮、去甲腎上腺素水平,促進血管平滑肌細胞增殖、巨噬細胞激活,從而導致動脈粥樣硬化形成和高血壓發生[13]。AGT基因定位于人染色體1q42-43,含5個外顯子和4個內含子,編碼血管緊張素前體多肽。AGT基因目前已發現50多個多態性位點,其中AGT基因2號外顯子704核苷酸處胸腺嘧啶被胞嘧啶代替可導致235號氨基酸由蛋氨酸轉變為蘇氨酸,該位點多態性被認為與高血壓的發病密切相關。有研究報道,AGT基因M235T多態性與心血管疾病、終末期腎病存在一定相關性[14]。ZITOUNI等[15]研究發現,AGT基因M235T多態性能夠增加子癇前期的發病風險,并與子癇前期嚴重程度密切相關。但目前國內鮮有AGT基因M235T多態性與HDCP關系的報道。
本研究兩組外周血ACE基因I/D、AGT基因M235T多態性分布均符合Hardy-Weinberg遺傳平衡定律,具有群體代表性。觀察組外周血ACE基因I/D、AGT基因M235T基因型分布和等位基因頻率與對照組比較均有統計學差異,說明ACE基因I/D、AGT基因M235T多態性可能增加HDCP的發病風險。有研究顯示,ACE基因I/D多態性與全身動脈性高血壓的發病風險增加顯著相關[16]。本研究比較了HDCP患者外周血ACE基因I/D、AGT基因M235T不同基因型者血清ACE、AGT水平差異,結果發現外周血ACE基因I/D DD基因型者血清ACE、AGT水平高于DI、II基因型者,外周血AGT基因M235T TT基因型者血清ACE、AGT水平高于MM、MT基因型者,說明ACE、AGT基因多態性可能影響外周血循環中ACE、AGT水平。進一步研究發現,ACE基因I/D多態性、AGT基因M235T多態性是HDCP發病的危險因素,其中外周血ACE基因I/D多態性中攜帶DD基因型孕婦罹患HDCP的風險是攜帶II基因型孕婦的1.324倍,外周血AGT基因M235T多態性中攜帶TT基因型孕婦罹患HDCP的風險是攜帶MM基因型孕婦的1.905倍。
綜上所述,外周血ACE基因I/D、AGT基因M235T多態性與HDCP的發病有關,攜帶ACE基因I/D DD基因型、AGT基因M235T TT基因型孕婦HDCP的發病風險更高。

