苯硼酸功能化納米金的合成及其對沙丁胺醇的可視化檢測*
賀茂芳,秦 蓓,張 博,胡婭琪,唐一梅,周 慧
(1.西安醫學院 藥學院,陜西 西安 710021;2.西安醫學院 藥物研究所,陜西 西安 710021)
沙丁胺醇(Salbutamol,SAL)是一種人工合成的選擇性β-受體激動劑,可以促進動物體內蛋白質的沉積和脂肪的分解,明顯加快和提高飼料轉化率,提高酮體的瘦肉率,因此被用作畜禽的促生長劑和飼料添加劑[1]。SAL易在人和動物的內臟、器官中殘留,嚴重危害人類的健康[2]。因此,高效、實用的檢測方法對于畜產品安全有著重要意義。目前,SAL的檢測方法主要有高效液相色譜法(HPLC)[3-4]、液相色譜-質譜法(LC-MS)[5-6]、氣相色譜-質譜法(GC-MS)[7]、電泳法(CE)[8-9],免疫分析法[10-11]等。然而,這些方法儀器昂貴,操作復雜,不易推廣普及。
與儀器分析法相比,基于納米金顆粒(Au NPs)的可視化檢測操作簡便、結果直觀,廣泛應用于生物、環境和食品分析。Au NPs可視化檢測的原理為單分散的Au NPs在溶液中呈現酒紅色,當加入被檢測物時,Au NPs表面的功能基團與被檢測物發生反應,引起交聯聚集,從而使顆粒間的等離子體耦合發生改變,吸收峰發生紅移,溶液的顏色由紅色變為紫色或藍色[12]。基于Au NPs的可視化檢測不依賴大型儀器,溶液顏色變化即可作為讀出信號,信號檢出速度較快,成本低廉,適合于現場檢測和不具備大型儀器的場所[13]。
根據硼親和原理,硼酸基在堿性條件下可與1,2-二羥基和1,3-二羥基結合,形成五元或六元環酯,從而實現對順式二羥基化合物的特異性識別[14]。SAL分子中含有1,3-二羥基和氨基,因此,作者首先以檸檬酸三鈉為穩定劑和還原劑制備Au NPs,然后將苯硼酸修飾于Au NPs表面。由于苯硼酸與1,3-二羥基特異性結合,同時,Au NPs表面的羧基與氨基通過靜電吸引力結合,從而拉近Au NPs顆粒之間的距離,引起交聯聚集,Au NPs溶液的顏色由酒紅色轉變為藍色,從而實現對SAL的可視化檢測。該方法簡便快捷,成本低廉,為SAL的檢測提供了新方法。
1 實驗部分
1.1 試劑與儀器
四水合氯金酸:質量分數99%,3-氨基苯硼酸:質量分數98%,N-羥基琥珀酰亞胺(NHS):質量分數99%,1-乙基-(3-二甲基氨基丙基)碳二亞胺鹽酸鹽(EDC):質量分數99%,上海阿拉丁生化科技股份有限公司;SAL標準品:質量分數99%,上海三愛思試劑有限公司;4-巰基苯硼酸:質量分數98%,北京百靈威科技有限公司;檸檬酸三鈉:分析純,國藥化學試劑有限公司。
電子天平:CPA225D,pH計:PB-10,賽多利斯科學儀器有限公司;集熱式恒溫加熱磁力攪拌器:DF-101S,鄭州長城科工貿有限公司;紫外可見分光光度計:Cary-60,安捷倫科技有限公司;透析袋:HT1134-5,Yobios生物科技有限公司;透射電鏡:H-7650,日立科技有限公司。
1.2 實驗方法
1.2.1 苯硼酸功能化納米金(Au@PBA)的制備
1.2.1.1 Au NPs的制備
參照文獻[15],向圓底燒瓶中加入10 mL超純水、92 μLc(氯金酸)=97 mmol/L的溶液,加熱煮沸后,在磁力攪拌下迅速加入1.0 mLc(檸檬酸三鈉)=38.8 mmol/L的溶液,繼續加熱攪拌10 min,可觀察到溶液顏色由淡黃色逐漸轉變為灰色,最終變為酒紅色;停止加熱,待溶液冷卻后轉移至透析袋中用水透析6 h,將得到的Au NPs溶液于4 ℃下避光保存備用。
1.2.1.2 EDC/NHS偶聯法合成Au@PBA
將3.32 mg 3-氨基苯硼酸、2.3 mg NHS溶解于2 mL醋酸-醋酸鈉緩沖液(pH=5.6)中,再加入3.83 mg EDC,45 ℃下反應1 h后,加入10 mL上述Au NPs溶液,調節溶液至pH=7.4,室溫下攪拌反應6 h,將反應液用水透析,直至水中無3-氨基苯硼酸的紫外吸收峰。
1.2.1.3 靜電自組裝法合成Au@PBA
取10 mL Au NPs溶液于小燒杯中,加入0.5 mg 3-氨基苯硼酸,室溫攪拌反應6 h,將反應液轉移至透析袋中用水透析,直至水中無3-氨基苯硼酸的紫外吸收峰。
1.2.1.4 配位共價鍵法合成Au@PBA
取10 mL Au NPs溶液于小燒杯中,用c(NaOH)=0.5 mol/L的溶液調節至pH≈11.0,攪拌下緩慢加入100 μLc(4-巰基苯硼酸)=0.1 mmol/L的溶液,室溫下攪拌反應12 h;將反應液轉移至透析袋中用水透析,直至水中無4-巰基苯硼酸的紫外吸收峰。
1.2.2 標準溶液的配制
稱取0.001 0 g SAL于10 mL容量瓶中,加入c(NH3-NH4Cl)=20 mmol/L緩沖液(pH=8.5)溶解,得到儲備液。使用時,用緩沖液稀釋至所需濃度即可。
1.2.3 檢測方法
將制備好的Au@PBA溶液用NH3-NH4Cl緩沖液(pH=8.5)稀釋10倍,取該溶液900 μL于2 mL離心管中,加入100 μL SAL標準溶液,反應10 min后掃描溶液的吸收光譜,對比SAL加入前后溶液最大吸收波長的變化。
1.2.4 Au@PBA用量的選擇
量取100、200、300 μLρ(SAL)=1.5 μg/mL的標準溶液,分別加入到900、800、700 μLAu@PBA溶液中,10 min后掃描溶液的吸收光譜,計算650與530 nm處吸光度的比值(A650/A530)。改變ρ(SAL)=1.0、0.50 μg/mL,方法同上。對比3種ρ(SAL)下A650/A530值,確定Au@PBA的最佳用量。
1.2.5 標準曲線
取900 μL Au@PBA于2 mL的離心管中,分別加入100 μLρ(SAL)=0.1、0.2、0.5、1.0、1.5 μg/mL的標準溶液(平行5份),反應10 min后,掃描溶液的吸收光譜,計算A650/A530,以A650/A530為縱坐標,ρ(SAL)為橫坐標作圖。
2 結果與討論
2.1 Au@PBA的合成與表征
首先,以檸檬酸三鈉為還原劑和穩定劑,合成了Au NPs;然后采用3種不同的方法向Au NPs表面修飾苯硼酸,得到Au@PBA。在EDC/NHS偶聯法中,Au NPs表面的羧基和3-氨基苯硼酸形成酰胺鍵;自組裝法的原理是Au NPs表面的羧基與3-氨基苯硼酸通過靜電吸引力結合;配位共價鍵法的原理是4-巰基苯硼酸與Au NPs形成金屬配位鍵。通過比較這3種方法所得Au@PBA的穩定性,選擇最佳合成方案。
經過多次的實驗發現,配位共價鍵法合成的Au@PBA溶液放置1 d后由酒紅色變為灰藍色,說明其性質極不穩定,發生了團聚。
EDC/NHS偶聯法和靜電自組裝法合成Au@PBA的紫外可見吸收光譜圖見圖1。
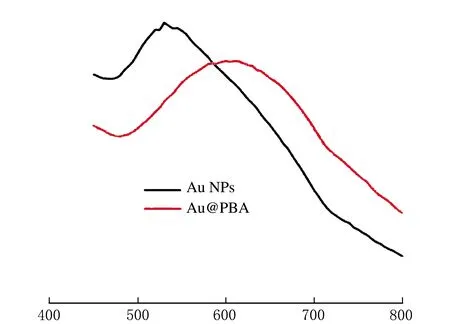
λ/nma EDC/NHS偶聯法
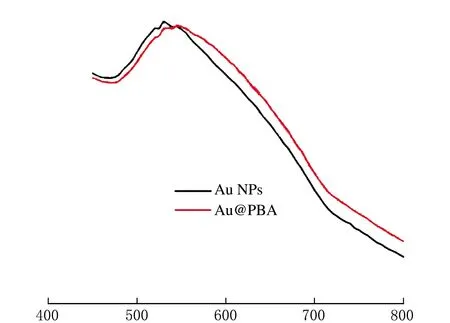
λ/nmb 靜電自組裝法圖1 EDC/NHS偶聯法和靜電自組裝法合成Au@PBA的紫外可見吸收光譜圖
由圖1可知,EDC/NHS偶聯法合成的Au@PBA相比于Au NPs發生了明顯的紅移,其最大吸收波長為610 nm,說明Au@PBA性質不穩定,發生了輕微的團聚;通過靜電自組裝法合成的Au@PBA的最大吸收波長為535 nm,相比于Au NPs幾乎沒有變化,這說明Au@PBA的性質穩定,基本沒有發生團聚。
Au NPs和靜電自組裝法合成的Au@PBA透射電鏡圖見圖2。
由圖2可知,靜電自組裝前的Au NPs粒徑約為15 nm,且分散性好、粒徑均勻;經過3-氨基苯硼酸修飾后,Au@PBA仍然分散良好、未發生團聚,這與紫外吸收光譜的結果一致。因此,選擇靜電自組裝法合成的Au@PBA進行SAL的檢測。

a Au NPs
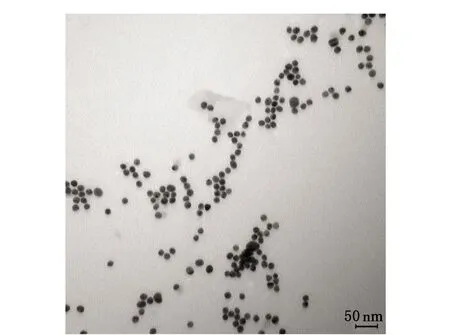
b 靜電自組裝法合成的Au@PBA圖2 Au NPs和靜電自組裝法合成的Au@PBA透射電鏡圖
2.2 Au@PBA對SAL的檢測原理
向900 μL Au@PBA溶液中加入100 μLρ(SAL)=1.5 μg/mL的溶液,反應10 min后,溶液顏色由淺紅色變為深藍色。
向Au@PBA中加入SAL前、后的紫外吸收光譜圖見圖3。

λ/nm圖3 向Au@PBA中加入SAL前、后的紫外吸收光譜圖
由圖3可知,加入SAL后,Au@PBA溶液的最大吸收波長由530 nm紅移至650 nm,這說明SAL與Au@PBA結合,使Au@PBA發生了交聯聚集。
向Au@PBA中加入SAL前、后的透射電鏡圖見圖4。

a 加入SAL前

b 加入SAL后圖4 向Au@PBA中加入SAL前、后的透射電鏡圖
由圖4可知,加入SAL前Au@PBA的分散良好,而加入SAL后Au@PBA發生了明顯的團聚,這一結果與紫外吸收光譜分析一致。
SAL與Au@PBA的結合原理見圖5。
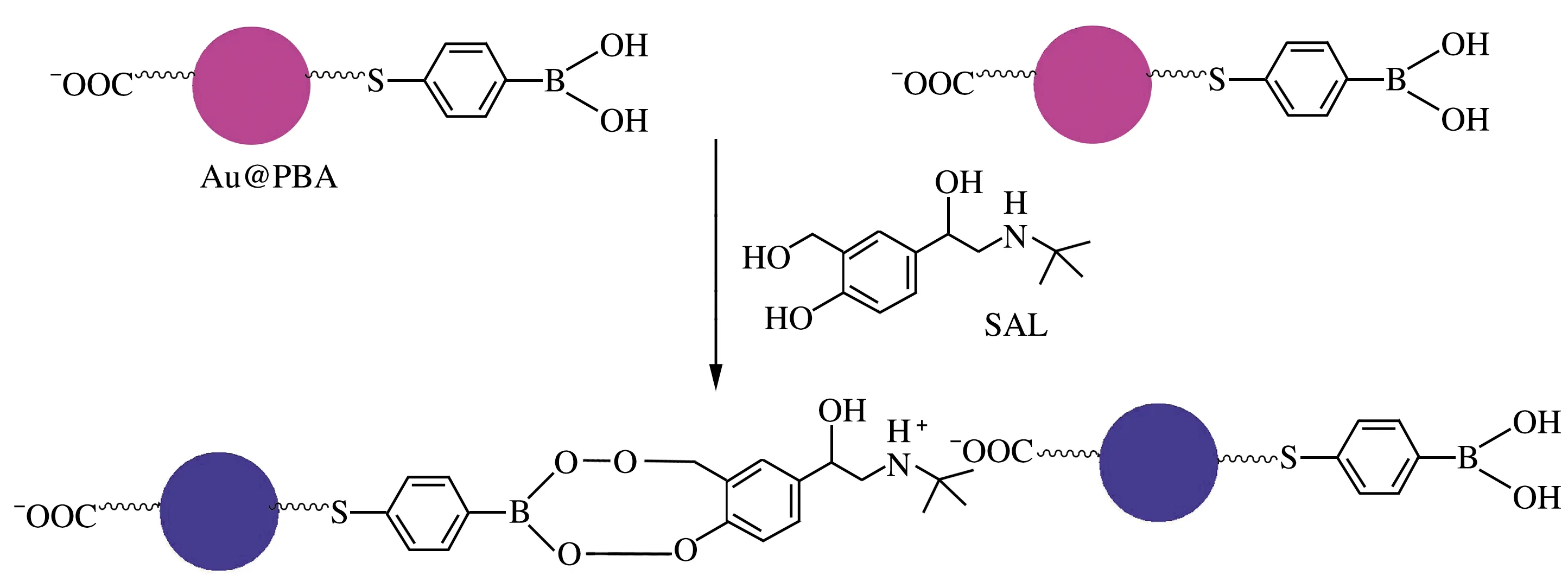
圖5 Au@PBA與SAL結合的示意圖
由圖5可知,SAL分子中含有1,3-二羥基和氨基,可分別與Au@PBA表面的硼酸基和羧基結合,使Au@PBA發生交聯聚集,因而最大吸收波長由530 nm紅移至650 nm,溶液由酒紅色變為深藍色。因此,根據兩波長下吸光度的變化與ρ(SAL)的關系,可實現對SAL的定量檢測。
2.3 Au@PBA用量的選擇
Au@PBA的用量是影響靈敏度的關鍵因素。在ρ(SAL)=0.5、1.0、1.5 μg/mL時,考察了V(Au@PBA)∶V(SAL)對吸光度的影響,結果見圖6。
由圖6可知,V(Au@PBA)∶V(SAL)=9∶1,A650/A530的值最大;并且隨著ρ(SAL)的增大,A650/A530也逐漸增大。因此,選擇V(Au@PBA)∶V(SAL)=9∶1時對SAL進行檢測,可獲得最高的靈敏度。

ρ(SAL)/(μg mL-1)圖6 V(Au@PBA)∶V(SAL)對A650/A530的影響
2.4 標準曲線
將100 μLρ(SAL)=0、0.1、0.2、0.5、1.0、1.5 μg/mL的溶液與900 μL Au@PBA溶液混合(分別記為1、2、3、4、5、6樣品),反應10 min后,可以觀察到溶液顏色變化,結果見圖7。

圖7 不同ρ(SAL)溶液與Au@PBA混合后溶液顏色的變化
由圖7可知,溶液顏色由酒紅變為藍灰色,并且ρ(SAL)越大,藍色越明顯,這是高ρ(SAL)溶液與Au@PBA結合,促使Au@PBA發生交聯聚集的結果。
以A650/A530為縱坐標、ρ(SAL)為橫坐標作圖,得到標準曲線,結果見圖8。
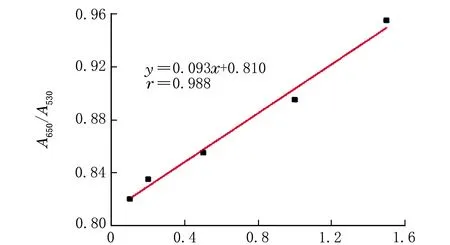
ρ(SAL)/(μg·mL-1)圖8 標準曲線
由圖8可知,線性關系良好,因此可用于對SAL的定量檢測。
3 結 論
對Au@PBA的3種合成方法進行了對比,其中,以檸檬酸三鈉為還原劑和穩定劑合成的Au NPs與3-羧基苯硼酸通過靜電自組裝得到的Au@PBA性質穩定,并成功應用于SAL的檢測。該方法簡便快捷、成本低廉、肉眼可見,并且能在10 min內得到檢測結果,具有良好的實際應用前景。

