碳化法制備擬薄水鋁石的研究進展
王棟斌,鄭峰偉,周 正,陳 凱,金建濤
(武漢科林化工集團有限公司,湖北 武漢 430223)
擬薄水鋁石(AlOOH·nH2O,n=0.08~0.62)也稱勃姆石、一水軟鋁石膠體或準一水軟鋁石,是一種組成復雜、結晶不完善的由無序到有序、弱晶態到晶態的演化系列,典型結構為很薄的褶皺片層[1-5]。擬薄水鋁石(PB)是具有特殊空間網狀結構的氧化鋁水合物,它具有零點電荷和界面吉布斯自由能高、孔隙率大、比表面高、分散性和膠溶性好以及觸變凝膠等優良特性,主要用作制備γ-Al2O3、α-Al2O3的原料和難以成型催化劑或催化劑載體的粘結劑[6-8]。
目前,PB的制備工藝主要有酸法、堿法、醇鋁法、碳化法、雙鋁法、碳酸鋁銨法等[9]。碳化法依托燒結法生產氧化鋁工藝流程,具有無可比擬的優越條件,一是NaAlO2溶液原料易得、質量相對穩定;二是含堿母液可送回氧化鋁生產流程循環利用,基本無廢棄料排出,環境污染小,同時避免了另建蒸發設備造成的額外投資;三是生產成本低廉,生產工藝簡單,產品種類多、質量好[10]。
最初,碳化法制備PB主要是用于生產催化裂化催化劑作分子篩的粘結劑,用來替代進口的SB粉[11]。隨著國內碳化法生產工藝的不斷完善,碳化法擬薄鋁石產品已逐漸用于生產加氫精制、加氫裂化、臨氫降凝、催化重整等催化劑載體,其性能甚至超過了進口產品[12]。本文對碳化法制備擬薄水鋁石的反應機理、成膠過程中的影響因素、老化過程、洗滌過程和干燥過程進行綜述,為尋求生產過程更加環保、成本更加低廉、產品更加完善的技術路線提供新的思路。
1 成膠機理
碳化法制備PB的NaAlO2溶液都含有一定濃度的NaOH,其苛性系數αk=1.4~1.8,溶液具有較高的穩定性,生產條件下很難發生分解反應,而苛性系數αk=1的NaAlO2溶液(即不含自由NaOH)瞬間分解[13]。楊清河等[14]研究發現,在碳化法工藝成膠過程中存在五種反應:NaOH與CO2的快速中和反應、NaAlO2與CO2的中和反應、NaAlO2自發水解反應、Na2CO3與CO2的中和反應以及CO2與生成的水合氧化鋁、Na2CO3的復合反應,即:

(1)

(2)

(3)

(4)

(5)
CO2混合氣通入NaAlO2溶液中,首先進行的是反應(1),生成Na2CO3,降低溶液的穩定性,當溶液苛性系數αk降低到一定的程度時NaAlO2開始分解。反應(2)生成的水合氧化鋁在適當的條件(合適的pH值、溫度等)下經老化、洗滌及干燥后轉化PB。反應(3)生成的水合氧化鋁為三水鋁石雜晶,分子式為β1-Al2O3·3H2O(或者α-Al2O3·3H2O),而且(2)與(3)兩個反應是平行反應。因此碳化法成膠過程中生成的水合氧化鋁究竟是PB,PB與三水鋁石的混合物,還是三水鋁石,取決于(2)、(3)兩個反應的反應速度及程度,這兩個反應的速度主要取決于成膠溫度、CO2濃度和流量等;反應程度主要取決于成膠終點pH值等。
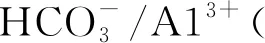
2 制備條件
2.1 NaAlO2溶液濃度
NaAlO2溶液濃度對生成物的類型和晶粒大小都有影響。從燒結法氧化鋁溶礦車間出來的NaAlO2溶液濃度和溫度都較高,一般在100~130 g Al2O3/L,為消除中和反應的放熱量對溶液穩定性的影響,其苛化比控制在0.75~0.85之間最佳,NaAlO2溶液濃度控制在80 g Al2O3/L左右[17]。
文獻[18-20]表明,在碳化法成膠過程中,NaAlO2溶液濃度≤80 g Al2O3/L時,生成的水合氧化鋁以PB為主,并且隨NaAlO2溶液濃度增加,晶粒的尺寸呈減小的趨勢;當NaAlO2溶液濃度低于60 g Al2O3/L,成膠效率低,生產成本高,焙燒后生成的γ-Al2O3孔體積小于0.42 mL/g,目前多用于作為制備催化裂化催化劑的粘結劑。當NaAlO2溶液濃度>80 g Al2O3/L時,晶粒的粒度隨濃度的增加而迅速變大,NaAlO2的水解速率迅速增大,生成物中的三水鋁石含量增加;當NaAlO2溶液濃度為100 g Al2O3/L時,生成物以三水鋁石為主。實驗進一步證明,通過進一步降低終點pH可以克服NaAlO2高溶液濃度下生成三水鋁石的問題,從而提高成膠效率;當把終點pH降低到9.9附近,濃度為100 g Al2O3/L的NaAlO2溶液同樣可以制備不含雜晶的PB,并且焙燒后生成孔體積較高的γ-Al2O3。
2.2 CO2濃度和流量
CO2濃度和流量影響著PB的晶粒大小、晶型結構和結晶度。文獻[14,21]表明,在成膠終點pH值為10.50、成膠溫度較低時,較大的CO2流量及濃度(CO2體積分數≥33%),會導致成膠過程以NaAlO2溶液的中和反應(2)為主,生成的是無定形水合氧化鋁和小晶粒的PB,經老化后轉化為無三水鋁石雜晶且晶粒較大的PB;CO2流量或濃度較低時(CO2體積分數≤25%),即使成膠終點pH值為10.50,由于NaAlO2溶液的中和反應(2)和NaAlO2的水解反應(3)同時進行,老化后的產物為PB與三水鋁石的混合物。而且成膠過程中一旦在較高的pH值下停止通入CO2混合氣,即便特別迅速地將沉淀物與母液分離,都不可避免地導致三水鋁石雜晶的生成。
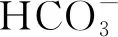
2.3 成膠溫度
成膠溫度對生成物的晶型、結晶度以及晶粒大小有很大的影響。
在成膠過程中,NaAlO2與CO2的中和反應是放熱反應,NaAlO2水解反應是吸熱反應。NaAlO2的水解反應是吸熱反應,因此在較高溫度時反應速度較快[13],生成物是以三水鋁石為主的水合氧化鋁。燒結法生產氧化鋁的“碳酸化分解”就是基于這個原理,即在比較高的溫度(>80 ℃)下,NaAlO2溶液中通入CO2混合氣,制備大晶粒的三水鋁石,以利于電解生成鋁,因此,較高的成膠溫度對擬薄水鋁石的制備不利。
當成膠溫度較低(≤55 ℃)時,生成物水合氧化鋁以PB為主,隨著溫度的逐漸升高,PB的晶粒尺寸和結晶度都呈現出增大的趨勢;當成膠溫度升高到一定程度(≥60 ℃)時,生成物為三水鋁石。進一步研究表明,即使成膠溫度較高(≥60 ℃)時,用純CO2代替CO2混合氣,也能夠抑制NaAlO2溶液水解反應的發生,從而制備出較純的PB[19]。
2.4 成膠終點pH值
成膠終點pH值對生成物的晶型、膠溶指數都有較大的影響,一般來說,控制較高和較低的反應終點,對于PB的晶型都不利,從而影響了它的膠溶性能[24]。
當成膠終點pH值從高至低變化時,生成物類型從三水鋁石變為PB,最后變為PB與絲鈉鋁石的混合物[15]。如果成膠終點pH值較高,生成的水合氧化鋁含有部分甚至全部為三水鋁石,主要因為NaOH與CO2的快速中和反應(1)導致NaAlO2溶液的苛性系數αk降低(≈1.0),未被中和的NaAlO2溶液極其不穩定,迅速發生NaAlO2自發水解反應(3)生成NaOH和三水鋁石,而且在這種條件下生成的小晶粒的PB和無定形水合氧化鋁經老化后部分甚至全部轉化為三水鋁石,并且成膠終點pH值越高,這種轉化就越完全[25],而且成膠過程中一旦生成了三水鋁石,在通常條件下,不能再轉化為PB。
在適當的成膠終點pH值下,成膠過程中NaAlO2溶液的中和反應占絕對優勢,這時NaAlO2轉化比較完全,得到的水和氧化鋁老化后變成PB。
此外,成膠終點pH值較低時,發生式(4)和式(5)所示的反應,生成的水和氧化鋁和CO2、Na2CO3反應生成絲鈉鋁石[15-16]。少量絲鈉鋁石的生成造成產品中Na2O質量分數超標,導致產品孔體積、比表面積均顯著下降。
2.5 老化過程
老化溫度、老化時間、老化提溫速率、老化堿度對產品的最終結構都有較大的影響[26-27]。老化過程就是使成膠過程中生成的絮狀、松散的水合氧化鋁凝膠進一步結晶,使晶粒尺寸長大,并經過脫水收縮使生成物(如無定型水合氧化鋁及小晶粒PB)趨于穩定態(大晶粒PB)的作用。
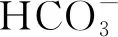
文獻[17,19]認為,隨著老化溫度和老化時間的增加,PB結晶度及晶粒大小迅速增加,但當老化時間進一步增加時,PB的物化性質變化不明顯,基本上趨于平穩;升溫速率快將導致老化后的顆粒變大變粗,過快的話會導致膠溶能力變差。
2.6 洗滌過程
文獻[17,30]認為,老化后的沉淀物以膠體形式存在于溶液中,膠體粒子自身帶有電荷,外層吸附了大量的堿金屬離子,膠體粒子之間也包裹著大量的堿金屬離子,而這些雜離子(如Na+)對PB的晶型結構、晶粒大小以及膠溶能力的控制都有極大的影響,從而可知洗滌工藝過程對產品的性能具有很重要的意義。文獻[19]表明,洗滌具有繼續老化、脫除雜離子兩種作用。洗滌過程尤其是第一次洗滌較大程度地增加了PB的結晶度,對晶粒尺寸大小的控制也有一定的影響。用稀的硝酸溶液和硝酸銨溶液作為洗滌介質,可較大程度地降低沉淀物中雜離子含量,提高洗滌效率,主要原因是式(6)和(7)生成的NaNO3溶解度要比Na2CO3高得多,反應如下:

(6)

(7)
2.7 干燥過程
干燥過程對PB的的顆粒大小、堆積密度、結晶度和膠溶指數有很大的影響,不僅影響催化劑制備工藝,而且對催化劑性能亦有很大影響。
納米顆粒的高表面活性使它們之間易形成一些弱連接而團聚在一起生成尺寸較大的團聚體,但這一般是軟團聚,可以通過機械外力消除;由于Al(OH)3(或AlOOH)沉淀中含有羥基,如果干燥溫度過高,相鄰納米顆粒表面的羥基發生縮聚反應,形成Al-O-Al鍵,沉淀物的孔道收縮,使晶粒形成致密的硬團聚,這種硬團聚難以消除而且不可逆[30]。
文獻[19,31]表明,隨著干燥溫度的升高,PB的膠溶指數迅速下降,然而不同干燥溫度下的PB的XRD譜圖并無明顯區別,說明PB的膠溶能力的改變并不是因為晶相發生了轉變。當干燥溫度從60 ℃增加到120 ℃時,膠溶指數從95.3%下降至17.5%。可見,未干燥的Al(OH)3(或AlOOH)濕濾餅中含有水,膠體顆粒表面的羥基和水通過氫鍵產生橋聯,水分子以氫鍵形式吸附在膠體表面,PB的膠溶性能正和這部分水分子有關,當干燥溫度升高至一定程度(>110 ℃)時,這種吸附水開始脫附,膠溶指數也隨著脫附量的增加而降低,當干燥溫度過高時,甚至使之不能膠溶。
3 制備工藝
3.1 傳統間歇中和碳化工藝
目前國內NaAlO2-CO2法制備擬薄水鋁石的工藝仍采用的是間歇中和碳化工藝,生產過程中NaAlO2的pH值隨著時間的推移逐步降低,中和反應生成的沉淀會貫穿整個成膠過程,生成的膠體粒子在漿液中的成核、團聚、長大的時間長短不一,最終形成的產品的晶型結構、晶粒大小、產品的粒度分布都有所不同。而且每一次反應過程中NaAlO2的濃度、CO2濃度和流量、反應的溫度、終點pH值等存在些許偏差,每批次的產品的物化性質存在波動,導致產品存在晶粒尺寸不均勻、孔徑分布彌散、質量不穩定、重現性差的缺點。同時由于間歇中和碳化工藝沒有實現連續化生產,存在設備利用率低,工人勞動強度大,不利于產業的規模化生產[32]。
3.2 連續中和碳化工藝
王晶晶等[32]采用多級串聯式反應器,生產過程中可實現穩定的進料和出料,同時引入用于氣液混合的預溶氣技術,改善CO2混合氣在NaAlO2溶液中的溶解效果。與傳統的鼓泡反應器和間歇釜式反應器的氣液混合方式相比,預溶氣技術同時吸入NaAlO2和CO2混合氣進入設備中,在葉輪的高剪切力場作用下,CO2混合氣被充分打碎,微氣泡的大小只有20~30 μm,氣液充分混合,CO2混合氣在NaAlO2溶液中的溶解基本達到飽和狀態,解決了傳統氣液混合工藝過程中大氣泡翻騰、氣體偏流的問題,預混后的氣液混合物進入后續的多級串聯式反應器后仍然保持良好的氣液溶解效果。實驗結果表明,采用預溶氣-多級串聯式連續碳化法制備出的PB,其各項性能指標均達到或超過目前工業應用的間歇中和碳化工藝生產的PB的性能指標,孔容相近、結晶度相當、且孔徑與粒度分布更為集中,性質均一穩定,具有很好的重復性和再現性,可實現擬薄水鋁石連續規模化生產。
3.3 超重力碳化工藝
超重力技術是一種強化傳質過程的工藝技術,其核心設備是旋轉填料床。利用其強大的離心力場,NaAlO2溶液在高速旋轉的離心力作用下剪切成微小的液滴、液絲和液膜,與CO2混合氣錯流接觸反應,改善了CO2混合氣和NaAlO2溶液間的傳質效果[21]。與傳統的鼓泡反應器和間歇釜式反應器制備技術相比,具有產品純度高、孔徑分布范圍窄、生產效率高、生產成本低、等突出優點。
郭奮等[33]利用超重力碳化工藝制備了直徑為1~10 nm,長度為100~300 nm的纖維狀PB。李友鳳等[28]采用空腔式螺旋型旋轉設備(RBHC),可制得三水氧化鋁雜晶含量低、純度較高、平均粒徑為5~10 nm的纖維狀PB。任曉晶等[21]采用錯流旋轉填料床與碳化法相結合制備了比表面積和孔容分別為322 m2/g、1.826 mL/g的納米級大孔纖維狀γ-Al2O3。研究結果表明,超重力連續碳化法所得產物純度高、孔徑分布均勻、生產效率高,適用于工業放大。
4 結 語
碳化法制備擬薄水鋁石工藝,原料便宜,生產成本低,便于大規模生產,缺點是鐵、硅、鈉雜質較高,含三水鋁石和絲鈉鋁石雜相,晶相純度低,工藝穩定性差,重復性差,不易把握其生產規律。未來碳化法生產PB的研究主要集中在以下幾個方面:(1)繼續探索碳化法制備擬薄水鋁石的成膠機理,積極開展NaAlO2中和反應和水解反應的動力學和熱力學研究,以促進工藝技術的改進;(2)NaAlO2-CO2連續中和碳化工藝是改善PB質量穩定性和重復性差的有效手段,與傳統間歇中和碳化工藝不同,兩者在反應規律上存在差異,需要對其反應機理進行系統的研究;(3)超重力連續碳化工藝,極大地強化了傳質-反應過程,反應時間比傳統攪拌反應器縮短近一半,處理能力6倍以上[34],對該工藝的影響因素需進一步摸索,爭取早日實現工業化應用;(4)PB的制備過程是膠體顆粒的成核、團聚和長大的階段,因此,常伴隨有顆粒的團聚和縮聚現象,導致膠體內部孔徑的變小。成膠過程中加入加入一定量的助劑可以改變擬薄水鋁石的表面性質和孔結構,未來對于助劑在碳化法制備擬薄水鋁石過程中的作用還需進行系統研究。

