肝細(xì)胞癌介入治療術(shù)后并發(fā)腫瘤溶解綜合征的診斷及治療(附9例報告)
王京艷,周霖,余強,王華明
中國人民解放軍總醫(yī)院第五醫(yī)學(xué)中心,北京100039
腫瘤溶解綜合征(Tumor Lysis Syndrome, TLS)是腫瘤細(xì)胞大量溶解,快速釋放細(xì)胞內(nèi)物質(zhì),導(dǎo)致人體發(fā)生代謝異常和電解質(zhì)紊亂[1]。既往報道[1~6],TLS多見于白血病、淋巴瘤、多發(fā)性骨髓瘤等血液系統(tǒng)腫瘤經(jīng)全身化療治療后患者,發(fā)病率高達(dá)25%[7],偶見于生長速度較快或?qū)χ委熋舾械膶嶓w腫瘤患者,如肝臟神經(jīng)內(nèi)分泌腫瘤[8]、肝細(xì)胞癌(Hepatocellular carcinoma ,HCC)[9]等。目前關(guān)于HCC腫瘤介入治療后并發(fā)TLS的相關(guān)報道較少。我們回顧性分析了9例腫瘤介入術(shù)治療合并急性TLS的HCC患者臨床資料,探討TLS的臨床特點、診斷及治療等。
1 臨床資料
選取2013年1月~2019年12月間解放軍總醫(yī)院第五醫(yī)學(xué)中心腫瘤介入治療科收治的HCC患者9例,其中男8例、女1例,年齡43~71歲,平均52歲;24 h尿量1 000~2 000 mL;均經(jīng)病理或影像學(xué)檢查,符合原發(fā)性肝癌的診療規(guī)范明確診斷為HCC;腫瘤直徑(12.59±3.68)cm;8例為慢性乙型病毒性肝炎(CHB);Child-Pugh分級為A級6例、B級3例;5例合并高血壓,1例合并2型糖尿病,1例同時合并高血壓病及2型糖尿病;7例存在門靜脈癌栓(PVTT),其中3例合并右支癌栓,3例合并主干癌栓,1例同時合并主干和右支癌栓;1例出現(xiàn)肺轉(zhuǎn)移,1例出現(xiàn)腹膜后淋巴結(jié)轉(zhuǎn)移瘤。9例患者中,7例接受經(jīng)導(dǎo)管肝動脈化療栓塞術(shù)(Transcatheter hepatic arterial chemoembolization,TACE)治療,1例接受了經(jīng)皮射頻消融(Radiofrequency ablation, RFA)治療,1例接受了肝動脈栓塞(Transcatheter hepatic arterial embolization, TAE)聯(lián)合RFA治療。
術(shù)后第2天,3例患者24 h尿量<400 mL,9例患者血清尿素氮(BUN)、肌酐(CR)、尿酸(UC)、鉀(K)、磷(P)水平均升高,鈣(CA)及甲胎蛋白(AFP)水平明顯降低,確診為TLS,進(jìn)行靜脈補液水化、應(yīng)用利尿劑、糾正電解質(zhì)紊亂、連續(xù)性腎臟替代治療(Continuous renal replacement therapy, CRRT)后,術(shù)后第7天,納入者血清各項指標(biāo)均明顯好轉(zhuǎn)。術(shù)前及術(shù)后第2、7 天時9例患者肝腎功能及電解質(zhì)指標(biāo)水平見表1。
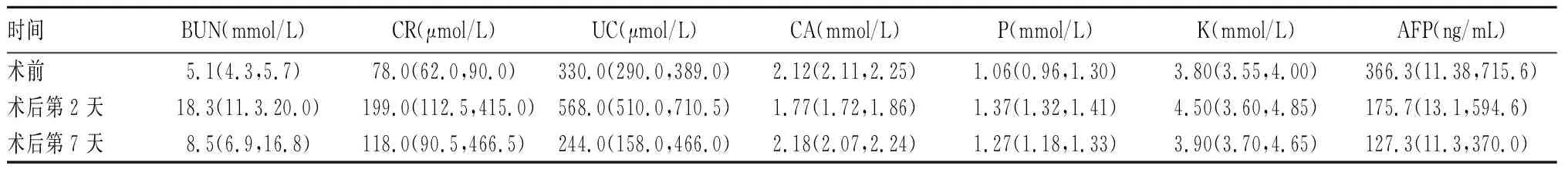
表1 術(shù)前及術(shù)后第2、7 天時9例患者肝腎功能及電解質(zhì)指標(biāo)水平[M(P25,P75)]
9例患者術(shù)后第2、7天血清AFP水平下降,說明腫瘤對治療敏感。其中1例患者術(shù)前腹部增強CT檢查可見肝左右葉交界處可見7.2×4.2 cm巨塊型病灶,有明顯包膜,血供豐富,TAE術(shù)中給以將微導(dǎo)管選擇性置于肝右及肝左動脈腫瘤供血血管處,再次造影腫瘤染色清晰,經(jīng)微導(dǎo)管緩慢漂注超液態(tài)碘化油,術(shù)后即刻行以CT引導(dǎo)下RFA治療,聯(lián)合治療第20天時腹部平掃CT可見腫瘤組織內(nèi)多發(fā)碘油沉積,腫瘤內(nèi)片狀壞死。
2 討論
TLS是指腫瘤負(fù)荷重、對治療極其敏感的惡性腫瘤經(jīng)過化療、放療以及其他診療手段治療后出現(xiàn)的腫瘤組織崩潰溶解,腫瘤細(xì)胞大量破壞,導(dǎo)致細(xì)胞內(nèi)容物快速釋放,引起機體內(nèi)電解質(zhì)紊亂及代謝異常的代謝紊亂[1],主要臨床表現(xiàn)為高鉀血癥、高尿酸血癥、高磷血癥、低鈣血癥,同時伴有腎功能不全及代謝性酸中毒等[2]。由于肝癌細(xì)胞對化療藥物抵抗的特性,HCC并發(fā)TLS的病例比較罕見,既往關(guān)于HCC相關(guān)的TLS有自發(fā)性、TACE治療術(shù)后、RFA術(shù)后、索拉菲尼靶向藥物治療術(shù)后等[9~12]。
TLS是腫瘤科常見的急癥,早發(fā)現(xiàn)、早診斷、早治療有利于降低患者的病死率。HCC患者并發(fā)TLS的高危因素包括:①腫瘤負(fù)荷過重(直徑>10 cm)、生長速度過快導(dǎo)致腫瘤細(xì)胞代謝產(chǎn)物增多,而機體清除代謝產(chǎn)物能力不足;②腫瘤細(xì)胞對化療藥物或抗腫瘤藥物或治療措施敏感,腫瘤細(xì)胞迅速凋亡;③乳酸脫氫酶升高(>2倍參考值上限);④白細(xì)胞計數(shù)升高(>25×109/L)[3,4,13]。TLS的發(fā)病機制是凋亡的腫瘤細(xì)胞釋放大量的核酸物質(zhì)、鉀、磷、細(xì)胞因子等入血,核酸的代謝終產(chǎn)物尿酸增多,超過了腎臟排泄的能力,從而導(dǎo)致這些物質(zhì)在血液中蓄積,并在腎小管沉積造成急性腎功能衰竭;高鉀血癥可能導(dǎo)致嚴(yán)重的低鈣血癥、心律失常;細(xì)胞因子可能造成全身炎癥反應(yīng)綜合征、多器官功能衰竭,進(jìn)而危及患者生命,甚至導(dǎo)致死亡[1,2]。
臨床上TLS多于初始治療后12~72 h出現(xiàn)癥狀,可表現(xiàn)為:①腎功能受損導(dǎo)致的排尿困難、腰痛、血尿、少尿或無尿等;②低鈣導(dǎo)致的惡心、嘔吐、痙攣、抽搐甚至意識障礙;③高鉀所致的心律失常、心悸甚至心跳驟停、猝死等;④體液超負(fù)荷所致的水腫、漿膜腔積液、呼吸困難、心悸等[3,14]。
Cairo等[1]將TLS分為兩種類型:臨床 TLS(clinical TLS,CTLS)和實驗室TLS (laboratory TLS,LTLS)。LTLS 是指在初始化療前3天或化療后7天內(nèi),出現(xiàn)≥2個以下代謝指標(biāo)異常:①血UC≥476 μmol/L(或8 mg/dL)或增高25%基線水平;②血K≥6.0 mmol/L(或6 mg/L)或增高25%基線水平;③(兒童)血P≥2.1 mmol/L,(成人)≥1.45 mmol/L,或增高25%基線水平;④血Ca≤1.75 mmol/L或降低25%基線水平。CTLS是指在LTLS的基礎(chǔ)上,合并≥1個以下臨床表現(xiàn):①血肌酐≥1.5倍經(jīng)年齡校正的正常值上線;②發(fā)生危及生命的心律失常或猝死;③癲癇發(fā)作。
本研究9例患者中,患者腫瘤直徑(12.59±3.68)cm,且均血供豐富,經(jīng)治療后腫瘤細(xì)胞迅速壞死,血清AFP水平迅速降低,故均有發(fā)生TLS的高危因素。其中1例患者于TACE術(shù)后第2~5天出現(xiàn)血肌酐、尿酸、尿素氮升高,合并血鉀、血磷明顯升高,血鈣降低,達(dá)到了LTLS及CTLS的診斷標(biāo)準(zhǔn)。3例行CRRT的患者不同程度合并腹腔積液、感染、肝損傷,1例病死患者合并了肝衰竭、感染性休克、腎功能衰竭等多器官功能衰竭導(dǎo)致了最終死亡。另5例患者因無尿量減少,無急診CRRT指征,經(jīng)過及時的補液水化、糾正電解質(zhì)紊亂、降尿酸等治療后,也逐漸恢復(fù)。
HCC患者發(fā)現(xiàn)腎功能不全時,需將TLS與肝腎綜合征相鑒別,如曾注射造影劑,也需與造影劑腎病相鑒別。三者在發(fā)病機制上完全不同,TLS是由于大量壞死腫瘤組織的代謝產(chǎn)物所致,肝腎綜合征多發(fā)生于合并失代償期肝硬化患者,多合并大量漿膜腔積液,導(dǎo)致腎臟相對血容量不足所致,也可能合并少尿、無尿、腎功能不全、高鉀血癥等,但經(jīng)過補充血容量、白蛋白治療后癥狀可逆[15]。造影劑腎病多于造影劑應(yīng)用48~72 h后發(fā)生,表現(xiàn)為血肌酐升高≥0.3 mg/dL 或較基線值升高≥1.5~1.9倍,可能同時合并少尿、無尿、電解質(zhì)紊亂、皮疹等[16]。三者治療上均需大量補液水化、糾正電解質(zhì)紊亂必要時行CRRT治療,由于初期均有可逆性,故早期發(fā)現(xiàn)、早期診斷、早期治療可大大改善患者的生存質(zhì)量。
一旦發(fā)現(xiàn)TLS明確診斷,要及時干預(yù),在密切監(jiān)測尿量和各項指標(biāo)的同時,給予大量補液、利尿、糾正電解質(zhì)酸堿平衡紊亂、降尿酸(別嘌呤醇及拉布立酶)等[3~5],注意液體出入平衡,必要時可給予CRRT治療,有助于迅速清除體內(nèi)毒素,降低腎臟負(fù)擔(dān),縮短臟器功能恢復(fù)時間,降低死亡率。行CRRT的指征包括:出現(xiàn)無法控制的①嚴(yán)重的少尿(<100 mL/24 h)或無尿(<400 mL/24 h);②持續(xù)性高鉀血癥;③內(nèi)科治療無法改善的高磷血癥誘導(dǎo)的低鈣血癥;④嚴(yán)重酸中毒和/或嚴(yán)重尿毒癥伴中樞神經(jīng)系統(tǒng)毒性;⑤容量過載引起的循環(huán)功能障礙等[1]。本文中9例患者均在術(shù)后第2~5天即明確診斷,及時給以補液、糾正電解質(zhì)紊亂等治療,3例及時給予CRRT治療,治療后尿量增多、血肌酐水平下降,停止CRRT治療后患者尿量仍穩(wěn)定、血肌酐水平仍持續(xù)下降,未發(fā)生嚴(yán)重的心律失常、癲癇等并發(fā)癥,且術(shù)后隨訪,腎功能逐漸恢復(fù)正常水平,并無病情反復(fù)。
綜上所述,對存在腫瘤負(fù)荷重、預(yù)計治療敏感等TLS高危因素的HCC患者,應(yīng)以預(yù)防TLS為主,治療目的應(yīng)該在盡量減少并發(fā)癥或在并發(fā)癥可耐受的前提下實施治療,嚴(yán)禁單純的為了治療而治療,造成本來可以避免的嚴(yán)重并發(fā)癥,不僅增加患者的痛苦及經(jīng)濟壓力,甚至可能加速患者死亡。治療過程中應(yīng)及時監(jiān)測患者的尿量、腎功能、電解質(zhì)等各項指標(biāo),一旦明確診斷TLS,應(yīng)及時補液、堿化尿液、降尿酸、利尿、糾正電解質(zhì)紊亂等,必要時及時行床旁CRRT治療,能大大降低TLS的病死率,提高TLS的治愈率。

