高爐煤氣脫硫凈化工藝的開發
張先茂,王 澤,王天元,金建濤,趙志杰,李興建,王國興
(武漢科林化工集團有限公司,湖北 武漢 430223)
高爐煤氣是煉鋼過程副產的一種氣體,每生產一噸鋼鐵大概有1300~1600 m3高爐煤氣產生[1],除了一部分作為熱源自用或發電外,大部分都作為廢氣排放,做成了很大的資源浪費。高爐煤氣各組分及其含量如表1所示。從表1可以看出高爐煤氣中CO含量約23%,若能有效利用,可以合成甲醇、乙二醇等產品,是一種優質的資源,但高爐煤氣中含有很多的雜質,如硫化物、O2、P、F、As等,其中硫化物不但含量高,而且種類繁多,氧含量也高達1%。硫化物會造成后續催化劑的中毒失活,大量的O2的存在會為下一步CO的分離提純及應用帶來不利影響,因此脫硫凈化是其得到應用的前提。
高爐煤氣脫硫凈化部分目前國內還沒有現成的可借鑒的技術方案,需要開發一套完善的高爐煤氣利用方案,以解決其綜合利用的難題。武漢科林充分發揮自己在煤化工領域脫硫凈化的優勢結合自身豐富的經驗積累,研發出了高爐煤氣脫硫凈化工藝并進行了工業測流實驗。
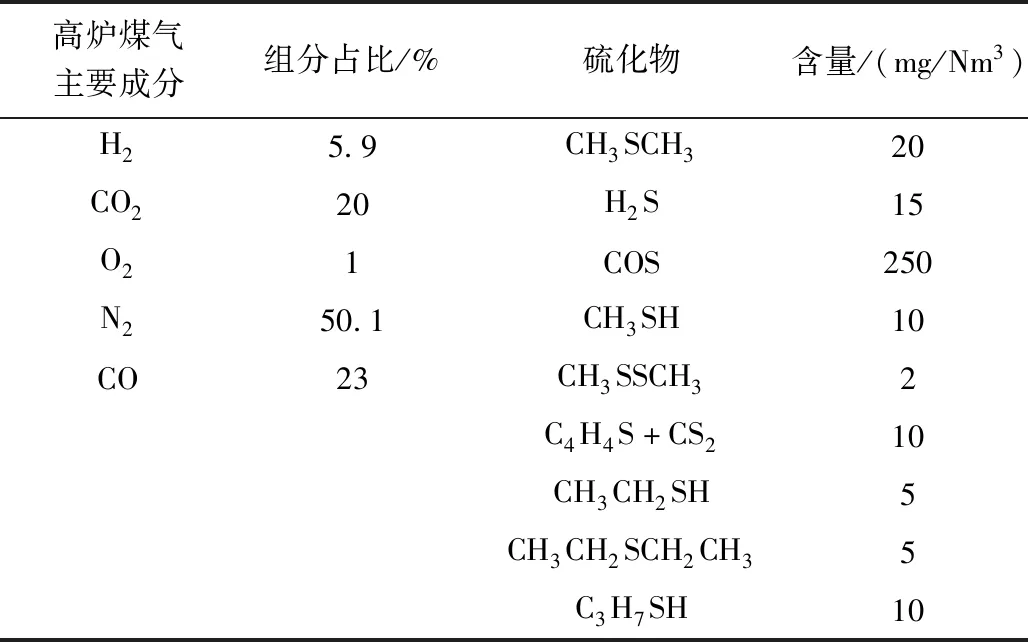
表1 高爐煤氣主要成分及硫化物含量
1 工藝原理
脫硫凈化工藝的重點是脫硫和脫氧,因此工藝的開發也從這兩點入手,以解決高爐煤氣綜合利用的問題。
1.1 脫 硫
由于原料氣中COS含量高達250 mg/Nm3,因此COS的脫除是工藝的重點和難點。COS的脫除一般有水解和氫解兩個方案。氫解即通過加氫的方法把COS轉化為硫化氫,再把產生的硫化氫脫除,從而達到脫COS的目的。化學反應方程式:COS+H2=H2S+CO,該反應需要在Co-Mo或Fe-Mo催化劑的作用下進行,通常在350~400 ℃下進行,會增加能耗,操作費用太高[2],并且催化劑使用前需要硫化,由于原料中含有過高的氧,使用過程不可避免發生反硫化現象,致使活性無法持續,該方法無法用于高爐煤氣脫COS。水解方案是COS在催化劑的作用下與H2O發生反應轉化為H2S。反應方程式:COS+H2O=H2S+CO2,其優勢是反應可以在低溫下進行,60 ℃就能將90%以上的COS的轉化為H2S,升溫雖可以在一定程度上提高的轉化率,但此反應受熱力學控制,溫度越高平衡轉化率越低[3],單次的COS轉化率一般不超過95%,為提高COS的脫除率需要采用多級水解的方式,把一級水解產生的硫化氫脫除,打破水解平衡后,進入二級水解,重新建立新的平衡,如此反復,直至將COS將至小于0.1 mg/Nm3。
1.2 脫 氧
目前,市場上的脫氧劑一般分為兩種,貴金屬催化劑和非貴金屬催化劑。其中貴金屬催化劑以Pd、Pt為主要活性組分,在一定的溫度下,原料氣中的H2、CO等與O2發生反應,該類催化劑具有使用溫度低、空速高、脫氧精度好的特點[4]。但該類催化劑在H2和CO共存時,由于H2及CO的競爭吸附,使用溫度會大幅度升高,一般在150 ℃以上才能將O2脫至小于50 μL/L。另外該催化劑對硫化物很敏感,微量的硫化物就能造成催化劑的永久中毒失活。且貴金屬催化劑價格昂貴,運行成本高,因此該類催化劑不適合高硫含量的高爐煤氣脫氧。
另一類脫氧劑為非貴金屬脫氧劑,該類脫氧劑分為硫化型和非硫化型,硫化型脫氧劑以Co-Mo為主要活性組分,使用前需要硫化處理,其主要組分為CoS和MoS3,該脫氧原理為原料中的氫氣和氧氣反生反應生成水[5],該類脫氧劑需要氣氛中含有一定量的H2,由于催化劑硫化后使用,也需要一定量的H2S才能避免催化劑反硫化。此類脫氧劑在耐硫低變等裝置中應用很多,技術相對成熟,但高爐煤氣中H2及H2S含量較低,因此該類催化劑不適合使用到高爐煤氣脫氧中。
針對以上脫氧催化劑存在的不足,武漢科林團隊開發出了適合高CO氣氛的非硫化型脫氧劑W902B,該催化劑是以MnO2/CuO/ZrO2為主要活性組分的復合氧化物脫氧劑,可以在80 ℃的條件下,催化CO與O2反應生成CO2,從而達到脫氧的目的,使用時不需要補氫,不會反硫化,并且具有一定的抗硫中毒的能力,特別適合在高爐氣中使用,以此催化劑為核心,搭配均溫反應器,開發出了脫氧工藝。
2 工藝介紹
根據上述工藝原理,結合武漢科林現有的脫硫凈化產品,開發出了高爐煤氣脫硫凈化工藝。工藝流程圖如圖1所示。
原料氣經換熱器或開工加熱器提溫至50~90 ℃后進入一級水解反應器,將原料氣中大部分COS水解轉化為H2S,一級水解后的氣體進入一級脫硫反應器,脫除一級水解產生的硫化氫。一級脫硫后的氣體進入二級水解反應器,將一級水解后剩余COS進一步水解轉化為H2S,二級水解后的氣體進入二級脫硫反應器,脫除二級水解產生的硫化氫。二級脫硫后的氣體進入三級水解反應器,將二級水解后剩余COS徹底水解轉化為H2S,三級水解后的氣體進入三級脫硫反應器,脫除三級水解產生的硫化氫。水解脫硫分別采用武漢科林公司開發的W504常溫有機硫水解催化劑、W103雙功能精脫硫,整個過程無需升降溫,有效的避免了“冷熱病”,并且脫硫劑均可再生使用,可以最大程度的降低運行成本。

圖1 高爐煤氣脫硫凈化工藝流程圖
脫氧后的氣體分兩路,一路經凈化氣冷卻器換熱降溫,經循環風機增壓后與三級水解脫硫后的氣體混合,再經換熱器降溫至50 ℃后進入脫氧反應器(經反應器內換熱后進催化劑床層溫度為80 ℃),脫氧采用武漢科林公司開發的W902B脫氧劑。因原料氣氧含量較高,脫氧采用部分循環工藝,降低入口氧含量,脫氧反應器采用先進的內換熱型均溫反應器,可降低床層溫升,減少循環氣量,降低能耗。為使脫氧劑在較低的溫度下長期穩定運行,循環風機進出口設副線,控制入口氧含量0.75%左右,脫氧出口溫度不高于160 ℃。脫氧后的氣體補入氫氣、蒸汽(控制加強反應氫氣含量8%~10%,蒸汽補入量約5%),提溫至320~370 ℃后進入有機硫加氫反應器,將高爐煤氣中有機硫加氫轉化為易于脫除的硫化氫,加氫轉化后的氣體進入中溫氧化鋅脫硫塔,脫除加氫產生的硫化氫,然后去下一工序,經此工藝處理后,硫含量小于0.1 mg/Nm3,氧含量小于30 μL/L。
3 測流實驗
3.1 實驗目的
為驗證開發的高爐煤氣脫硫凈化工藝的可靠性,以山西某鋼鐵廠正常運行的高爐煤氣為氣源,進行了為期30天工業測流實驗。通過測流實驗考查以下幾個方面:①W501有機硫水解催化劑在高氧含量的情況下,轉化COS的能力;②W103活性炭脫硫劑的脫硫效果;③考察W902B脫氧劑的脫氧效果,是否能滿足小于30 mg/Nm3的要求;④考察W904有機硫加氫催化劑轉化有機硫的能力;
3.2 測流工藝流程
原料氣經緩沖罐后進入壓縮機,加壓后的氣體提溫至60 ℃后進入一級水解反應器R-101,采用W504有機硫水解催化劑,將轉爐煤氣中的COS水解轉化為H2S,水解后的氣體進入一級脫硫反應器R-102,反應器內裝有W103雙功能精脫硫劑,用于脫除氣體中的硫化氫,脫硫后的氣體進入二級水解反應器R103,內裝W504有機硫水解催化劑,將轉爐煤氣中的COS水解轉化為H2S,水解后的氣體進入二級脫硫反應器R-104,反應器內裝有W103雙功能精脫硫劑,用于脫除第二次水解產生的H2S,精脫硫后的氣進入脫氧反應器R105,在溫度為80 ℃的條件下脫除原料氣中的氧氣,脫氧后的氣體提溫至320 ℃進入加氫反應器,使原料中的有機硫轉化為硫化氫,反應器內采用科林公司開發的W904有機硫加氫催化劑,此反應器留有補入氫氣的接口,實驗過程約補入5%的氫氣。
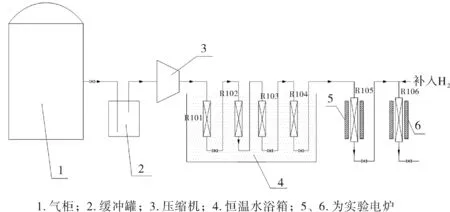
圖2 測流實驗流程圖
3.3 結果與討論
為精簡實驗流程,只保留了兩級水解工藝,加氫反應器后未設置中溫氧化鋅脫硫劑。由于氣源上游操作的周期性波動的,造成原料氣中硫化物和氧含量也在變化,現場實測氧含量及硫化物含量和設計值存在一定的差別,實驗過程某一周期脫硫凈化效果如表2所示。
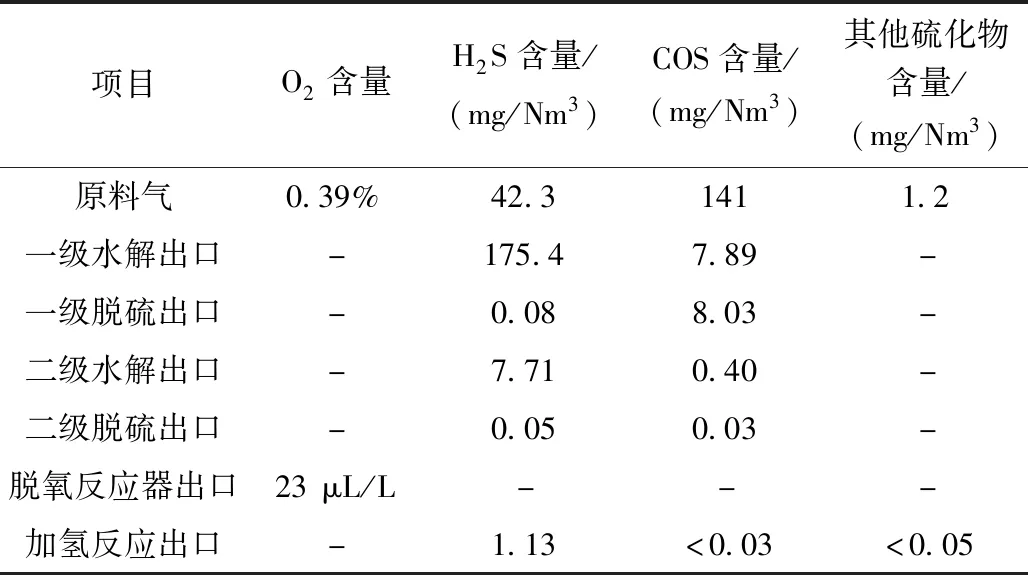
表2 測流實驗數據
從表2可以看出,經過兩級水解后可以將COS降至0.03 mg/Nm3,有機硫水解催化劑在高氧含量的情況下,仍具有較強的轉化COS能力。W103精脫硫可以在60 ℃的工況下將H2S降至0.05 mg/Nm3,避免了傳統“夾心餅”工藝中存在的“冷熱病”。應用自主開發的W902B復合氧化物脫氧劑在低溫下可以將氧降至23 μL/L,后續加氫催化劑可將有機硫將至<0.1 mg/Nm3。表2數據說明,開發的高爐煤氣脫硫凈化工藝可以滿足凈化氣硫含量小于0.1 mg/Nm3,氧含量小于30 μL/L的技術要求,盡管測流實驗原料氣體中硫化物含量和設計值有區別,但已能驗證工藝的可行性,可以將開發的工藝進行工業推廣應用。
4 結 論
(1)根據高爐煤氣高氧高硫的特點,開發出了相應的脫硫凈化工藝,采用多級水解脫硫工藝,確保COS完全轉化脫除,再進行脫氧,能避免脫氧催化劑硫中毒,確保脫氧催化劑長期穩定運行。
(2)針對高爐煤氣氧含量高的特點,通過循環控制裝置入口氧含量至0.75%以下,同時采用內換熱式均溫反應器和耐高氧能力強的非貴金屬低溫還原態脫氧催化劑,使脫氧床層溫升平穩,最大限度延長催化劑使用壽命,保證裝置安全穩定運行。
(3)工業測流實驗表明,該工藝可將硫降至小于0.1 mg/Nm3,氧含量降至小于30 μL/L,完全能滿足技術指標的要求,適合工業推廣應用。

