雪松松針乙醇提取物的抗氧化活性及構效關系研究
徐乾達,周志強,何 強,孫 群,曾維才,,*
(1.四川大學食品工程系,四川成都 610065;2.四川大學食品科學與技術四川省高校重點實驗室,四川成都 610065;3.四川大學生命科學學院,四川成都 610065)
雪松(Cedrusdeodara)又名喜馬拉雅松,是一種松科(Pinaceae)松屬(Pinus)的常綠喬木,廣泛分布于我國北方地區及長江流域,其葉外形似針,故稱“松針”。傳統中醫認為,雪松松針性溫,輕身益氣,主風濕瘡,生毛發,安五臟[1]。現代科學研究表明,雪松松針中含有豐富的活性多酚、生物黃酮、揮發油等活性成分,具有鎮痛、解痙、抗菌、抗炎、抗癌等臨床藥理作用[2]。隨著人們對其食用價值的認識,雪松松針已被陸續開發為茶、飲料和保健酒等產品,在食品加工領域展現出廣闊的開發和利用前景。
氧化應激狀態下,生物體內會產生和蓄積大量的自由基[3],過量的自由基會引起細胞膜脂質、細胞蛋白及DNA的氧化損傷,從而破壞細胞及組織器官,導致和加速機體衰老并誘發各種慢性疾病[4]。在實際應用中,雖然化學合成的抗氧化劑具有明顯的抗氧化作用,但因其對人體潛在的毒性和危害而逐漸在食品中被限制使用[5],而從天然原料中制取安全、高效的天然抗氧化劑則開始成為食品及相關領域的研究熱點。
國內外相關工作者研究了雪松松針不同有機溶劑提取物的組成,也對其抗褐變作用等與抗氧化活性有關的生物活性進行了測定[1,6-7],研究發現,萜類、多酚類、苯丙素類、有機酸類和多糖類等化合物是雪松松針的主要成分,其中以多酚類化合物為代表的生物活性物質是雪松松針發揮抗氧化功能的主要成分。上述研究及應用方向主要集中在生物和醫藥領域,所使用的萃取溶劑也大多為正丁醇和石油醚等毒性較大的有機溶劑,這類溶劑在食品工業中并不允許使用。在少數使用乙醇進行提取的實驗中,石曉峰等[8]將雪松松針進行提取(95%乙醇)和純化,并測定了純化前后提取物清除ABTS和DPPH自由基的能力。結果發現,自由基清除能力的大小依次為:抗壞血酸>經過純化的松針提取物>BHT>未經純化的松針提取物。現有研究并未找到松針乙醇提取物中具有抗氧化活性的物質基礎,也未能闡明提取物具有抗氧化能力的內在機理。
本文研究雪松松針乙醇提取物的體外抗氧化活性,并進一步對其主要成分和構效關系進行初步分析,為雪松松針資源在食品加工與貯藏領域的開發與利用提供實驗基礎與理論指導。
1 材料與方法
1.1 材料與儀器
雪松松針 采集于四川大學校園內,蒸餾水洗凈,55 ℃烘干8 h后粉碎為粉末,備用;ABTS(2,2′-azinobis-3-ethylbenzthiazoline-6-sulphonate,2,2′-聯氮-二(3-乙基-苯并噻唑-6-磺酸)二銨鹽)、DPPH(1,1-diphenyl-2-picrylhydrazine,1,1-二苯基-2-三硝基苯肼)、Folin-Ciocalteu試劑 上海阿拉丁生化科技股份有限公司;丁基羥基茴香醚(BHA)、無水乙醇、鐵氰化鉀、三氯乙酸、三氯化鐵、硫酸亞鐵、過氧化氫、水楊酸等其他化學試劑 均為國產分析純,購于成都科龍化工試劑廠;實驗用水 為蒸餾水;色譜分析用水 為超純水。
ESJ210-4A型電子天平 沈陽龍騰電子有限公司;UV-2000型紫外可見分光光度計 尤尼柯(上海)儀器有限公司;DHP-9082型電熱恒溫培養箱 上海一恒科技有限公司;RV 10 型旋轉蒸發儀 德國IKA公司;LCJ-30F型冷凍干燥機 北京松源華興科技發展有限公司;Milli-Q Element超低元素型超純水系統 上海晶儀科學儀器有限公司;DZ-400/2E型真空包裝機 上海祥正機械有限公司;安捷倫1290型高效液相色譜-質譜聯用系統 美國安捷倫公司;AV II 600 MHz 核磁共振分析儀 瑞士Bruker公司。
1.2 實驗方法
1.2.1 雪松松針乙醇提取物的制備 在預實驗的基礎上并結合相關參考文獻[9]確定了雪松松針乙醇提取物的制備方法。取雪松松針干粉539.2 g,加入4000 mL乙醇溶液(75%,V/V),25 ℃攪拌浸提15 h,減壓抽濾得到提取液,將提取液于45 ℃真空濃縮,取濃縮后得到的上清液于-60 ℃冷凍干燥36 h,得松針乙醇提取物83.2 g(該條件下提取率為15.4%),所得提取物于-20 ℃真空干燥保存,備用。
1.2.2 ABTS自由基清除實驗 ABTS自由基工作液的配制方法參照文獻[10],取0.1 mL不同濃度(0.1~1.6 mg/mL)的松針乙醇提取物溶液與3.9 mL ABTS自由基工作液混合,25 ℃條件下孵育6 min,于波長734 nm處測量反應混合溶液的吸光度,用蒸餾水替代提取物溶液作空白對照,BHA作陽性對照,計算松針乙醇提取物對ABTS自由基的清除能力。
式中:A1為實驗組的吸光度;A0為空白組的吸光度。
1.2.3 DPPH自由基清除實驗 DPPH自由基工作液的配制方法參照文獻[10],取2.0 mL不同濃度(5~80 μg/mL)的松針乙醇提取物溶液與2.0 mL DPPH工作液混合,25 ℃避光孵育30 min,于波長517 nm處測定反應混合溶液的吸光度,用95%乙醇替代提取物溶液作空白對照,BHA作陽性對照,計算松針乙醇提取物對DPPH自由基的清除能力。
式中:A1為實驗組的吸光度;A0為空白組的吸光度。
1.2.4 羥自由基清除實驗 取1 mL不同濃度的松針乙醇提取物溶液(0.4~2.4 mg/mL),與1 mL硫酸亞鐵溶液(3 mmol/L)和1 mL過氧化氫溶液(3 mmol/L)混勻,37 ℃孵育10 min,加入1 mL水楊酸,37 ℃反應30 min,于波長510 nm處測定反應混合溶液的吸光度[10],用蒸餾水替代提取物溶液作空白對照,BHA作陽性對照,計算松針乙醇提取物對羥自由基的清除能力。
式中:A1為實驗組的吸光度;A0為空白組的吸光度。
1.2.5 過氧化氫清除實驗 取4 mL不同濃度的松針乙醇提取物樣品液(20~100 μg/mL)與6 mL過氧化氫溶液(40 mmol/L,用0.1 mol/L、pH7.4的磷酸鹽緩沖液配制)混勻,于波長230 nm處快速測定混合溶液的吸光度、提取物樣品液的吸光度,用蒸餾水作空白對照[11],BHA作陽性對照。
式中:A2為實驗組的吸光度;A1為樣品組的吸光度;A0為空白組的吸光度。
1.2.6 脂質過氧化抑制能力測定 以10%(V/V)的鴨蛋黃勻漿作為脂質媒介進行實驗。取0.3 mL不同濃度的松針乙醇提取物溶液(1~16 mg/mL)與1.2 mL鴨蛋黃勻漿和50 μL硫酸亞鐵溶液(70 mmol/L)充分混勻,37 ℃孵育30 min,加入1.5 mL的乙酸溶液(20%,V/V)和1.5 mL硫代巴比妥酸溶液(0.8%,m/V,用1.1%十二烷基硫酸鈉溶液配制),振蕩混勻,95 ℃水浴反應60 min,迅速冷卻,加入5 mL正丁醇,4000 r/min離心8 min,于波長532 nm處測定上清液的吸光度[10]。用蒸餾水替代提取物溶液作空白對照,BHA作陽性對照,計算松針乙醇提取物對脂質過氧化的抑制率。
式中:A1為實驗組的吸光度;A0為空白組的吸光度。
1.2.7 鐵離子還原能力測定 取2.5 mL不同濃度的松針乙醇提取物溶液(50~800 μg/mL)與2.5 mL磷酸鹽緩沖溶液(pH6.6)和2.5 mL鐵氰化鉀溶液(1%,w/V)混勻,50 ℃孵育20 min,迅速冷卻,加入2.5 mL三氯乙酸溶液(10%,w/V),5000 r/min離心10 min,取2.5 mL上清液,加入2.5 mL蒸餾水和0.5 mL 三氯化鐵溶液(0.1%,w/V),測定反應溶液于波長700 nm處的吸光度[10],以溶液吸光度值的大小表征樣品的還原能力,吸光度值越大,表示樣品的還原能力越強,BHA作陽性對照。
1.2.8 總酚含量的測定 分別吸取0.1 mL不同濃度(0.1、0.2、0.3、0.4、0.5、0.6 mg/mL)的沒食子酸標準溶液與8.0 mL碳酸鈉溶液(7.5%,w/V)混合,加入0.9 mL用蒸餾水對倍稀釋的Folin-ciocalteu試劑,45 ℃反應30 min,于波長760 nm處測定反應混合液的吸光度,繪制總酚含量測定標準曲線,建立總酚含量(x)與吸光度(y)之間的線性回歸方程:y=1.7141x+0.0156,R2=0.9987。取濃度為8 mg/mL的松針乙醇提取物溶液0.1 mL替代沒食子酸標準溶液,按照上述步驟進行反應,將所測吸光度值代入回歸方程,計算得到松針乙醇提取物的總酚含量[12]。
1.2.9 總黃酮含量的測定 分別吸取0.1 mL不同濃度(0.1、0.2、0.4、0.6、0.8、1.0 mg/mL)的蘆丁標準溶液與0.1 mL亞硝酸鈉溶液(5%,w/V)和2.0 mL 蒸餾水混合,25 ℃孵育6 min,加入0.2 mL三氯化鋁溶液(10%,w/V)及0.6 mL蒸餾水,混勻,25 ℃反應5 min,于波長420 nm處測定混合液的吸光度,繪制總黃酮含量測定標準曲線,建立總黃酮含量(x)與吸光度(y)之間的線性回歸方程:y=0.5776x-0.0019,R2=0.9996。取濃度為8 mg/mL的松針乙醇提取物溶液0.1 mL 替代蘆丁標準溶液,按照上述步驟進行反應,將所測吸光度值代入回歸方程,計算得到松針乙醇提取物的總黃酮含量[13]。
1.2.10 高效液相色譜-質譜聯用分析 色譜條件:色譜柱:ODS-3反相柱(Inertsil PREP-ODS-3,4.6×250 mm i.d.,5 μm,日本GL-Science公司);流動相:A相為甲醇,B相為含0.1%甲酸的超純水;洗脫程序:0~20 min,0~50% A;20~25 min,50%~60% A;25~30 min,60%~70% A;30~35 min,70%~80% A;35~40 min,80%~90% A;40~45 min,90%~100% A;45~60 min,100% A;檢測波長:320 nm;參比波長:360 nm;柱溫:25 ℃;進樣量:20 μL;樣品濃度:10 mg/mL(超純水作溶劑,0.45 μm濾膜過濾)。
質譜條件:掃描范圍50~1200 m/z;毛細管電壓140 V;干燥氣流速1 L/min;干燥溫度200 ℃;霧化氣壓力14 psi;離子化方式ESI(-)。
1.2.11 核磁共振分析 取經HPLC分離和制備得到的各主要洗脫峰物質2 mg,經重水(D2O)交換和氘代甲醇(CD3OD)溶解,置于核磁管內用于核磁共振(1H-NMR,400 MHz;13C-NMR,100 MHz)分析。
1.3 數據處理
每組實驗重復三次,結果以“平均值±標準差”的形式表示。實驗結果用SPSS 20.0(Version 20.0 for Windows,SPSS Inc.,CO,USA)進行統計分析,顯著性差異P<0.05。
2 結果與分析
2.1 雪松松針乙醇提取物對ABTS自由基的清除作用
ABTS是一類商業化生產的氮族自由基,能準確測定多成分混合物的抗氧化能力,無需復雜的反應步驟及苛刻的反應條件,被廣泛用于天然產物抗氧化活性的測定[14]。雪松松針乙醇提取物對ABTS自由基清除的清除作用如圖1所示。
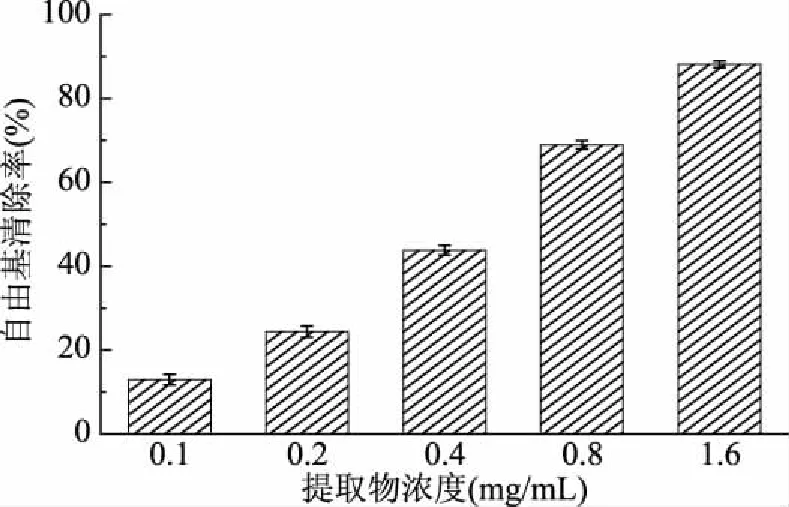
圖1 松針乙醇提取物的ABTS自由基清除能力
由圖1可知,隨著受試濃度的增加(0.1~1.6 mg/mL),提取物對ABTS自由基的清除能力逐漸增大(12.94%~88.18%),展現出良好的劑量-效應關系,其半數有效濃度(Half effective concentration,EC50)值為(0.48±0.01) mg/mL(陽性對照BHA的EC50值為5.31±0.42 mg/mL)。
2.2 雪松松針乙醇提取物對DPPH自由基的清除作用
DPPH也是一種商業化生產的氮族自由基,與其他自由基反應體系相比較,其性質較為穩定,靈敏度高,受環境影響小,實驗方法簡單且結果重復性好,是評價天然產物抗氧化活性的一種常用方法[14]。雪松松針乙醇提取物對DPPH自由基的清除作用如圖2所示。
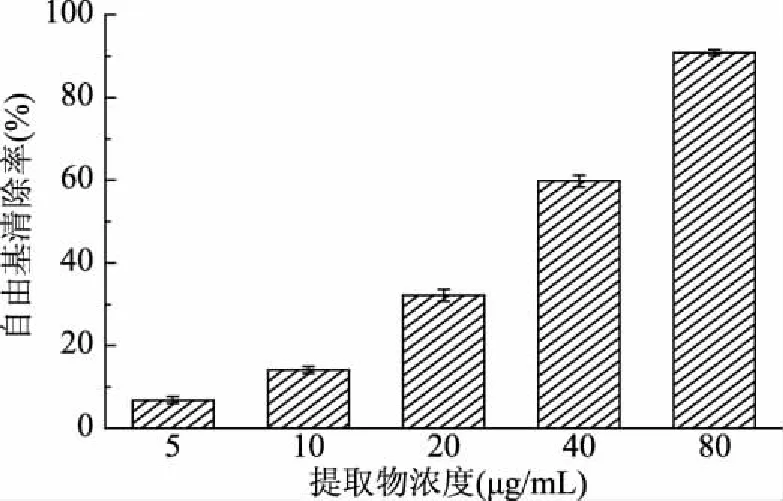
圖2 松針乙醇提取物的DPPH自由基清除能力
由圖2可知,在受試濃度范圍內(5~80 μg/mL),雪松松針乙醇提取物對DPPH自由基具有顯著的清除作用,且隨提取物濃度的增大而增大(6.86%~90.91%),具有良好的劑量-效應關系。提取物對DPPH自由基清除作用的EC50值為(32.40±0.76) μg/mL,明顯低于陽性對照BHA的EC50值(4.86±0.49) mg/mL。
2.3 雪松松針乙醇提取物對羥自由基的清除作用
羥自由基是氧氣單質的三電子還原產物,反應活性強,具有很高的電子還原電勢(2310 mV),為生物體內最強的氧化劑,能與生物細胞內的大部分物質發生氧化還原反應,造成細胞內生化代謝紊亂,引發組織的氧化損傷,加速器官的病變與機體衰老,對人體健康危害極大[15]。通過Fenton反應產生羥自由基,進而觀察雪松松針乙醇提取物對羥自由基的清除作用,結果如圖3所示。
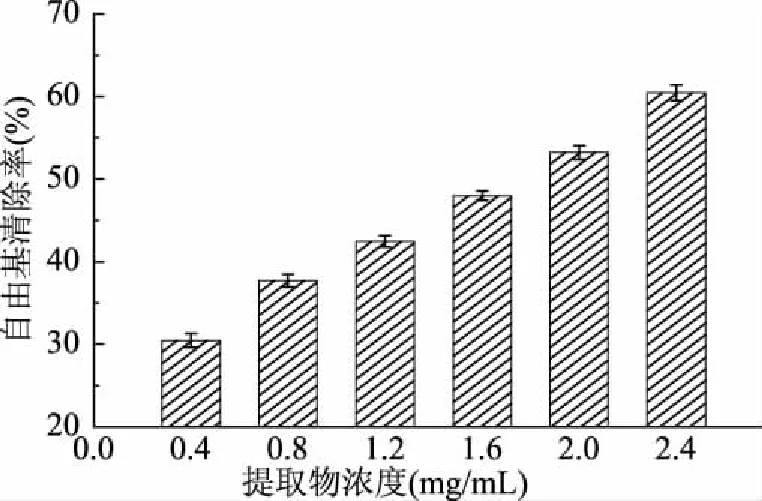
圖3 松針乙醇提取物的羥自由基清除能力
由圖3可知,在0.4~2.4 mg/mL的受試濃度范圍內,雪松松針乙醇提取物對羥自由基展現出良好的清除作用,且符合劑量-效應關系。其對羥自由基清除作用的EC50值為(1.73±0.01) mg/mL,低于陽性對照BHA的EC50值(3.23±0.01) mg/mL。
2.4 雪松松針乙醇提取物對過氧化氫的清除作用
過氧化氫是人體新陳代謝過程中產生的中間產物,當機體處于氧化應激狀態時,過量的過氧化氫會蓄積在細胞內造成機體的氧化損傷。同時,其也會進一步在酶的作用下生成羥自由基,加劇對細胞和組織的氧化損傷[16]。松針乙醇提取物的過氧化氫清除能力如圖4所示。
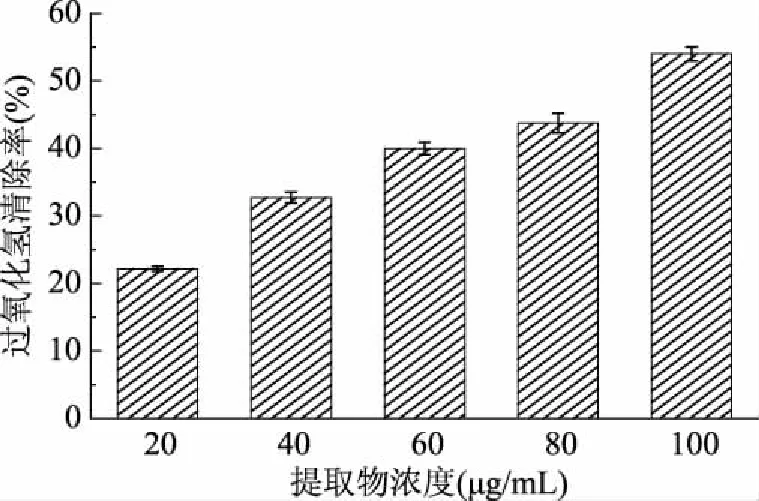
圖4 松針乙醇提取物的過氧化氫清除能力
由圖4可知,在20~100 μg/mL的受試濃度范圍內,雪松松針乙醇提取物能較好地清除實驗體系中的過氧化氫,清除率在22.16%~54.00%的范圍內,顯示出良好的劑量-效應關系。其對過氧化氫清除作用的EC50值為(89.48±0.54) μg/mL,低于陽性對照BHA的EC50值(123.66±0.56 μg/mL)。
2.5 雪松松針乙醇提取物的脂質過氧化抑制能力
脂質過氧化是一類典型的自由基鏈式反應,為多不飽和脂肪酸在氧氣作用下逐步發生的一種氧化變質現象。在生物體內發生的脂質過氧化反應會產生大量的有毒物質,如過氧化物和丙二醛等,引起生物膜的功能缺失,誘發細胞的氧化損傷,導致組織、器官的氧化病變,對人體健康產生負面影響[17]。雪松松針乙醇提取物對脂質過氧化的抑制能力如圖5所示。
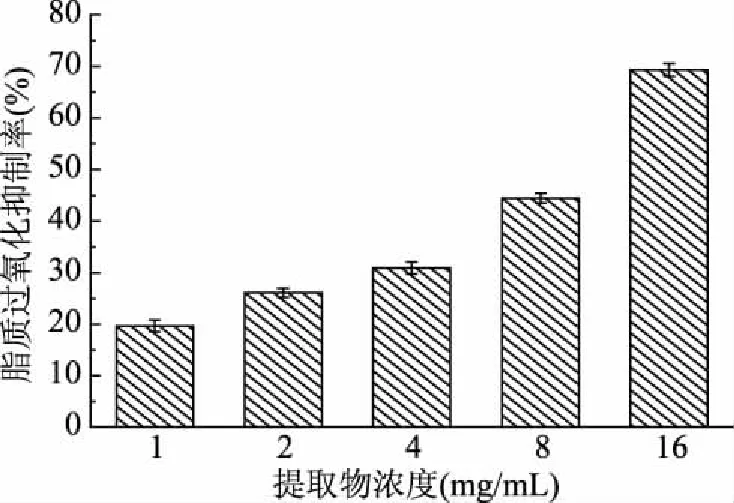
圖5 松針乙醇提取物對脂質過氧化的抑制作用
由圖5可知,雪松松針乙醇提取物對實驗體系中的脂質過氧化反應有明顯的抑制作用,隨提取物受試濃度的增加(1~16 mg/mL),脂質過氧化的抑制率也逐漸增大(19.66%~69.31%),其EC50值為(9.85±0.14) mg/mL(陽性對照BHA的EC50為7.36±0.51 mg/mL)。
綜上,雪松松針乙醇提取物能有效地清除供試反應體系中的自由基和活性氧,并對卵黃磷脂源引發的脂質過氧化有顯著的抑制作用,展現出良好的體外抗氧化活性。為了進一步剖析其抗氧化作用機理,實驗對提取物的還原能力進行了測定。
2.6 雪松松針乙醇提取物的還原能力
物質還原能力的強弱既是其抗氧化活性的重要表現,也是對其抗氧化作用進行合理分析與解釋的重要方面[18]。松針乙醇提取物的還原能力如圖6所示。
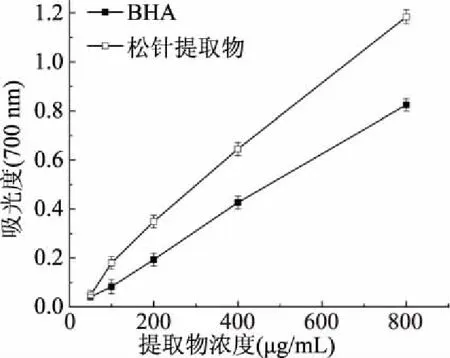
圖6 松針乙醇提取物的還原能力
由圖6可知,隨提取物濃度的增大,反應體系的吸光度逐漸增強,且在相同濃度條件下,實驗組的吸光度均高于陽性對照BHA組的吸光度,說明雪松松針乙醇提取物具有比BHA更加優良的還原能力。研究表明,還原能力是指物質在反應中失去電子的能力,物質發揮其抗氧化作用是通過自身的還原作用,在反應中給出電子而清除自由基,故物質的還原能力越強,其抗氧化作用越強。
為了從物質成分的角度探討和剖析雪松松針乙醇提取物優良的體外抗氧化作用和還原能力,實驗進一步測定了提取物中抗氧化成分酚類及黃酮類化合物的總量。
2.7 松針乙醇提取物的總酚和總黃酮含量
多酚類化合物和黃酮類化合物是植物中天然存在的次生代謝物,廣泛存在于茶、酒、水果、蔬菜或其他植物性飲食來源中[19],能夠通過多種途徑清除多種體內外存在的自由基,從而發揮良好的抗氧化能力[20],酚類物質含量的多少決定了提取物抗氧化能力的強弱[21]。
松針乙醇提取物的中總酚含量為(40.30±2.13) mg沒食子酸當量/g提取物,總黃酮含量為(56.62±1.53) mg蘆丁當量/g提取物。結果表明,松針乙醇提取物的總酚和總黃酮含量較高,可能為其發揮抗氧化活性提供良好的物質基礎。
單一植物中往往含有種類繁多的酚類化合物,不同種類的酚類化合物之間存在穩定性和反應活性的差異,且相互作用方式也各不相同,這些因素最終會對提取物的抗氧化活性產生較大的影響[22-23]。為了從活性物質組成方面系統探究和揭示雪松松針乙醇提取物優良的抗氧化活性,實驗通過HPLC-MS及NMR技術對提取物中的主要化合物進行了鑒定,并進一步分析和討論了其發揮抗氧化作用的構效關系,進而對其抗氧化作用機理進行研究。
2.8 雪松松針乙醇提取物主要成分的鑒定及構效關系分析
通過高效液相色譜-質譜聯用(HPLC-MS)及核磁共振(1H-NMR、13C-NMR)的分離純化與結構鑒定,從雪松松針乙醇提取物中鑒定出六種主要的成分,結果如圖7所示。
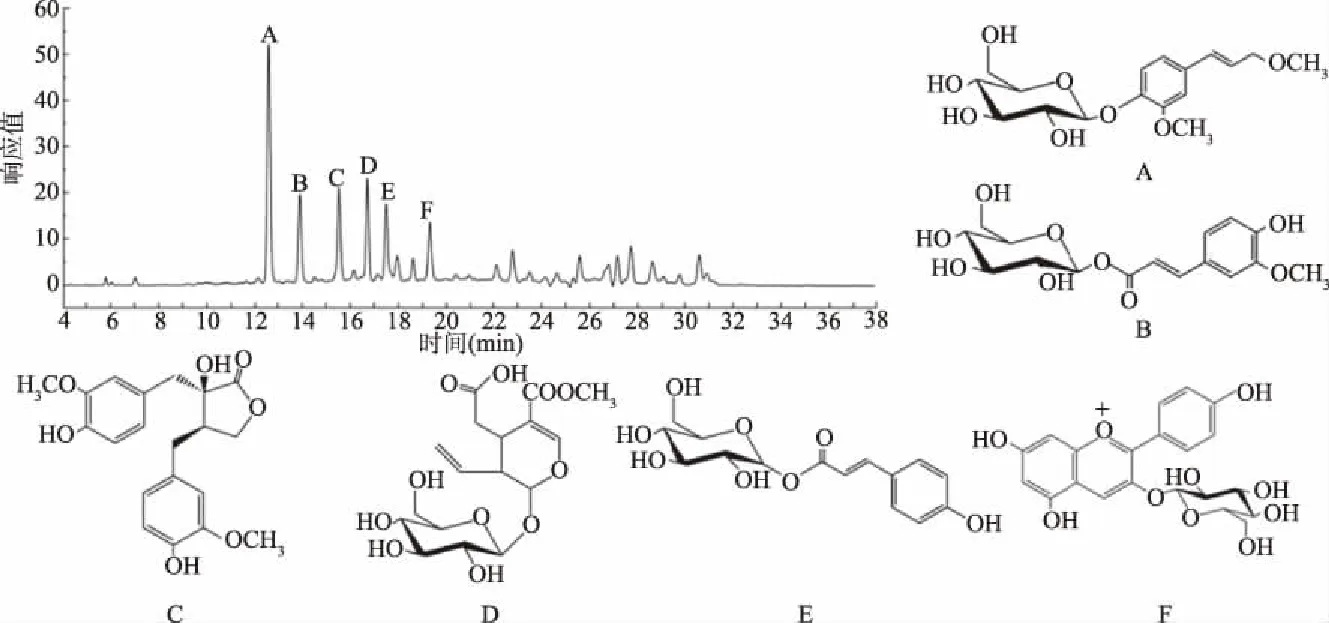
圖7 雪松松針乙醇提取物的主要成分的分離及鑒定結果
提取物中六種主要成分的色譜分析數據具體如下:
洗脫峰A對應的化合物:ESI-MS準分子離子峰m/z:355.1[M-H]-。1H-NMR(CD3OD,400 MHz)δ:7.06(1H,d,J=8.4 Hz,H-5),7.02(1H,d,J=1.2 Hz,H-2),6.97(1H,dd,J=8.4,1.2 Hz,H-6),6.56(1H,d,J=14.4 Hz,H-7),6.38(1H,dt,J=14.4 Hz,5.2 Hz,H-8),4.81(1H,d,J=7.2 Hz,H-1′),4.27(2H,d,J=5.2 Hz,H-9),3.81(3H,s,-OCH3),3.48(3H,s,H-11),3.31~3.95(6H,m,H2′-6′);13C-NMR(CD3OD,100 MHz)δ:134.69(C-1),112.83(C-2),151.65(C-3),148.79(C-4),18.67(C-5),122.97(C-6),132.15(C-7),128.47(C-8),66.89(C-9),152.64(C-11),103.71(C-1′),76.86(C-2′),78.37(C-3′),72.59(C-4′),79.31(C-5′),63.24(C-6′),56.78(-OCH3)。由以上波譜分析數據得到化合物的分子式為C17H24O8,與相關文獻報道基本一致[24],故鑒定該化合物為甲基松柏苷(Methylconiferin)。
洗脫峰B對應的化合物:ESI-MS準分子離子峰m/z:355.1[M-H]-。1H-NMR(CD3OD,400 MHz)δ:7.71(1H,d,J=15.7 Hz,H-7),7.46(1H,d,J=1.6 Hz,H-2),7.21(1H,dd,J=8.3,1.6 Hz,H-6),7.15(1H,d,J=8.3 Hz,H-5),6.57(1H,d,J=15.6 Hz,H-8),5.18(1H,d,J=7.3 Hz,H-1′),3.89(3H,s,3-OCH3),3.52(1H,dd,J=4.2,3.3 Hz,H-6′),3.44(1H,dd,J=4.1,1.7 Hz,H-6′),3.16~3.39(4H,m,H2′-5′);13C-NMR(CD3OD,100 MHz)δ:131.29(C-1),114.71(C-2),152.28(C-3),151.49(C-4),117.79(C-5),121.36(C-6),145.27(C-7),116.54(C-8),172.61(C-9),103.13(C-1′),76.46(C-2′),79.35(C-3′),73.55(C-4′),77.41(C-5′),64.62(C-6′),56.53(-OCH3)。由以上波譜分析數據得到化合物的分子式為C16H20O9,與相關文獻報道基本一致[24],故鑒定該化合物為阿魏酸-β-D-吡喃葡萄糖苷(Ferulic acid-β-D-glucoside)。
洗脫峰C對應的化合物:ESI-MS準分子離子峰m/z:373.1[M-H]-。1H-NMR(CD3OD,400 MHz)δ:8.91(1H,br s,4-OH),8.77(1H,br s,4′-OH),6.81(1H,d,J=1.7 Hz,H-2),6.70(1H,d,J=8.2 Hz,H-5),6.66(1H,d,J=1.9 Hz,H-5′),6.63(1H,d,J=7.86 Hz,H-2′),6.57(1H,dd,J=1.65,8.2 Hz,H-6),6.53(1H,dd,J=1.7,7.89 Hz,H-6′),6.27(1H,s,8′-OH),3.97(1H,d,J=8.81 Hz,H-9),3.92(1H,d,J=8.6 Hz,H-9′),3.75(3H,s,-OCH3),2.97(1H,d,J=13.61 Hz,H-7),2.62(1H,dd,J=2.63,12.05 Hz,H-7′),2.34(1H,m,H-8);13C-NMR(CD3OD,100 MHz)δ:179.1(C-9),146.9(C-4′),147.1(C-4),145.5(C-3′),144.8(C-3),130.6(C-1′),128.3(C-1),123.7(C-6),121.1(C-6′),115.8(C-5′),115.4(C-5),114.7(C-2),113.2(C-2′),76.1(C-8),70.5(C-9),55.8(-OCH3),55.3(-OCH3),43.2(C-8′),40.5(C-7),30.4(C-7′)。由以上波譜分析數據得到化合物的分子式為C20H22O7,與相關文獻報道基本一致[25],故鑒定該化合物為蕘花酚(Wikstromol)。
洗脫峰D對應的化合物:ESI-MS給出準分子離子峰m/z:403.1[M-H]-。1H-NMR(CD3OD,400 MHz)δ:7.35(1H,s,H-3),5.53(1H,m,H-8),5.35(1H,d,J=4.1 Hz,H-1),5.18(1H,s,H-10a),5.05(1H,m,H-10b),4.57(1H,d,J=8.5 Hz,H-1′),3.55(3H,s,-OCH3),3.11(1H,m,H-5),2.76(1H,dd,J=17.01,5.2 Hz,H-6a),2.71(1H,m,H-9),2.13(1H,dd,J=16.6,9.2 Hz,H-6b);13C-NMR(CD3OD,100 MHz)δ:175.8(C-7),167.5(C-11),154.1(C-3),135.6(C-8),121.2(C-10),110.6(C-4),99.6(C-1′),98.2(C-1),78.4(C-3′),78.2(C-5′),75.1(C-2′),71.5(C-4′),63.1(C-6′),51.4(-OCH3),44.9(C-9),35.7(C-6),28.9(C-5)。由以上波譜分析數據得到化合物的分子式為C17H24O11,與相關文獻報道基本一致[26],故鑒定化合物D為斷氧化馬錢苷(Secoxyloganin)。
洗脫峰E所對應的化合物:ESI-MS給出準分子離子峰m/z:325.1[M-H]-。1H-NMR(CD3OD,400 MHz)δ:7.71(1H,d,J=16.5 Hz,H-3),7.56(2H,d,J=7.7 Hz,H-2′,6′),7.18(2H,d,J=7.9 Hz,H-3′,5′),6.35(1H,d,J=15.8 Hz,H-2),4.95(1H,d,J=4.9 Hz,H-1′),3.86(1H,dd,J=11.7,2.4 Hz,H-6″b),3.71(1H,dd,J=12.2,4.5 Hz,H-6″a),3.32-3.51(4H,m,H-2″,H-3″,H-4″,H-5″);13C-NMR(CD3OD,100 MHz)δ:171.1(C-1),161.1(C-4′),145.6(C-3),130.6(C-2′,6′),130.1(C-1′),117.8(C-3′,5′),117.2(C-2),102.6(C-1″),75.5(C-5″),77.6(C-3″),74.6(C-2″),72.2(C-4″),62.5(C-6″)。由以上波譜分析數據得到化合物的分子式為C15H18O8,與相關文獻報道基本一致[27],故鑒定該化合物為(E)-1-O-對香豆酰-α-D-吡喃葡萄糖苷((E)-1-O-p-coumaroyl-α-D-glucopyranoside)。
洗脫峰F對應的化合物:ESI-MS給出準分子離子峰m/z:433.2[M-H]-。1H-NMR(CD3OD,400 MHz)δ:8.92(1H,s,H-4),8.55(2H,d,J=9.5 Hz,H-2′,6′),7.08(2H,d,J=9.8 Hz,H-3′,5′),6.85(1H,d,J=0.9 Hz,H-8),6.65(1H,d,J=1.2 Hz,H-6),5.23(1H,d,J=7.8 Hz,H-1 glc),3.79(1H,dd,J=2.5,12.7 Hz,H-6b glc),3.61(1H,dd,J=6.3,12.2 Hz,H-6a glc),3.58(1H,dd,J=7.9,9.5 Hz,H-2 glc),3.51(1H,ddd,J=2.1,6.3,9.7 Hz,H-5 glc),3.45(1H,dd,J=9.3,9.5 Hz,H-3 glc),3.32(1H,dd,J=9.3,9.6 Hz,H-4 glc);13C-NMR(CD3OD,100 MHz)δ:166.2(C-2),145.5(C-3),138.7(C-4),160.2(C-5),104.3(C-6),171.8(C-7),95.6(C-8),158.6(C-9),114.7(C-10),120.9(C-1′),136.5(C-2′),118.7(C-3′),170.5(C-4′),118.3(C-5′),136.8(C-6′),103.9(C-1 glc),76.2(C-2 glc),78.7(C-3 glc),72.5(C-4 glc),79.1(C-5 glc),63.2(C-6 glc)。由以上波譜分析數據得到化合物的分子式為C21H22O10,與相關文獻報道基本一致[28],故鑒定該化合物為天竺葵素-3-O-葡萄糖苷(Pelargonidin-3-O-glucoside)。
根據相關研究可知,提取物主要成分中的蕘花酚、(E)-1-O-對香豆酰-α-D-吡喃葡萄糖苷和天竺葵素-3-O-葡萄糖苷等酚類化合物具有較強的自由基清除作用,這可能是提取物展現出明顯抗氧化作用的重要原因[25,27-28]。同時,從上述色譜分離與波譜鑒定結果可知,提取物主要成分的結構中均含有大量的酚羥基和甲氧基等酚類化合物的活性官能團,而上述官能團在氧化反應體系中具有良好的給出氫原子進而淬滅活潑自由基或活性氧的作用,為提取物發揮良好的抗氧化能力提供了結構方面的基礎。相關研究表明,酚類化合物結構中的酚羥基等活性官能團可通過氫原子轉移(Hydrogen atom transfer,HAT)或單電子轉移(Single electron transfer,SET)的方式與途徑實現酚類化合物在反應體系中對自由基的清除作用,進而發揮其良好的抗氧化活性[29]。同時,研究指出,酚類化合物苯環上的甲氧基對化合物基于HAT機制的抗氧化活性有顯著的提高效應,可增強化合物與體系中活性氧的反應,降低整個體系的氧化態勢[30]。其次,雪松松針乙醇提取物主要成分的結構中存在大量的芐基,根據前期基于密度泛函理論對不同酚類化合物前線分子軌道、分子靜電勢和電離勢的研究,酚類物質結構中芐基的C-H鍵解離能低于O-H鍵的解離能,可使其在反應體系中能給出氫原子參與捕捉自由基,進而顯著提升提取物的抗氧化活性[12,31]。再者,相關研究指出,植物提取物中不同多酚類物質在抗氧化反應中可能會出現協同效應,其結構中活性官能團的氫原子和電子轉移能力可在相互作用中得到提升,進而增強提取物的抗氧化能力[32]。此外,雪松松針乙醇提取物的主要成分通過糖苷鍵與糖分子形成糖苷,使其水溶性及穩定性得到提高,也在一定程度上提升了酚類化合物結構中酚羥基與甲氧基的氫原子給予能力,從而對提取物抗氧化作用的發揮產生積極地影響[33]。
3 結論
雪松松針乙醇提取物含有豐富的活性多酚類化合物,具有良好的抗氧化作用;能有效清除自由基,抑制脂質過氧化,并展現出較強的還原能力;甲基松柏苷(A)、阿魏酸-β-D-吡喃葡萄糖苷(B)、蕘花酚(C)、斷氧化馬錢苷(D)、(E)-1-O-對香豆酰-α-D-吡喃葡萄糖苷(E)和天竺葵素-3-O-葡萄糖苷(F)是提取物中主要的成分。化合物B、C、E、F中所含的酚羥基,化合物A、B、C、D所含的甲氧基,化合物A、B、C、E所含的芐基以及其它具有氫原子轉移或單電子轉移活性的基團,是雪松松針乙醇提取物發揮抗氧化活性的結構基礎。研究工作為雪松松針在食品、醫藥和日化等領域的資源化利用提供了實驗基礎。

