“宏觀辨識與微觀探析”核心素養在教學中的應用
莫梅


【摘要】? 化學是從微觀層面解釋宏觀性質的學科,宏觀與微觀的聯系是化學學科不同于其他學科最具特征的思維方式,宏觀辨識和微觀探析也正是中學化學核心素養要求之一。三大守恒的微觀分析是高中的一大難點,大部分學生會覺得混亂,解題有難度,本課例希望能突破這難點。
【關鍵詞】? 宏觀辨識和微觀探析 三大守恒 微粒觀教學
【中圖分類號】? G633.8? ? ? ? ? ? ? ?? ? 【文獻標識碼】? A 【文章編號】? 1992-7711(2020)17-082-03
0
三大守恒內容是比較難學的,該部分內容要求學生具有抽象的微粒觀、形成建模整體思想,但由于學生從宏觀到微觀的思維發展還不全面,同時該部分知識還具有知識面廣、理論性強等特點,因此對老師的教學是一大挑戰。
一、教學主題內容及教學現狀分析
1.教學主題內容
守恒法是中學化學中的重要思想之一。“溶液中三大守恒”位于選修4《化學反應原理》第三章第三節鹽類水解專題內容,電解質溶液中的三大守恒關系包括電荷守恒、物料守恒以及質子守恒3種關系。教學上能達到:一是要熟練掌握三個守恒的基本原理;二是要理清思路,準確分析出溶液中存在的所有微粒,從微粒角度分析溶液中微粒的變化,能從溶液中微粒種類和來源、微粒間的相互作用以及相互作用的結果,找出它們的相互關系。
2.教學現狀分析
三大守恒內容是高中化學電解質溶液的教學的難點和重點之一,也是高考的熱點之一,但是當前文獻在這方面研究偏少,教學方式上也偏向于傳統教學:給出原理-解釋-習題應用-鞏固,學生只是被動地接受知識,對于三大守恒的微粒觀本質并沒有清晰的認識,所以題目一變學生思維又引起混亂,解題有難度,出錯率增大。
二、教學思想與創新點
微粒作用觀是微觀角度的核心,用微粒作用觀統領化學學習,可以有效的豐富學生的微觀認識,并能夠指導對物質及其變化規律的理解和研究。只有從微粒作用觀角度建構學生的化學認識,才能使學生在本質層面理解化學,形成真正的有意義學習。
基于“宏觀辨識與微觀探析”的核心素養下對《溶液中三大守恒》的研究,引導學生從微粒角度分析溶液中微粒的變化,能從溶液中微粒種類和來源、微粒間的相互作用以及相互作用的結果,找出它們的相互關系,幫助學生更好接受和理解本節內容,突破本節重點難點。
三、教學目標
1.掌握電荷守恒、物料守恒、質子守恒的基本原理。
2.從微粒觀角度認識三大守恒原理,形成基本的建模思維。
3.發展學生的認知方式,促進其微粒觀(微粒的種類、數量、來源、去向)及動態觀(基于平衡的動態觀)的進一步深化,形成定量觀及系統觀。
四、教學流程
五、教學實錄
【環節一】電荷守恒微粒教學突破
在電解質溶液中,不管溶液中離子類型有幾種,溶液本身應該是一直呈現中性水平的,也就是說陰離子所帶的負電荷總數應該與陽離子所帶的正電荷數量相等。學生的易錯點在于離子所帶電荷數和守恒式系數關系,所以微觀教學中重點突出電荷數,然后列守恒式。學生設計活動見圖1所示。
學生對電荷守恒的分析完成了一個建模的思維過程。先分析溶液中的電離和水解過程,找全溶液中的離子種類。然后突破易錯點,用黏土把離子所帶電荷標注出來,清楚電荷數和離子之間的關系。最后由電荷守恒的原理,把微觀分析用符號表征出來,正確寫出電荷守恒式。
學生的活動結果如圖2所示:
【環節二】物料守恒微粒教學突破
電解質溶液中某些離子會在化學反應過程中發生水解或電離,這會導致離子種類的激增,但無論它的種類變化為多少種,它其中所涵蓋的特定元素原子總數應該呈現標準的守恒關系。以Na2CO3溶液為例設計見圖3所示:
學生對物料守恒的分析完成了一個建模的思維過程。找準某兩種元素的原子數量等式,然后找各自形式,通過水解前后的微觀過程對比,找出物料守恒關系式。
學生的活動結果如圖4所示:
【環節三】質子守恒微粒教學突破
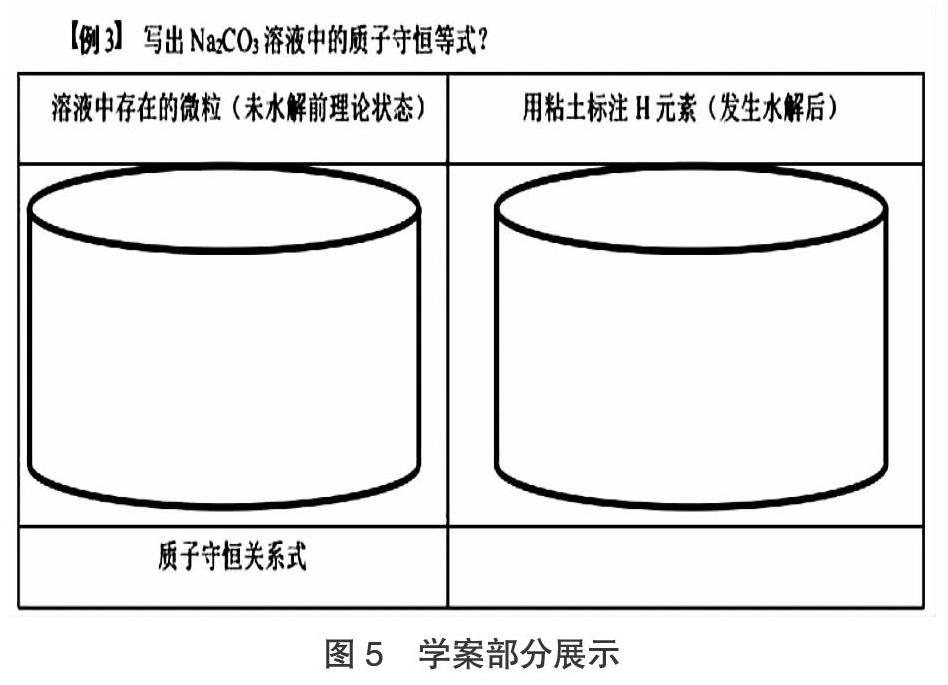
在我所學習的電解質溶液質子守恒關系中,我知道粒子會電離出H+,而它的總數應該與粒子接受的H+總數與水溶液中的H+總數相加之和相等,依然以Na2CO3溶液為例設計如圖5所示:
學生對質子守恒的原理進行微觀角度的分析,H原子的數量、來源、去向通過這個模型對比可以把抽象變直觀,更好的列出質子守恒關系式。
學生的活動結果如圖6所示:
六、教學效果與反思
三大守恒內容的設計有利于學生微粒觀的建構,能從某種微粒的來源、數量、去向來分析三大守恒原理,能夠有效地突破難點。同時課堂上有效的建模活動,引導學生建立化學知識體系,強調學生自主建構知識,符合當代學生的發展需求,也有利于為新課改提供教學思路。
物質微粒觀的培養對學生的化學學習是有意義的,在高中生的頭腦中構建較為合理且較為高層次的物質微粒觀是可實現的。基于物質微粒觀的教學讓學生學習化學的思路一下清晰起來,突然發現所有的化學問題都可以通過微粒間的相互作用來解釋,零碎的化學知識通過物質微粒觀很好的串聯起來。
[ 參? 考? 文? 獻 ]
[1]辛慧敏.“鹽類的水解”專題學生學習困難分析與教學對策研究[D].遼寧師范大學,2017.
[2]王立萍.高中生鹽類水解問題解決障礙成因分析及對策研究[D].華中師范大學,2019.
[3]岳峻楠.《化學反應原理》教學中學生微粒觀的建構研究[D].福建師范大學,2017.
[4]張瑛美.淺談電解質溶液中“三個守恒”關系的書寫方法[J].中學化學教學參考,2017(06):63.
[5]劉爽.電解質溶液中離子濃度大小與“三大守恒”的解析[J].中國校外教育,2018(02):116.
[6]郭軒林.綜合運用“三大守恒”判斷電解質溶液中粒子濃度的大小[J].中學化學教學參考,2017(20):61.
[7]劉雙媛.電解質溶液中離子濃度大小關系的應對策略[J].農家參謀,2017(19):160.
[8]陳曉娜,閆春更,周禮,周青.高中生鹽類水解心智模型的研究[J].化學教育(中英文),2018,39(19):41-46.
[9]王敏.“鹽類的水解”教學設計[J].化學教育,2010,31(S2):65-67.
[10]于少華,王磊,支瑤.發展學生認識角度和深度的化學教學轉變——以“化學反應原理”模塊為例[J].化學教育,2015,36(03):14-18.

