9種獲批上市的抗PD-1/PD-L1單抗藥物的特征綜述
趙秋玲 楊琳 謝瑞祥
摘 要 目的:為臨床合理使用抗程序性死亡受體1(PD-1)或程序性死亡受體配體1(PD-L1)單抗藥物提供參考。方法:以“PD-1抗體”“PD-L1抗體”“單克隆抗體”“結構”“藥動學”“PD-1 antibodies”“PD-L1 antibodies”“Monoclonal antibodies”“Pharmacokine- tics”為中英文關鍵詞,在中國知網、萬方數據、維普網、PubMed等數據庫中組合查詢2010年1月1日-2019年12月31日發表的相關文獻,對目前上市的幾種抗PD-1/PD-L1單抗藥物的結構特征及生物學特點、人源化程度、適應證、用法用量、免疫原性、藥動學等內容進行總結。結果與結論:不同抗PD-1/PD-L1單抗藥物在穩定性、親和力、Fc段特征、給藥劑量、適應證、免疫原性、藥動學方面各有不同。作用于靶點PD-1的納武利尤單抗、帕博利珠單抗、西米普利單抗、特瑞普利單抗、信迪利單抗、卡瑞利珠單抗均為人源化或完全人免疫球蛋白G4(IgG4)抗體;作用于靶點PD-L1的阿特朱單抗、阿維魯單抗和度伐魯單抗是人源化或完全人的IgG1抗體。納武利尤單抗主要與PD-1的N環結構結合,帕博利珠單抗主要與PD-1的C′D環結構結合,特瑞普利單抗和信迪利單抗主要與PD-1的FG環結合,卡瑞利珠單抗主要與PD-1的C C′環和 FG環結合,阿特朱單抗主要通過覆蓋PD-L1的BC、C C′、C′C″和 FG 環中的殘基來主導結合,阿維魯單抗的結合表位區域主要由PD-L1的C鏈、C′鏈、F鏈、G鏈和C C′環構成,度伐魯單抗的結合區域是PD-L1上的C C′環和 N 末端區域。納武利尤單抗、帕博利珠單抗的適應證較廣,可用于黑色素瘤、非小細胞肺癌、霍奇金淋巴瘤、尿路上皮癌等,而信迪利單抗和卡瑞利珠單抗目前只獲批用于復發/難治性霍奇金淋巴瘤的治療。抗PD-1/PD-L1單抗藥物多具有較低的分布容積,大多數分布于血管和細胞間隙中,半衰期及達到穩態時間較長,代謝消除方式包括非特異性消除(如蛋白水解作用)和靶點介導的消除(包括靶點結合、蛋白水解和內化作用)。抗PD-1/PD-L1單抗藥物不經過細胞色素P450酶和其他藥物代謝酶代謝,因此較少存在藥物相互作用。臨床醫務人員深入了解抗PD-1/PD-L1單抗藥物的結構及藥動學特點可有助于臨床合理用藥,更好地發揮抗PD-1/PD-L1單抗藥物的療效、減少不良反應。
關鍵詞 抗PD-1/PD-L1單抗藥物;PD-1抗體;PD-L1抗體;單克隆抗體;結構;藥動學
中圖分類號 R967;R730.5 文獻標志碼 A 文章編號 1001-0408(2020)18-2294-06
DOI 10.6039/j.issn.1001-0408.2020.18.21
2013年《科學》雜志將腫瘤免疫療法列為十大科學突破之首,免疫檢查點抑制劑已經成為腫瘤免疫治療領域的研究焦點[1]。現有研究表明,程序性死亡受體1(PD-1)/程序性死亡受體配體1(PD-L1)信號通路可通過抑制T細胞活化來誘導腫瘤特異性T細胞凋亡,并導致T細胞抵抗,在腫瘤、慢性炎癥等病理情況下起到免疫逃逸、免疫抑制等作用[2]。針對PD-1/PD-L1靶點的抑制劑在臨床應用中展現出了顯著的治療效果[3-8]。目前,已有不少PD-1/PD-L1抑制劑上市,但不同的PD-1/PD-L1抑制劑在抗體來源、類型、穩定性、特異性、親和力、適應證、用法用量、免疫原性、藥動學等方面均有一定差異。為幫助臨床合理選擇PD-1/PD-L1抑制劑,筆者以“PD-1/PD-L1抑制劑”“PD-1抗體”“PD-L1抗體”“單克隆抗體”“藥動學”“PD-1/PD-L1 inhibitors”“PD-1 antibodies”“PD-L1 antibodies”“Monoclonal antibodies”“Pharmacokinetics”等為關鍵詞,在中國知網、維普網、萬方數據、PubMed等中英文數據庫中組合查詢2010年1月1日-2019年12月31日發表的相關文獻。現對PD-1及PD-L1的結構、作用機制以及目前已上市的抗PD-1/PD-L1單抗藥物的特點和應用進展進行綜述,以期為該類藥物的臨床合理使用提供參考。
1 PD-1及PD-L1的結構
PD-1隸屬免疫球蛋白超家族CD28/B7,是由288個氨基酸組成的Ⅰ型跨膜糖蛋白,為免疫抑制性受體,其結構由胞外結構域、疏水性跨區和胞質區組成,其中,胞外結構域包含一個IgV(免疫球蛋白可變區)結構域,與細胞毒性T淋巴細胞抗原4(CTLA-4)等其他共刺激分子具有22%~33%的同源性[9],同時含有4個能被糖基化的位點。胞質尾部含有氨基端和羧基端兩個酪氨酸殘基,分別構成一個免疫受體酪氨酸抑制基序(ITIM)和一個免疫受體酪氨酸轉換基序(ITSM)。PD-1介導抑制的分子基礎取決于ITSM內的酪氨酸殘基是否磷酸化,其在免疫應答中起著重要的負向調控作用[10]。PD-1的主要配體為PD-L1(又稱B7-H1),是一種由人CD274基因編碼的Ⅰ型跨膜糖蛋白。PD-L1含IgV樣區、IgC(免疫球蛋白恒定區)樣區、跨膜區和細胞質尾區,其中細胞質尾區與細胞內的信號轉導相關;IgV區和IgC區則參與細胞間的信號轉導[11]。
2 PD-1/PD-L1的作用機制
PD-1與PD-L1結合時,通過發生磷脂酰肌醇-3-激酶的磷酸化、蛋白激酶B的進一步激活、刺激性T細胞信號通路的活化、葡萄糖代謝以及干擾素的分泌等,導致T細胞活化的下游信號受阻,進而有效抑制T細胞的轉錄,最終抑制T細胞的免疫功能,在免疫應答的負性調控方面發揮著重要作用[12]。因此,阻斷PD-1/PD-L1信號通路可使T 細胞活化上調,激活內源性抗腫瘤免疫反應,從而發揮對腫瘤的治療作用。
3 目前獲批上市的幾種抗PD-1/PD-L1單抗藥物
3.1 單克隆抗體的結構特征
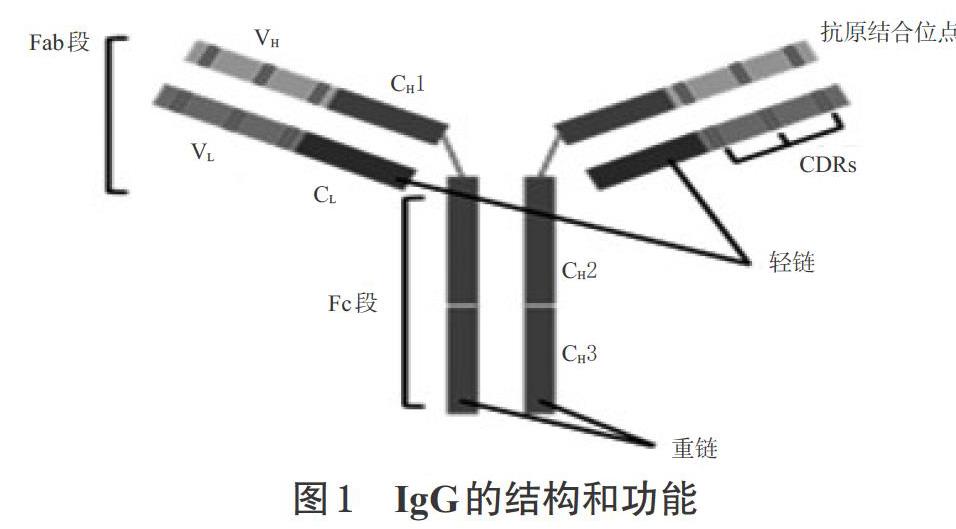
大部分單克隆抗體是由免疫球蛋白G(IgG)框架構成,抗PD-1/PD-L1單抗藥物的基本框架也是IgG。IgG是由2條輕鏈和2條重鏈組成的四肽鏈糖蛋白,輕鏈包含氨基端可變區(VL)和恒定區(CL),重鏈包括氨基端可變區(VH)和3個恒定區(CH1、CH2、CH3)。人體內有4種不同的IgG亞群(IgG1、IgG2、IgG3、IgG4),其主要區別在于 CH1 和 CH2 之間的鉸鏈大小、鏈內二硫鍵連接位置及數量。IgG 不同亞群之間不僅結構不同,功能上也有區別。輕鏈和重鏈靠 CL和 CH1之間的二硫鍵連接,其中輕鏈的VL、CL及重鏈的VH、CH1形成Fab段;來自VH和VL結構域的互補決定區(CDR)形成抗原結合位點;CH1和CH2之間是柔性鉸鏈,該鉸鏈將Fab連接到包含CH2和CH3域的可結晶片段(Fc區)[13]。Fc能夠決定抗體在血清中的半衰期,并介導免疫反應,如激活補體依賴的細胞毒作用(CDC)、抗體依賴細胞介導的細胞毒作用(ADCC)和抗體依賴性細胞吞噬作用(ADCP)等[14]。IgG的結構和功能見圖1。
3.2 抗PD-1/PD-L1單抗藥物的結構特征及生物學特點
目前,經美國FDA批準上市的抗PD-1單抗藥物有6種,分別為納武利尤單抗(Nivolumab)、帕博利珠單抗(Pembrolizumab)、西米普利單抗(Cemiplimab)、特瑞普利單抗(Toripalimab)、信迪利單抗(Cindilimab)和卡瑞利珠單抗(Camrelizumab);抗PD-L1單抗藥物有3種,分別為阿特朱單抗(Atezolizumab)、阿維魯單抗(Avelumab)和度伐魯單抗(Durvalumab)。抗PD-1單抗藥物的基本結構為IgG4,因為具有較短的鉸鏈區及不穩定的二硫鍵,所以具有較大的靈活性。在體內,IgG4可以與其他IgG4分子進行Fab段交換,即形成“半分子交換”:兩個單特異性IgG4分子互相交換自身的一條重鏈以及與這條重鏈相連的輕鏈,從而產生新的IgG4分子,而這種新的IgG4分子可能因此獲得雙特異性[15]。核心鉸鏈基序228位的絲氨酸是“半分子交換”所需的關鍵元素,通過點突變將絲氨酸替換為脯氨酸(S228P位點),可阻止IgG4的Fab段交換[16-17]。因此,抗PD-1單抗藥物均經S228P修飾[18-19],以穩定鏈間二硫鍵,阻止Fab段交換,克服因IgG4的不穩定性所引起的療效和毒性的不可預測性。抗PD-L1單抗藥物的基本結構為IgG1,核心鉸鏈基序228位的脯氨酸比較穩定,不存在上述“半分子交換”現象。
對單抗藥物的Fc區進行改造可影響其ADCC、CDC、ADCP等效應的發揮。IgG1與Fc受體(FcR)親和力較低,IgG1比IgG4能夠更加高效地介導ADCC和CDC作用。ADCC由Fc與Fc-γ受體(FcγR)結合后引發,其結合力明顯受CH2結構域中N-聚糖的影響,例如提高唾液酸化糖型可以降低Fc對FcγR的親和力,從而減弱ADCC和CDC效應[20];而降低或去除核心糖結構中的巖藻糖則可增強ADCC 效應[21]。IgG型單抗一般在Fc區的天冬酰胺(Asn)-297處有一個保守的氨基糖基化位點,阿特朱單抗通過突變位點(N297A)消除Fc區的ADCC效應。通過對度伐魯單抗恒定區的3個氨基酸進行突變,亦可去除其ADCC活性。阿維魯單抗則保留有完整ADCC野生型IgG1λ型構架[22]。
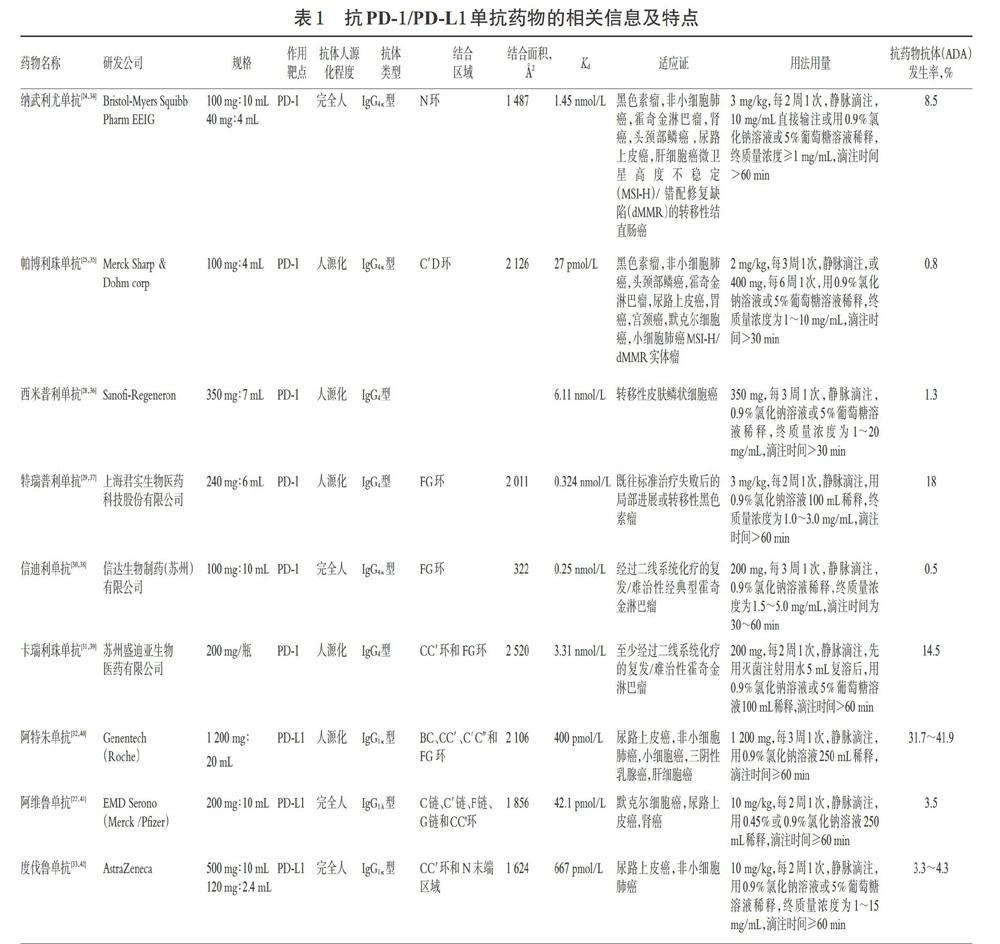
親和力是影響單抗類藥物療效、臨床的最佳劑量和部分毒副作用程度的因素之一,由結合區域、結合面積與抗原決定簇之間立體構型的合適度共同決定[23]。親和力可用解離常數(Kd)表征,Kd值越小,親和力越大。PD-1分子胞外段的主要結構為從氨基末端至羧基末端依次排列的“A”“B”“C”“C′”“D”“E”“F”“G”8個β折疊、連接它們的氨基酸所構成的各種“環”結構(如BC環、C′D環、FG環等)以及從氨基末端至“A”的結構(稱為N環)[24-25];PD-L1分子胞外段的主要結構為從氨基末端至羧基末端依次排列的“A”“B”“C”“C′”“C″”“D”“E”“F”“G”9個β折疊、連接它們的氨基酸所構成的各種“環”結構(如BC環、C C′環、C′C″環、FG環等)以及從氨基末端至“A”的結構(稱為N末端區域)[26-27]。例如,納武利尤單抗的主要結合位點是PD-1的“N環”結構,結合面積約為1 487 ?2,Kd為1.45 nmol/L[24] ;帕博利珠單抗結合的主要部位是C′D環結構,結合面積約為2 126 ?2,結合面積越大,Kd值最小,為27 pmol/L,是目前親和力最強的PD-1/PD-L1抑制劑[25];西米普利單抗的結合部位及結合面積未見報道,其Kd值為6.11 nmol/L[28];特瑞普利單抗主要與FG環結合,結合面積約為2 011 ?2,Kd值為0.324 nmol/L[29];信迪利單抗主要與FG環結合,結合面積為322 ?2,Kd為0.25 nmol/L[30];卡瑞利珠單抗主要與CC′環和 FG環結合,結合面積為2 520 ?2,Kd值為3.31 nmol/L[31]。阿特朱單抗通過來自重鏈的3個CDR 環和來自輕鏈的1個CDR環結合PD-L1的前β-折疊,即主要通過覆蓋BC、CC′、C′C″和 FG 環中的殘基來主導結合,結合面積為2 106 ?2,Kd值400 pmol/L[32];阿維魯單抗的結合表位區域主要由PD-L1的C鏈、C′鏈、F鏈、G鏈和CC′環構成,結合面積為1 856 ?2,Kd值為42.1 pmol/L[22];度伐魯單抗的結合區域是PD-L1上的CC′環和 N 末端區域,結合面積為1 624 ?2,Kd值為667 pmol/L[33]。抗PD-1/PD-L1單抗藥物的相關信息及特點見表1。
3.3 抗PD-1/PD-L1單抗藥物的人源化程度、適應證及給藥劑量
[ 5 ] HERBST RS,BAAS P,KIM DW,et al. Pembrolizumab versus docetaxel for previously treated,PD-L1-positive,advanced non-small-cell lung cancer(KEYNOTE-010):a randomised controlled trial[J]. Lancet,2016,387(10027):1540-1550.
[ 6 ] RITTMEYER A,BARLESI F,WATERKAMP D,et al. Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer(OAK):a phase 3,open-label,multicentre randomised controlled trial[J]. Lancet,2017,389(10066):255-265.
[ 7 ] KAUFMAN HL,RUSSELL J,HAMID O,et al. Avelumab in patients with chemotherapy-refractory metastatic Merkel cell carcinoma:a multicentre,single-group,open- label,phase 2 trial[J]. Lancet Oncol,2016,17(10):1374- 1385.
[ 8 ] MASSARD C,GORDON MS,SHARMA S,et al. Safety and efficacy of durvalumab(MEDI4736),an anti-programmed cell death ligand-1 immune checkpoint inhibitor,in patients with advanced urothelial bladder cancer[J]. J Clin Oncol,2016,34(26):3119-3125.
[ 9 ] OKAZAKI T,HONJO T. The PD-1-PD-L pathway in immunological tolerance[J]. Trends Immunol,2006,27(4):195-201.
[10] YAO S,CHEN L. PD-1 as an immune modulatory receptor[J]. Cancer J,2014,20(4):262-264.
[11] OKAZAKI T,HONJO T. PD-1 and PD-1 ligands:from discovery to clinical application[J]. Int Immunol,2007,19(7):813-824.
[12] CHENG X,VEVERKA V,RADHAKRISHNAN A,et al. Structure and interactions of the human programmed cell death 1 receptor[J]. J Biol Chem,2013,288(17):11771- 11785.
[13] 邱曉,羅建輝.重組單克隆抗體藥物制劑處方的作用及相關審評要點[J]. 中國新藥雜志,2019,28(16):1947-1954.
[14] LOWE D,DUDGEON K,ROUET R,et al. Aggregation,stability,and formulation of human antibody therapeutics[J]. Adv Protein Chem Struct Biol,2011,84(84):41-61.
[15] KOLFSCHOTEN MV,SCHUURMAN J,LOSEN M,et al. Anti-inflammatory activity of human IgG4 antibodies by dynamic Fab arm exchange[J]. Science,2007,317(5844):1554-1557.
[16] YANG X,WANG F,ZHANG Y,et al. Comprehensive analysis of the therapeutic IgG4 antibody pembrolizumab:hinge modification blocks half molecule exchange in vitro and in vivo[J]. J Pharm Sci,2015,104(12):4002-4014.
[17] CRESCIOLI S,CORREA I,KARAGIANNIS P,et al. IgG4 characteristics and functions in cancer immunity[J]. Curr Allergy Asthma Rep,2016,16(1):7-9.
[18] DUMET C,POTTIER J,GOUILLEUX-GRUART V,? et al. Insights into the IgG heavy chain engineering patent landscape as applied to IgG4 antibody development[J]. MAbs,2019,11(8):1341-1350.
[19] 于傳飛,曹興軍,王文波,等. LC-MS法對抗PD-1信迪利單抗藥物分子鉸鏈區序列改構穩定性的研究[J].藥學學報,2019,54(1):122-129.
[20] SCALLON B,TAM S H,MCCARTHY S G,et al. Higher levels of sialylated Fc glycans in immunoglobulin G molecules can adversely impact functionality[J]. Mol Immu,2007,44(7):1524-1534.
[21] ABES R,TEILLAUD J. Impact of glycosylation on effector functions of therapeutic IgG[J]. Pharmaceuticals,2010,3(1):146-157.
[22] LIU K,TAN S,CHAI Y,et al. Structural basis of anti- PD-L1 monoclonal antibody avelumab for tumor therapy[J]. Cell Res,2017,27(1):151-153.
[23] LEE HT,LEE SH,HEO YS. Molecular interactions of antibody drugs targeting PD-1,PD-L1,and CTLA-4 in immuno-oncology[J]. Molecules,2019,24(6):1190-1195.
[24] TAN S,ZHANG H,CHAI Y,et al. An unexpected N-terminal loop in PD-1 dominates binding by nivolumab[J]. Nat Comm,2017,8(1):14369-14369.
[25] NA Z,YEO SP,BHARATH SR,et al. Structural basis for blocking PD-1-mediated immune suppression by therapeutic antibody pembrolizumab[J]. Cell Res,2017,27(1):147-150.
[26] LEE HT,LEE JY,LIM H,et al. Molecular mechanism of PD-1/PD-L1 blockade via anti-PD-L1 antibodies atezolizumab and durvalumab[J]. Sci Rep,2017,7(1):5532- 5532.
[27] LIU K,TAN S,CHAI Y,et al. Structural basis of anti-PD-L1 monoclonal antibody avelumab for tumor therapy[J]. Cell Res,2017,27(1):151-153.
[28] MARKHAM A,DUGGAN S. Cemiplimab:first global approval[J]. Drugs,2018,78(17):1841-1846.
[29] LIU H,GUO L,ZHANG J,et al. Glycosylation-independent binding of monoclonal antibody toripalimab to FG loop of PD-1 for tumor immune checkpoint therapy[J]. MAbs,2019,11(4):681-690.
[30] HOY SM. Sintilimab:first global approval[J]. Drugs,2019,79(3):341-346.
[31] ANTHONY M,SUSAN JK. Camrelizumab:first global approval[J]. Drugs,2019,79(12):1355-1361.
[32] ZHANG F,QI X,WANG X,et al. Structural basis of the therapeutic anti-PD-L1 antibody atezolizumab[J]. Oncotarget,2017,8(52):90215-90224.
[33] TAN S,LIU K,CHAI Y,et al. Distinct PD-L1 binding characteristics of therapeutic monoclonal antibody durvalumab[J]. Protein Cell,2018,9(1):135-139.
[34] FDA. Center for drug evaluation and research:application number:125554 ORIG1S000:clinical pharmacology and bio-pharmaceutics review(s)[EB/OL].(2014-12-22)?[2019-12-31]. https://www.accessdata.fda.gov/drugsatfda_docs/nda/2014/125554Orig1s000ClinPharmR.pdf.
[35] FDA. Center for drug evaluation and research:application number:125514 ORIG1S000:clinical pharmacology and bio-pharmaceutics review(s)[EB/OL].(2014-09-04)?[2019-12-31] . https://www.accessdata.fda.gov/drugsatfda_docs/nda/2014/125514Orig1s000ClinPharmR.pdf.
[36] FDA. Center for drug evaluation and research:application number:125514 ORIG1S000:clinical pharmacology and bio-pharmaceutics review(s)[EB/OL].(2018-09-28).[2019-12-31]. https://www.accessdata.fda.gov/drugsatfda_docs/nda/2018761097Orig1s000ClinPharmR.pdf.
[37] 國家藥品監督管理局藥品評審中心.受理號:CXSS1800- 006[EB/OL].(2018-03-20)[2019-12-31]. http://www. cde.org.cn/news.do?method=changePage&pageName=service&frameStr=19/2019/03/CXSS18 00006.
[38] 國家藥品監督管理局藥品評審中心.受理號:CXSS1800-?008[EB/OL].(2018-04-19)[2019-12-31]. http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=19/2019/03/CXSS1800008.
[39] 國家藥品監督管理局藥品評審中心.受理號:CXSS1800-?009[EB/OL].(2018-04-23)[2019-12-31]. http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=19/2019/07/CXSS18 00009
[40] FDA. Center for drug evaluation and research:application number:761034 ORIG1S000:clinical pharmacology and bio-pharmaceutics review(s)[EB/OL].(2016-05-18).[2019-12-31] https://www.accessdata.fda.gov/drugsatfda_docs/nda/2016/761034Orig1s000ClinPharmR.pdf.
[41] FDA. Center for drug evaluation and research:application number:761049 ORIG1S000:clinical pharmacology and bio-pharmaceutics review(s) [EB/OL].(2017-03-23)[2019-12-31]. https://www.accessdata.fda.gov/drugsatfda _docs/nda/2017/761049Orig1s000ClinPharmR.pdf.
[42] FDA. Center for drug evaluation and research:application number:761069 ORIG1S000:clinical pharmacology and bio-pharmaceutics review(s)[EB/OL].(2017-05-01)?[2019-12-31]. https://www.accessdata.fda.gov/drugsatfda_docs/nda/2017/761069Orig1s000ClinPharmR.pdf.
[43] 岳雅麗,尹駿,高向東,等.雙特異性抗體藥物在腫瘤治療領域的研究進展[J].中國藥科大學學報,2019,50(3):289-298.
[44] 吳夢儀,徐雯,王洪允.固定劑量給藥在抗腫瘤單抗藥物中的選擇和應用[J].中國臨床藥理學雜志,2019,35(19):2471-2474.
[45] SHI S. Biologics:an update and challenge of their pharmacokinetics[J]. Curr Drug Metab,2014,15(3):271-290.
[46] LIU B,GUO H,XU J,et al. Acid-induced aggregation propensity of nivolumab is dependent on the Fc[J]. MAbs,2016,8(6):1107-1117.
[47] LEE JW. ADME of monoclonal antibody biotherapeutics:knowledge gaps and emerging tools[J]. Bioanalysis,2013,5(16):2003-2014.
(收稿日期:2020-02-25 修回日期:2020-08-19)
(編輯:孫 冰)

