曲美他嗪對穩定型心絞痛合并陣發性心房顫動患者療效的研究
陳海燕,李 強,傅曉丹
(東莞市濱海灣中心醫院心內科,廣東 東莞 523900)
隨著我國正步入老年化社會,冠心病及陣發性心房顫動(房顫)患者發病率呈逐年攀升[1-2],同時冠心病合并陣發性房顫患者患病率也較高,且因患者冠狀動脈存在狹窄,一旦發生陣發性房顫則快心室率會加重患者心絞痛癥狀。因此,急需探尋有效減輕冠心病合并陣發性房顫患者癥狀的治療方案。曲美他嗪(trimetazidine,TMZ)在心肌缺血時通過改善心肌能量代謝及抗炎等作用能有效減輕心絞痛發作[3],但TMZ在房顫中的研究報道較少,既往研究發現TMZ可延緩高血壓病伴射血分數正常的心力衰竭患者左房重構[4],而心房重構在房顫發生及進展中發揮了重要作用。因此,本研究重點觀察TMZ對穩定型心絞痛合并陣發性房顫患者的療效。
1 資料與方法
1.1一般資料:選取2010年8月~2016年12月在我院住院或門診的穩定型心絞痛伴陣發性房顫患者320例為研究對象,年齡37~68歲,均符合穩定型心絞痛和陣發性房顫的診斷標準,排除高血壓病3級,不穩定型心絞痛、急性心肌梗死、急性左心衰、肥厚型心肌病、擴張型心肌病、心臟瓣膜病、嚴重肝腎功能不全、甲狀腺功能亢進等疾病。320例患者隨機分為采用常規治療的對照組160例,男82例,女78例;在常規治療基礎上加用TMZ治療的治療組160例,男79例,女81例。兩組病例分布差異無統計學意義(P>0.05),具有可比性。
1.2治療方法:對照組中使用β受體阻滯劑控制心率及控制血壓(富馬酸比索洛爾5 mg,1次/d,研究期間均服用),部分血壓較高患者加用CCB控制血壓(苯磺酸氨氯地平片5 mg,1次/d,研究期間均服用)、阿托伐他汀調脂(20 mg,1次/d,研究期間均服用)、拜阿司匹林抗血小板聚集(100 mg,1次/d,研究期間均服用)。如果患者CHA2DAS2VASC評分在2或以上則將拜阿司匹林更換為華法林(INR控制在2~3之間)抗凝治療。TMZ治療組在相同美托洛爾及CCB的劑量及用藥周期基礎上加用TMZ 20 mg/次,3次/d。兩組觀察時間為12個月,隨訪過程中對照組9例(5女,4男)患者退出本研究,治療組13例患者(6男,7女)退出本研究。
1.3研究方法
1.3.1試驗設計:本研究為單中心研究,研究者遵循臨床研究倫理學規范,入組患者簽署知情同意書。該研究觀察期為12個月,在研究的最初2周內患者繼續服用原來藥物,目的是在此期間評估病情的穩定性。后續隨訪期間,分別在第6個月及第12個月時檢測相應觀察指標。
1.3.2心絞痛的評估:分別記錄治療前、治療后6個月及治療后12個月時各組住院或門診患者的心絞痛持續時間及每月發作頻次,通過向入組患者發放預先設計好的“心絞痛簡易評估表”進行記錄。
1.3.3心臟彩超指標檢測:通過M型超聲測量患者左心房舒張末內徑(LAEDD)、左心室射血分數(LVEF)、左心室后壁厚度等。
1.3.4心房顫動頻次及負荷評估:分別于研究的第6個月及第12個月行24 h 動態心電圖檢測(分別在觀察的這2個月內各做4次動態心電圖),分別計算房顫發作頻率及房顫負荷(房顫負荷定義為:24 h內房顫發作持續時間百分比)。

2 結果
2.1兩組患者心絞痛情況比較:同對照組相比,治療6個月后治療組中患者心絞痛每月發作頻次顯著減少,差異有統計學意義(P=0.014,P<0.05);每次心絞痛持續時間有所縮短,但差異無統計學意義(P=0.095,P>0.05)。而治療12個月后治療組中患者心絞痛持續時間(5 min vs. 3 min)及每月發作頻次均顯著減少(2.5次/月vs. 2.1次/月),差異均有統計學意義(P=0.031,P<0.05)。見表1。
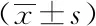
表1 兩組治療前后心絞痛發作頻次及持續時間變化
2.2兩組患者心臟超聲指標比較:同對照組相比,治療6個月后治療組中患者LAEDD有所縮短,但差異無統計學意義(P>0.05);治療12個月后治療組中患者的LAEDD顯著縮短(36.81±1.07 mm vs. 34.35±1.09 mm),差異有統計學意義(P=0.027,P<0.05)。見表2。

表2 兩組患者治療前后心臟超聲指標LAEDD比較
2.3兩組患者房顫發作頻率及房顫負荷的比較:同對照組相比,治療6個月后治療組中患者房顫每月發作頻率及房顫負荷有所降低,但差異無統計學意義(P>0.05);治療12個月后治療組中患者的房顫每月發作頻率(1.5次/月 vs. 0.9次/月)及房顫負荷(1.1 h/24 h vs. 0.7 h/24 h)均顯著降低,差異有統計學意義(P<0.05)。見表3。
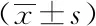
表3 兩組治療前后房顫發作頻率及房顫負荷變化
3 討論
冠心病患者合并陣發性心房顫動者眾多且危害嚴重,既往多項研究證實:冠心病并發陣發性房顫患者比例較高[5],我國老年冠心病患者并發陣發性房顫的比例高達20.9%[6]。房顫與冠心病互為風險因素,房顫顯著增加冠心病患者心血管事件及死亡風險[7]。穩定型心絞痛合并陣發性房顫患者內科藥物治療仍然是主要的方法,但藥物治療的效果依然不理想,因此迫切需要優化冠心病合并陣發性房顫患者的藥物治療方案。
既往研究發現:心房重構是房顫形成及維持的主要機制[8-9],因而抑制心房重構是房顫防治的重要方法。本研究發現:TMZ可通過減少心絞痛發作頻率及持續時間、抑制心房重構及減輕房顫負荷,從而提高穩定型心絞痛合并陣發性心房顫動患者的療效;TMZ治療組左心房舒張末內徑顯著縮短,提示TMZ能夠在美托洛爾等控制房顫心室率及改善心臟功能藥物的基礎上進一步減小LAEDD。既往大量基礎及臨床研究均顯示,左心房增大即是心房顫動的易發因素,也是心房顫動的結果,兩者互為惡性循環,因此抑制左心房重構有利于減輕房顫負荷。
心臟是富含線粒體的高耗能器官[10],對能量需求較大,心房顫動時心房率可高達300次/min以上,因此房顫期間心臟耗能顯著增加。TMZ作用于線粒體代謝關鍵酶[11],通過減少ATP的消耗,在心肌缺氧或缺血情況下通過改善心肌能量代謝,從而維持離子泵的正常功能,進而維持細胞內環境的穩定。因而TMZ可能通過改善心房肌能量代謝,從而抑制心房肌重構,進而減少房顫發作頻次及房顫負荷。此外,心絞痛發作時疼痛及患者過度緊張勢必引起交感神經興奮,從而加重心房重構。TMZ可能通過減少心絞痛發作頻次及持續時間,從而抑制交感神經過度激活,從而改善心房重構。自噬在心房重構過程中發揮著重要作用,最近研究證實TMZ可通過促進自噬流進而減輕心肌缺氧性損[12],TMZ是否通過促進自噬流改善心房重構值有待進一步研究。

