三元材料中鎳、鈷、錳檢測方法研究
邸衛利
(大連博融新材料有限公司 QEHS部,大連 116450)
三元是指,鋰電池里面的正極材料名稱。常規的電池正極材料是鈷酸鋰LiCoO2,三元材料則是鎳鈷錳酸鋰Li(NiCoMn)O2,三元復合正極材料前驅體產品,是以鎳鹽、鈷鹽、錳鹽為原料,里面鎳鈷錳的比例可以根據實際需要調整,三元材料做正極的電池相對于鈷酸鋰電池安全性高,能量密度高,成本相對較低,循環性能優異,是目前量產的正極材料中潛力最大最有發展前景的一種。
三元材料中鎳、鈷、錳沒有固定的檢測方法,現將試樣溶解后稀釋,然后采用電感耦合等離子體原子發射光譜(ICP-AES)法[2]進行檢測,誤差大,不能滿足三元材料鎳、鈷、錳檢測要求。基于這一情況,開發三元材料中鎳、鈷、錳檢測方法非常重要。本實驗用過量的鐵氰化鉀對試樣中的鈷完全氧化;然后利用電位滴定儀[3],通過硫酸鈷標準溶液對過量的鐵氰化鉀進行返滴定[4],得到鈷含量;利用高錳酸鉀標準溶液對溶液中二價錳進行滴定,得到錳含量,這兩步滴定均使用DMI140氧化還原[5]復復合電極進行滴定;用EDTA-2Na絡合重新溶解的試樣,用氫氧化鈉進行滴定,得到三元材料中鎳、鈷、錳總含量,該步驟使用DGI111-SC復合電極進行滴定,在這一環節中堿金屬元素雜質對檢測結果無影響,其它與EDTA二鈉發生絡合反應的雜質對鎳檢測結果有正向影響,當雜質含量總和小于0.03mmol時,對鎳檢測結果影響可以忽略不計;最后用總含量減掉鈷和錳的含量得到鎳的含量。
1 實驗部分
1.1 錳的檢測原理
利用焦磷酸鈉做絡合劑,在中性條件下,通過高錳酸鉀對試樣中二價錳進行滴定,得出試樣中二價錳的含量。
4Mn2++MnO4-+8H+→SMn3++4H2O
1.2 鈷的檢測原理
在檸檬酸銨存在的介質中,用過量的鐵氰化鉀對試樣中的鈷進行氧化,然后通過電位滴定儀用鈷標準溶液對過量的鐵氰化鉀進行滴定,得出樣品中的鈷含量。
1.3 鎳鈷錳總和檢測原理
Na2H2Y+Mn2+→Na2MnY+2H+
Na2H2Y+Co2+→Na2CoY+2H+
Na2H2Y+Ni2+→Na2NiY+2H+
HCl+NaOH=NaCl+H2O
1.4 鎳檢測原理
鎳含量=鎳、鈷、錳檢測總量-鈷含量-錳含量。
1.5 儀器及試劑
T50 電位滴定儀(梅特勒-托利多);DMI140氧化還原復核電極(梅特勒-托利多);DGI111-SC復合電極(梅特勒-托利多);XSE204分析天平(梅特勒-托利多); ML3002精密天平(梅特勒-托利多);2mL、5mL大肚吸管。硫酸銨(AR,國藥);濃氨水(AR,國藥);硫酸銨(20%,國藥)檸檬酸銨(AR,國藥);檸檬酸銨(30%,國藥);七水硫酸鈷(工作基準,分子量281.10,國藥);鐵氰化鉀(AR,分子量329.248,國藥);高錳酸鉀(AR,國藥);硫酸(GR)(國藥);硫酸溶液(8+92,GR);硫酸溶液(1+11,GR);十水焦磷酸鈉(分析純);飽和十水焦磷酸鈉(120g/L);硫酸錳(SP,分子量169.02,一水);氫氧化鈉(GR);鹽酸標準溶液(1.017mol/L)有證標準物質;氫氧化鈉標準溶液(0.5000mol/L,國家標準物質中心);鹽酸(GR,國藥);硫酸鎳(99.9%,六水,分子量262.86,阿拉丁);EDTA-2Na(AR,國藥)。
1.6 鈷標準溶液(0.05mol/L)
準確稱取硫酸鈷(1.4.6) 3.5144g于250mL燒杯中,加入100mL三級水,加熱溶解后冷卻,轉移至250mL容量瓶中,補水至刻度。
1.7 鐵氰化鉀標準溶液的配制與標定(0.05mol/L)
1.7.1鐵氰化鉀標準溶液的配制
準確稱取鐵氰化鉀4.1000g(1.4.8)于250mL燒杯中,加入100mL三級水,加熱溶解后冷卻,轉移至250mL容量瓶中,補水至刻度。
1.7.2鐵氰化鉀標準溶液的標定
準確移取5mL鐵氰化鉀標準溶液,加少量水稀釋,加入15mL硫酸銨,30mL檸檬酸銨,50mL氨水,補水至150mL左右,用硫酸鈷標準溶液滴定,計算出鐵氰化鉀標準溶液的濃度。
1.8 硫酸錳標準溶液的配制
準確稱取1.6700g左右的硫酸錳(1.4.16)于250mL燒杯中,加水至150mL左右,加熱溶解,冷卻后轉移至250mL容量瓶中,用三級水定容至刻度。
1.9 氫氧化鈉標準溶液配制與標定
1.9.1氫氧化鈉標準溶液配制
(1)稱取110 g氫氧化鈉(1.4.18),溶于100mL無二氧化碳水中,搖勻,注入聚乙烯容器中,密閉放置至溶液清亮。
(2)氫氧化鈉標準滴定溶液(0.5 mol/L):用塑料管量取上層清液27mL,用無二氧化碳的水稀釋至1000mL,搖勻,待標定。
1.9.2氫氧化鈉標準溶液的標定
準確稱取5mL鹽酸標準溶液于250mL燒杯中,加無二氧化碳的水至150mL,用電位滴定儀,DGI111-SC復合電極,以氫氧化鈉標準滴定溶液(1.4.20.1 b)作為滴定劑進行滴定,同時做空白實驗。
1.10 高錳酸鉀標準溶液配制與標定
1.10.1高錳酸鉀標準溶液的配制
稱取13.0 g高錳酸鉀于5L燒杯中,加水至3L,加熱至沸騰,并保持微沸1h,冷卻到室溫,補水至3L。于暗處放置兩周后,用3#砂芯漏斗(在此高錳酸鉀溶液中緩慢煮沸5min)過濾,用少量濾液潤洗棕色試劑瓶,棄去潤洗液,將高錳酸鉀濾液移至該試劑瓶中置于暗處常溫保存,待標定。
1.10.2高錳酸鉀溶液的標定
準確移取20mL硫酸錳標準溶液,加入30mL飽和焦磷酸鈉溶液,用硫酸和氨水調節pH至7±0.5,至電位滴定儀上,用高錳酸鉀標準溶液滴定至終點,計算出高錳酸鉀的濃度。
1.11 硫酸鎳溶液(200g/L)
準確稱取50.0000克左右的硫酸鎳于250mL燒杯中,加水至150mL左右,加熱溶解,冷卻后轉移至250mL容量瓶中,用三級水定容至刻度。
1.12 EDTA-2Na(50g/L)
稱取EDTA二鈉(1.4.25)50.0g于500mL燒杯中,加入蒸餾水約500mL左右,加熱溶解后冷卻,最后轉移至1000mL容量瓶中,加水至刻度。
1.13 樣品溶解及預處理
稱取試樣0.2000g左右于250mL燒杯中,加入5mL鹽酸(1.4.22)微熱至樣品完全溶解后,繼續蒸發使樣品濃縮至近干。
2 樣品檢測過程
2.1 錳的檢測過程
向上述玻璃杯中加入20mL飽和焦磷酸鈉溶液,用10%的硫酸和氨水調節pH至7.0±0.5,加水至150mL,放在電位滴定儀上,用高錳酸鉀滴定至終點。
2.2 鈷的檢測過程
將上述溶液轉移至500mL燒杯中,加入15mL硫酸銨溶液,30mL檸檬酸銨溶液,準確加入20mL鐵氰化鉀標準溶液,50mL濃氨水,補水至250mL,用鈷標準溶液滴定至終點。
2.3 鎳、鈷、錳總量測定
稱取試樣0.2000g左右于250mL燒杯中,加入5mL鹽酸微熱至樣品完全溶解后,繼續蒸發使樣品濃縮至近干。加入20mL EDTA二鈉(1.4.26),補水至150mL左右,放在電位滴定儀上,用氫氧化鈉標準溶液滴定至終點。
2.4 鎳含量檢測
通過鎳、鈷、錳總量檢測結果、鈷含量檢測結果、錳含量檢測結果計算出鎳含量檢測結果。
3 結果與討論
3.1 鐵氰化鉀標準溶液的標定(表1)

表1 硫酸鈷標定鐵氰化鉀
3.2 氫氧化鈉標準溶液的標定(表2)

表2 鹽酸標定氫氧化鈉
3.3 高錳酸鉀的標定(表3)

表3 硫酸錳標定高錳酸鉀
3.4 方法回收率實驗
3.4.1鈷的加標回收率實驗(表4、圖1)

表4 鈷加標回收率
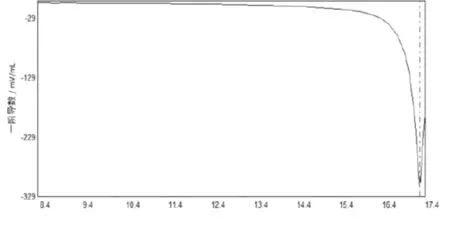
圖1 鈷加標回收實驗譜圖
3.4.2錳加標回收率實驗(表5、圖2)

表5 錳加標回收率

圖2 錳加標回收實驗譜圖
3.4.3鎳加標回收率實驗(表6、圖3)

表6 鎳加標回收率
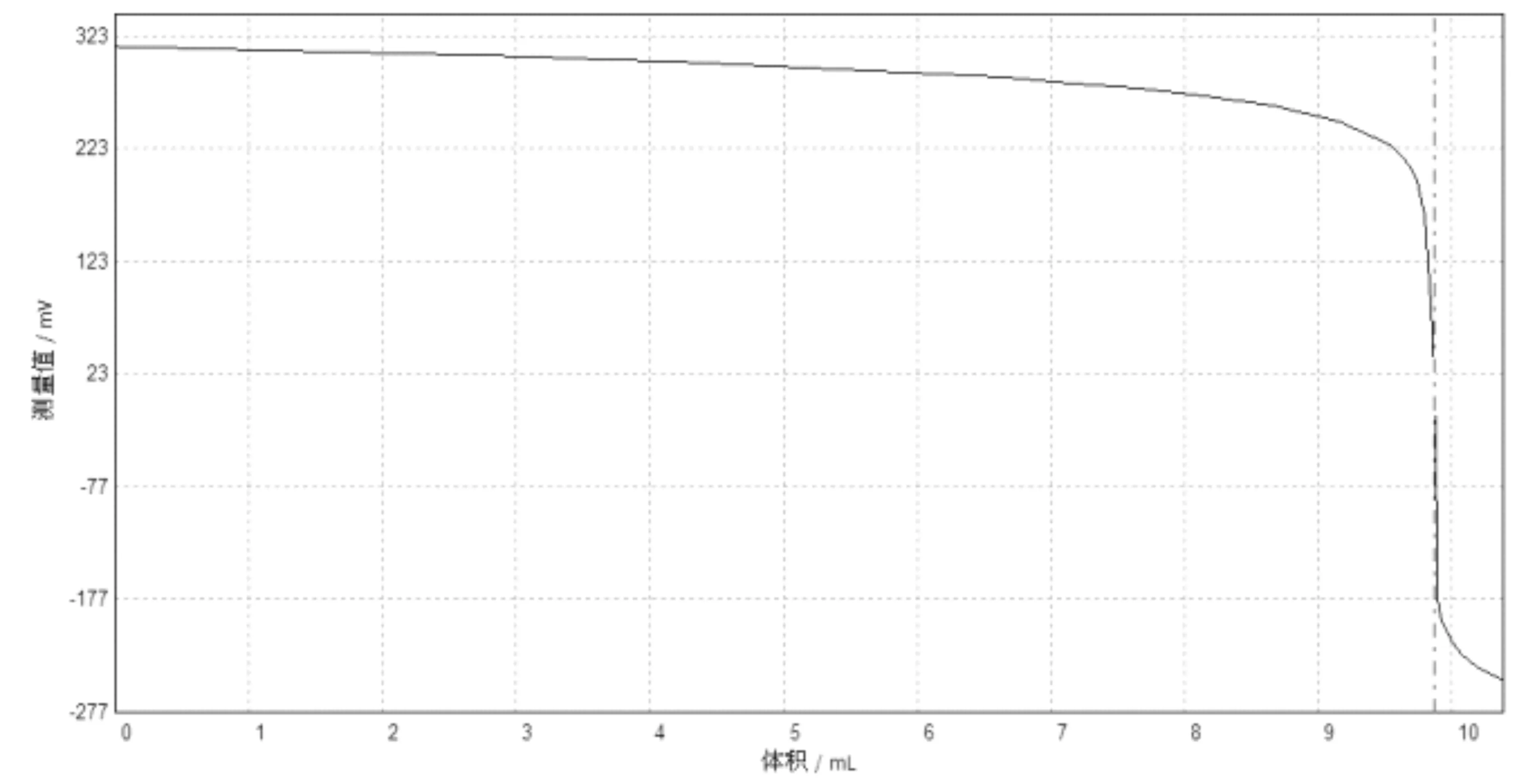
圖3 鎳加標回收實驗譜圖
3.5 鎳鈷錳三元材料樣品檢測與ICP法檢測對比(表7)

表7 滴定法與ICP法測定三元材料樣品數據對比
3.5.1ICP法與本方法相比較
ICP法測定結果誤差較大,相對誤差:Mn%:15.26%,Co%:9.33%,Ni%:1.19%,無法精確地指導生產; 本方法測定結果相對誤差為:Mn%:1.30%,Co%:1.00%,Ni%:1.00%,滿足檢測需求。
3.5.2從檢測時間方面比較
ICP檢測時間大約在2h左右,本方法檢測時間大約在0.5h左右。
3.5.3本方法與ICP法主要影響因素
(1)本方法:鐵氰化鉀要避光保存,現用現配,現標定;錳檢測時pH值調節要保證在pH值在7.0±0.5;鈷檢測要注意試劑加液順序;鎳、鈷、錳檢測要注意EDTA-2Na加入量。
(2)ICP法:標線的范圍要合理,線性關系要好;樣品中Ni、Co、Mn要在標線范圍之內。
4 結論
本方法解決了三元材料中鎳、鈷、錳含量快速檢測問題,在鎳、鈷、錳三元材料中,鈷加標回收率在99.05~99.22之間,錳加標回收率在99.77~100.68之間,鎳加標回收率在99.44~100.02之間,檢測速度滿足檢測需求;樣品檢測準確性滿足客戶與生產需求。

