腹腔鏡手術治療胃腸道間質瘤的效果及預后分析
李亞平,朱明杰,蔣鴻元
胃腸道間質瘤(gastrointestinal stromal tumor,GIST)是臨床最常見的間葉源性消化道腫瘤,發病率為0.6%~3%,其中60%~70%的GIST發生于胃,20%~30%GIST發生于小腸,還可見于食管、結直腸及腹膜等部位[1-2]。GIST生物學行為可為良性或惡性,缺少統一病理分級標準。目前臨床上多根據GIST的腫瘤最大直徑、有絲分裂計數和腫瘤起源部位等分類指標進行危險度評估,并為其治療方案選擇和預后判斷提供參考依據[3]。GIST以多學科治療(multidisciplinary team, MDT)為基礎,由于其對放化療敏感性較差,分子靶向藥物治療尚在發展階段,故根治性手術被認為是現階段的最佳治療手段,腫瘤直徑>2 cm或直徑≤2 cm但存在高危因素的GIST患者應及時手術切除,并盡可能保證切緣陰性以避免二次手術[4-5]。隨著微創外科技術的發展,腹腔鏡在腹部疾病中應用逐漸增多,本研究探討了腹腔鏡手術和開腹手術治療GIST的效果及預后情況,旨在為臨床選擇合理手術方案提供依據。現報告如下。
1 資料與方法
1.1一般資料 回顧性分析我院2011年6月—2014年6月收治的157例GIST患者的臨床資料。①納入標準:術后病理確診為GIST;術后能完成隨訪且患者臨床資料保存完整;患者及家屬知曉本研究并簽署同意書。②排除標準:合并其他類型原發惡性腫瘤;已發生遠處轉移者。根據手術方案將患者分為腹腔鏡組84例和開腹組73例。腹腔鏡組男38例,女46例;年齡43~79(61.27±10.38)歲,腫瘤直徑<5 cm者61例,≥5 cm者23例;病灶位置:胃57例,小腸18例,直腸9例;腫瘤風險分級[6]:高風險16例,中風險25例,低風險43例。開腹組男31例,女42例;年齡45~76(60.74±10.63)歲,腫瘤直徑<5 cm者56例,≥5 cm者17例;病灶位置分別為胃52例,小腸13例,直腸8例;腫瘤風險分級高風險11例,中風險23例,低風險39例。2組性別、年齡、腫瘤直徑、病灶位置等比較差異無統計學意義(P>0.05),具有可比性。
1.2方法 2組患者術前均完善血生化、影像學及內鏡等相關檢查并做好術前準備,均采用氣管插管全身麻醉。腹腔鏡組患者取仰臥分腿位,常規于臍下緣穿刺,建立CO2人工氣腹并維持壓力為12~14 mmHg,臍部作10 mm切口為觀察孔,然后根據腫瘤位置選擇左側或右側鎖骨中線肋緣下2~4 cm處為操作孔,采用30°腹腔鏡探查腹腔和盆腔情況,明確腫瘤位置、大小及形態并選擇適當手術方式進行切除,將標本自臍部切口取出送病理科進行冷凍切片和石蠟切片檢查。開腹組患者取仰臥位,作腹部正中切口并自邊緣2~3 cm處切除腫瘤組織送病理檢查。2組術后均給予胃腸減壓、腹腔引流及抗感染治療,患者排氣后拔除胃管并進流質飲食,次日根據引流情況酌情拔除引流管。
1.3觀察指標 ①圍術期指標:記錄2組手術時間、術中出血量、排氣時間、引流時間及住院時間等。②并發癥:比較2組術后切口感染、肺部感染及吻合口瘺等發生率。③預后情況:2組術后均隨訪5年并觀察患者總體生存率(OS)和無復發生存率(RFS),同時比較不同部位和不同危險分級GIST患者隨訪期間OS和RFS。
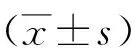
2 結果
2.1圍術期指標比較 腹腔鏡組手術時間、術中出血量、排氣時間、引流時間及住院時間均少于開腹組(P<0.05)。見表1。
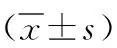
表1 2組GIST患者圍術期指標比較
2.2術后并發癥比較 腹腔鏡組術后并發癥總發生率低于開腹組(P<0.05)。見表2。

表2 2組GIST患者術后并發癥比較[例(%)]
2.3隨訪期間生存情況比較 2組術后5年OS分別為85.71%、79.52%,RFS分別為72.60%、65.81%。2組5年OS和RFS比較差異無統計學意義(P>0.05)。見圖1。

圖1 2組GIST患者隨訪5年OS和RFS比較A. 2組GIST的OS比較; B.2組GIST的RFS比較;GIST為胃腸道間質瘤,OS為總體生存率,RFS為無復發生存率
2.4不同部位GIST患者隨訪期間生存情況比較 157例GIST患者中發生于胃部占69.43%(109/157),該部位患者的5年OS為86.20%,RFS為74.30%;發生于小腸及直腸占30.57%(48/157),該部位OS、RFS分別為75.04%和58.30%。小腸及直腸GIST患者的RFS顯著低于胃GIST(P<0.05),但二者OS比較差異無統計學意義(P>0.05)。見圖2。

圖2 不同位置GIST患者隨訪5年OS和RFS比較A.不同部位GIST的OS比較;B.不同部位GIST的RFS比較;GIST為胃腸道間質瘤,OS為總體生存率,RFS為無復發生存率
2.5不同危險分級GIST患者隨訪期間生存情況比較 157例GIST患者的風險度分別為高風險17.20%(27/157),中風險30.57%(48/157),低風險52.23%(82/157),3組5年OS分別為65.41%、83.32%和89.22%,RFS分別為51.90%、66.71%和76.82%。中、高風險GIST患者5年OS和RFS均低于低風險GIST患者,且高風險GIST患者低于中風險GIST患者(P<0.05)。見圖3。

圖3 不同危險分級GIST患者隨訪5年OS和RFS比較A.不同危險分級GIST患者OS比較;B.不同危險分級GIST患者RFS比較;GIST為胃腸道間質瘤,OS為總體生存率,RFS為無復發生存率
3 討論
1983年Mazur和Clark對27例胃壁間葉來源腫瘤進行免疫組化分析并提出GIST概念,該類患者缺乏特異性臨床表現,早期常無明顯自覺癥狀,其診斷主要依據影像學檢查、免疫組化和基因檢測[7-8]。GIST可見于各年齡段,但50歲以上患者占比超過80%,不同國家和地區發病率存在一定差異,總體約為1/10萬,近年來隨著影像學和病理診斷技術的不斷發展,其檢出率呈明顯上升趨勢,因此探討更為安全有效的GIST治療方案具有重要臨床意義[9]。
目前GIST常用手術方案包括腹腔鏡、內鏡和開放手術,內鏡的療效與開腹手術相當,且在術中出血量和術后康復速度方面均具有明顯優勢,但內鏡平均切除直徑僅1.7 cm,因此多用于直徑<2 cm的患者治療[10-12]。隨著腹腔鏡技術的快速發展,其在GIST病灶切除中的效果已獲得認可,腹腔鏡手術較傳統開腹手術具有創傷小和康復快等微創優勢。近年來國內外均有報道稱腹腔鏡可用于直徑≥5 cm的GIST切除且2010年后NCCN指南已不再將腫瘤體積列為禁忌證[13-14]。腹腔鏡GIST手術根據腫瘤位置和大小可采用不同術式,以胃楔形切除、胃大部切除或全胃切除等應用較為廣泛。本研究結果顯示,腹腔鏡組手術時間、術中出血量、排氣時間、引流時間及住院時間均明顯少于開腹組,且術后并發癥發生率較開腹組明顯降低,切口感染、肺部感染、術后出血、吻合口瘺及腸梗阻發生情況較少。表明腹腔鏡手術治療GIST有利于減輕手術創傷和并發癥,對促進患者術后康復具有積極作用,與Pelletier等[15]、Cui等[16]報道結果基本一致。GIST患者預后情況普遍較好,Ntahompagaze等[17]報道,腹腔鏡手術和開腹手術后1、3、5年生存率分別為98.5%、92.9%、87.4%和91.7%、85.2%、76.8%,兩種手術方案患者預后相近。本研究結果顯示,腹腔鏡組和開腹組5年OS分別為85.71%、79.52%,RFS分別為72.60%、65.81%,2組整體生存情況比較差異無統計學意義。表明腹腔鏡手術治療GIST臨床效果與開腹手術相當。
GIST預后與生物學行為關系密切,目前主要綜合腫瘤解剖形態、組織病理和臨床癥狀等多方面進行危險度評估來判斷預后情況,以美國國立衛生研究院(NIH)共識方案應用較為廣泛,其評估內容大致包括腫瘤最大徑、有絲分裂計數和起源部位等方面,胃部GIST生物學行為大多呈一定惰性,但小腸和直腸等部位GIST則具有較強侵襲性,可能導致患者術后復發或轉移風險增加[18-19]。本研究結果顯示,胃部患者術后5年OS為86.20%,RFS為74.30%;小腸及直腸患者術后5年OS為75.04%,RFS為58.30%,且2組RFS比較差異有統計學意義,表明胃部GIST患者預后情況相對更好。李鵬等[20]研究認為腫瘤直徑及核分裂象是GIST患者預后重要危險因素,而兩者均是NIH危險分級的主要內容。本研究結果顯示高、中、低風險GIST患者術后5年OS分別為65.41%、83.32%和89.22%,RFS分別為51.90%、66.71%和76.82%,三者間比較差異均有統計學意義。表明隨著危險程度增加,GIST患者遠期存活率明顯降低,因此對高風險GIST患者術后應加強隨訪,觀察腫瘤有無復發或轉移,并及時給予合理干預。
綜上所述,腹腔鏡手術與開腹手術治療GIST均具有良好效果,且腹腔鏡具有減輕手術創傷和并發癥等微創優勢。另外胃部和高危險度GIST患者預后情況相對較差,術后需加強隨訪。

