黃原膠添加對堿法誘導魔芋膠凝膠特性及凝膠機制的影響
李曉飛,李培源,李安琪,余文艷,郭綽,楊曦,郭玉蓉
黃原膠添加對堿法誘導魔芋膠凝膠特性及凝膠機制的影響
李曉飛,李培源,李安琪,余文艷,郭綽,楊曦,郭玉蓉
(陜西師范大學食品工程與營養科學學院,西安 710119)
【】探究黃原膠添加量對魔芋膠凝膠特性及凝膠機制的影響,為相關凝膠食品的開發利用提供理論依據和技術參考。以2%的魔芋膠溶膠為基質,通過添加不同濃度的黃原膠,制備混合多糖體系,并在2%的堿濃度(Na2CO3)及90℃的高溫下加熱混合體系2 h,冷卻后制得不同黃原膠含量(0-1.5%,w/v)的混合凝膠。通過測定混合凝膠強度,研究去離子水浸泡、2%檸檬酸溶液浸泡和凍融處理對凝膠樣品的影響。同時,采用掃描電鏡觀察不同處理凝膠的微觀形貌,探究不同處理及黃原膠添加量對魔芋膠凝膠結構的影響。另外,基于流變學、X-射線衍射以及熱重分析等手段,探究魔芋膠-黃原膠混合體系在熱堿處理過程中凝膠網絡的形成過程,揭示凝膠化機制。90℃恒溫加熱2 h后,隨黃原膠含量增加,混合凝膠強度反而降低,表明90℃加熱過程中,黃原膠的存在影響了魔芋膠凝膠網絡的形成。但室溫條件下,黃原膠含量越高,混合凝膠強度也越高,表明冷卻過程中黃原膠可能加強了凝膠網絡。經去離子水、2%檸檬酸溶液浸泡后,各處理凝膠強度均呈下降趨勢,以2%檸檬酸溶液浸泡處理后的凝膠強度降低最明顯。此外,凍融處理后,魔芋膠凝膠出現明顯的析水現象,析水率可達50%,但加入黃原膠后,混合凝膠的析水作用顯著降低,黃原膠含量越高,析水作用越弱。流變學測試結果表明,在90℃恒溫加熱2 h的過程中,隨黃原膠添加量增加,體系凝膠化速率減小,表明加入黃原膠降低了魔芋膠凝膠網絡的形成。隨后對該混合體系進行降溫掃描,發現當溫度從90℃降低至60℃時,凝膠彈性模量呈明顯降低趨勢,當溫度繼續降低至室溫時,凝膠彈性模量呈明顯增加趨勢,轉折點所對應的溫度為60℃,溫度越低,彈性模量越高,表明黃原膠分子在60℃時開始與魔芋膠網絡發生協同結合作用。黃原膠添加可顯著提高堿法誘導的魔芋膠凝膠在室溫下的凝膠強度,同時可改善該凝膠的凍融穩定性,該結論可為魔芋膠凝膠相關食品的開發提供有益參考。
魔芋膠;黃原膠;凝膠強度;流變學特性;凍融穩定性
0 引言
【研究意義】魔芋()屬天南星科多年生草本植物,在我國西南部地區和中西部地區有著悠久的種植歷史,魔芋膠(KGM)的主要成分是魔芋葡甘聚多糖,存在于球狀塊莖中[1-3],是一種低熱能、低蛋白質、高膳食纖維的物質,并且富含人體所需的十幾種氨基酸和微量元素,對高血壓、肥胖癥、糖尿病、便秘等有一定療效,可作為功能性食品食用[3-6]。魔芋膠還具有良好的水溶、增稠、穩定、懸浮、凝膠、成膜、粘結等多種優良的理化特性,可作為食品添加劑[1-2,7]。魔芋膠屬于非凝膠多糖,但在強堿性加熱條件下,魔芋膠會發生脫乙酰基反應形成熱不可逆凝膠[8-9]。然而,該凝膠存在凝膠強度低、析水明顯等缺點,一定程度上限制了魔芋膠食品的開發應用[10]。黃原膠(Xanthan)又稱黃膠、漢生膠,是由甘藍黑腐病野油菜黃單胞菌以碳水化合物為主要原料,經過好氧發酵產生的一種高黏度水溶性微生物胞外多糖[3,11]。在冷水和熱水中,黃原膠均可溶解[12],黃原膠溶液黏度很高,具有顯著的觸變性,且耐高溫、對pH不敏感等,在食品工業中常作為增稠劑、穩定劑,被廣泛應用[3,13-14]。黃原膠也屬于非凝膠多糖,但有研究表明[3,8],黃原膠與魔芋膠能形成協同凝膠,這種凝膠在室溫下有較好的粘彈性,但是在加熱條件下會由凝膠轉變為溶膠,是熱可逆凝膠,從而限制了該凝膠的進一步應用。本研究基于魔芋膠堿法誘導的凝膠特性以及魔芋膠與黃原膠協同凝膠化原理,制備出將兩種凝膠網絡貫穿為一體的凝膠。這種凝膠不僅具有熱不可逆的特性,而且兼具魔芋膠與黃原膠協同凝膠的優勢,可有效解決堿法誘導的魔芋膠凝膠在室溫下凝膠強度較低、析水明顯等問題,以期為魔芋膠相關食品的開發利用提供理論依據。【前人研究進展】游東宏等[15]研究發現,在pH為9.0、溫度75℃、以碳酸氫鈉為膠凝劑的條件下,魔芋葡甘聚糖凝膠的凝膠強度較大。GENEVRO等[16]研究表明,冷凍速度是影響魔芋膠凝膠最終物理性質的重要因素,冷凍速率緩慢時,凝膠網絡呈各向同性,且孔徑較大;冷凍速率較快時,網絡孔徑較小且網孔排列規整。此外,較高溫度條件下(-8℃)冷凍的水凝膠比低溫(-28℃)冷凍的水凝膠具有更高的穿透模量。ZHOU等[17]研究表明,與Na2CO3混合后,KGM鏈立即發生脫乙酰反應,誘導凝膠化,當溫度上升到70℃以上時,凝膠化才能完成,這表明KGM鏈的分子聚集不僅與氫鍵有關,而且與疏水相互作用有關。王元蘭等[11]將魔芋膠與黃原膠復配,發現在魔芋膠與黃原膠質量比為3﹕7時,復配凝膠表現出最高的黏度,且黏度隨溫度升高而下降。倪俊杰等[18]研究表明,魔芋膠-黃原膠復配體系具有假塑性,當魔芋膠的添加比例逐漸增大時,復配體系黏度系數K增大,流體系數n減小,當魔芋膠與黃原膠質量比為6﹕4時,復配體系的K值達到最大、n值最小,具有最強的假塑性及黏彈性。YANG等[19]測定了總膠濃度為1%的條件下,去離子水中魔芋膠與黃原膠的最佳協同比,發現當兩者比例為魔芋膠﹕黃原膠=6﹕4時,凝膠強度最大,這與倪俊杰等[18]研究結果一致。此外,YANG等[20]基于混合多糖體系的一般原理,研究了魔芋膠和海藻酸鈉的兼容性,并以魔芋膠和海藻酸鈉的混合體系為基質,制備出一類具有粘彈性、觸變性和涂抹性的乳液凝膠。上述結果表明,混合多糖體系可以改善單一多糖的缺點,擴大多糖在凝膠特性改良方面的應用范圍。【本研究切入點】雖然前人對魔芋膠凝膠形成條件以及魔芋膠-黃原膠協同凝膠方面進行了深入研究,但尚未解決魔芋膠凝膠強度較低、凍融穩定性差等缺點,也未能將魔芋膠-黃原膠協同凝膠的特性拓展應用于魔芋膠凝膠改性方面。本研究根據食品膠復配原理,首次將魔芋膠凝膠網絡與魔芋膠-黃原膠協同凝膠網絡貫穿在一起,制備出兼具兩種凝膠網絡優點的復合網絡凝膠,具有較深理論基礎及良好的應用前景。【擬解決的關鍵問題】基于流變學、電子顯微學、X-射線衍射以及熱重分析等手段,探究魔芋膠-黃原膠混合多糖體系在熱堿處理過程中凝膠網絡的形成過程,揭示兩層網絡之間的相互作用。
1 材料與方法
試驗于2019年8—11月在陜西師范大學食品工程與營養科學學院進行。
1.1 材料與試劑
魔芋膠、黃原膠,上海源葉生物科技有限公司;無水碳酸鈉,天津市天力化學試劑有限公司;檸檬酸,天津市科密歐化學試劑有限公司;以上均為分析純。
1.2 儀器與設備
PL203電子天平;EYELA OSB-2100恒溫水浴鍋;TA. XT. Plus質構儀,英國stable micro system公司;FD-1A-50真空冷凍干燥機,北京博醫康實驗儀器有限公司;Quanta 200環境掃描電子顯微鏡,FEI公司;AR-G2流變儀,美國TA公司;D8 Advance粉末X射線衍射儀,德國布魯克公司;Q1000DSC+LNCS+ FACS Q600SDT熱分析系統,美國TA公司。
1.3 方法
1.3.1 樣品制備 母液配置:用分析天平準確稱取30.00 g魔芋膠粉末溶解于1 L去離子水中,用去離子水溶解時一邊添加魔芋膠粉末一邊快速攪拌,隨后置于90℃的水浴鍋中加熱,不斷攪拌至完全水化,在室溫下平衡12 h,配置成3%的魔芋膠母液,備用。用分析天平準確稱取50.00 g黃原膠粉末溶解于1 L的去離子水中,用去離子水溶解時一邊添加黃原膠粉末一邊快速攪拌,隨后置于90℃的水浴鍋中加熱,不斷攪拌至完全水化,在室溫下平衡12 h,配置成5%的黃原膠母液,備用。水化過程中,用去離子水補償魔芋膠和黃原膠溶液因水分蒸發造成的損失。
取7個干凈的250 mL燒杯,編號為0—6號,按表1配方添加配置好的3% KGM母液、5% Xanthan母液和去離子水,置于90℃的水浴鍋中加熱,用玻璃棒攪拌至完全混合均勻,另外準確稱取4.00 g Na2CO3用10 mL去離子水溶解,緩慢加入到0—5號燒杯中,快速攪拌1 min,攪拌均勻后倒入100 mL燒杯中,用保鮮膜密封,在90℃水浴鍋加熱2 h后取出,在室溫下平衡12 h,制備的凝膠為圓柱形,大小和100 mL燒杯一致。同時,準確稱取4.00 g Na2CO3用6.7 mL去離子水溶解,緩慢加入到6號燒杯中,快速攪拌1 min,攪拌均勻后倒入100 mL燒杯中,用保鮮膜密封,在90℃水浴鍋中加熱2 h后取出,室溫下平衡12 h。

表1 樣品制備各組分添加量
1.3.2 凝膠強度測定 在90℃的條件下,將制備好的復合凝膠樣品用質構儀進行凝膠強度的測定[19,21]。參數設定:TPA壓縮模式,探頭P/0.5(直徑0.5英寸的圓柱狀平頭探頭),測試前速度:1.5 mm·s-1,測試速度:1.0 mm·s-1,測試后速度:1.0 mm·s-1,感應力:2 g,凝膠破裂點的力為凝膠強度,每個樣品重復3次。
此外,將制備好的樣品在室溫下平衡12 h,按照上述方法測定凝膠強度。
1.3.3 微觀結構觀察 將所有凝膠切割成邊長約為2 cm的立方塊,立刻將凝膠小塊浸沒于液氮中速凍。液氮浸沒約3 min后,將凍住的凝膠立刻轉移至真空冷凍干燥機中,在-50℃條件下凍干48 h。將凍干的凝膠折斷后,用導電雙面膠固定到樣品臺上,斷面朝上,噴金,采用Quanta 200環境掃描電鏡觀察凝膠斷面形貌,觀察時選擇高真空模式,高壓為20.0 kV,放大倍數800×[19,22]。
1.3.4 凍融穩定性 將制備好的凝膠在-18℃冷凍12 h,然后在室溫下解凍6 h后[5],參照1.3.2中的方法測定凝膠強度,并參照1.3.3中的方法觀察微觀結構。
此外,凝膠凍融后出現明顯的析水現象,因此也測定凝膠的析水率。具體操作如下:用分析天平準確稱取凍融前凝膠的質量記為1,準確稱取凍融處理后凝膠的質量記為2。每個樣品重復3次。按照以下公式計算樣品的析水率:
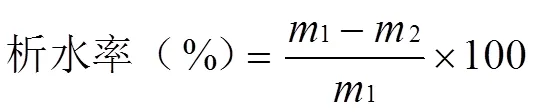
1.3.5 溶脹特性 將制備好的復合凝膠樣品分別浸泡在去離子水和2%檸檬酸溶液中12 h[8],參照1.3.2中的方法測定凝膠強度,并參照1.3.3中的方法觀察微觀結構。
1.3.6 流變學特性測定 時間掃描:按照表1添加配置好的3% KGM母液、5% Xanthan母液和去離子水,在室溫下攪拌均勻,準確稱取4.00 g的Na2CO3用10 mL去離子水溶解,加入燒杯中快速攪拌至均勻,移取3 mL混合樣品置于已經升溫至90℃的樣品臺上,立刻進行時間掃描,監測儲能模量G'與損耗模量G"的變化趨勢[23-24]。采用直徑為20 mm的轉子,平行板間隙設置為1 mm,應變為1%,頻率為1 Hz,時間為2 h,在轉子邊緣涂抹低密度硅油,防止試驗過程中樣品水分蒸發。
降溫掃描:時間掃描過程結束后,立刻進行降溫掃描,監測G'與G"的變化趨勢。采用直徑為20 mm的轉子,平行板間隙設置為1 mm,應變為1%,頻率為1 Hz,溫度從90℃降低到20℃,降溫速率為2 ℃·min-1,在轉子邊緣涂抹低密度硅油,防止試驗過程中水的蒸發[3,18]。
頻率掃描:當樣品溫度降低至20℃后,在該溫度條件下平衡10 min,然后在1—100 rad·s-1頻率范圍內進行頻率掃描,應變為1%[18]。
方程擬合:為了進一步分析凝膠在相同的堿濃度(2%)、溫度(90℃)條件下的凝膠化過程,本研究把上述時間掃描的G'匯總,并采用如下方程進行擬合:
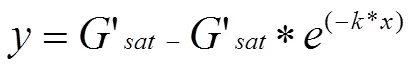
其中,G'為在無限的加熱時間下,的極限值;為凝膠化速率參數;為時間;為儲能模量。
1.3.7 X-射線衍射測定 將經過真空冷凍干燥的樣品置于60℃的烘箱中保持干燥,取干燥樣品進行X-射線衍射測定,XRD掃描范圍為2θ=5-80°[22,25-26]。
1.3.8 熱重分析 取大約10 mg樣品,以氮氣作為保護氣體,從室溫(20℃)加熱到600℃,加熱速率為10 ℃·min-1。結果分析采用TA Universal 2000 software[25]。
1.3.9 數據處理 上述所有測定均重復3次,每次測試均需更換樣品。所有圖表均使用Origin 2018軟件進行繪制,利用IBM SPSS22.0軟件進行差異顯著性分析(<0.05為差異顯著)。
2 結果
2.1 90℃和室溫下的凝膠強度
凝膠強度是反映凝膠內部網絡結構的一個重要參數。如圖1所示,在90℃下,所有樣品均表現出較低的凝膠強度,并且隨著黃原膠添加量的增加,樣品的凝膠強度呈下降趨勢,可能是因為黃原膠添加不利于魔芋膠凝膠網絡形成。冷卻至室溫后,樣品的凝膠強度急劇增加,隨著黃原膠添加量的增加,樣品的凝膠強度呈上升趨勢,一方面是因為總多糖濃度增加,另一方面是因為隨黃原膠添加量的增加,更多的黃原膠可以與魔芋膠分子形成協同凝膠。由于濃度高于5%的黃原膠母液較難制備,因此本研究并未進一步增加黃原膠添加量。

相同處理中,標注不同字母表示樣品間差異顯著(P<0.05)。下同
2.2 微觀結構
凝膠微觀網絡結構的致密程度與凝膠強度密切相關。如圖2所示,在黃原膠添加量為0的情況下,魔芋膠凝膠呈現出層狀結構;當黃原膠添加量為0.25%時,復合凝膠層狀結構更加明顯;隨黃原膠添加量進一步增加,復合凝膠層狀結構逐漸轉變為有交聯的網絡結構;隨著黃原膠添加量持續增加,復合凝膠網絡更加致密,表明黃原膠的添加能夠增大整個凝膠體系的網絡致密度,從而增強凝膠強度,一方面是因為總多糖濃度增加,另一方面是因為隨黃原膠添加量的增加,更多的黃原膠可以與魔芋膠分子形成協同凝膠。這與凝膠在室溫下測定的凝膠強度結果一致。
2.3 凍融穩定性
由圖3-A、B可知,在黃原膠添加量為0—1.0%時,凍融后凝膠樣品的強度增大,這是因為凍融導致水分析出,造成凝膠體積收縮,致使凝膠網絡致密度增加。然而當黃原膠添加量大于1.0%時,樣品凍融后凝膠強度顯著降低(<0.05)。此外,由圖3-C可看出,隨黃原膠添加量增加,凍融后樣品的析水率顯著降低(<0.05),說明添加黃原膠可改善魔芋膠凝膠的析水行為。由圖3-D可以看出,在黃原膠添加量為0的情況下,魔芋膠凝膠的層狀結構更加緊密,當黃原膠添加量為0.25%時,復合凝膠層狀結構轉變為有交聯的網絡結構,相較于未經過凍融處理的樣品凝膠網絡結構更加致密。當黃原膠添加量大于1.0%時,復合凝膠網絡網孔明顯增大。
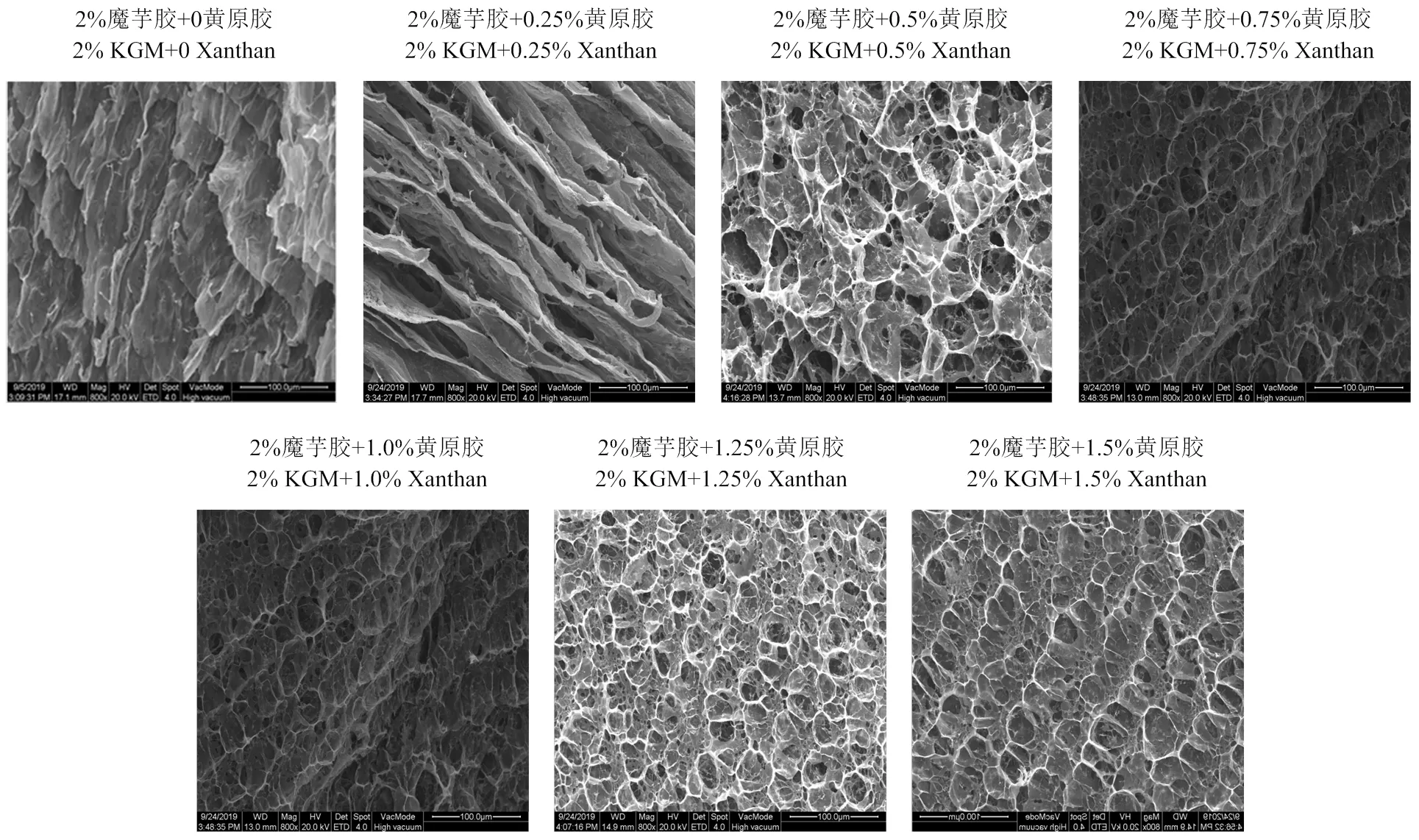
圖2 樣品的微觀結構
2.4 去離子水與檸檬酸溶液浸泡對凝膠強度和微觀形貌的影響
由圖4可以看出,在去離子水和2%檸檬酸溶液中浸泡后,樣品的凝膠強度均呈現降低趨勢;浸泡在2%檸檬酸溶液中的樣品的凝膠強度更低,可能是因為制樣過程中添加了Na2CO3,浸泡過程中檸檬酸與Na2CO3反應生成CO2氣體,引起凝膠網絡結構被輕微擾亂。當黃原膠添加量為0時,魔芋膠凝膠網絡結構不明顯,以片層狀結構為主,當黃原膠添加量為0.25%時,復合凝膠開始呈現網絡結構,黃原膠添加量越高,網絡結構越密集。此外,與去離子水相比,2%檸檬酸溶液浸泡后的復合凝膠網絡孔徑略大。
2.5 凝膠化過程監測及凝膠流變學特性
2.5.1 時間掃描 魔芋膠凝膠化過程是時間依賴型的過程,在相同的堿濃度(2%)、溫度(90℃)條件下,隨時間的變化,魔芋膠的凝膠強度也會隨之變化。因此,本研究對2% KGM(對照)、2% KGM+0.25% Xanthan、2% KGM+0.5% Xanthan、2% KGM+0.75% Xanthan、2% KGM+1.0% Xanthan和2% Xanthan進行90℃下的時間掃描,如圖5所示。可以看出,在最初的1 200 s內,G'和G''迅速增加,表明在此階段隨著時間的延長,凝膠網絡迅速形成;在2 400 s后,G'和G''雖然仍有增加,但增加趨勢明顯變緩,說明凝膠網絡基本形成;且只有2.0% KGM和2.0% KGM+0.25% Xanthan監測到G'與G''的交點,其他混合體系未監測到,可能是因為黃原膠的存在,使整個復合體系表現出G'>G''的特點。此外,從圖5-F中可以看出,2% Xanthan在相同的堿濃度(2%)、溫度(90℃)條件下,G'總是大于G",說明黃原膠表現出類似弱凝膠的結構,但隨著時間的延長,其模量逐漸降低,這可能是因為黃原膠分子在堿性條件下加熱發生降解,導致黃原膠分子量減小[27]。
2.5.2 黃原膠添加量對復合體系中魔芋膠凝膠化過程的影響 對樣品的G'進行擬合,發現擬合度2均在0.98以上,表現出較高的擬合精度。擬合的G'sat和k值見表2。
從表2和圖6可以看出,2% KGM(對照)的G'sat和k最大,隨著黃原膠添加量的增多,G'sat和k都降低,說明黃原膠的添加,不僅降低了魔芋膠凝膠最終的凝膠強度,而且減緩了魔芋膠凝膠網絡的形成速率,這與在90℃下測得的凝膠強度一致。
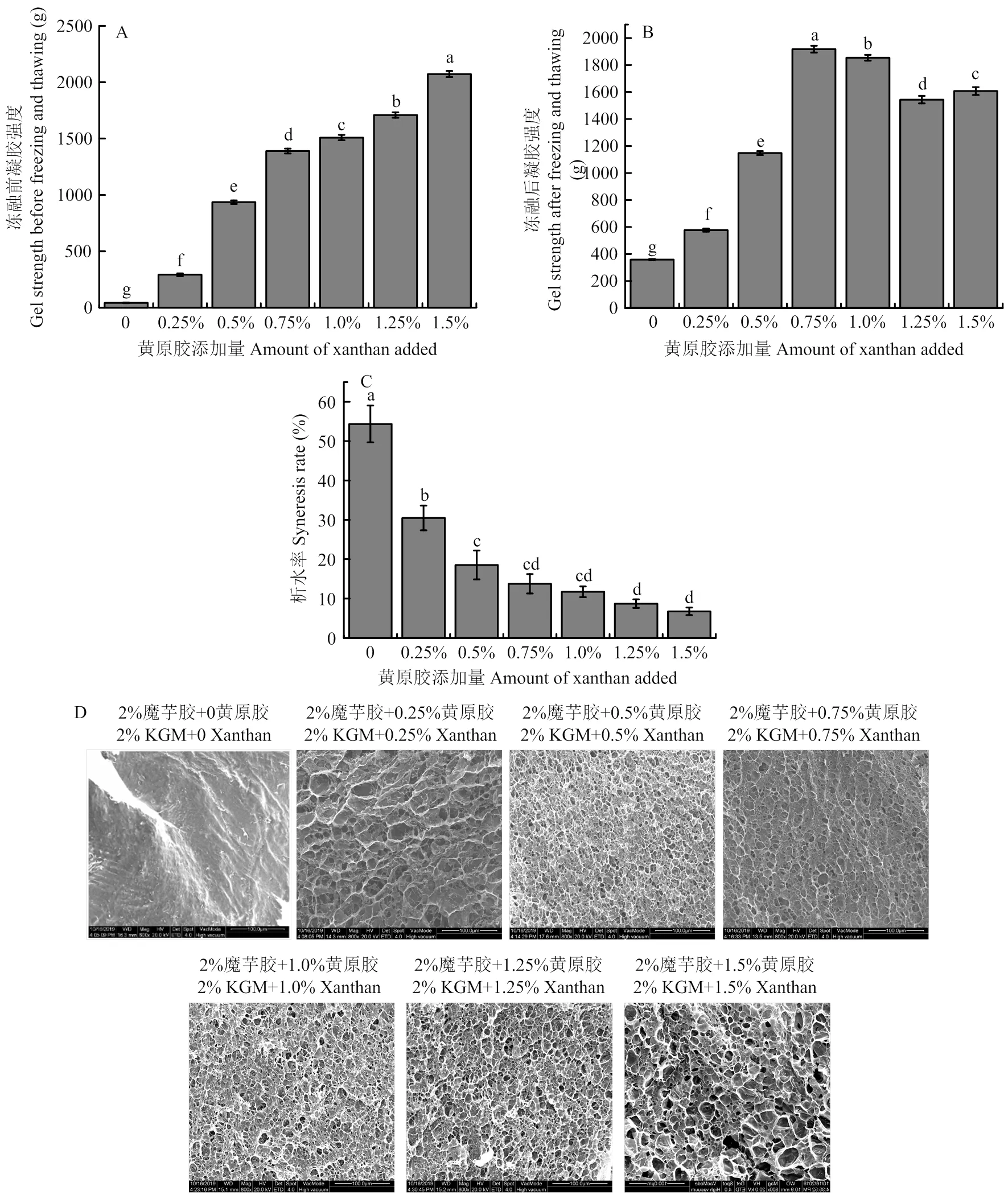
圖3 樣品在凍融處理前后凝膠強度、析水率及微觀結構

表2 不同黃原膠添加量的復合凝膠90℃加熱時凝膠網絡G'變化趨勢一級動力學擬合參數
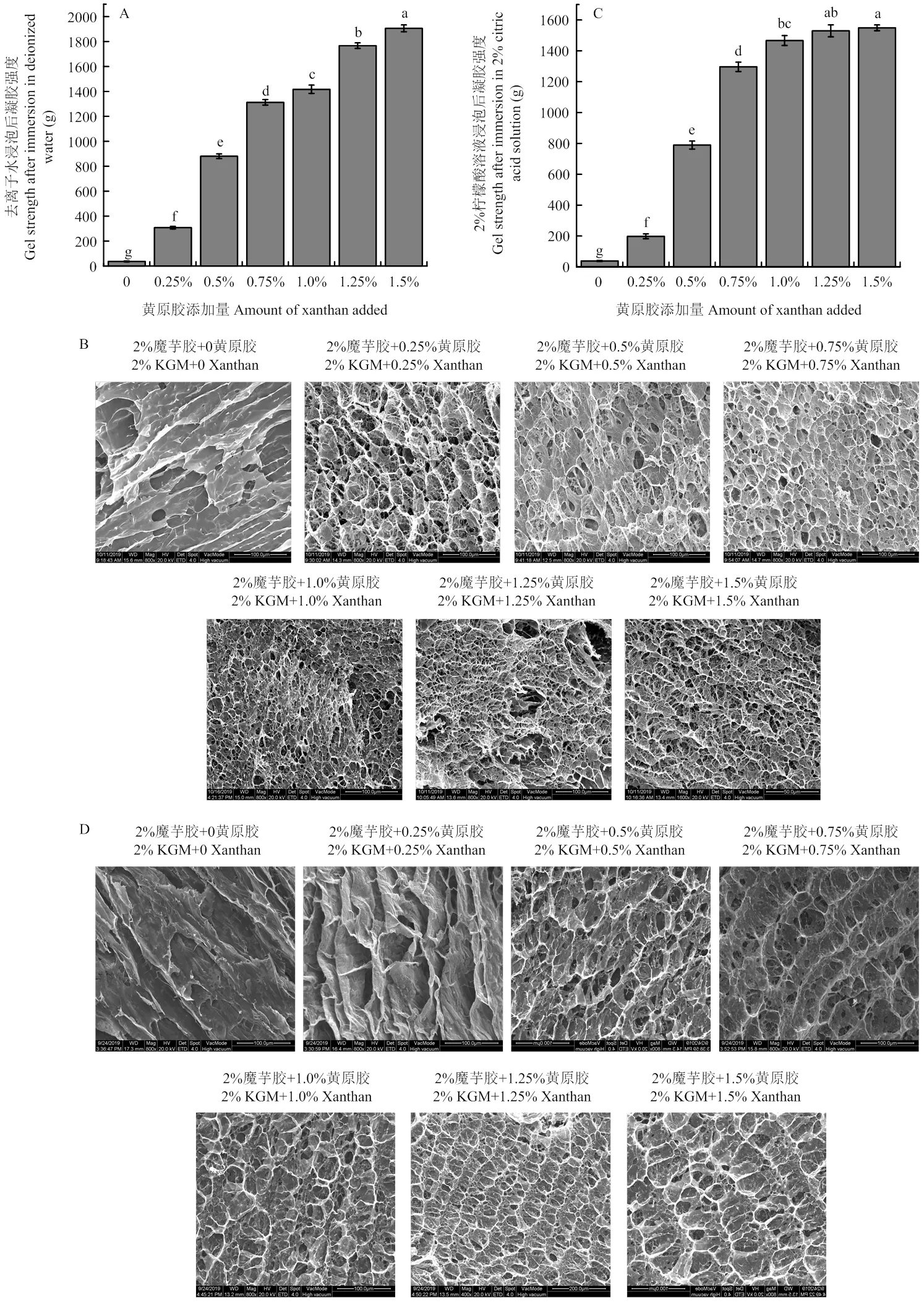
圖4 樣品在去離子水和2%檸檬酸溶液中浸泡后的凝膠強度以及微觀結構

a:2.0%魔芋膠;b:2.0%魔芋膠+0.25%黃原膠;c:2.0%魔芋膠+0.5%黃原膠;D:2.0%魔芋膠+0.75%黃原膠;e:2.0%魔芋膠+1.0%黃原膠;f:2.0% 黃原膠

圖6 樣品時間掃描的儲能模量以及擬合曲線
2.5.3 降溫掃描 魔芋膠-黃原膠協同凝膠的形成與溫度有關,體系在90℃加熱2 h后,對其進行自然冷卻降溫,在此過程中,黃原膠分子可能與魔芋膠網絡結合,起到加固凝膠體系的作用。如圖7所示,2% KGM+0.5% Xanthan和2% KGM+1.0% Xanthan在整個溫度范圍內都表現出G'>G",說明整個體系為較強的凝膠;隨著溫度的降低,體系的儲能模量(G')表現出先下降后上升的趨勢,上升的拐點約為60℃。下降的原因可能是在降溫過程中,魔芋膠凝膠網絡疏水相互作用力減弱,降低了魔芋膠凝膠網絡的縛束力,這與在高溫下魔芋膠凝膠強度較大,在低溫下魔芋膠凝膠強度較小這一性質相一致。當溫度降低至60℃左右時,黃原膠分子與魔芋膠凝膠網絡發生協同作用,開始加固整個凝膠體系,G'不斷增大,隨著溫度進一步降低,這種加固作用更明顯,這與在室溫下測得的整個體系的凝膠強度較大相一致。從圖7還可以看出,2% KGM+1.0% Xanthan體系的儲能模量(G')大于2% KGM+0.5% Xanthan體系,說明隨著黃原膠添加量增多,體系的凝膠強度越大。此外,無論黃原膠添加量為0.5%還是1.0%,拐點對應的溫度均約為60℃,表明黃原膠分子與魔芋膠凝膠網絡的協同結合溫度不隨黃原膠添加量的變化而改變。
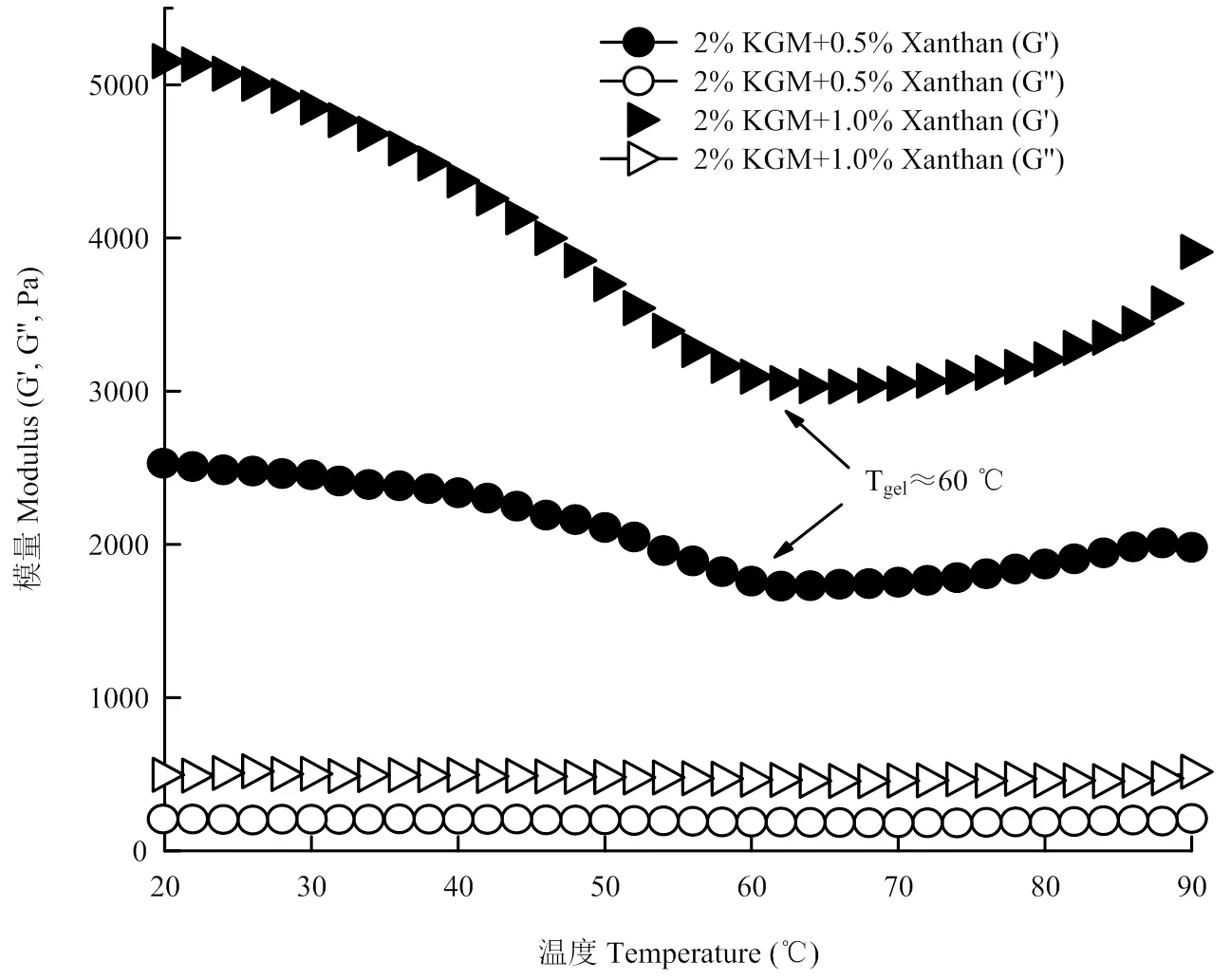
圖7 樣品降溫掃描過程中儲能模量變化趨勢
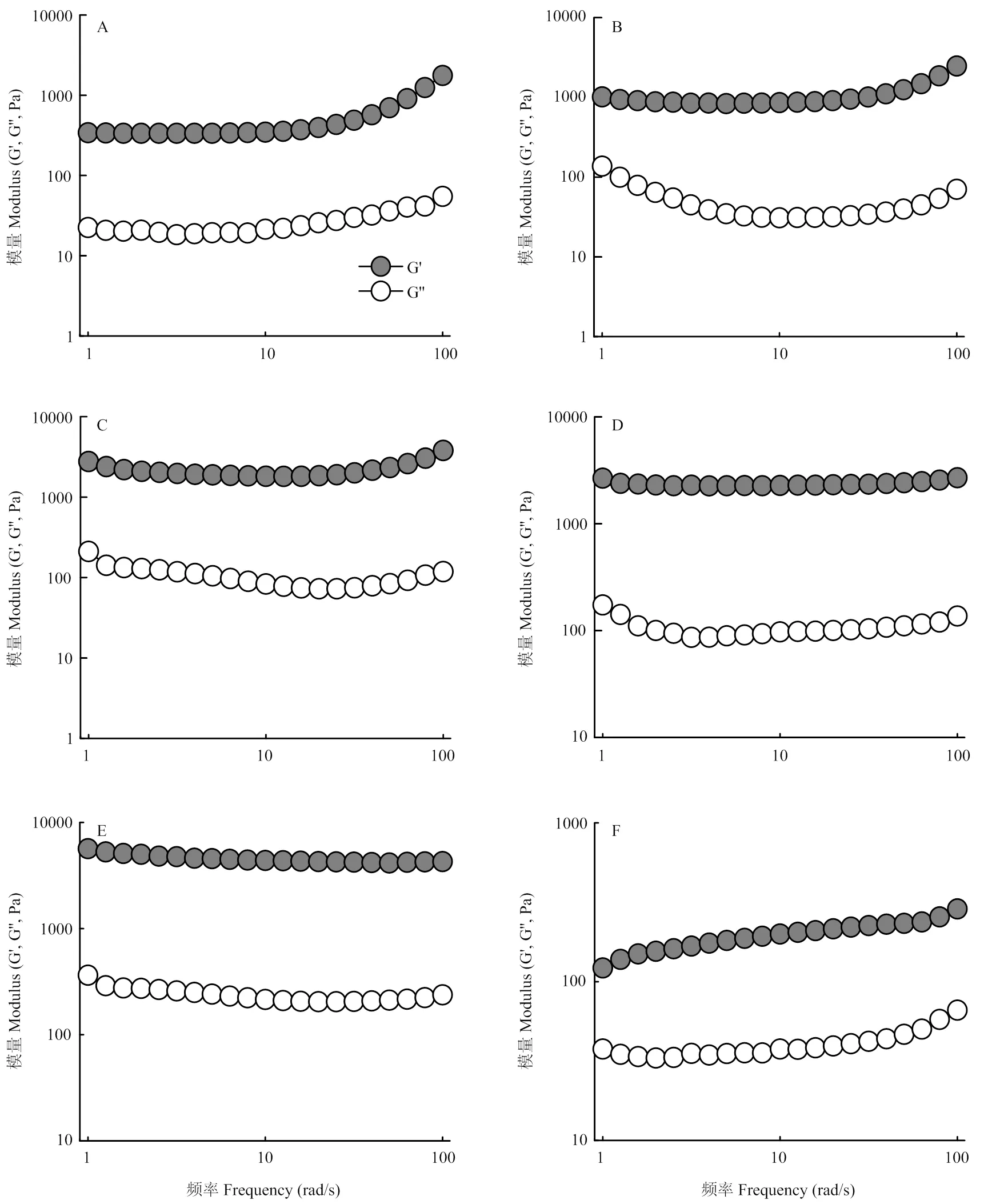
2.5.4 頻率掃描 當整個體系溫度降低到20℃時,對其進行頻率掃描,頻率范圍為1—100 rad·s-1,掃描結果如圖8所示。由圖8可知,在整個頻率范圍內,樣品都表現出G'>G"的特點,并且有明顯的平臺區出現,說明所有的復合體系均形成了較強的凝膠。由圖8-F可知,黃原膠也表現出G'>G",說明黃原膠也有類似凝膠的特性,但隨著頻率增加,黃原膠體系的G'和G"都呈現出輕微增加的趨勢,說明黃原膠體系是一種弱凝膠。
2.6 X-射線衍射測定
X-射線衍射是表征聚合物結晶情況的常用手段。如圖9所示,在2θ=20—80°的衍射角度范圍內,Na2CO3有若干尖銳的散射峰,表明Na2CO3以高度結晶化的晶體結構存在,這是典型無機化合物的特點。2% KGM凝膠的散射峰在35°左右,但其并不明顯,說明該體系以無定型狀態以及由若干微晶區存在。2% Xanthan體系的散射峰非常小;不同量黃原膠的添加,體系的散射峰仍然存在,說明黃原膠的添加并沒有改變2% KGM體系微晶區的結構。
2.7 熱重分析
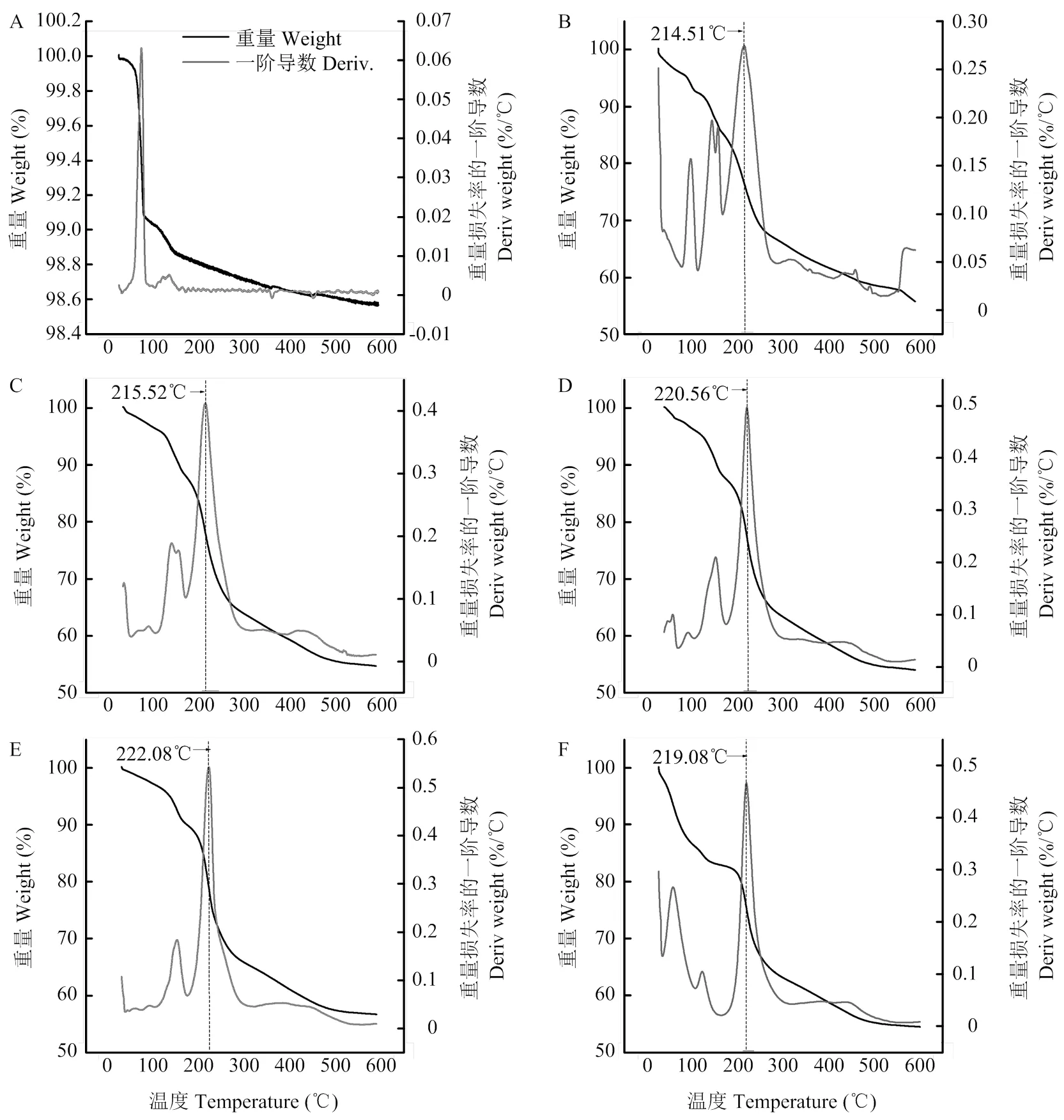
凍干后凝膠樣品的熱穩定性見圖10。從圖10-A可以看出,Na2CO3在100℃以內出現一個明顯的重量降低階段,很可能是由于水分喪失而引起。其余5個樣品均出現2—3個明顯的重量降低階段,在100℃內的重量損失可能是樣品游離水喪失而引起,在150℃左右出現的重量損失可能是由于結合水喪失而引起,在200—300℃,所有凝膠樣品有一個明顯的重量降低趨勢,這可能是多糖分子的熱降解所致。隨著黃原膠添加量的增加,多糖分子熱降解的溫度輕微增大,說明整個凝膠體系的熱穩定性增加,進一步表明凝膠網絡結構更加致密。
a:2.0%魔芋膠;b:2.0%魔芋膠+0.25%黃原膠;c:2.0%魔芋膠+0.5%黃原膠;D:2.0%魔芋膠+0.75%黃原膠;e:2.0%魔芋膠+1.0%黃原膠;f:2.0% 黃原膠

圖9 樣品X-射線衍射
3 討論
3.1 堿法誘導的魔芋膠-黃原膠混合體系凝膠化的理論基礎
在堿性條件下加熱魔芋膠溶液即可獲得魔芋膠凝膠,這種方式是魔芋膠凝膠的傳統制備方式[28]。近年來,有研究表明[3],混合魔芋膠和黃原膠也可制得凝膠,凝膠化原理在于魔芋膠分子和黃原膠分子之間存在協同結合作用。然而,這兩種方式制得的魔芋膠凝膠各有優缺點。本試驗基于對上述兩種凝膠形成過程及機制的理解,提出以下假設:在堿性條件下加熱魔芋膠和黃原膠的混合體系時,魔芋膠因為去乙酰基作用而首先發生分子間交聯,形成三維網絡結構,隨后冷卻混合體系時,黃原膠分子可能和魔芋膠網絡進一步結合,從而加固整個凝膠網絡體系。通過這種方法制備的凝膠理論上應具有上述兩種凝膠網絡的優點,即該凝膠既是熱不可逆凝膠,而且在室溫下可以克服熱堿法誘導的魔芋膠凝膠強度較差、析水嚴重等缺點。基于此設想,本研究成功制備出了復合凝膠。此外,雖然魔芋膠和kappa-卡拉膠也具有明顯的協同效應[29-30],但由于魔芋膠凝膠制備時需要在堿性條件下長時間加熱,kappa-卡拉膠會發生明顯的分子降解而極大降低與魔芋膠協同結合的能力。因此,本試驗未采用kappa-卡拉膠和魔芋膠的混合體系制備凝膠,而是選擇具備優良熱穩定性以及酸堿穩定性的黃原膠。
a:2.0%魔芋膠;b:2.0%魔芋膠+0.25%黃原膠;c:2.0%魔芋膠+0.5%黃原膠;D:2.0%魔芋膠+0.75%黃原膠;e:2.0%魔芋膠+1.0%黃原膠;f:2.0% 黃原膠
3.2 堿法誘導的魔芋膠-黃原膠復合凝膠體系的形成過程
當在堿性條件下加熱混合溶膠體系時,魔芋膠分子聚集速率(k值)及聚集程度(G′sat)明顯受到抑制。原因很可能是由于堿性條件下加熱時,一部分碳酸鈉參與了黃原膠分子的降解,因此只有一部分碳酸鈉誘導魔芋膠發生凝膠化,意味著該復合體系中誘導魔芋膠分子發生凝膠化的碳酸鈉有效濃度降低了。有研究表明[31],魔芋膠在熱堿性條件下的凝膠化速率和魔芋膠濃度、魔芋膠乙酰化程度、堿濃度以及加熱溫度等因素密切相關,即魔芋膠濃度越高、堿濃度越大、加熱溫度越高,凝膠化速率越快。在堿性條件下加熱魔芋膠和黃原膠的復合體系2 h后,立刻測定了各個混合凝膠體系的凝膠強度,發現隨黃原膠添加量增加,復合體系的凝膠強度呈顯著降低趨勢(<0.05),進一步說明黃原膠的添加抑制了魔芋膠分子聚集速率及聚集程度。
堿性條件下加熱魔芋膠和黃原膠混合溶膠體系2 h后,冷卻凝膠體系至室溫,發現室溫條件下,該凝膠體系的強度極大增加,且黃原膠添加量越多,凝膠強度越高。例如,當黃原膠添加量增加至1.5%時,室溫下測得的凝膠強度高達2 000 g,是該凝膠體系在90℃條件下的20倍以上。通過對魔芋膠和黃原膠混合凝膠體系進行降溫掃描,發現在90℃至20℃的溫度范圍內,所有凝膠的彈性模量總是高于黏性模量,沒有發現兩者的交點,這是由于在整個溫度范圍內,魔芋膠和黃原膠混合體系均表現出凝膠的特性,因此其彈性模量占主導。此外,發現當凝膠體系的溫度從90℃降低至60℃時,凝膠彈性模量呈明顯降低趨勢,這可能是由于疏水作用力是維持魔芋膠三維網絡結構的主要因素,溫度降低時,疏水作用力減弱,導致魔芋膠三維網絡松散[28];然而,當溫度降低至60℃時,凝膠彈性模量開始呈現明顯的增加趨勢,溫度越低,彈性模量越高,這是因為當溫度降低至60℃時,黃原膠分子開始與魔芋膠凝膠網絡發生協同結合作用,氫鍵是維持黃原膠分子與魔芋膠凝膠網絡的主要作用力,隨溫度降低,協同結合作用越明顯,使整個凝膠體系在室溫條件下表現出較大的凝膠強度。此外,研究還發現,魔芋膠和黃原膠協同結合的溫度與黃原膠添加量無關,對于黃原膠添加量為0.5%和1.0%的混合體系,協同作用的起始溫度均為60℃。
3.3 復合凝膠體系的凍融穩定性
魔芋膠分子上的乙酰基是影響魔芋膠水溶解性的關鍵因素[28]。乙酰基含量越高,魔芋膠分子水化越容易。堿性條件下,魔芋膠分子上的乙酰基逐漸脫除,雖然可以誘導魔芋膠分子發生聚集,形成三維凝膠網絡結構,但是也降低了魔芋膠分子的親水性。尤其是凍融處理后,魔芋膠凝膠出現明顯的析水現象,原因是冷凍過程中魔芋膠分子在冰晶體的擠壓作用下形成分子間結合區。當冷凍的凝膠解凍后,形成的分子間交聯能夠很好地保留,雖然一定程度上增加了凍融后的凝膠強度。但冰晶體仍然會轉變為液態水從凝膠網絡中流出。單純魔芋膠凝膠析水率可達50%,然而,當魔芋膠凝膠體系中含有黃原膠后,該凝膠體系的析水作用顯著降低,這是因為黃原膠表現出較強的親水性和凍融穩定性,當黃原膠加入魔芋膠凝膠體系時,黃原膠對水分子的親和力更強,有效減弱凝膠在冷凍過程中的水分子結晶現象。此外,當黃原膠添加量在0—1.0%的情況下,凍融后復合凝膠均出現凝膠強度增加的現象,原因可能是冷凍過程中,不斷長大的冰晶體迫使魔芋膠分子彼此靠近,形成局部的高濃度,有利于魔芋膠分子間形成規整有序的結合區。當凝膠解凍后,這樣的結合區也不會消失,因此引起凝膠強度增加。然而,當黃原膠添加量大于1.0%的情況下,凍融后復合凝膠出現凝膠強度降低的趨勢,原因可能是在黃原膠添加量大于1.0%的情況下,復合凝膠冷凍過程中冰晶體生成破壞了凝膠原有的網絡結構,且這種破壞作用大于冷凍過程對凝膠的促進作用,從而使整個凝膠體系解凍后凝膠強度降低。
4 結論
以碳酸鈉作為堿性調節劑,采用高溫條件下加熱魔芋膠和黃原膠混合體系的方式,制備出雙重凝膠網絡的復合凝膠,該凝膠兼具魔芋膠凝膠網絡、魔芋膠與黃原膠協同凝膠網絡二者的優點,不僅保持了魔芋膠凝膠的熱不可逆性,也改善了魔芋膠凝膠強度低、凍融穩定性差等缺點。隨著黃原膠濃度增加,復合凝膠的強度不僅表現出增加趨勢,且凝膠凍融后析水現象明顯降低。本研究提出的魔芋膠凝膠改性方法簡單可行、可操作性強,能夠將魔芋膠凝膠機制和魔芋膠與黃原膠協同結合機制合二為一,可為魔芋膠凝膠相關食品的設計提供理論依據和技術參考。
致謝:感謝陜西師范大學化學與化工學院大型儀器共享平臺的儀器支持及管理老師在測樣過程中的指導和幫助。
[1] 黃明發, 張盛林. 魔芋葡甘聚糖的增稠特性及其在食品中的應用. 中國食品添加劑, 2008(6): 127-131.
HUANG M F, ZHANG S L. The thickening characteristics of Konjac Glucomanan and its application in food industry., 2008(6): 127-131. (in Chinese)
[2] 龐杰, 吳春華, 溫成榮, 尹娜, 姚閩娜. 魔芋葡甘聚糖凝膠研究進展及其問題. 中國食品學報, 2011, 11(9): 181-187.
PANG J, WU C H, WEN C R, YIN N, YAO M N. Research advances in Konjac Glucomannan gel and its problem., 2011, 11(9): 181-187. (in Chinese)
[3] 曾瑞琪, 李葦舟, 趙欣, 張甫生, 鄭炯. 魔芋膠-黃原膠復配體系流變學特性及其凝膠形成動力學分析. 食品科學, 2018, 39(9): 39-46.
ZENG R Q, LI W Z, ZHAO X, ZHANG F S, ZHENG J. Rheological properties and gelation kinetics of Konjac Gum-Xanthan gum mixtures., 2018, 39(9): 39-46. (in Chinese)
[4] 丁保淼, 徐焱春, 熊洪錄, 徐振明, 田志宏. 以黃原膠為改良劑的復配膠魔芋豆腐的制備. 食品科技, 2014, 39(1): 65-69.
DING B M, XU Y C, XIONG H L, XU Z M, TIAN Z H. Preparation of Konjac-Xanthan mixed gum bean curd using Xanthan gum modifier., 2014, 39(1): 65-69. (in Chinese)
[5] 鄧林, 劉延嶺. 魔芋膠的流變學及加工特性的研究. 食品工業科技, 2017, 38(18): 56-59.
DENG L, LIU Y L. Study on rheological and processing characteristics of Konjac gum., 2017, 38(18): 56-59. (in Chinese)
[6] MA S P, ZHU P L, WANG M C. Effects of Konjac Glucomannan on pasting and rheological properties of corn starch., 2019, 89: 234-240.
[7] GAO S J, NISHINARI K. Effect of degree of acetylation on gelation of Konjac Glucomannan., 2004, 5(1): 175-185.
[8] 賀丹, 鄔應龍. 魔芋-黃原膠復合凝膠溶脹性能的研究. 現代食品科技, 2006, 22(3): 79-81.
HE D, WU Y L. The study on the swelling properties of Konjac and Xanthan complex gel., 2006, 22(3): 79-81. (in Chinese)
[9] ANNABLE P, WILLIAMS P A, NISHINARI K. Interaction in Xanthan-Glucomannan mixtures and the influence of electrolyte., 1994, 27: 4204-4211.
[10] CHEN Y L, SONG C Z, LV Y K, QIAN X. Konjac glucomannan/ kappa carrageenan interpenetrating network hydrogels with enhanced mechanical strength and excellent self-healing capability., 2019, 184: 121913.
[11] 王元蘭, 李忠海, 魏玉. 黃原膠與魔芋膠復配體系的流變特性及影響因素. 中南林業科技大學學報, 2010, 30(11): 125-128.
WANG Y L, LI Z H, WEI Y. Study of rheological properties and influence factor of solution Xanthan/Konjac gum mixtures., 2010, 30(11): 125-128. (in Chinese)
[12] KUMAR A, RAO K M, HAN S S. Application of Xanthan gum as polysaccharide in tissue engineering: A review., 2018, 180: 128-144.
[13] 李肖蒙. 基于丙酮酸含量的變化調控黃原膠與魔芋葡甘聚糖復配協同作用及凝膠特性[D]. 杭州: 浙江工商大學, 2018.
LI X M. Effect of pyruvate group on synergistic effect and gel properties from mixtures of Xanthan and Konjac Glucomannan [D]. Hangzhou: Zhejiang Gongshang University, 2018. (in Chinese)
[14] LUTFI Z, ALAM F, NAWAB A, HAQ A, HASNAIN A. Effect of NaCl on physicochemical properties of Xanthan gum-Water chestnut starch complexes., 2019, 131: 557-563.
[15] 游東宏, 江雪秀. 不同因素對魔芋葡甘聚糖凝膠穩定性的研究. 寧德師范學院學報(自然科學版), 2013, 25(4): 380-382.
YOU D H, JIANG X X. The study of different factors on the stability of Konjac glucomannan gel.(), 2013, 25(4): 380-382. (in Chinese)
[16] GENEVRO G M, DE MORAES M A, BEPPU M M. Freezing influence on physical properties of glucomannan hydrogels., 2019, 128: 401-405.
[17] ZHOU Y, JIANG R S, PERKINS W S, CHENG Y Q. Morphology evolution and gelation mechanism of alkali induced Konjac glucomannan hydrogel., 2018, 269: 80-88.
[18] 倪俊杰, 曹連鵬, 傅玉穎, 李可馨, 沈亞麗, 王美. 魔芋葡甘聚糖與黃原膠復配凝膠的協同作用及其流變特性. 中國食品學報, 2018, 18(10): 58-68.
NI J J, CAO L P, FU Y Y, LI K X, SHEN Y L, WANG M. The synergy of mixed gels of Konjac Glucomannan and Xanthan and its rheological behavior., 2018, 18(10): 58-68. (in Chinese)
[19] YANG X, GONG T, LI D, Li A Q, SUN L J, GUO Y R. Preparation of high viscoelastic emulsion gels based on the synergistic gelation mechanism of Xanthan and Konjac Glucomannan., 2019, 226: 115278.
[20] YANG X, GONG T, LU Y H, Li A Q, SUN L J, GUO Y R. Compatibility of sodium alginate and konjac glucomannan and their applications in fabricating low-fat mayonnaise-like emulsion gels., 2020, 229: 115468.
[21] 楊貞. 堿性條件下魔芋膠對小麥淀粉凝膠流變和質構特性的影響[D]. 鄭州: 河南農業大學, 2018.
YANG Z. Effect of Konjac Gum on the rheological and texture properties of wheat starch gel under alkaline condition [D]. Zhengzhou: Henan Agricultural University, 2018. (in Chinese)
[22] NING Y J, CUI B, YUAN C, ZOU Y Y, LIU W Z, PAN Y. Effects of Konjac Glucomannan on the rheological, microstructure and digestibility properties of debranched corn starch., 2020, 100:105342.
[23] GONG T, HOU Y J, YANG X, GUO Y R. Gelation of hydroxyethyl cellulose aqueous solution induced by addition of colloidal silica nanoparticles., 2019, 134: 547-556.
[24] YANG X, NISAR T, LIANG D, HOU Y J, SUN L J, GUO Y R. Low methoxyl pectin gelation under alkaline conditions and its rheological properties: Using NaOH as a pH regulator., 2018, 79: 560-571.
[25] LI J W, MA J W, CHEN S J, HE J M, HUANG Y D. Characterization of calcium alginate/deacetylated Konjac Glucomannan blend films prepared by Ca2+crosslinking and deacetylation., 2018, 82: 363-369.
[26] YANG X, HOU Y J, GONG T, SUN L J, XUE J, GUO Y R. Concentration-dependent rheological behavior and gelation mechanism of high acyl gellan aqueous solutions., 2019, 131: 959-970.
[27] REINOSO D, MARTIN-ALFONSO M J, LUCKHAM P F, MARTINEZ- BOZA F J. Rheological characterization of Xanthan gum in brine solutions at high temperature., 2019, 203: 103-109.
[28] MAO C F, CHEN C H. A kinetic model of the gelation of Konjac Glucomannan induced by deacetylation., 2017, 165: 368-375.
[29] 侯團偉, 張虹, 畢艷蘭, 池娟娟. 食品膠體的凝膠機理及協同作用研究進展. 食品科學, 2014, 35(23): 347-353.
HOU T W, ZHANG H, BI Y L, CHI J J. Recent progress in gelation mechanism and synergistic interaction of common gums., 2014, 35(23): 347-353. (in Chinese)
[30] WILLIAMS P A, CLEGG S M, LANGDON M J, NISHINARI K, PICULELL L. Investigation of the gelation mechanism in κ-carrageenan/ konjac mannan mixtures using differential scanning calorimetry and electron spin resonance spectroscopy.1993, 26(20): 5441-5446.
[31] Huang L, Takahashi R, Kobayashi S, KAWASE T, NISHINARI K. Gelation behavior of native and acetylated Konjac Glucomannan., 2002, 3(6): 1296-1303.
Effects of Xanthan Addition on the Gel Properties and Gel Mechanism of Alkaline-Induced Konjac Glucomannan Gels
LI XiaoFei, LI PeiYuan, LI AnQi, YU WenYan, GUO Chuo, YANG Xi, GUO YuRong
(College of Food Engineering and Nutritional Science, Shaanxi Normal University, Xi’ an 710119)
【】The effects of xanthan addition amounts on the gel properties and gelation mechanism of konjac glucomannan (KGM) gels were investigated, which was expected to provide a theoretical basis and technique references for developing KGM-related gel foods.【】The mixed KGM and xanthan systems were prepared by adding different concentrations of xanthan into 2% KGM solution, and then the mixed polysaccharide systems were subjected to heating at 90℃ for 2 h in the presence of 2% Na2CO3. After cooling to room temperature, the composite KGM-xanthan gels were prepared. By determining the gel strength, the effects of deionized water immersion and 2% citric acid immersion as well as freeze-thaw treatment on the composites were investigated. Meanwhile, scanning electron microscope was used to visualize the microstructures of the composite gels, and then the effects of different treatment methods and xanthan addition amounts on the gel structures were also revealed. Moreover, based on rheology, X-ray scattering and thermogravimetric analyses, the gel formation process of the mixed KGM and xanthan systems during heating at hot alkaline condition was explored, and the gelation mechanism was also revealed.【】During heating at 90℃ for 2 h, it was found that with the increasing of xanthan addition, the gel strength of the composite gels was decreased, indicating that the presence of xanthan negatively affected the formation of KGM gel network in this process. However, at room temperature, with increasing xanthan content, the gel strength of the composite gels was increased. The higher the xanthan content, the greater the gel strength, indicating that xanthan might strengthen the composite gels during cooling. After dezionized water and 2% citric acid immersion, gel strength decreased, and the gel samples with citric acid immersion showed a more pronounced decreased trend. Besides, after freeze-thaw treatment, KGM gels exhibited significant syneresis effect, with an approximately 50% of syneresis rate. However, after adding xanthan, the syneresis rate of the composite gels was significantly decreased. The higher the xanthan content, the lower the syneresis rate. Rheological test results suggested that during heating at 90℃ for 2 h, with the increasing of xanthan content, the gelling rate of the mixed KGM-xanthan system was decreased, indicating that the addition of xanthan decreased the formation of KGM gel network. Subsequent decreasing temperature sweep results showed that when the temperature decreased from 90℃ to 60℃, the elastic modulus of the composite gels exhibited a decreasing trend. When the temperature was continuously decreased to room temperature, the elastic modulus showed an increasing trend, and the transition temperature was corresponding to 60℃, suggesting that xanthan began to synergistically bind with KGM gel network at this temperature.【】The addition of xanthan significantly improved the gel strength of alkali-induced KGM gels at room temperature, and also enhanced the freeze-thaw stability of the gels. This result could provide valuable reference to development of KGM gel-related food.
konjac glucomannan; xanthan; gel strength; rheological properties; freeze-thaw stability

10.3864/j.issn.0578-1752.2020.14.017
2019-12-02;
2020-04-29
農業部現代蘋果產業技術體系建設專項(CARS-27)
李曉飛,E-mail:xiaofeili@snnu.edu.cn。通信作者郭玉蓉,E-mail:yrguo730@snnu.edu.cn
(責任編輯 趙伶俐)

