豬肺磷脂注射液聯合高頻振蕩通氣對NRDS患兒血清CK-MB、ET-1、Cys-C的影響
郭錦華
【摘要】 目的:探討豬肺磷脂注射液聯合高頻振蕩通氣(HFOV)對新生兒呼吸窘迫綜合征(NRDS)患兒血清肌酸肌酶同工酶(CK-MB)、內皮素(ET-1)、血清胱抑素(Cys-C)的影響。方法:選取2018年
1月-2019年1月本院收治的NRDS患兒80例,參考隨機數字表法分為對照組和觀察組,各40例。兩組均采用基礎治療,對照組在此基礎上采用HFOV治療,觀察組在對照組治療基礎上采用豬肺磷脂注射液治療,比較兩組治療前和治療3 d后CK-MB、ET-1、Cys-C水平、血氣指標以及不良反應發生情況。結果:治療3 d后,兩組血清CK-MB、ET-1、Cys-C水平均低于治療前,且觀察組上述指標均低于對照組,差異均有統計學意義(P<0.05);治療3 d后,兩組動脈血氧分壓(PaO2)、氧合指數(PaO2/FiO2)水平均高于治療前,動脈血二氧化碳分壓(PaCO2)水平低于治療前,且觀察組變化幅度均高于對照組,差異均有統計學意義(P<0.05);兩組不良反應發生率比較,差異無統計學意義(P>0.05)。結論:將豬肺磷脂注射液聯合HFOV用于NRDS患兒中的效果較好,能有效降低血清CK-MB、ET-1、Cys-C水平,改善氧合指數,且不會增加不良反應發生率。
【關鍵詞】 呼吸窘迫綜合征 新生兒 高頻振蕩通氣 豬肺磷脂注射液 肌酸肌酶同工酶 內皮素血清胱抑素
[Abstract] Objective: To investigate the effects of Poractant Alfa Injection combined with high-frequency oscillatory ventilation (HFOV) on serum kinase creatase isoenzyme (CK-MB), endothelin (ET-1) and serum cystatin (Cys-C) in children with neonatal respiratory distress syndrome (NRDS). Method: Eighty children with NRDS treated in our hospital from January 2018 to January 2019 were selected and divided into the control group and the observation group according to the random number table method, 40 cases in each group. Two groups were given basic treatment, the control group was treated with HFOV, and the observation group was treated with Poractant Alfa Injection based on the treatment of the control group. The levels of CK-MB, ET-1, Cys-C, blood gas indicators before and 3 d after treatment and the incidence of adverse reactions of two groups were compared. Result: 3 d after treatment, the levels of serum CK-MB, ET-1, and Cys-C in two groups were lower than those of before treatment, and the above indicators in the observation group were lower than those in the control group, the differences were statistically significant (P<0.05). 3 d after treatment, the arterial oxygen partial pressure (PaO2) and oxygenation index (PaO2/FiO2) levels of two groups were higher than those of before treatment, and the arterial blood carbon dioxide partial pressure (PaCO2) levels were lower than those of before treatment, and the observation group had a larger change range, the differences were statistically significant (P<0.05). The incidence of adverse reactions in two groups were compared, the difference was not statistically significant (P>0.05). Conclusion: The combined use of Poractan Alfa Injection and HFOV in children with NRDS has a better effect, it can effectively reduce the levels of serum CK-MB, ET-1 and Cys-C, improve oxygenation indexes, and will not increase the incidence of adverse reactions.
[Key words] Respiratory distress syndrome Newborn High-frequency oscillatory ventilation Poractan Alfa Injection Creatine creatase isoenzyme Endothelin Serum cystatin
First-authors address: Jiamusi Maternal and Child Health Hospital, Jiamusi 154002, China
doi:10.3969/j.issn.1674-4985.2020.18.007
新生兒呼吸窘迫綜合征(NRDS)是一種呼吸系統較為常發的危急重癥,治療難度大,復發率、病死率居高不下且呈上升趨勢,且該病發病機制尚無明確定論,一般認為由肺內原因和/或肺外原因引起的肺表面活性物質缺乏[1-2]。臨床主要進行呼吸機輔助通氣治療該病,但對于難治性的急性加重期NRDS而言,不能有效改善預后,需找到更合適的治療方案來滿足NRDS急性加重期患兒的臨床治療要求[3]。近些年,豬肺磷脂注射液逐漸廣泛用于NRDS患兒的臨床治療中,且取得了一定的效果,但是針對兩者聯合對患兒血清肌酸肌酶同工酶(CK-MB)、內皮素(ET-1)、血清胱抑素(Cys-C)的相關報道甚少。基于此,本研究探討豬肺磷脂注射液聯合高頻振蕩通氣(HFOV)對NRDS患兒血清CK-MB、ET-1、Cys-C的影響。現報告如下。
1 資料與方法
1.1 一般資料 選取2018年1月-2019年1月本院收治的NRDS患兒80例。納入標準:符合NRDS與《內科學》[4]中診斷標準。排除標準:藥物嚴重過敏;伴有其他呼吸系統疾病及器官病變;機械通氣異常;存在精神疾病;合并惡性腫瘤;免疫系統異常。參考隨機數字表法分為對照組和觀察組,各40例。該研究已經倫理學委員會批準,患兒家屬知情同意并簽署知情同意書。
1.2 方法 兩組均采用止咳化痰、平喘吸氧、清創抗感染、維持電解質平衡等常規治療。對照組在此基礎上進行HFOV治療:在HFOV通氣前,使用鎮靜藥物使新生兒處于相對鎮靜狀態,以減少患兒的不安(建議RASS評分保持在-3~0分),且先進行吸痰處理。選擇SLE5000新生兒呼吸機,且所有新生兒在嚴格無菌操作下經口氣管插管,選取合適的通氣模式,實施小潮氣量肺保護通氣策略,在進行通氣過程中,保持患者呼吸道通暢,防止在治療過程中發生窒息,吸氧持續時長>48 h,吸入氧濃度(FiO2)>40%。觀察組在對照組治療基礎上經氣管滴入豬肺磷脂注射液(生產廠家:Chiesi Farmaceutici S.p.A,批準文號:H20181202,規格:
3 mL︰0.24 g),1.5~3.0 mL/kg,12 h/次。兩組均持續治療3 d。
1.3 觀察指標與評價指標 兩組均隨訪至患兒出院后,評估治療效果。(1)血清CK-MB、ET-1、Cys-C水平:分別于治療前及治療3 d后清晨采集兩組動脈血3 mL,采用血氣分析儀測定檢測CK-MB、
ET-1、水平,使用免疫透射比濁法測定Cys-C水平。(2)氧合指數:分別于治療前及治療3 d后清晨采集兩組動脈血3 mL,采用血氣分析儀測定動脈血氧分壓(PaO2)、氧合指數(PaO2/FiO2)、動脈血二氧化碳分壓(PaCO2)。(3)不良反應:比較兩組治療期間休克、心律失常、電解質紊亂、敗血癥發生情況。
1.4 統計學處理 采用SPSS 20.0軟件對所得數據進行統計分析,計量資料用(x±s)表示,組間比較采用t檢驗,組內比較采用配對t檢驗;計數資料以率(%)表示,比較采用字2檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 兩組一般資料比較 觀察組男20例,女20例;日齡1~16 d,平均(8.91±3.42)d;病程1~6 d,平均(3.13±0.95)d。對照組男19例,女21例;日齡2~18 d,平均(9.46±0.79)d;病程1~6 d,平均(3.24±0.63)d。兩組一般資料相比,差異均無統計學意義(P>0.05),具有可比性。
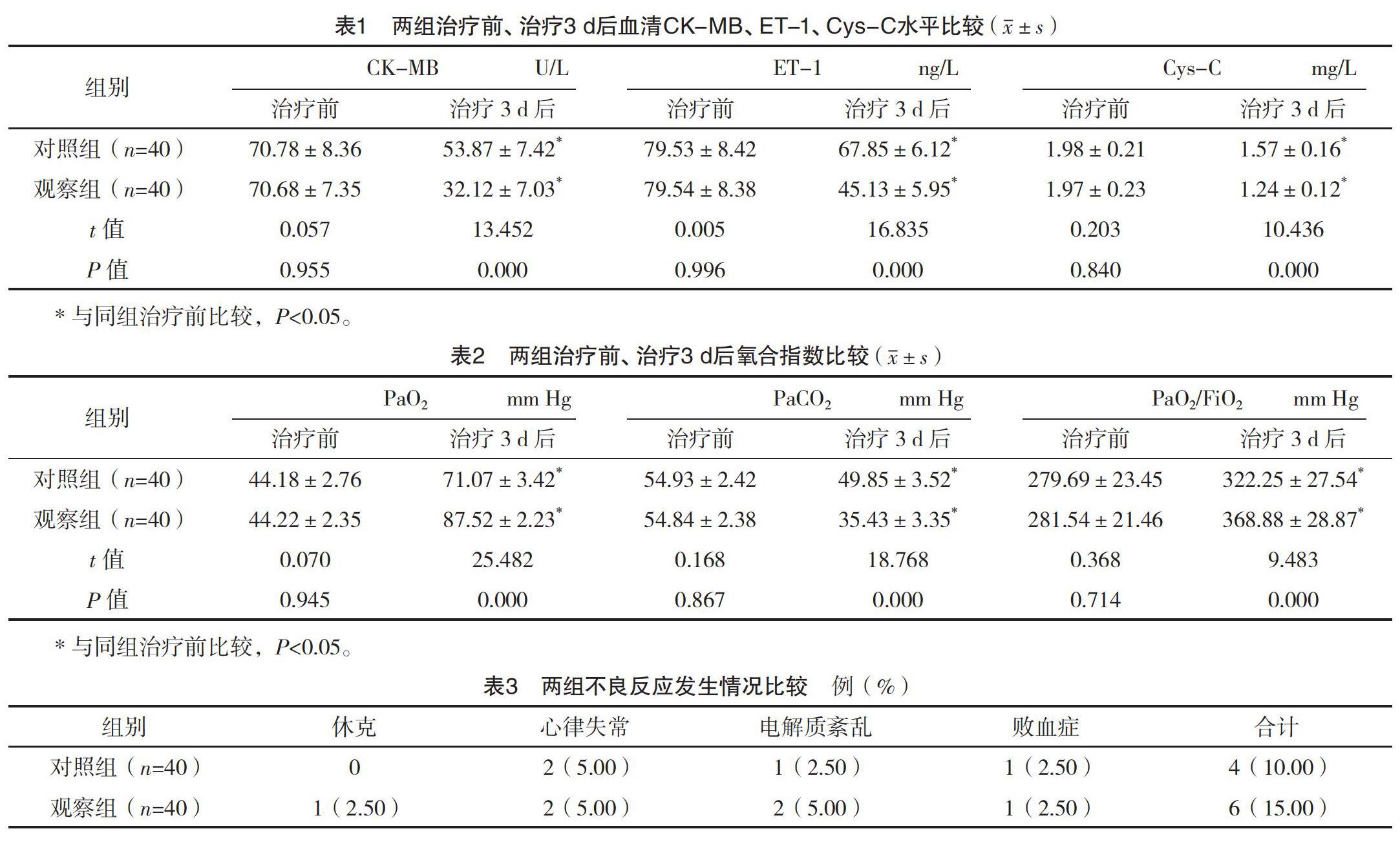
2.2 兩組治療前、治療3 d后血清CK-MB、ET-1、Cys-C水平比較 治療前,兩組CK-MB、ET-1、Cys-C水平比較,差異均無統計學意義(P>0.05);治療3 d后,兩組血清CK-MB、ET-1、Cys-C水平均低于治療前,且觀察組上述指標均低于對照組,差異均有統計學意義(P<0.05)。見表1。
2.3 兩組治療前、治療3 d后氧合指數比較 治療前,兩組PaO2、PaCO2、PaO2/FiO2水平對比,差異均無統計學意義(P>0.05);治療3 d后,兩組PaO2、PaO2/FiO2水平均高于治療前,PaCO2水平低于治療前,且觀察組各指標變化幅度均高于對照組,差異均有統計學意義(P<0.05)。見表2。
2.4 兩組不良反應發生情況比較 兩組不良反應發生率比較,差異無統計學意義(字2=0.457,P=0.499),見表3。
3 討論
NRDS大部分在出生后72 h內出現,多為急性起病,病程一般在7 d內[5]。除了原發病的相應癥狀和體征表現外,最先出現的是呼吸加快,并且表現為進展性持續加重的呼吸障礙、發紺,并伴有煩躁、焦慮以及出汗等癥狀[6]。呼吸困難的主要特征是呼吸深而快,較為費力,患兒出現胸廓緊束、嚴重憋氣,此時即為呼吸窘迫,常規的吸氧療法不能有效改善臨床呼吸窘迫癥狀[7]。如果不能采取有效的治療方案來控制病情,改善呼吸循環系統,則隨著病情的發展會造成意識模糊,甚至死亡,威脅新生兒的生命健康[8]。
CK-MB是心肌細胞特有一種酶原物質,CK-MB的升高表明心肌細胞受損,是早期診斷心肌損傷的重要指標,具有較高的敏感性和特異性[9];ET-1是血管活性物質,為內源性血管收縮肽,在血管內皮細胞中廣泛分布,起到很好的收縮血管的作用[10]。ET-1升高會刺激肺動脈壓力增高、肺小動脈痙攣,收縮支氣管平滑肌,加大氣道內部的阻力,最終導致呼吸窘迫。Cys-C在體液中有著較為廣泛的存在,在腎臟功能被損害時,Cys-C水平會出現明顯的增加,與病情的嚴重程度呈正相關[11]。本研究中,治療3 d后,兩組血清CK-MB、ET-1、Cys-C水平均低于治療前,且觀察組上述指標均低于對照組,差異均有統計學意義(P<0.05)。表明,豬肺磷脂注射液聯合HFOV可緩解NRDS患兒心肌損傷,改善呼吸窘迫癥狀。因為HFOV是一種高頻率的震蕩通氣模式,該種模式下能夠保持正常的肺泡內壓,實現萎陷的肺泡有效復張,并維持其一直處于開放的狀態,降低氣道阻力的同時,減少肺表面活性物質的損耗,增加肺泡容積,清除二氧化碳,增加和改善了氧合指數[12-13]。同時,HFOV有著較高的氣道,能夠有效避免肺泡過度擴張,以及反復開放所帶來的損害,在常規頻率機械通氣治療失敗的患兒中較為適用[14-15]。胡娟娟[16]也在研究指出,在呼吸衰竭患兒中進行HFOV治療是使用較小的潮氣量,用較高的通氣頻率不僅能夠有效維持正常的肺功能殘氣量,而且加大了氧氣的獲取,利于改善患兒的呼吸窘迫癥狀。而豬肺磷脂注射液是一種磷脂和特異性蛋白質為主的混合物,能夠補充肺表面活性物質[16]。同時其還可加速肺泡合成并分泌肺表面活性物質,維持肺泡的穩定,能夠有效防止肺泡在呼氣末萎縮陷,維持整個通氣循環系統有著較為充分的氣體交換[17-18]。此外,該藥給藥后能效減輕因為機械通氣給肺部及氣道所帶來的損傷,利于改善新生兒臨床癥狀及肺功能[19-20]。本研究結果顯示,兩組治療3 d后PaO2、PaO2/FiO2水平均高于治療前,PaCO2水平低于治療前,且觀察組變化幅度均高于對照組,差異均有統計學意義(P<0.05)。而兩組不良反應發生率比較,差異無統計學意義(P>0.05)。表明,聯合治療能改善患兒呼吸功能,且安全性高。
綜上所述,豬肺磷脂注射液聯合HFOV治療可降低NRDS患兒血清CK-MB、ET-1、Cys-C水平,改善氧合指數,且較為安全,利于改善預后。
參考文獻
[1] Thompson B T,Chambers R C,Liu K D.Acute Respiratory Distress Syndrome[J].N Engl J Med,2017,377(6):562-572.
[2]吳愛萍,王金柱,韓芳,等.基于柏林標準診斷的急性呼吸窘迫綜合征患者預后影響因素研究[J].中國全科醫學,2019,22(18):2176-2181.
[3] Amigoni A,Pettenazzo A,Stritoni V,et al.Surfactants in Acute Respiratory Distress Syndrome in Infants and Children:Past,Present and Future[J].Clin Drug Investig,2017,37(10):1-8.
[4]葛均波,徐永健,王辰.內科學[M].9版.北京:人民衛生出版社,2018:132.
[5] Balzer F,Menk M,Ziegler J,et al.Predictors of survival in critically ill patients with acute respiratory distress syndrome(ARDS):An observational study[J].Bmc Anesthesiology,2016,16(1):35-40.
[6]中華醫學會重癥醫學分會.急性肺損傷/急性呼吸窘迫綜合征診斷和治療指南(2006)[J].中國危重病急救醫學,2006,18(12):706-710.
[7]楊國輝,劉益.PiCCO監測在急性呼吸窘迫綜合征患者中的臨床應用[J].重慶醫學,2017,46(13):1807-1809.
[8]孫兵,唐曉,李緒言,等.2017-2018年冬春季重癥流感病毒性肺炎所致急性呼吸窘迫綜合征的臨床特點及預后危險因素分析[J].中華結核和呼吸雜志,2019,42(1):9-14.
[9]陸葉,崔云,周益平,等.心型脂肪酸結合蛋白預測兒童肺炎合并急性呼吸窘迫綜合征預后[J].中國小兒急救醫學,2018,25(5):351-355.
[10]賀嵐.血必凈注射液聯合大劑量氨溴索治療重癥肺炎合并急性呼吸窘迫綜合征的療效及對血漿TXB2、ET-1、IL-8表達的影響[J].現代中西醫結合雜志,2016,25(36):4023-4025.
[11]李毅,潘頻華,劉帥.急性呼吸窘迫綜合征生物標志物研究進展[J].中華結核和呼吸雜志,2016,39(12):969-972.
[12]中華醫學會呼吸病學分會呼吸危重癥醫學學組.急性呼吸窘迫綜合征患者機械通氣指南(試行)[J].中華醫學雜志,2016,96(6):404-424.
[13]宋邵華,田惠玉,楊秀芬,等.氣道壓力釋放通氣應用于急性肺損傷/急性呼吸窘迫綜合征患者的臨床研究[J].中華危重病急救醫學,2016,21(1):15-21.
[14]朱文英,袁玉峰,張海燕,等.兩種無創正壓通氣模式聯合固爾蘇治療新生兒呼吸窘迫綜合征的療效比較[J].江蘇醫藥,2017,43(24):1826-1827.
[15]劉莉,呂蓉蓉,陳光耀,等.肺表面活性物質聯合HFO對新生兒呼吸衰竭的療效及對血清CK-MB、ET-1、Cys-C的影響[J].國際呼吸雜志,2018,38(13):996-1000.
[16]胡娟娟.高頻振蕩通氣聯合肺泡表面活性物質對新生兒ARDS氧合功能的影響[J].包頭醫學院學報,2017,33(2):19-20.
[17]楊麗娟,袁玉芳,趙賽,等.肺表面活性物質對選擇性剖宮產患兒預防新生兒呼吸窘迫綜合征的臨床研究[J].中國醫師進修雜志,2016,39(11):1005-1008.
[18]吳本清,高飛,蘇錦珍,等.布地奈德聯合肺表面活性物質治療早產兒支氣管肺發育不良的臨床研究[J].國際兒科學雜志,2019,46(1):61-65.
[19]杜鳳玲,董文斌,趙帥,等.布地奈德聯合豬肺磷脂注射液預防早產兒支氣管肺發育不良[J].中華實用兒科臨床雜志,2016,31(11):846-850.
[20]關楚翹.豬肺磷脂注射液結合持續呼吸道正壓通氣用于新生兒呼吸窘迫綜合征治療的臨床療效[J].中國醫學創新,2016,13(24):97-99.
(收稿日期:2019-11-27) (本文編輯:程旭然)

