廢舊三元鋰離子電池回收技術研究新進展
張英杰,寧培超,楊軒,董鵬,林艷,孟奇
(1 昆明理工大學冶金與能源工程學院,鋰離子電池及材料制備技術國家地方聯合工程實驗室,云南省先進電池材料重點實驗室,云南昆明650093;2 昆明理工大學材料科學與工程學院,鋰離子電池及材料制備技術國家地方聯合工程實驗室,云南省先進電池材料重點實驗室,云南昆明650093)
中國科技部國家高技術研究發展計劃中電動汽車專項的啟動推動了電動汽車產業的快速發展,同時也為動力電池產業提供了發展新動能[1]。預計到2020年,新能源汽車生產能力達200萬輛、累計產銷量超過500萬輛,在新能源汽車高速發展的拉動下,Avicenne Energy預計,到2020年全球鋰離子電池總銷量將會增長到65GW·h,2025年將增長到97.70GW·h。
鋰離子電池(LIBs)經過數百次循環充放電后,電池內部結構會發生不可逆的改變,進而堵塞Li+擴散的通道,最終造成LIBs的失活報廢[2],所以鋰離子電池的平均壽命只有1~3年[3]。隨著鋰電池需求量和產量的逐年增加,會井噴式產生大量的退役鋰電池[4]。據預測,到2030年全球廢LIBs的處置量將超過1100 萬噸,產值將達到237.2 億美元[5]。而中國的形勢更為嚴峻,預計到2020 年累計退役動力電池將超過50 萬噸,并且我國將比全球總體水平有更快的鋰電池報廢速度,2020 年可達百億級的市場規模[6]。
廢舊LIBs 中主要含有正負極材料、電解質、隔膜和黏結劑,這些組分對環境有極大的危害性。電解質如六氟磷酸鋰(LiPF6)、碳酸乙烯酯(EC)、二甲基碳酸酯(DMC)、碳酸二乙酯(DEC)、碳酸甲乙酯(EMC),黏結劑如聚偏氟乙烯(PVDF),隔膜有聚丙烯(PP)、聚乙烯(PE)、偏氟乙烯(VDF)等,這些會造成氟污染和有機物污染[7];碳材和石墨容易造成粉塵污染;而正極材料則會造成重金屬污染[8]。
目前,動力電池市場的正極材料主要有磷酸鐵鋰、錳酸鋰、三元正極材料(鎳鈷錳酸鋰NCM 或鎳鈷鋁酸鋰NCA),其中三元正極材料是當前鋰離子電池的主力正極材料,2018 年其市場份額達到50%,預計未來將成為動力電池的主流正極材料。據預測三元正極材料在2021 年退役量將達到13.5GWh,具體數據見圖1。三元動力鋰離子電池中含有大量的有價金屬[9],通常,Co 占5%~20%,Ni占5%~12%,Mn占7%~10%,Li占2%~5%[10]。因此,研究廢舊三元鋰離子電池資源化回收技術具有重要意義和實用價值。其中最具有回收利用價值的是正極和負極材料,但同時電解液回收也有一定的經濟價值,因此針對這三個方面的技術現狀和研究進展進行論述。
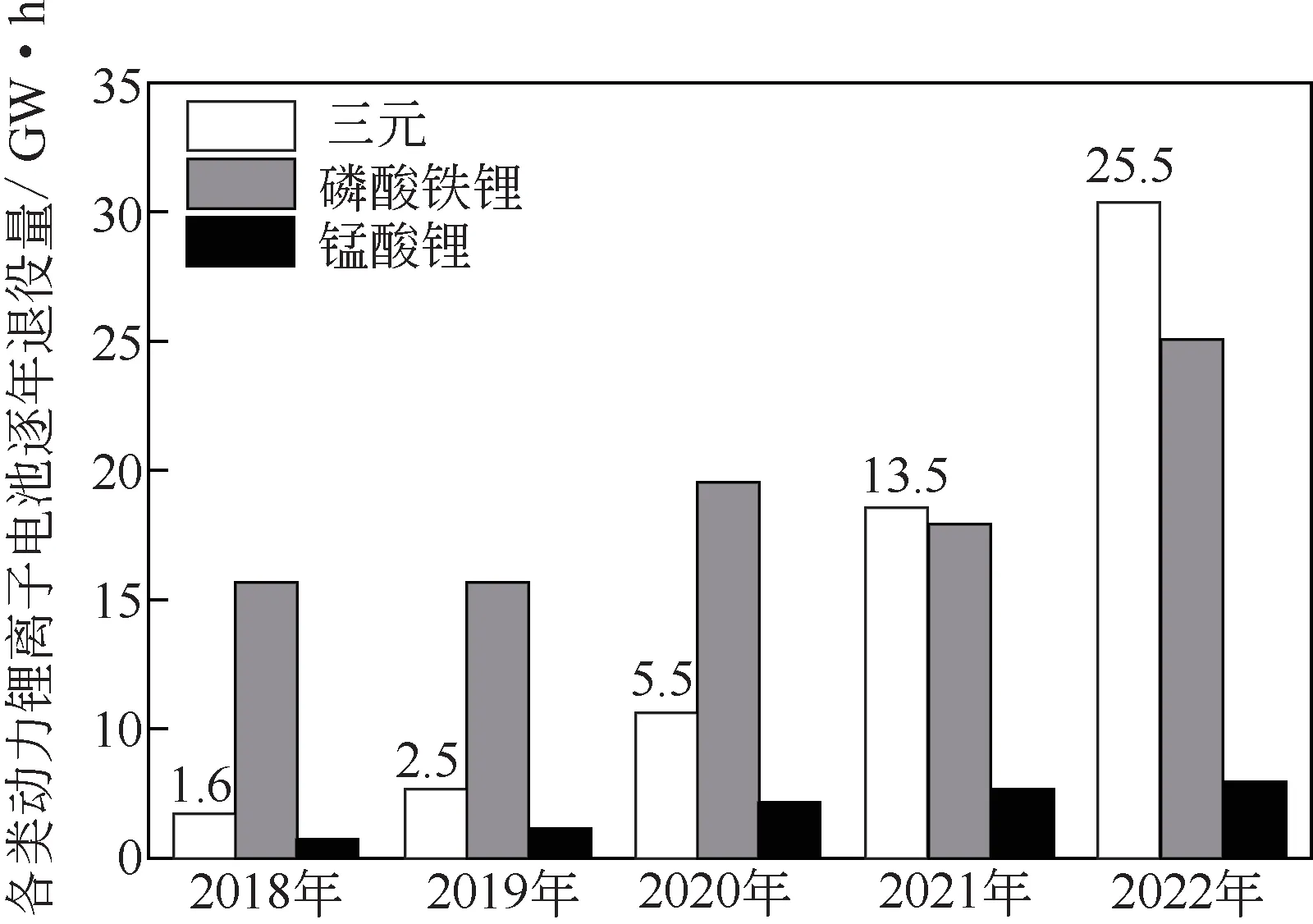
圖1 2018—2022年各類動力電池逐年退役量預測
退役的鋰離子電池直接拆卸會導致短路從而產生巨大的熱量,所以要對廢舊電池進行前處理,然后對放電后的電池進行拆解破碎及篩選分離,分選出正極、負極、隔膜和外殼等,最后進行分離和回收。通常,正極主要回收處理鋁箔和正極材料,負極回收處理石墨和銅箔。
1 正極材料回收
當前,根據鋰離子電池失效模式的差異,三元正極材料回收與再生的技術路線主要有兩種:一是物理修復再生,對于只是失去活性鋰元素的三元正極材料,直接添加鋰源通過高溫燒結法進行原位逆向補鋰修復再生,對于嚴重容量衰減、表面晶體結構發生改變的正極材料,進行水熱處理和短暫的高溫燒結再生;二是冶金法回收,主要有火法、濕法、生物浸出法[11-12]。火法處理工藝較簡單,但能耗高,會產生大量廢氣。研究和應用最多的是濕法處理,主體技術有預處理、浸出、萃取分離[13-15]、共沉淀制備等工藝。萃取分離存在處理量低、有機物易污染、流程復雜等不足,回收產品的再生利用研究較少,且相關產業化實踐應用少。生物浸出法效率高、成本低、環保,但細菌較難培養,浸出周期長而且浸出率較低,這限制了其工業化進程。
1.1 物理法修復再生
物理法修復再生是一種能夠快速實現退役鋰離子電池正極材料循環利用的回收技術,但其對于廢舊LIBs正極材料的電化學性能要求較高。
通常對于只是失去活性鋰元素的三元正極材料采用直接在其中補加一定量的鋰源,然后在氧氣氣氛下進行高溫煅燒,最終可以合成新的正極材料。Zhang 等[16]首先使用三氟乙酸(TFA)將正極材料與鋁箔完全分離,并將正極材料在700℃煅燒5h以除去聚偏氟乙烯(PVDF)和碳,再用NaOH除去雜質Al。然后補加鎳鹽、錳鹽、鈷鹽、鋰鹽調節其成分,最后450℃煅燒5h,900℃煅燒20h得到再生的LiNi1/3Co1/3Mn1/3O2,再生材料的電化學性能良好。Zhou等[17]用一種綠色、簡單的技術再生了LiNi0.5Co0.2Mn0.3O2正極材料,通過添加乙酸鋰固相彌補材料晶格中鋰的缺失,同時發現裂解和破碎的顆粒消失,LiMn2O4/NiO被完全去除,大部分LiF/Li2CO3被消耗。在1C 倍率下放電比容量為147mA·h/g,循環100圈后,仍然可以提供131mA·h/g的放電比容量,容量保持率為89.12%。楊桃等[18]將失效的LiNi0.6Co0.2Mn0.2O2與碳酸鋰球磨均勻后,并在800℃下進行燒結從而再生了LiNi0.6Co0.2Mn0.2O2,實驗發現n(Li)/n(Ni+Co+Mn)=1.05 為最佳工藝條件。電化學測試表明,在0.2C倍率下放電比容量為173.8mA·h/g,循環55 次容量保持率為99.5%,說明向失鋰的鎳鈷錳酸鋰材料中添加鋰源,通過高溫燒結法可以使鋰重新填充因失去活性鋰造成的空位,使失效的材料恢復成原始晶體狀態,實現原位可逆修復,且得到的材料性能指標接近原新鮮材料,說明此方法是簡單可行的。
Meng 等[19]對廢舊鋰離子電池和含釩渣同時進行處理,通過噴霧干燥法在電極材料表面包覆一層V2O5,從而再生制備出LiNi1/3Co1/3Mn1/3O2/V2O5復合電極材料。當V2O5包覆量為5%時,具有最好的電化學性能。在0.1C倍率下充放電循環100次后,放電比容量依然有156.3mA·h/g,容量保持率為90.6%,與傳統冶金技術相比,該工藝采用綠色化學原理,可實現高性能正極材料再生,無需引入萃取化學品,并且對環境的影響要小得多。
Zhang 等[20]用草酸浸出廢LIBs 并成功再生LiNi1/3Co1/3Mn1/3O2正極材料。首先將0.6mol/L草酸和廢正極粉末放入反應器中,固液比為20g/L,水浴溫度保持在70℃,隨著反應時間的延長,鋰溶解到溶液中,過渡金屬轉變成草酸鹽沉淀物并沉積在正極材料表面,實現了鋰和過渡金屬的分離。在90℃下將飽和Na2CO3加入到沉淀濾液中得到Li2CO3,然后將草酸鹽沉淀物與未反應的NCM 和一定量的Li2CO3混合后,直接煅燒成新正極材料。實驗發現浸出10min 再生的NCM 電化學性能最佳,0.2C 倍率下初始放電比容量為168mA·h/g,循環150 次后放電比容量為153.7mA·h/g,容量保持率為91.5%。該工藝可以充分利用廢電池中的有價金屬,Ni、Co和Mn 的回收率大于98.5%,并提供了從廢LIBs 中回收正極材料的新視角。
Wei 等[21]基于簡單的熱處理法將廢舊鋰離子電池中的Ni-Co-Mn 氧化物制備成空氣電極,從而再生了100%有價金屬(Co、Ni 和Mn)。首先將正極材料在600℃下煅燒5h,Ni-Co-Mn 氧化物發生從α-NaFeO2型結構到尖晶石結構的顯著相變,然后得到再生的Ni-Co-Mn 氧化物并顯示出氧還原反應(ORR)的四電子通路。電化學測試表明,再生的Ni-Co-Mn氧化物在KOH電解質中的析氧和氧還原反應表現出顯著的雙功能催化活性。將Ni-Co-Mn氧化物粉末應用于空氣電池中,在10mA/cm2的電流密度下能量效率為75%,優于商用鋅-空氣電池性能。
對于容量嚴重衰減、表面晶體結構發生改變的正極材料,進行水熱處理和短暫的高溫燒結再生。Shi等[22]將正極材料粉末加入到含有4mol/L LiOH 溶液的高壓釜里,220℃水熱進行鋰化4h,然后與Li2CO3(Li 過量5%)混合在氧氣中850℃燒結4h,得到再生正極材料。與直接固相燒結的新材料相比,具有相當的電化學性能。這種方法可以消除NCM 材料表面的陽離子混排(Li、Ni)、巖鹽相NiO以及尖晶石相,從而修復材料。其主要的反應機理見式(1)。

固相法對廢舊電池品質的要求(活性物質表面的Li/Ni 混排較低、結構破壞低)較高,如果能夠對廢舊電池進行品質篩選,然后篩選出具有一定電化學性能的電池去進行補鋰再生和水熱補鋰修復再生,就可以縮減回收的成本。同時如何高效地補鋰也是值得思考的問題。
1.2 冶金法回收再生
冶金法回收再生三元正極材料,目前廣泛采用濕法冶金工藝,主要工藝流程包括預處理、浸出、再生等工序。
1.2.1 預處理
由于正極活性物質涂覆在Al 箔上,為了將活性物質從Al 箔上剝離下來,通常必須對廢舊電池進行預處理。一般利用NaOH 與Al 反應生成H2和NaAlO2,從而將活性物質剝離下來[23]。He等[24]將廢舊NCM 正極片浸泡于70℃的N-甲基吡咯烷酮(NMP)中,通過超聲處理90min 將活性物質從Al箔上剝離下來。Song 等[25]對廢正極片在450℃下煅燒2h,除去PVDF,然后攪拌過400 目篩得到正極材料的富集物。機械粉碎研磨、離心分離、靜電分離等方法也用來分離正極材料和Al 箔。常見的正極片預處理方法見表1。
堿溶液浸泡處理正極片簡單有效,有機溶劑浸泡處理溫度較高,可能會造成有機溶劑的揮發,對環境污染較大。機械粉碎研磨、離心分離、靜電分離能夠分離大量的鋁箔和正極材料,但是富集物的產率較低和純度較低,也就限制了其工業化的推廣。
1.2.2 浸出
根據廢舊三元正極材料浸出體系不同,大致可分為酸浸、堿浸和微生物浸出三大類。
(1)酸浸 酸浸通常是用酸將金屬轉化成對應的金屬離子,并轉入到浸出液中。酸通常包括無機酸、有機酸或者有機酸和無機酸組成的混合酸。
Joulié 等[30]首先比較了在沒有還原劑條件下,H2SO4、HCl 對廢舊NCM 正極材料的浸出效果。在硫酸中的溶解受溫度影響較大,而在鹽酸中,它受溫度、酸濃度及其相互作用的影響,主要原因是氯化物顯示出一些氧化還原性質而表現出較高活性。同時將Cu、Al(相對較低的氧化還原電位)作為還原劑分別加入到浸出溶液中,在H2SO41mol/L、溫度30℃、wNCM/wCu=1/1.2的條件下,NCM材料經過1h全部溶解。NMC/Al比為1/0.7時,由于鋁的水解及金屬鋁與水的反應導致生成氧化鋁,溶解速率降低,經過24h才反應完全。
為了提高酸浸的效率,研究工作者開發了還原焙燒和濕法冶金聯合浸出法。Liu 等[31]首先將廢舊電極材料與10%的焦炭混合均勻并在650℃下焙燒30min,然后將焙燒產物用水浸出得到富Li 溶液,最后通過蒸發結晶得到了Li2CO3。過濾掉Li的濾渣用H2SO4酸浸(無添加還原劑)獲得了含有二價金屬離子的溶液,Li、Ni、Co 和Mn 的浸出率分別為93.67%、93.33%、98.08%、98.68%。這種方法降低了還原劑帶來的成本,并且金屬溶液可用于制備三元前體,從而實現再循環。Zhang 等[23]用碳質還原劑焙燒正極廢料,然后采用碳酸化水從焙燒產物中選擇性地提取Li。最后,將所得殘余物浸入硫酸溶液中以回收Co、Ni和Mn。通過向浸出系統中注入CO2可以顯著地提高Li的浸出率,并且在低液固比下,在10min內浸出80%以上的Li,通過直接蒸發從浸出液中制備出高質量的Li2CO3。在硫酸鹽用量為理論值的1.15倍、時間2.5h、溫度55℃、液固比3.5mL/g 的條件下,提取超過96%的Ni、Co 和Mn。酸浸工藝更有效和經濟,這歸因于還原焙燒后高價態金屬向低價態轉變。Hu 等[32]應用還原焙燒 將LiNixCoyMnzO2轉 化 分 解 成Li2CO3、Ni、Co 和MnO,然后使用碳酸水浸出處理焙燒產品,并蒸發濾液制備出純Li2CO3,瀝濾殘余物用H2SO4溶解并再循環其他金屬。結果表明,在碳含量為19.9%、650℃下焙燒3h 的條件下,通過碳酸水浸出回收84.7%的Li,通過酸浸可以回收99%以上的Ni、Co和Mn。最 后,得 到 了Li2CO3、NiSO4、CoSO4和MnSO4。該工藝具有很大的潛力,可以進行對廢LIBs進行工業化回收。
與有機酸相比,無機酸通常具有更高的浸出效率,但存在有毒氣體排放(主要是Cl2、SO3及NOx等)、酸廢液難處理等環保問題。采用酸性較強的有機酸作為浸出劑,則可降低二次污染。Li等[33]用抗壞血酸作為浸出劑和還原劑來浸出正極材料,得到的最佳實驗條件為:抗壞血酸1.25mol/L、溫度70℃、時間20min、固液比25g/L,在此條件下Co、Li 的浸出率分別為94.8%、98.5%。該方法提供了從廢LIBs 回收有價值材料的有效方法,并且它可以按比例放大用于商業化應用。He 等[34]用天然L-酒石酸浸出LiNi0.5Co0.2Mn0.3O2,在H2O24%(體積分數)、酒石酸2mol/L、固液比17g/L、溫度70℃、時間30min最優條件下,Li、Mn、Co、Ni的浸出率分別為99.07%、99.31%、98.64%、99.31%。Gao等[35]用乙酸將Li、Co、Ni 和Mn 選擇性地浸出到溶液中,同時Al 以金屬形式保留。得到的最佳浸出條件為:3.5mol/L 乙酸、溫度60℃、固液比40g/L、H2O24%(體積分數),在此條件下,Co、Li、Mn和Ni 的浸出率分別可達93.62%、99.97%、96.32%和92.67%,但僅浸出2.36%的Al。

表1 廢舊NCM的正極片預處理方法
由于單純的無機酸或有機酸浸出均存在著無法完全克服的缺點,為綜合兩種酸體系的優勢,研究工作者用有機酸加無機酸的混合酸進行實驗,從而獲得較高的浸出率和低的污染性。Zhuang等[36]提出了一種新型的濕法冶金工藝,用磷酸(浸出劑)和檸檬酸(浸出劑和還原劑)組成的混合酸浸出LiNi0.5Co0.2Mn0.3O2正極材料。在H3PO40.2mol/L、C6H8O70.4mol/L、時間30min、溫度90℃、固液比20g/L 的浸出條件下,Li、Ni、Co、Mn的浸出率分別為100%、93.38%、91.63%、92.00%。
(2)堿浸 一般酸浸法對不同金屬(Li、Ni、Co、Mn以及Fe、Cu)的選擇性較差,使金屬從浸出液中的分離和純化比較復雜,并常導致過量的廢水排放。采用堿性體系,則有望實現Co、Ni 的選擇性浸出,從而降低后續金屬分離的困難。有研究表明,氨水是一種理想的選擇性浸出Cu、Ni 以及Co的浸出劑。在適當的pH范圍下,其反應過程見式(2)和式(3)。
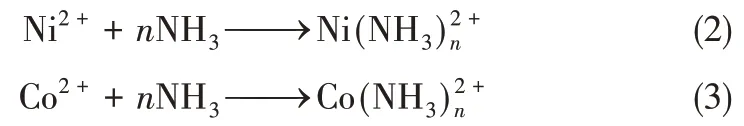
Ku 等[37]使用由氨、碳酸銨和亞硫酸銨組成的氨基浸出體系對混合廢料進行了氨浸,在浸出過程中可以完全浸出Co 和Cu,而Mn 和Al 幾乎不被浸出,Ni 顯示出一定的浸出效率。Ni 和Co 的浸出在40min內完成,而Cu的浸出率在不到10min內迅速達到100%。Ni和Co的浸出行為遵循反應控制的收縮核模型,Ni 和Co 的活化能分別為57.4kJ/mol、60.4kJ/mol。實驗結果表明最佳的浸出條件為:1mol/L NH3·H2O、 0.5mol/L (NH4)2SO3、 1mol/L(NH4)2CO3、溫度80℃、時間1h,這種回收工藝可以減少氫氧化鈉的消耗,簡化Mn 和Al 的分離工序,相比于酸浸具有流程短、效率高等工藝優勢。
Liu 等[38]提出了一種環保工藝,主要包括還原焙燒和逐步浸出,以從廢LiNixCoyMn1-x-yO2材料中回收Li、Ni、Co 和Mn。并結合熱力學分析(E-pH圖),在最佳條件下,Li、Ni、Co和Mn的浸出率分別 達 到93.68%、 99.56%、 99.87% 和99.90%。Zheng 等[39]通過引入氨-硫酸銨-亞硫酸鈉浸出體系來浸出三元正極材料,得到的最佳條件為:NH34mol/L、(NH4)2SO41.5mol/L、Na2SO30.5mol/L、溫度80℃、固液比10g/L、時間5h。在第一步浸出液中Ni、Co和Li的總選擇性大于98.60%,而Mn的選擇性僅為1.36%。對渣的分析發現,Mn 從Mn4+先還原成Mn2+,然后以(NH4)2Mn(SO3)2·H2O 的形式沉淀到殘余物中,Ni、Co 和Li 則以金屬離子或氨絡合物的形式保留在溶液中。
Chen 等[40]提出了一種熱處理-氨浸工藝來處理廢舊LIBs,首先將正極活性粉末在300℃和550℃空氣氣氛中煅燒,用(NH4)2SO4-(NH4)2SO3體系進行氨浸。在最佳條件下,Ni、Co、Mn和Li可有效浸出,浸出率分別為98%、81%、92%和98%。然而,隨著氨濃度的增加,發現Co和Mn以(NH4)2Co(SO4)2·H2O、(NH4)2Mn(SO3)2·H2O和(NH4)2Mn(SO4)2·6H2O的形式沉淀入渣。基于此研究,可通過控制復鹽的形成來實現選擇性浸出。
為進一步提高氨浸的效率,研究工作者采用兩步氨浸法進行廢舊LIBs 的處理。Meng 等[41]使用氨溶液作為浸出劑,亞硫酸鈉作為還原劑,對LiNixCoyMn1-x-yO2(x=1/3、0.5、0.8)進行浸出,在對錳渣分析后發現,錳首先以Mn2+形式進入浸出液,而后在添加劑亞硫酸鈉的作用下,轉化為Mn3O4,最終以(NH4)2Mn(SO3)2·H2O 沉淀入渣。與緊密包裹在未反應材料表面的(NH4)2Mn(SO3)2·H2O 相比,松散多孔的Mn3O4更有利于離子擴散和浸出反應。通過兩步浸出工藝,Li、Ni 和Co 的浸出率分別為93.3%、98.2%和97.9%,遠高于一步氨浸法。該方法用于處理LiNi0.5Co0.2Mn0.3O2時,Li、Ni 和Co的浸出率分別為94.4%、99.7%和99.5%;用于處理LiNi0.8Co0.1Mn0.1O2時,Li、Ni 和Co 的浸出率分別達到95.0%、98.4%和96.9%。
氨浸法是一種可實現Ni、Co、Mn 選擇性分離的有效方法,Mn 以復合鹽形式進入浸出渣,可簡化Mn 和Ni、Co 的分離工序。相比于一步氨浸法,兩步氨浸法具有更高的浸出效率。但與酸浸法相比,由于氨氣對環境也造成了較大的危害,是該方法大規模應用于工業化的瓶頸。昆明理工大學林艷等[42]發明的加壓氨浸法-蒸氨聯合工藝,是一種廢舊三元正極材料的低成本、短流程回收再利用新工藝。通過控制溶液的酸堿度和氨濃度,調控合成過程中Ni、Co 和摻雜鹽的配比,可實現浸出、共沉淀的循環作業和氨氣的閉路循環,加壓氨浸工序的Ni、Co、Li等有價金屬綜合浸出率達到92%,再生制備的三元正極材料前體可以滿足不同系列三元正極材料的制備需求。
(3)微生物浸出 微生物浸出是一種由微生物輔助的礦物生物氧化過程,在此過程中,不溶性金屬氧化物轉化為水溶性金屬硫酸鹽,從而可以實現廢舊電池材料的浸出。其性能主要取決于微生物將不溶性固體化合物轉化為可溶和可提取形式的能力[7]。
Xin 等[43]比較了嗜酸性硫氧化細菌(SOB)、鐵氧化細菌(IOB)和混合細菌體系(MS-MC)這3種生物浸出系統對電極材料的浸提性能,純SOB系統可以從LiFePO4中浸出98%的Li,MS-MC系統可以從LiMnO2中浸出95%的Li和96%的Mn。通過pH 調節,MS-MC 系統可以從LiNixCoyMn1-x-yO2中浸出超過95%的金屬。浸出機制主要是細胞不斷產生的H2SO4和細胞的接觸機制賦予了生物浸提性能,Co、Ni 和Mn 的溶解浸出主要是由于Fe2+還原和酸溶解的共同作用。為了提高其浸出的固液比,Niu 等[44]研究了固液比對金屬浸出的影響規律,發現當固液比從1%增加到4%時,Co 的浸出率從52%降低到10%,Li 的浸出率從80%降低到37%。通過控制反應溫度,增加混合能量底物的劑量以及調節pH 后發現,固液比為2%時,Co、Li 的最大浸出率分別為89%、72%。Bajestani 等[45]使用酸性氧化鐵硫桿菌在pH=2.5、溫度30℃的條件下,即使增加瀝濾時間且Fe2+作為催化劑,Co和Li的瀝濾效率也相當低。而Zeng等[46]發現Cu2+也可以用作酸性氧化鐵硫桿菌浸出過程中的催化劑,在銅離子為0.75g/L 的條件下,生物浸出6 天后,幾乎所有Co(99.9%)都進入溶液,研究表明銅離子對Co 溶解的增強作用主要機理是LiCoO2與銅離子發生陽離子交換反應,在樣品表面形成CuCo2O4,從而加快了反應速率。
可以發現細菌的浸出過程要求較低的pH 且變化較小,這無疑增加了浸出的成本。如果能找到一種在較寬pH范圍生存且對金屬有高浸出率的菌類,那么將能夠代替細菌浸出。Biswal 等[47]比較了黑曲霉菌株MM1和SG1以及酸性硫代氧化硫桿菌80191對廢LIBs 中Co 和Li 的生物浸出率。最后發現真菌對金屬的浸出率很高,甚至比細菌或酸浸更好。在菌 株MM1 中 觀 察 到 大 量 的Co (82%) 和Li(100%)溶解,但是在80191 菌株中金屬溶解性很差,只有22%的Co 和66%的Li 溶解。這項研究的結果表明,真菌生物浸出可能是一種環境友好的方法,可用于從廢LIBs中溶解和回收大量金屬。
與傳統方法相比,生物冶金過程發生在溫和的條件下,能耗較低,使其成為一種環保技術。然而,動力學緩慢和固液比低是生物冶金過程應用于工業生產時的致命弱點。因此,處置廢LIBs 的生物冶金方法盡管在節能方面具有顯著優勢,但仍遠非工業應用。
1.2.3 再生
從廢舊正極材料的浸出液中完全分離出各種有價金屬,存在流程長、成本高、回收率低等缺點,而合成純化法能夠直接實現新電極材料的再生,可避免直接分離金屬的困難。目前,用于再生正極材料的制備方法主要有沉淀分離法、溶膠-凝膠法、共沉淀法。
(1)沉淀分離法 沉淀分離法是將經過拆解分離得到的廢舊LiNixCoyMnzO2正極材料用無機酸或有機酸溶解,得到含有Li+、Ni2+、Co2+和Mn2+等離子的浸出液;而后加入相關的沉淀劑,實現上述離子的選擇性沉淀并分別回收的方法。
Wang 等[48]在HCl 4mol/L、溫度80℃、時間1h、固液比0.02g/mL 的條件下,獲得超過99%的Co、Mn、Ni 和Li。為了進一步分離出各種金屬,首先將浸出液中的Mn選擇性地與KMnO4試劑反應,Mn以MnO2和Mn(OH)2沉淀回收。而后,二甲基乙二肟選擇性提取浸出液中的Ni。隨后,用1mol/L NaOH 將溶液pH 調至11,Co 以氫氧化鈷的形式沉淀。最后將飽和Na2CO3溶液加入到濾液中,Li+就以Li2CO3形式沉淀出來。整個流程回收的Li、Mn、Co 和Ni 的粉末純度分別為96.97%、98.23%、96.94%和97.43%。
Chen等[49]用檸檬酸和D-葡萄糖在時間120min、溫度80℃、檸檬酸1.5mol/L、S/L=20g/L、還原劑添加量0.5g/g的條件下浸出LiNi1/3Co1/3Mn1/3O2,Li、Ni、Co和Mn的浸出率分別為99%、91%、92%和94%。隨后,使用H2C2O4和H3PO4直接沉淀Ni、Co和Li等金屬,在優化的沉淀條件下,Ni、Co 和Li 的回收率分別約為96%、97%和93%。
Sattar 等[50]首先用硫酸浸出LiNixCoyMnzO2正極材料,在H2SO43.0mol/L、溫度50℃、H2O24%(體積分數)、固液比20g/L、時間30min的條件下,Li、Ni、Co和Mn的浸出率均大于98%。并通過三步法分離獲得了相應的金屬鹽產品,第一步先調節溶液pH=2.5,控制n(KMnO4)∶n(Mn2+)=1.2,同時溫度和時間分別固定在80℃和1h,98%的Mn2+以MnO2形式沉淀。第二步將除去Mn 的溶液pH 調至5.0 左右,在溫度80℃、時間1h 的條件下,當n(DMG)∶n(Ni2+)=2.0時,99%的Ni2+以Ni-DMG形式沉淀,并且DMG 可再生使用,從而實現了Mn 和Ni 的選擇性沉淀。隨后,在pH=5.0 和萃取相比(O/A)為1條件下,使用0.64mol/L Cyanex 272(50%皂化)2階段溶劑萃取回收高純度的CoSO4溶液。最后,Li+以Li2CO3形式沉淀,從而實現了廢LIBs的再循環。
Barik等[51]在固液比1∶5、HCl 1.75mol/L、溫度50℃、時間2h的條件下浸出正極材料,Co、Mn和Li浸出率均大于99%。在30℃下將NaOCl溶液加入到浸出液[pH=1.5、n(NaOCl)/n(Mn2+)=1.5,摩爾比]中反應30min,發現沉淀物為MnO2、Na0.55Mn2O4·1.5H2O和Mn3O4等錳氧化物的混合物,Co和Mn的總回收率分別為90%和95%。
Meshram 等[52]用硫酸和亞硫酸氫鈉浸出廢LIBs。最佳的浸出條件為:H2SO41mol/L、NaHSO30.075mol/L、溫度95℃、固液比20g/L、反應時間4h,在此條件下Li、Co、Ni和Mn的浸出率分別為96.7%、91.6%、96.4%和87.9%。而后首先采用草酸將Co2+轉化為草酸鈷(CoC2O4·2H2O)沉淀,Co的回收率>98%。然后從Co 的貧化溶液中沉淀出MnCO3(pH=7.5)、NiCO3(pH=9)和Li2CO3(pH=14)。通過該方法,以碳酸鹽和草酸鹽的形式,分別實現Li、Co、Ni、Mn 的選擇性分離,可獲得較高的綜合回收率。現有報道的Li、Ni、Co、Mn 的沉淀分離原理見表2。
沉淀分離法處理三元正極材料的浸出液,具有Ni、Co、Mn、Li 元素的回收率高、產品純度高等優 點, 回 收 產 品 有Li2CO3、 MnO2、 Mn(OH)2、CoSO4、CoC2O4·2H2O、MnCO3、NiCO3等,但該方法的工藝流程相對較為復雜,控制參數較多,同時會產生各種有危害的氣體,造成二次污染。
(2)溶膠-凝膠法 溶膠-凝膠法是用有機酸作為浸出劑,然后調節金屬離子成分,在液相下將這些原料均勻混合,并進行水解、縮合化學反應,在溶液中形成穩定的透明溶膠體系,凝膠經過干燥、燒結固化再生出三元正極材料。
Li等[54]分別用乙酸和馬來酸浸出LiNi1/3Co1/3Mn1/3O2,并再合成出LiNi1/3Co1/3Mn1/3O2,結果表明用馬來酸浸出液合成的正極材料具有更好的性能。這主要是因為馬來酸通過酯化可建立穩定的網絡來螯合金屬離子,而乙酸的弱螯合作用則導致雜質的形成。Li 等[55]用檸檬酸加雙氧水體系處理LiCoO2、LiCo1/3Ni1/3Mn1/3O2、LiMn2O4的混合廢料,浸出率均達到95%以上。而后,采用溶膠-凝膠法合成LiCo1/3Ni1/3Mn1/3O2正極材料,在0.2C 放電倍率下,初始容量為149.8mA·h/g,循環160 圈后,廢舊電池容量和新合成的電極材料放電比容量分別為140.7mA·h/g和121.2mA·h/g。在1C的放電倍率下,循環300圈,廢舊電池和新合成的電池放電比容量分別為113.2mA·h/g和78.4mA·h/g。
Li等[56]采用乳酸作為浸出劑浸出LiNi1/3Co1/3Mn1/3O2,最佳實驗條件為:乳酸濃度1.5mol/L、固液比20g/L、浸出溫度70℃、H2O20.5%(體積分數),Li、Ni、Co 和Mn 的 浸 出 效 率 分 別 為97.70%、98.20%、98.90%和98.40%。并通過溶膠-凝膠法再生出LiNi1/3Co1/3Mn1/3O2,0.5C倍率下循環100次后放電容量為138.2 mA·h/g,容量保持率為96%,與新材料電化學性能相當。

表2 廢舊NCM中金屬離子的分離原理
Yao等[57]用檸檬酸和H2O2浸出LiNi1/3Co1/3Mn1/3O2,在檸檬酸1.0mol/L、固液比80g/L、H2O212%(體積分數)、溫度60℃、反應時間40min 的最佳浸出條件下,金屬浸出率超過98%。然后通過添加LiNO3、Ni(NO3)2·6H2O、Co(NO3)2·6H2O 和Mn(NO3)2,將金屬離子比調節至3.05∶1∶1∶1,pH 調節至8.0,在80℃水浴中加熱得到透明溶膠,然后在110℃下干燥24h,最后將干燥凝膠在350℃下煅燒2h,750℃下煅燒12h,獲得再生的正極材料。電化學測試結果顯示其與商業LiNi1/3Co1/3Mn1/3O2的電化學性能相當。
(3)共沉淀法 共沉淀法是指向浸出液中加入沉淀劑,經緩慢的沉淀反應后,可得到各種成分均一的前體,最后混鋰煅燒成所需的正極材料。
Yang等[58]從混合型廢正極材料的浸出液中成功再生了0.2Li2MnO3·0.8LiNi1/3Co1/3Mn1/3O2。結果表明,在pH≈10.5 和NH30.5mol/L 條件下,得到粒度和結晶度良好的球形前體,再生正極材料具有良好的R-3m 組層狀結構,并且陽離子混排程度低。此外,分別在0.1C、0.5C 和1C 的放電倍率下循環50 次后,再生正極材料的放電比容量分別可達到248.3mA·h/g、196.4mA·h/g 和167.0mA·h/g,并且容量保持率可以維持在80%以上。
Liu 等[59]首先將LiNi1/3Co1/3Mn1/3O2與10%(質量分數)炭黑在氬氣氣氛下、600℃煅燒0.5h,還原焙燒得到Li2CO3、NiO、MnO、Ni、Co。然后在常溫下水浸,90℃蒸發結晶,將Li+轉化為Li2CO3,隨后,用H2SO4浸出濾渣,得到Ni2+、Co2+和Mn2+的溶液,調節n(Ni2+)∶n(Co2+)∶n(Mn2+)=5∶2∶3,并將NaOH 溶液(7mol/L)和氨(7.5mol/L)泵入5L 攪拌釜反應器,在攪拌速度300r/min、pH=10.7~10.8、溫度55℃、反應時間30h 的條件下,得到氫氧化物前體。制備的NCM與商業NCM的形態和結構相似。電化學測試表明,再生NCM 的初始放電比容量為172.9mA·h/g(2.5~4.3V,0.2C),循環50次后也可以提供160.9mA·h/g的放電比容量,容量保持率為93.08%。
每幅圖(表)應冠以中、英文圖(表)題。說明性資料應置于圖(表)下方注釋中。文中所有圖請用矢量圖或Word圖的形式,必須是可修改的(不能使用照片格式)。
He 等[60]將正極材料溶解在1mol/L H2SO4和1%(體積分數)H2O2的溶液中,通過加入NiSO4·6H2O、CoSO4·7H2O和MnSO4·H2O,將浸出液中Ni∶Co∶Mn的摩爾比調節為1∶1∶1。然后在pH=7.5、溫度60℃的條件下反應12h,將沉淀物Ni1/3Co1/3Mn1/3CO3在500℃下煅燒5h,得到(Ni1/3Co1/3Mn1/3)3O4中間體。然后將該金屬氧化物與Li2CO3以摩爾比1.06充分混合。最后將混合物在500℃下預熱5h,然后在空氣氣氛下900℃燒結12h,得到再生的LiNi1/3Co1/3Mn1/3O2。再生的LiNi1/3Co1/3Mn1/3O2在0.1C 倍率下的初始放電比容量為163.5mA·h/g,1C倍率下的放電比容量為135.1mA·h/g,循環50 次容量保持率為94.1%。這些結果表明再生的LiNi1/3Co1/3Mn1/3O2與新合成的正極材料具有相當的電化學性能。
Yang等[61]開發了一種基于共萃取和共沉淀的廢舊電池處理新方法,以回收有價金屬和再生正極材料。采用二(2-乙基己基)磷酸(D2EHPA)+煤油的萃取體系,實現100%Mn、99%Co 和85%Ni 的共萃取,并實現與Li分離。然后,通過沉淀法將Li以Li2CO3形式從萃余液中回收,Li2CO3純度達到99.2%。并用0.5mol/L H2SO4反萃有機負載相,然后通過共沉淀法直接從反萃液中再生LiNi1/3Co1/3Mn1/3O2。再生正極材料為球形狀,無任何雜質,符合中國LiNi1/3Co1/3Mn1/3O2生產標準,具有良好的電化學性能。此外,還引入了廢電池管理模型,以保證廢舊電池回收的材料供應。
Sencanski等[62]將6.262g廢LiNi1/3Co1/3Mn1/3O2正極材料,用2mol HNO3和H2O2溶解,然后用10mol/L NaOH 調節浸出液pH=14。在磁力攪拌下形成深藍色沉淀物,通過離心分離沉淀物并將沉淀物與Li2CO3混合,在700℃下煅燒得到LiCo0.415Mn0.435Ni0.15O2。最后通過在6mol/L NaNO3溶液中進行Li-Na 電化學交換得到NaCo0.415Mn0.435Ni0.15O2。在100mA/g 的電流密度下,放電比容量為93mA·h/g。
共沉淀法主要通過碳酸鹽、氫氧化物、草酸鹽沉淀法合成正極材料的前體,下面以合成LiNi1/3Co1/3Mn1/3O2的前體為例,其反應機理如下。
①碳酸鹽法反應機理如式(4)、式(5)所示。
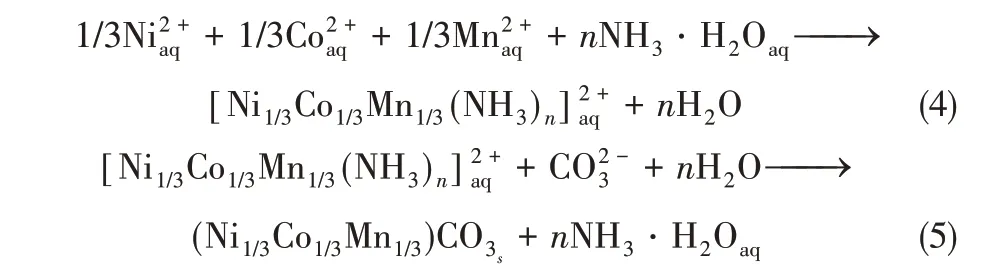
②氫氧化物沉淀法反應機理如式(6)、式(7)所示。

③草酸鹽沉淀法反應機理如式(8)所示。
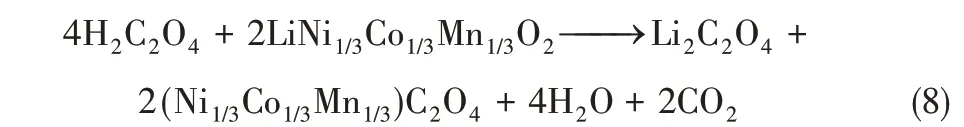
2 負極材料回收
廢舊LIBs 負極材料中有質量分數12%~21%的石墨并有大量銅箔[63],占鋰離子電池材料總成本的25%~28%。回收石墨和銅箔對緩解電池級石墨和精銅資源短缺具有重要意義,目前主要通過煅燒酸浸、機械浮選分離等方法來收集石墨。
楊悅等[64]首先通過兩段煅燒收集廢石墨,然后在HCl 1.5mol/L、時間60min、固液比100g/L 的條件下,將收集的石墨進行簡單的酸浸純化。通過控制pH,先調節至7后再調節至9,分段從浸出液中除去99.9%的鋁和99.9%的銅,并在浸出液中加入碳酸鈉回收了高純度(>99%)的Li2CO3。電化學測試結果表明,再生石墨具有高的初始比容量,循環100 次容量保持率為97.9%,在372mA/g 的電流密度下也顯示出優異的循環性能。Ma 等[65]將正極材料進行粉碎、篩分,在室溫下用5mol/L H2SO4和35%(質量分數)H2O2進行酸浸處理,并過濾得到石墨濾餅,將浸出后的石墨與熔融劑NaOH粉末在500℃下燒結40min,去除大部分雜質,并用去離子水洗滌,干燥,最后得到了精制石墨(PG),回收的石墨在0.1C倍率下的放電比容量為377.3mA·h/g,具有良好的電化學性能。通過煅燒酸浸法回收石墨,產品純度高,但工序復雜、效率低。
與煅燒酸浸法相比,機械浮選分離法在處理廢舊石墨電極時,具有更高的效率也更容易實現工業化。Wang 等[66]通過機械分離銅集流體來收集石墨(SG),用去離子水洗滌5 次除去大部分雜質,干燥、研磨后進行電化學測試,可以很好地恢復石墨的電化學活性,經過100次循環后,回收的石墨依然有345mA·h/g的比容量,與商用石墨相當,這種方法既不需要有害化學物質也不需要高溫操作。Wang等[67]首先將廢舊LIBs粉碎成0.25mm大小的粉末,然后在450℃下煅燒15min,最后通過浮選工藝有效地分離成LiCoO2和石墨濃縮物。Co、Mn、Cu 和Al 的富集率分別為1.35、1.29、1.25 和1.19,回 收 率 分 別 為97.66%、 93.66%、 90.14% 和86.29%。Yu 等[26]將混合電極粉末(40g/L)、鋼球、收集劑200g/t 和起泡劑(甲基異丁基甲醇MIBC 和200g/t 正十二烷)共研磨5min,然后進行反浮選,石墨和LiCoO2濃縮物可分別從浮選槽的底部和泡沫層獲得。LiCoO2和石墨的精礦品位分別為97.19%和82.57%,回收率分別為49.32%和73.56%。
Zhan等[68]首先將電極材料從集流體上刮下并進行干磨,進行70目篩分(小于210μm),并用蒸餾水沖洗至少5次,以去除多余的電解質,最后用煤油和甲基異丁基甲醇(MIBC)作為收集劑和起泡劑進行浮選,實驗優化發現總回收率為74.3%。Zhang等[69]開發了一種新的機械破碎與熱解-強化浮選相結合的新工藝,采用熱解技術解決了電極材料浮選效率低的問題。研究發現,殘留的有機黏結劑和電解質是導致電極材料浮選效率低的主要原因,最佳浮選條件是以10℃/min 的加熱速率加熱到550℃并保溫15min,在此條件下電極材料純度為94.72%,回收率為83.75%。兩步熱解增強浮選工藝可進一步使電極材料純度提高到98.00%。本研究開發的新方法為廢舊鋰離子電池的回收利用提供了新思路。
廢舊石墨負極的增值化利用也是目前研究的熱點。Natarajan 等[70]首先將負極片在氬氣氣氛中700℃煅燒3h,得到石墨負極,然后將石墨與KMnO4添加到濃硫酸中,冰浴攪拌2h,并添加H2O2以減少殘留的KMnO4,隨后,用5%HCl 溶液和水洗滌直到濾液的pH達到7。最后,60℃下干燥24h 制備出氧化石墨烯(GO),并使用金屬外殼進行GO還原,得到還原氧化石墨烯(rGO)。電化學測試表明其在25A/g 的電流密度下顯示出20000 次循環的高循環穩定性,由廢舊LIBs 合成的rGO 可以成為下一代高性能超級電容器的材料。梁風等[71]將退役石墨負極進行深度除雜后,經成型處理得到純石墨棒或石墨塊,并將其作為等離子體制備石墨烯等碳納米材料的原材料。該方法通過改變等離子體氣氛種類與壓力大小,可以對所制備碳納米材料的種類和品質進行控制,是一種回收石墨制備高附加值碳納米材料的有效手段,具有極大的產業化潛力。
3 電解液回收
廢舊LIBs 中有大量的電解液,傳統拆解會引起電解液的揮發,LiPF6易水解[72]形成化合物,特別是HF,由于其化學侵蝕性和毒性,會嚴重阻礙或破壞工業化回收進程,而且會對環境和人體健康造成危害,所以非常有必要將其回收處理。同時電解液里含有價金屬鋰,如果可以將其回收處理既有利于環境也能創造一定的經濟效益。通常廢LIBs都有一定的老化[73],液體電解液會部分分解為固體和氣體產物,通常表現為“干燥”,未分解的電解液就會存在于電極的更深層中,并固定在固體電解質的分解產物中。因此,無論是簡單去除還是后續分離,都難以回收。目前主要通過超臨界CO2萃取、溶解蒸餾沉淀等方法將其回收。
Liu 等[74]采用超臨界CO2萃取(SFE)廢舊LIBs中的有機碳酸酯類電解液,并通過響應曲面法得到最優工藝參數為:壓力23 MPa、溫度40℃、時間45min,在此工藝條件下電解質的產率可以達到85.07%±0.36%,實驗結果表明,萃取壓力是電解液萃取的主要影響因素。Grützke 等[75]開發了用超臨界和液態二氧化碳(Sc和liq CO2)萃取電解液的方法,研究發現線性碳酸酯如碳酸二甲酯(DMC)和碳酸乙基甲基酯(EMC)用liq CO2萃取效率較高,而環狀碳酸乙烯酯(EC)用Sc CO2萃取回收率更高,而對LiPF6最為有效的方法是向CO2中添加溶劑,提高所有成分的回收率。最佳工藝為用liq CO2(25℃,60bar)和0.5mL/min 乙腈(ACN)/碳酸亞丙酯(PC)混合物萃取30min,最高回收率為73.5%±3.6%(質量分數)。Liu 等[76]研究了超臨界CO2萃取電解液時組分的萃取行為,研究發現較高的壓力提高了總提取率,這歸因于超臨界CO2的高極性。然而,EC 的提取率與壓力相反,由此可見極性起著比超臨界流體密度更重要的作用,在最佳工藝條件下總體最高回收率是88.71%±0.87%(質量分數),同時建議應使用非極性或弱極性萃取介質萃取非極性碳酸鹽,極性碳酸鹽應使用極性溶劑萃取,或在非極性溶劑中添加中等極性助溶劑。
除了用超臨界CO2萃取電解液,還有溶解蒸餾沉淀法。He 等[77]制造了一種特殊的復合水性脫皮劑,即去角質和萃取液(AEES),并將其應用于該工藝中。結果表明,通過弱化正極材料與金屬箔之間的黏結力,可以使正極材料從鋁箔中剝離。電解液中的碳酸亞乙酯(EC)和碳酸亞丙酯(PC)溶于AEES,通過蒸餾可以回收95.6%有機混合物。由于LiPF6可與AEES 反應生成水溶性鋰鹽和NaPF6,可通過蒸發結晶得到Li2CO3和NaPF6。在最佳AEES濃度下,電解液、鋁箔、銅箔和電極材料的回收效率分別為95.6%、99.0%、100%和接近100%。該方法有效地避免了電解液雜質分解滲透到電極材料中,并且對于工業應用、環境是友好的。
通過超臨界CO2萃取、溶解蒸餾沉淀法可以很好地收集電解液,但是對于電解液的品質沒有進行進一步提升,可能無法繼續循環利用到電池中,為了更好地循環利用回收的電解液,Liu 等[78]通過超臨界CO2萃取,樹脂和分子篩純化以及組分補充一系列工藝純化回收了電解液。所得電解液在20℃下顯示出0.19mS/cm的高離子電導率,這非常接近于具有相同成分的市售電解液。此外,在線性掃描伏安法(LSV)測量中,電解液在高達5.4V(vs. Li/Li+)的情況下也是電化學穩定的。Li/LiCoO2半電池測試結果表明,放電倍率為0.2C 時,初始放電比容量為115mA·h/g,循環100 次后,容量保持率為66%。這一循環回收工藝為電解液的循環再利用提供了新的思路。
4 結語
新能源汽車是國家戰略性新興產業,而動力電池的研發與回收是其可持續發展的瓶頸。隨著動力電池井噴式退役,實現其高效清潔回收利用,既是資源安全供給的現實保障,又是生態文明建設的戰略需求。針對三元鋰離子電池回收再生技術,由于物理法修復再生對廢舊電池品質的要求(活性物質表面的Li/Ni 混排較低,結構破壞低)較高,現階段的研究重點仍以濕法浸出回收工藝為主,廢舊正極材料的物理法修復再生技術、有機-無機混合酸浸法、加壓氨浸-蒸氨聯合新工藝、酸浸-共沉淀法等新技術已取得重要進展,均是具有商業化應用和競爭優勢的有效方法;其中負極材料回收主要是機械浮選分離法、rGO、等離子體廢舊石墨等高值化利用技術;電解液回收以超臨界CO2萃取技術為主、溶解蒸餾沉淀法為輔都取得了較大的進展。但縱觀當前廢舊鋰離子電池回收工藝及產業現狀,還存在回收機理研究不深入、定向轉化技術不成熟、綜合利用不成體系、工藝裝備水平落后、回收產品附加值低、二次污染嚴重等問題。因此,加強產學研合作,探明退役三元鋰離子電池材料的失效模式,構建材料失效模式及其稟賦特征的評定標準;基于材料失效模式差異,建立退役材料稟賦特征與定向轉化/梯級回收各技術間的對應關系,取得多技術協同、集成互補的“因材施策”定向轉化與梯級回收機制,開發自動化程度高、綠色環保、高效短流程的廢舊三元鋰離子電池回收再利用新技術是實現我國電動汽車產業可持續發展的迫切需要。

