長期肌內注射青霉素致雙臀部大面積鈣鹽沉積癥一例
曹子龍 馬玲
山東大學齊魯醫院燒傷整形科,濟南250012
患者女,68歲,因雙側臀部異物性結節30余年,多發破潰2 年,于2016 年4 月入院。患者40 年前因雙側輸卵管結扎術后反復腹痛伴發熱,診斷為盆腔感染,雙側臀部肌內注射青霉素抗感染,隨病情反復間斷注射。最長連續注射時間達3 個月,80 萬U 每 日2 次。治療5 年后,因雙側臀部注射部位變硬,進展為結節,改為靜脈用藥。質硬部位無明顯不適感,未治療,但質硬部位逐漸擴大、融合,累及至大腿中上部。2年前質硬部位破潰,有大量乳白色黏稠滲液,遂就診。
體檢:雙側臀部及大腿后側大范圍凹凸不平質硬區域(圖1),皮下組織廣泛硬化,與皮膚粘連緊密,局部觸及皮下波動感,有壓痛。多處皮膚破潰,擠壓可見乳白色黏稠無味滲液。雙下肢屈髖活動度輕度受限。CT 影像學檢查:雙側臀部及股骨近端皮下脂肪壞死,可能有鈣鹽沉積。實驗室檢查:血常規、血鈣、血磷、堿性磷酸酶、25-羥基維生素D水平均正常。
診斷:雙臀部及大腿鈣鹽沉積癥。
治療:手術切除鈣鹽沉積組織。患者雙側皮損范圍廣,為減少手術風險,分別于2016年4月及9月,治療左右兩側。手術在全身麻醉下進行,沿病變范圍切開皮膚,皮下筋膜層見大片色白質硬鈣化樣物質(圖2A),伴紅黃渾濁液體流出;部分病灶與皮膚黏連緊密,呈囊性擴張,剖開可見內部豆腐渣樣壞死物存留(圖2B)。將肉眼所見病灶完整切除,應用負壓吸引裝置治療覆蓋創面。1 周后清創探查,創面新鮮,清除殘余病灶及壞死皮膚,拉攏縫合皮膚,無法縫合處予植皮。術后12 ~14 d 拆線,愈合良好。分泌物細菌培養陰性。切除病灶組織病理:皮下脂肪組織壞死,纖維組織增生,玻璃樣變性,廣泛鈣化;另見擴張的囊性結構,內含黏性液體(圖3)。術后2 年隨訪,原雙側臀部及大腿后側皮膚質地較前明顯柔軟,未觸及質硬結節,下肢活動良好。
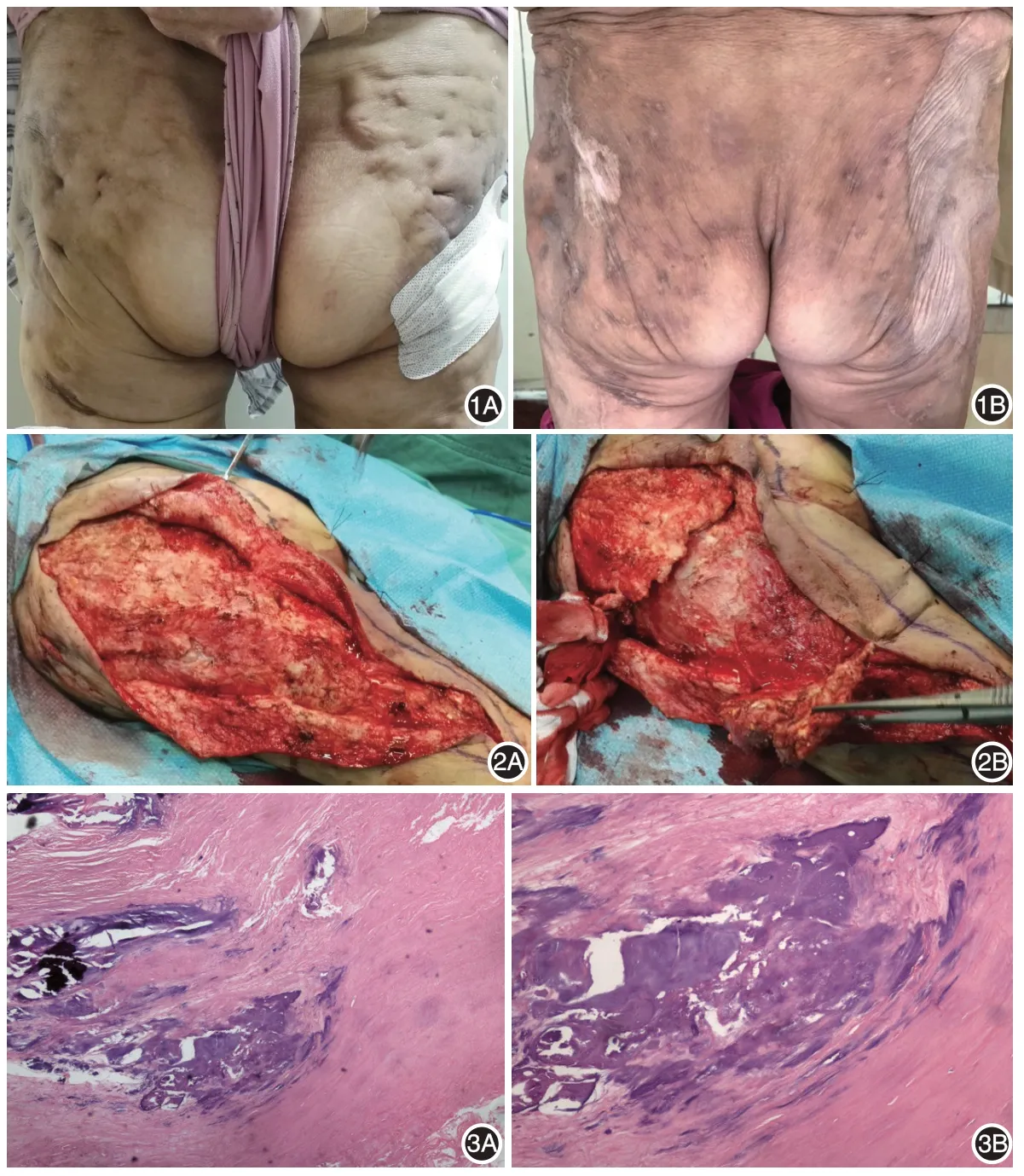
圖1 患者治療前后皮損表現 1A:就診時雙側臀部及大腿后側大范圍凹凸不平質硬區域;1B:術后2年,原雙側臀部及大腿后側皮膚質地較前明顯柔軟,未觸及質硬結節 圖2 手術切除病灶 2A:皮下筋膜層見大片色白質硬鈣化樣物質;2B:部分病灶與皮膚黏連緊密,呈囊性擴張,剖開可見內部豆腐渣樣壞死物存留圖3 手術切除病灶組織病理 3A:皮下脂肪組織壞死并纖維組織增生玻璃樣變性,廣泛鈣化(HE×40);3B:見擴張的囊性結構,內含黏性液體(HE×100)
討論皮膚鈣鹽沉積癥是一類鈣磷沉積于皮膚軟組織引起的疾病,可由非特異的各種外界刺激引起,也可作為內在疾病的臨床表現之一。按照病因,皮膚鈣鹽沉積癥可分離為轉移型、鈣化防御型、醫源型、營養不良型及特發型。轉移型與機體代謝紊亂及血液中鈣磷維生素D 水平有關;營養不良型鈣化主要指鈣鹽沉積于受損外傷及風濕免疫疾病誘發的組織中,多是由于局部慢性炎癥及纖維結締組織變性所致[1-3]。此病常累及大關節周圍皮下軟組織,如肘關節、肩關節、髖關節等[4],隨病情進展也可累及肌肉、骨質等。
本例皮膚鈣鹽沉積癥患者血鈣磷水平正常,病變部位30余年前有明確的長期肌內注射史,符合局部創傷所致營養不良型鈣鹽沉積癥。由于發病時間久遠,無法明確皮下鈣化是由治療藥物還是注射因素所引起。青霉素治療引起皮膚的不良反應主要為過敏反應,未發現類似引起鈣鹽沉積癥的報道。因此,推測藥物本身引起鈣化可能性較小。可能的誘因包括,青霉素試劑中存在雜質;使用含鈣液體如氯化鈣作為佐劑;不規范的注射操作,可能注射至真皮或皮下;同一部位的反復刺激;注射速度過快等。以上原因均可導致皮下出血、脂肪液化壞死、炎癥反應發生,病灶逐漸包裹機化,形成肉芽腫,最終鈣化。本例患者臀部及下肢形成的鈣化,在日常擠壓、摩擦活動過程中,炎癥逐漸蔓延,病變擴大,最終形成較大范圍的病灶。
目前,對于較大范圍的鈣鹽沉積癥,以手術治療為主。對于較小范圍的病灶,可采用二氧化碳激光治療[5]。徹底清創是治療成功的關鍵,對于創面感染嚴重,一期無法明確病變范圍的情況下,可術后應用負壓吸引裝置治療[6]。5 ~7 d 后,行二期手術,根據創面情況清除殘余病灶。若皮膚壞死較多,無法直接拉攏縫合時,可考慮植皮。本例患者術后2年時,原雙側臀部及大腿后側皮膚質地較前明顯柔軟,下肢活動良好。
利益沖突所有作者均聲明不存在利益沖突

