新型含2,4-二氯苯基的1,2,4-三唑喹唑啉衍生物的合成及抑菌活性
張貴強, 郭晴晴, 易君明, 趙廷淵, 王 梅, 邢林娜
(興義民族師范學院 貴州省化學合成及環境污染控制和修復技術特色重點實驗室,貴州 興義 562400)
柑橘潰瘍病、煙草青枯病、水稻百葉枯病是常見的農作物疾病,對農作物的質量和產量造成了不利影響,導致了嚴重的經濟損失。現有農藥抑菌劑受耐藥性影響,防治效果不太理想。開發高效、低毒、環境友好型的新型殺菌劑成為農藥領域的研究熱點。
2,4-二氯苯基、1,2,4-三唑和喹唑啉作為活性藥效基團[1-7],在新農藥創制中應用廣泛。戊菌唑、糠菌唑、己唑醇、戊菌唑和啶斑肟等農藥中含2,4-二氯苯基結構;三唑酮、亞胺唑、唑蚜威等高效低毒的農藥中含有1,2,4-三唑結構;喹螨醚、氟喹唑等農藥中含有喹唑啉基團。
1,3,4-噻二嗪也是重要的藥效基團,具有抗菌、調節植物生長、殺蟲和抗病毒等藥理活性[8-11]。喹唑啉結構具有良好的農藥抑菌活性[12-14]。高元磊等[15]合成的喹唑啉化合物對小麥赤霉病菌和蘋果腐爛病菌的抑制率優于對照藥劑噁霉靈。楊緒紅等[16]合成的喹唑啉化合物對煙草青枯病菌的抑制率優于對照藥劑噻菌酮。
拼接高活性藥效基團,常能得到高活性農藥制劑。如烯唑醇、亞胺唑、唑啶草酮、氟醚唑,同時含有2,4-二氯苯基和1,2,4-三唑基團;氟喹唑同時含有2,4-二氯苯基、1,2,4-三唑基團和喹唑啉基團。本文根據活性基團拼接原理,將2,4-二氯苯基、1,2,4-三唑、1,3,4-噻二嗪結構引入喹唑啉結構中,設計并合成了13個未見文獻報道的含2,4-二氯苯基的1,2,4-三唑1,3,4-噻二嗪喹唑啉化合物(9a~9m, Scheme 1),收率59%~74%,其結構經1H NMR,13C NMR,19F NMR和MS表征。采用濁度法測試目標化合物對柑橘潰瘍病菌(Xac)、煙草青枯病菌(Rs)、水稻百葉枯病菌(Xoo)的抑制活性。
1 實驗部分
1.1 儀器與試劑
X-5型熔點儀;JEOL-ECX 400 MHz型核磁共振儀(DMSO-d6為溶劑,TMS為內標);TSQ 8000/MSD三級四級桿氣相色譜質譜。
化合物1~5[3], 2-(2-氯乙酰氨基)-3-甲基-N-甲基苯甲酰胺(8)[17]按文獻方法合成;2,4-二氯苯甲酸,2-氨基-3-甲基苯甲酸,上海阿拉丁試劑有限公司;其余所用試劑均為分析純。
1.2 9a~9m的合成通法
將中間體52 mmol和1%KOH溶液100 mL加入250 mL反應瓶中,攪拌至澄清;緩慢滴加中間體80.51g(2.1mmol)的乙醇(40 mL)溶液,滴畢,攪拌下于50 ℃反應至終點(TLC檢測)。冰浴冷卻,抽濾,濾餅用冰乙醇洗滌,經硅膠柱層析[洗脫劑:V(石油醚)/V(乙酸乙酯)=3/1]純化得9a~9m。
3-(2,4-二氯苯基)-6-(4-溴苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9a): 白色晶體, 產率62%, m.p.164~166 ℃;1H NMR(DMSO-d6,400 MHz)δ: 7.95(d,J=8.0 Hz, 1H, quinazoline-H), 7.86(s, 1H, 2,4-2ClPh-H), 7.64(s, 3H, 2,4-2ClPh-H+NH), 7.53(d,J=8.0 Hz, 2H, 4-BrPh-H), 7.41(t,J=8.0 Hz, 1H, quinazoline-H), 7.34(d,J=8.0 Hz, 2H, 4-BrPh-H), 7.25(d,J=4.0 Hz, 1H, quinazoline-H), 5.59(d,J=4.0 Hz, 1H, SCH), 5.26(t,J=4.0 Hz, 1H , NCH), 3.74(s, 3H, NCH3), 2.34(s, 3H, CH3);13C NMR(125 MHz, DMSO-d6)δ: 161.96, 153.93, 150.12, 144.92, 142.10, 136.78, 136.59, 135.58, 135.52, 134.96, 134.24, 131.98, 129.88, 129.76, 128.20, 127.40, 125.34, 124.36, 121.71, 120.50, 57.78, 30.55, 17.08; MSm/z: 615.0{[M+H]+}。
3-(2,4-二氯苯基)-6-苯基-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9b): 白色晶體, 產率59%, m.p.156~158 ℃;1H NMR(DMSO-d6, 400 MHz)δ: 8.15(d,J=8.0 Hz, 1H, quinazoline-H), 7.62(d,J=4.0 Hz, 1H, 2,4-2ClPh-H), 7.56(d,J=1.6 Hz, 1H, Ph-H), 7.50(d,J=4.0 Hz, 1H, quinazoline-H), 7.43(t,J=8.0 Hz, 1H, quinazoline-H), 7.35(dd,J=4.0 Hz, 4.0 Hz, 1H, Ph-H), 7.27~7.29(m, 4H, Ph-H+NH), 7.26(s, 1H, ArH), 7.20(d,J=8.0 Hz, 1H, Ph-H), 5.44(d,J=4.0 Hz, 1H, SCH), 5.01(t,J=4.0 Hz, 1H, NCH), 3.75(s, 3H, NCH3), 2.60(s, 3H, CH3);13C NMR(125 MHz, DMSO-d6)δ: 161.94, 154.03, 150.14, 144.98, 142.35, 137.31, 136.54, 135.58, 135.20, 134.94, 134.18, 129.89, 129.08, 128.47, 128.17, 127.45, 127.08, 125.43, 124.36, 120.46, 58.67, 41.92, 30.53, 17.06; MSm/z: 536.1{[M+H]+}。

Scheme 1
3-(2,4-二氯苯基)-6-(3,4,5-三甲氧基苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9c): 白色晶體, 產率62%, m.p.196~198 ℃;1H NMR(DMSO-d6,400 MHz)δ: 7.93(d,J=8.0 Hz, 1H, quinazoline-H), 7.85(d,J=1.6 Hz, 1H, 2,4-2ClPh-H), 7.64(d,J=8.0 Hz, 1H, quinazoline-H), 7.63(d,J=1.6 Hz, 1H, 2,4-2ClPh-H), 7.66(s, 1H, 2,4-2ClPh-H), 7.42(t,J=8.0 Hz, 1H, quinazoline-H), 6.69(d,J=8.0 Hz, 2H, methoxyPh-H), 7.12(t,J=4.0 Hz, 1H, NH), 6.69(d,J=5.6 Hz, 1H, SCH), 5.10(d,J=4.0 Hz, 8.0 Hz, 1H, NCH), 3.80(s, 3H, OCH3), 3.74(s, 3H, CH3), 3.70(s, 6H, OCH3), 2.62(s, 3H, CH3);13C NMR(125 MHz, DMSO-d6)δ: 161.89, 153.75, 153.31, 150.21, 145.01, 142.81, 137.63, 136.53, 135.52, 135.21, 134.83, 134.10, 132.71, 129.94, 128.14, 127.38, 125.27, 124.37, 120.46, 105.22, 60.41, 59.92, 42.36, 30.68, 17.06; MSm/z: 626.2{[M+H]+}。
3-(2,4-二氯苯基)-6-(2-氟苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9d): 白色晶體, 產率68%, m.p.176~178 ℃;1H NMR(DMSO-d6,400 MHz)δ: 7.93(d,J=8.0 Hz, 1H, quinazoline-H), 7.82(s, 1H, 2,4-2ClPh-H), 7.62~7.64(m, 3H, 2,4-2ClPh-H+NH), 7.32~7.41(m, 2H, Ph-H), 7.20~7.25(m, 2H, Ph-H), 7.15(d,J=8.0 Hz, 1H, Ph-H), 7.09(d,J=8.0 Hz, 1H, Ph-H), 5.59(d,J=5.2 Hz , 1H, SCH), 5.40(t,J=4.0 Hz, 1H , NCH), 3.73(s, 3H, NCH3), 2.26(s, 3H, CH3);13C NMR(125 MHz, DMSO-d6)δ: 161.95, 161.04, 158.60, 153.28, 149.78, 145.02, 142.62, 136.58, 135.64, 135.17, 134.87, 134.15, 130.87, 130.78, 129.87, 128.46, 128.42, 128.18, 127.37, 125.34, 125.30, 125.27, 125.20, 124.31, 120.49, 116.32, 116.10, 56.51, 53.91, 42.54, 30.45, 30.43, 19.03, 16.74;19F NMR(DMSO-d6, 400 MHz)δ: -115.72, -117.07; MSm/z:554.2{[M+H]+}。
3-(2,4-二氯苯基)-6-(2-羥基-5-溴苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9e): 白色晶體, 產率64%, m.p.201~202 ℃;1H NMR(DMSO-d6, 400 MHz)δ: 7.96(d,J=8.0 Hz, 1H, quinazoline-H), 7.86(d,J=8.0 Hz, 1H, 2,4-2ClPh-H), 7.68(d,J=8.0 Hz, 1H, quinazoline-H), 7.61(d,J=4.0 Hz, 1H, 2,4-2ClPh-H), 7.37~7.41(m, 5H, Ph-H), 6.82(d,J=8.0 Hz, 1H, NH), 6.00(d,J=8.0 Hz , 1H, SCH), 5.49(t,J=4.0 Hz, 8.0 Hz , 1H, NCH), 4.82(s, 1H, OH), 3.42(s, 3H, CH3), 2.39(s, 3H, CH3);13C NMR(125 MHz, DMSO-d6)δ: 167.52, 161.98, 161.61, 157.75, 157.25, 151.82, 150.97, 150.18, 149.06, 144.99, 144.52, 137.17, 136.73, 136.01, 135.53, 135.23, 133.84, 133.59, 133.18, 129.95, 129.50, 128.86, 128.59, 128.03, 127.85, 127.72, 127.60, 126.91, 124.40, 124.35, 120.85, 120.75, 120.26, 112.99, 112.73, 112.63, 87.15, 63.73, 60.23, 38.02, 30.60, 25.96, 19.03, 17.28, 17.18, 16.89, 14.55; MSm/z: 631.3{[M+H]+}。
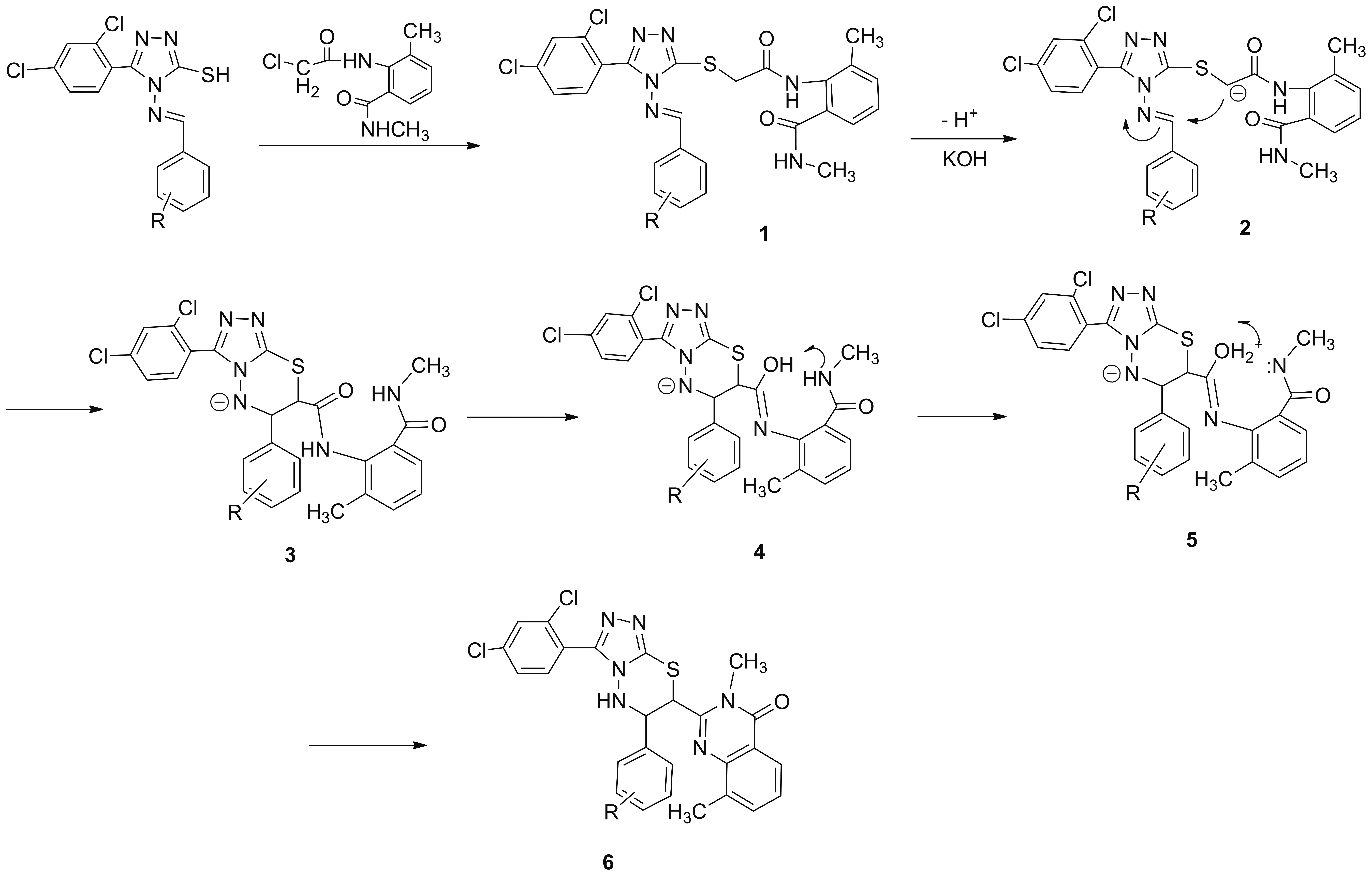
Scheme 2
3-(2,4-二氯苯基)-6-(2-羥基-5-甲基苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9f): 白色晶體, 產率63%, m.p.186~188 ℃;1H NMR(DMSO-d6,400 MHz)δ: 14.11(s, 1H, OH), 7.96(d,J=8.0 Hz, 1H, quinazoline-H), 7.91(d,J=4.0 Hz, 1H, 2,4-2ClPh-H), 7.64(d,J=8.0 Hz, 1H, quinazoline-H), 7.58(dd,J=4.0 Hz, 4.0 Hz, 1H, Ph-H), 7.43(t,J=8.0 Hz, 1H, Ph-H), 7.31(d,J=8.0 Hz, 1H, Ph-H), 7.13(d,J=4.0 Hz, 1H, Ph-H), 7.00(d,J=8.0 Hz, 1H, Ph-H), 6.67(d,J=8.0 Hz, 1H, NH), 6.58(s, 1H, Ph-H), 6.15(t,J=4.0 Hz, 8.0 Hz, 1H, SCH), 5.90(d,J=4.0 Hz, 1H, SCH), 3.62(s, 3H, CH3), 2.34(s, 3H, CH3), 2.19(s, 3H, CH3);13C NMR(125 MHz, DMSO-d6)δ: 167.56, 162.05, 156.18, 151.34, 149.11, 144.59, 137.03, 136.01, 135.35, 135.21, 133.93, 130.91, 130.54, 129.94, 128.01, 127.64, 126.14, 125.92, 124.33, 124.23, 120.74, 110.04, 86.66, 63.57, 30.60, 20.85, 15.93; MSm/z: 565.1{[M+H]+}。
3-(2,4-二氯苯基)-6-(2-羥基苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9g): 白色晶體, 產率65%, m.p.206~208 ℃;1H NMR(DMSO-d6, 400 MHz)δ: 14.14(s, 1H, OH), 7.96(d,J=8.0 Hz, 1H, quinazoline-H), 7.86(d,J=4.0 Hz, 1H, 2,4-2ClPh-H), 7.63(d,J=8.0 Hz, 1H, quinazoline-H), 7.54(dd,J=4.0 Hz, 4.0 Hz, 1H, Ph-H), 7.44(t,J=8.0 Hz, 1H, ArH), 7.17~7.35(m, 4H, Ph-H), 6.99(s, 1H, Ph-H), 6.92(t,J=8.0 Hz, 1H, Ph-H), 6.80(d,J=8.0 Hz, 1H, ArH), 6.29(t,J=4.0 Hz, 1H, SCH), 5.83(s, 1H, SCH), 3.61(s, 3H, CH3), 2.33(s, 3H, CH3);13C NMR(125 MHz, DMSO-d6)δ: 167.52, 162.02, 158.43, 151.13, 149.11, 144.54, 136.99, 136.03, 135.30, 135.24, 135.20, 133.71, 130.63, 129.89, 127.89, 127.65, 125.87, 125.81, 124.33, 124.15, 121.81, 120.75, 110.53, 86.52, 63.11, 60.23, 30.56, 21.23, 16.87, 14.56; MSm/z: 551.1{[M]+}。
3-(2,4-二氯苯基)-6-(4-甲氧基苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9h): 白色晶體, 產率56%, m.p.216~218 ℃;1H NMR(DMSO-d6,400 MHz)δ: 7.94(d,J=8.0 Hz, 1H, quinazoline-H), 7.86(s, 1H, 2,4-2ClPh-H), 7.63~7.71(m, 3H, Ph-H+NH), 7.43(t,J=8.0 Hz, 1H, quinazoline-H), 7.29(d,J=8.0 Hz, 2H, 4-OCH3Ph-H), 7.12~7.17(m, 1H, Ph-H), 6.85(d,J=8.0 Hz, 2H, 4-OCH3Ph-H), 5.55(d,J=4.0 Hz, 1H, SCH), 5.14(t,J=4.0 Hz, 1H, NCH), 3.59~3.83(m, 6H, CH3+OCH3), 2.38(s, 3H, CH3);13C NMR(125 MHz, DMSO-d6)δ:161.91, 159.56, 159.28, 154.07, 150.24, 145.00, 142.43, 136.52, 135.58, 135.22, 134.95, 134.20, 129.88, 129.03, 128.77, 128.38, 128.17, 127.94, 127.37, 125.45, 124.37, 120.44, 115.26, 114.42, 60.56, 58.52, 55.53, 42.03, 30.55, 17.11; MSm/z: 566.1{[M+H]+}。
3-(2,4-二氯苯基)-6-(2,4-二氟苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9i): 白色晶體, 產率66%, m.p.191~193 ℃;1H NMR(DMSO-d6,400 MHz)δ: 7.93(d,J=8.0 Hz, 1H, quinazoline-H), 7.84(d,J=8.0 Hz, 1H, 2,4-2ClPh-H),7.62~7.64(m, 3H, Ph-H+NH), 7.40(t,J=8.0 Hz, 1H, quinazoline-H), 7.27~7.34(m, 2H, Ph-H), 7.04~7.12(m, 2H, Ph-H), 5.57(d,J=4.0 Hz , 1H, SCH), 5.36(t,J=4.0 Hz、8.0 Hz, 1H, NCH), 3.71(s, 2H, CH3), 2.27(s, 2H, CH3);19F NMR(DMSO-d6, 400 MHz)δ: -111.02, -109.02, -109.63, -111.18, -112.56, -113.02;13C NMR(125 MHz, DMSO-d6)δ: 161.72, 158.26, 153.19, 152.03, 149.82, 149.02, 147.04, 145.09, 144.99, 142.53, 136.91, 136.60, 135.34, 135.21, 135.06, 134.26, 134.19, 134.16, 130.09, 129.87, 128.30, 128.19, 126.93, 125.23, 124.36, 120.50, 120.24, 105.64, 30.51, 30.46, 17.05, 16.77; MSm/z: 571.1{[M+H]+}。
3-(2,4-二氯苯基)-6-(2,4,6-三氟苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9j): 白色晶體, 產率64%, m.p.182~184 ℃;1H NMR(DMSO-d6, 400 MHz)δ: 7.93(d,J=8.0 Hz, 1H, quinazoline-H), 7.84(d,J=8.0 Hz, 1H, 2,4-2ClPh-H), 7.62~7.64(m, 3H, Ph-H +NH), 7.41(t,J=8.0 Hz, 1H, quinazoline-H), 7.27~7.34(m, 1H, Ph-H), 7.04~7.12(m, 2H, Ph-H), 5.61(t,J=8.0 Hz, 1H, NCH), 5.55(d,J=4.0 Hz, 1H, SCH), 3.64(s, 3H, CH3), 2.33(s, 3H, CH3);19F NMR(DMSO-d6,400 MHz)δ: -106.50, -108.78;13C NMR(125 MHz, DMSO-d6)δ: 161.75, 152.31, 150.25, 144.77, 143.32, 136.60, 135.66, 135.40, 134.73, 134.18, 129.95, 128.78, 127.70, 125.05, 124.43, 120.47, 102.16, 101.87, 54.59, 43.46, 30.62, 16.74; MSm/z: 589.1{[M+H]+}。
3-(2,4-二氯苯基)-6-(4-氟苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9k): 白色晶體, 產率62%, m.p.189~191 ℃;1H NMR(DMSO-d6, 400 MHz)δ: 7.95(d,J=8.0 Hz, 1H, quinazoline-H), 7.86(s, 1H, 2,4-2ClPh-H), 7.63-7.67(m, 3H, Ph-H), 7.40~7.45(m, 3H, Ph-H), 7.22(d,J=8.0 Hz, 1H, quinazoline-H), 7.17(t,J=8.0 Hz, 1H, quinazoline-H), 5.58(d,J=8.0 Hz, 1H, SCH), 5.24( t,J=8.0 Hz, 4.0 Hz, 1H, NCH), 3.72(s, 3H, CH3), 2.35(s, 3H, CH3);19F NMR(DMSO-d6,400 MHz)δ: -114.06;13C NMR(125 MHz, DMSO-d6)δ: 163.29, 161.94, 160.85, 153.98, 150.16, 144.94, 142.23, 136.57, 135.58, 135.22, 134.96, 134.22, 133.56, 133.53, 129.89, 129.73, 129.66, 128.18, 127.39, 125.37, 124.37, 120.47, 116.02, 115.80, 57.99, 55.39, 41.75, 30.56, 17.10; MSm/z: 553.1{[M+H]+}。
3-(2,4-二氯苯基)-6-(2-氯-4-氟苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9l): 白色晶體, 產率61%, m.p.187~189 ℃;1H NMR(DMSO-d6, 400 MHz)δ: 7.91(d,J=8.0 Hz, 1H, quinazoline-H), 7.83(s, 1H, 2,4-2ClPh-H), 7.56~7.63(m, 4H, Ph-H+NH), 7.45(dd,J=4.0 Hz, 4.0 Hz, 1H, Ph-H), 7.40(t,J=4.0 Hz, 1H, Ph-H), 7.16~7.23(m, 2H, Ph-H), 5.74(d,J=8.0 Hz, 1H, SCH), 5.48(t,J=8.0 Hz, 1H, NCH), 3.72(s, 3H, CH3), 2.34(s, 3H, CH3);19F NMR(DMSO-d6, 400 MHz)δ: -110.23, -110.88;13C NMR(125 MHz, DMSO-d6)δ: 163.11, 161.73, 161.36, 160.63, 153.07, 153.00, 150.36, 149.21, 145.02, 144.88, 143.02, 142.68, 136.55, 136.14, 136.07, 135.56, 135.31, 135.14, 134.92, 134.87, 134.76, 134.53, 134.22, 131.60, 130.17, 130.08, 129.85, 128.05, 127.88, 127.56, 127.39, 125.32, 125.09, 124.38, 120.33, 119.89, 117.84, 117.59, 115.34, 115.13, 58.20, 57.81, 42.50, 31.00, 30.00, 17.12, 16.79; MSm/z: 587.1{[M+H]+}。
3-(2,4-二氯苯基)-6-(2,5-二氯苯基)-7-[3,8-二甲基喹唑啉-4(3H)-酮]-5H-1,2,4-三唑[3,4-b][1,3,4]噻二嗪(9m): 白色晶體, 產率61%, m.p.182~184 ℃;1H NMR(DMSO-d6,400 MHz)δ: 7.91(d,J=8.0 Hz, 1H, quinazoline-H), 7.83(d,J=2.0 Hz, 1H, Ph-H), 7.56~7.63(m, 4H, Ph-H), 7.50(d,J=8.0 Hz, 1H, Ph-H), 7.42(d,J=4.0 Hz, 1H, Ph-H), 7.40(s, 1H, Ph-H), 7.21(d,J=8.0 Hz, 1H, Ph-H), 5.68(d,J=8.0 Hz, 1H, SCH), 5.48(t,J=8.0 Hz, 1H, SCH), 3.72(s, 3H, CH3), 2.34(s, 3H, CH3).13C NMR(125 MHz, DMSO-d6)δ: 161.83, 153.38, 150.25, 144.85, 143.31, 137.14, 136.62, 135.57, 135.33, 134.86, 134.16, 132.58, 132.23, 131.99, 130.46, 129.92, 128.63, 128.10, 127.58, 125.02, 124.39, 120.35, 58.24, 42.61, 31.10, 17.13; MSm/z: 605.1{[M+H]+}。
1.3 抑菌活性測試
供試藥劑濃度為100 μg/mL和50 μg/mL。采用濁度法測試目標化合物對柑橘潰瘍病菌、煙草青枯病菌、水稻百葉枯病菌的抑制活性[13]。
2 結果與討論
2.1 反應機理
TLC跟蹤結果顯示,中間體1生成后,隨即就有中間體3出現,最終全部轉化為6。由此,分析可能的反應機理見Scheme 2:首先生成了硫醚,由于C=O的強吸電子作用,使CH2變得活潑,在KOH堿性下,CH2生成碳負離子,作為親核試劑與C=N雙鍵發生分子內親核加成反應得中間體3;在堿性條件下,受1,2,4-三唑[3,4-b][1,3,4]噻二嗪環的吸電子誘導效應影響,酰胺鍵烯醇化,然后發生分子內閉環脫去H2O后生成喹唑啉酮。
2.2 表征
以化合物9c(Chart 1)的為例,分析了1H NMR數據。δ7.93處特征峰為1-H的吸收峰,受2-H耦合作用影響,裂分為雙重峰。δ7.64處特征峰為3-H的吸收峰,受2-H耦合作用影響,裂分為雙重峰。δ7.42處特征峰為2-H的吸收峰,1-H和3-H耦合作用影響,裂分為三重峰。δ7.85處特征峰為8-H的吸收峰,受9-H耦合作用影響,裂分為兩重峰。δ7.63處特征峰為9-H的吸收峰,受8-H耦合作用影響,裂分為雙重峰。δ7.66處特征峰為10-H的吸收峰,為單峰。δ6.69處特征峰為4-H和5-H的吸收峰,化學環境相同,為單峰。δ 7.12處特征峰為N—H的吸收峰,受6-H耦合作用影響,裂分為兩重峰。δ6.69處特征吸收峰為S—C—H吸收峰,受6-H耦合作用的影響,裂分為兩重峰。δ5.10處特征吸收峰為6-H吸收峰,受7-H耦合作用的影響,裂分為三重峰。

表1 9a~9m對植物病菌的抑制率*
*A: 100 μg/mL, B: 50μg/mL。

Chart 1
2.2 抑菌活性
表1為目標化合物對水稻白葉枯病菌(Xoo)、柑橘潰瘍病菌(Xac)和煙草青枯病菌(Rs)的抑制活性。從表1可以看出,目標化合物對植物病菌的抑制作用與取代基性質有關。化合物9d、9i、9j、9k、9l的結構中含有氟原子,活性相對較高,可能是氟原子的電子效應,使目標化合物分子的電荷分布產生變化,提高了電子云密度,進而增強了此類化合物在細菌體中的吸收、傳遞速度和穿透力。當R為羥基取代時,化合物活性相對較好,原因可能是羥基的引入提高了化合物的溶解性,使目標化合物更容易與受體結合。當濃度為100 μg/mL時,化合物9d、9i、9j對柑橘潰瘍病菌的抑制率分別為63.5%、 65.2%、 58.3%,與對照藥劑噻菌酮(57.2%)和葉枯唑(65.3%)相當。當濃度為50 μg/mL時,化合物9j對柑橘潰瘍病菌的抑制率為56.4 %,與對照藥劑葉枯唑(54.9%)相當。當濃度為100 μg/mL時,化合物9i、9j對水稻百葉枯病菌的抑制率分別為65.3%和62.3%,和對照藥劑噻菌酮(50.2%)、葉枯唑(64.9%)相當。當濃度為50 μg/mL時,化合物9j對水稻百葉枯病菌的抑制率為48.5%,和對照藥劑噻菌酮(37.2%)和葉枯唑(45.2%)相當。
合成了13個新型的含2,4-二氯苯基的1,2,4-三唑1,3,4-噻二嗪喹唑啉酮化合物(9a~9m),并采用濁度法測試了生物活性。結果表明,化合物9k和9j對柑橘潰瘍病菌和水稻百葉枯病菌的抑制率和對照藥劑相當,具備進一步開發的價值。

