褚橙精油納米乳的制備及抑菌性
劉如楠, 黃 凱, 管 驍*, 李 森, 劉 靜, 宋洪東
(1.上海理工大學 醫療器械與食品學院,上海200093;2.上海海事大學 信息工程學院,上海200135)
褚橙是云南著名特產,以味甜皮薄而著稱,含有大量維生素C,營養價值較高。柑橘類精油是最重要的柑橘類副產品,主要從果皮中提取,具有特殊芳香和抗菌、抗炎、抗氧化等性能[1-2],因此被廣泛應用于食品和化妝品行業中[3-4]。隨著人們健康意識的提高,消費者對天然食品添加劑的需求不斷增長,而褚橙精油因其天然性而備受青睞。但褚橙精油通常具有柑橘類精油的穩定性差、易揮發、水溶性差等通病,因此該精油的應用受到很大程度的限制[1,5]。
水包油(O/W)納米乳被廣泛報道可用于解決精油溶解度的問題[6]。納米乳液是液滴尺寸在20~300 nm之間的乳液[7]。納米乳是熱力學不穩定,但動力學穩定的系統[8]。這種體系由于表面活性劑或其他乳化劑的存在而使油水界面張力降低,從而使乳液穩定。通過將精油乳化,親脂性成分可以快速分散到水基食品系統中。此外,由于優異的分散性、穩定性以及滲透能力,納米乳的活性可以得到改善[1]。
本研究的目的是分析褚橙植物精油的化學成分,制備褚橙精油納米乳液并提升其穩定性,以及比較乳液與純精油的抗菌活性差異。結果顯示,以Tween 80和Span 80復配質量比為1∶2作為表面活性劑制備的褚橙精油乳液穩定性、分散性良好,并且抗菌性顯著高于褚橙精油,從而解決了褚橙精油在生產加工中水溶性差的問題,并且為褚橙精油在工業中作為添加劑、防腐劑等奠定了基礎。
1 材料與方法
1.1 材料與試劑
褚橙:購于超市;Tween 80、Span 80、二甲基亞楓:國藥控股化學試劑有限公司產品;大腸桿菌(Escherichia coli)、變形桿菌(Proteus vulgaris)、枯草芽孢桿菌(Bacillus subtilis):所有供試細菌均來源于上海理工大學微生物實驗室;牛肉膏蛋白胨培養基:牛肉浸膏3 g/L,蛋白胨10g/L,氯化鈉5 g/L,蒸餾水 1 000 mL;pH 7.2~7.4。
1.2 儀器與設備
Milli-Q超純水設備:美國密理博公司產品;流變儀:美國TA公司產品;Agilent 7890A GC-5975c氣相色譜質譜聯用儀:Agilent公司產品;HPINNOWAX 毛細管柱 (30 m×0.25 mm×0.25 μm):Agilent公司產品;多角度激光散射粒度分析儀:美國布魯克海文儀器公司產品;馬爾文激光粒度儀:英國馬爾文儀器有限公司產品;多重光散射儀Turbiscan MA 2000:法國Formulaction公司產品;高速剪切機(ULTRA-TURRAX T18):德國IKA公司產品;透射電子顯微鏡(JEM-2100F):日本電子株式會社(JEOL)產品;立式高壓蒸汽滅菌器:上海申安醫療器械廠制造。
1.3 實驗方法
1.3.1 褚橙精油的制備 稱取一定量的褚橙皮,適當剪碎,置于Clevenger型裝置中,在100℃下蒸餾來獲得精油。將得到的精油與水分離,用無水Na2SO4干燥,并在4℃下儲存。
1.3.2 氣相色譜-質譜分析 通過GC-MS分析鑒定褚橙精油的成分[9]。色譜條件:色譜柱型號為HPINNOWAX 毛細管柱 (30 m×0.25 mm×0.25 μm);升溫程序設定為:40℃開始并保持5 min,然后以8℃/min的速度升至250℃,并保持5 min,分離比為5∶1。載氣為氦氣,流速設定為1 mL/min。質譜條件:EI電離源為70 eV,離子源溫度設定為230℃,四極溫度為150℃,界面溫度為250℃。掃描范圍m/z為 30~400。
1.3.3 乳液制備 將Tween 80和Span 80以一定比例混合,然后以不同的質量濃度分別添加到2.5 g褚橙精油中。在25℃下以1 000 r/min的恒定速度磁力攪拌30 min來制備油相。將充分混合的油相滴定至攪拌的水相(去離子水)中。乳液的總質量保持恒定在50 g。滴定后,通過高速剪切機12 000 r/min剪切20 min制備褚橙精油納米乳。
1.4 乳液測量
1.4.1 粒度分布 使用多角度激光散射粒度分析儀測定乳液粒徑分布,設定溫度25℃、散射角90°、樣品平衡時間5 min、檢測時間為5 min。在分析之前,將每種乳液樣品稀釋100倍。
1.4.2 ζ-電位的測定 通過使用馬爾文激光粒度儀測定乳液的ζ-電位大小,測定溫度為25℃,等待時間為120 s,平衡時間設置為180 s。每個樣品至少測試了3遍,在分析之前,將每種乳液樣品稀釋100倍。
1.4.3 流變黏度 通過使用配備有同心圓筒夾具的剪切流變儀來測量具有不同表面活性劑濃度的褚橙精油納米乳液的黏度。測量溫度25℃,測定剪切速率從0.01~200 s-1遞增,通過隨附的軟件記錄每個剪切速率下的剪切黏度。
1.4.4 乳液的微觀結構 用磷酸鹽緩沖液稀釋適量的納米乳樣品,然后滴到覆蓋有碳膜的銅網中。負染色用質量分數為2.0%的磷鎢酸進行40 s,使用JEM-2100F透射電子顯微鏡觀察褚橙精油納米乳的形貌。
1.4.5 乳液的背向散射(BS)曲線和Turbiscan穩定性指數(TSI) 使用Turbiscan MA 2000儀器,獲得了乳液在24 h內的背散射光變化(BS)曲線。測量時,將褚橙精油納米乳液樣品置于20 mL樣品池中,測量探頭從樣品池的底部到樣品池的頂部每40 μm測量一次,在測試期間乳液保持穩定。此外,還獲得了Turbiscan穩定性指數(TSI)以評估乳液的穩定性。
1.5 褚橙精油及乳液的抗菌活性
使用濾紙片法測定褚橙精油和乳液對3種供試細菌抑菌活性。純精油用1%二甲基亞砜(DMSO)稀釋到與乳液含油量相同,將供試細菌在營養瓊脂上于37℃生長18~24 h。挑取一環接種到滅菌的培養基中,制備細菌懸浮液,將100 μL的試樣涂布在營養瓊脂固體培養基上。將培養基分為3個區域,在各個區域中間放置準備好的6 mm的濾紙片,移液槍分別吸取10 μL稀釋的純精油,褚橙精油納米乳液及1%的DMSO(對照)滴至濾紙片中間,迅速蓋上培養皿蓋。并將平板在37℃下培養24 h。平行3次,計算并比較精油和乳液抑制區直徑。
1.6 統計分析
所有實驗和測量均為3份,并將結果記錄為平均值和標準偏差。使用SPSS Statistics Software(IBM)對數據進行ANOVA差異顯著性分析,p<0.05為顯著性差異。
2 結果與分析
2.1 褚橙精油納米乳的制備
2.1.1 不同表面活性劑的復配比對褚橙精油納米乳粒徑分布和ζ-電位值的影響 選用Tween 80與Span 80作為本實驗的表面活性劑,將 Tween 80與Span 80 按照 1∶0、4∶1、2∶1、1∶1、1∶2、1∶4、0∶1 的質量比分別混合均勻,將不同比例的混合表面活性劑加入到2.5 g褚橙精油中并在磁力攪拌器上充分攪拌,混合均勻后,以1 mL/min的速度加入到水相。體系總質量為50 g。用高速剪切機剪切20 min,得到均勻的納米乳液,測定粒徑和ζ-電位大小。ζ-電位的大小提供了乳液體系潛在穩定性的指標[10],絕對值較高的ζ-電位顆粒之間相互排斥。ζ-電位顯示出物理穩定性,ζ-電位的絕對值越大,乳液越穩定。
由圖 1(a)可知,隨著 Span 80比例的增大,納米乳的粒徑先減小后增大,當Tween 80∶Span 80從1∶0到 2∶1,粒徑分布均呈現雙峰,但平均有效粒徑呈逐漸減小的趨勢,當Tween 80∶Span 80從1∶1到0∶1有效粒徑逐漸增大。Tween 80與Span 80質量比為2∶1時,達到最小粒徑 70 nm。Tween 80∶Span 80為1∶2時,粒徑分布最窄且呈現單峰分布。從圖1(b) 可以看出,Tween 80 與 Span 80 的從 1∶0 到 1∶2時,ζ-電位的絕對值顯著增加(p<0.05),即穩定性顯著增加。但當 Tween 80∶Span 80為 1∶2時再增加Span 80的量,ζ-電位的絕對值變化不顯著 (p>0.05)。由于粒徑分布圖在復配比為1∶2時為單峰分布,同時具有較高的ζ-電位絕對值。在隨后的實驗中選擇Tween 80∶Span 80復配比1∶2制備乳液。
2.1.2 不同質量濃度表面活性劑對褚橙精油納米乳粒徑分布、ζ-電位值及流變黏度的影響 乳液的性質與其表面活性劑的質量濃度密不可分,因此研究了表面活性劑質量濃度對褚橙精油納米乳液性能的影響。將Tween 80與Span 80按照復配比1∶2的比例混合均勻, 再按照質量濃度 1、2、3、4、5 g/dL分別加入到2.5 g褚橙精油混合均勻,以1 mL/min的速度加入到水相,使乳液的總質量為50 g。用高速剪切機剪切20 min測定乳液的粒徑分布、ζ-電位以及黏度。

圖1 不同表面活性劑復配比對褚橙油乳液粒徑分布和ζ-電位值的影響Fig.1 Effect of different ratios of surfactants on particle size distribution and zeta potential of Chu orange essential oil emulsion
如圖2(a)所示,表面活性劑質量較低的褚橙精油納米乳含有較大的粒徑,在較低的表面活性劑質量濃度下,其粒徑分布呈雙峰分布。這是由于當表面活性劑的用量較低時,表面活性劑不足以覆蓋新油滴的表面,導致油滴相互碰撞和堆積而形成較大的液滴[7]。當表面活性劑質量濃度超過3 g/dL時,乳液液滴直徑變化很小且分布變得不均。這是由于非離子表面活性劑穩定小液滴曲率的能力有限,在表面活性劑分子過量的情況下,限制了乳液液滴粒徑的進一步減小[11]。
從圖2(b)中ζ-電位圖可以看出,隨著表面活性劑質量濃度從1 g/dL增加到3 g/dL,乳液的ζ-電位絕對值顯著增加(p<0.05),褚橙精油納米乳ζ-電位絕對值的增加為乳液液滴之間提供了高能量屏障,從而具有了良好的靜電排斥[12]。但表面活性劑質量濃度從3 g/dL增加到5 g/dL,ζ-電位絕對值的變化不顯著(p>0.05),這與乳液粒徑的變化趨勢是一致的。因此,當表面活性劑質量濃度為3 g/dL時,褚橙精油納米乳的粒徑分布和ζ-電位基本保持不變。所以,質量濃度為3 g/dL的表面活性劑可以形成比較穩定的褚橙精油納米乳液,此質量濃度最適合褚橙精油納米乳的制備。
流變黏度影響乳液加工的適用性,直接關系到流體的穩定性[13]。因此研究表面活性劑質量濃度與褚橙精油乳液流變黏度之間的關系很有必要。如圖3所示,隨著表面活性劑的量的增加,乳液流變黏度增加,褚橙精油納米乳的黏度范圍在1.08~1.65 mPa·s,隨著表面活性劑質量濃度的增加,乳液的黏度有所增加,表面活性劑的質量濃度從4 g/dL增加到5 g/dL時,可以看到黏度發生更大的增量,這是由于過量的表面活性劑遷移到水相中,導致褚橙精油納米乳液的表觀黏度急劇增加。
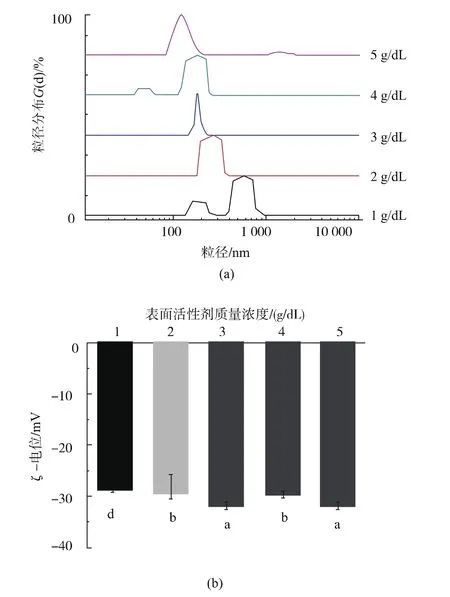
圖2 表面活性劑質量濃度對褚橙精油乳液粒徑和電位的影響Fig.2 Effect of surfactant concentration on the particle size and zeta potential of the Chu orange essential oil emulsion
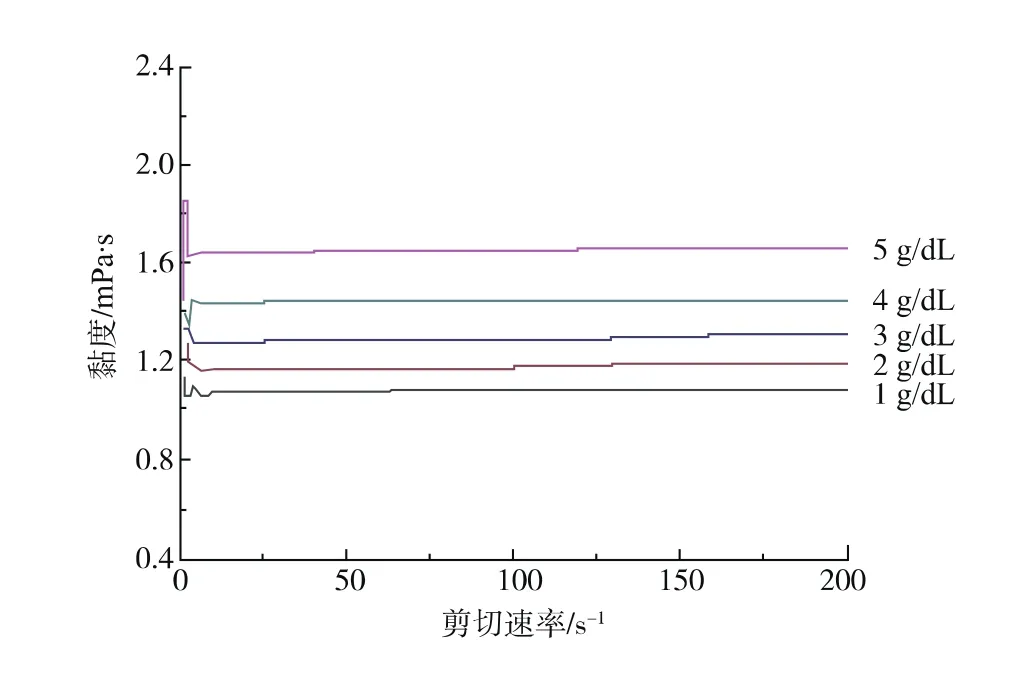
圖3 表面活性劑質量濃度對褚橙精油乳液流變黏度的影響Fig.3 Effect of surfactant concentration on rheological viscosity of Chu orange essential oil emulsion
2.1.3 不同剪切速度對褚橙精油納米乳粒徑分布、ζ-電位值及離心穩定性的影響 將質量濃度為3 g/dL的復合表面活性劑(Tween 80∶Span 80 為 1∶2)加入到2.5 g油相混合均勻,將混合物加入到一定量的去離子水中,使體系總質量為 50 g。分別以3 000、6 000、9 000、12 000、15 000 r/min 在高速剪切機上剪切20 min,測定粒徑、ζ-電位及離心穩定性。由圖4(a)可知,隨著剪切速度的增加,納米乳粒徑逐漸減小,當剪切速度達到12 000 r/min時,納米乳粒徑分布變為單峰分布,此時,再增大剪切速率,乳液粒徑變化很小,且乳液粒徑變為雙峰分布。這可能是由于剪切速率過大,使得乳液液滴過小,顆粒之間布朗運動加快、相互碰撞次數增多而發生液滴聚集現象。這說明并非剪切速率越大,乳液的分散性越好。從圖4(b)可以看出,剪切速率從3 000 r/min增加到12 000 r/min時,ζ-電位絕對值顯著增大 (p<0.05),在15 000 r/min時ζ-電位絕對值反而減小。即褚橙精油納米乳液在剪切速率為12 000 r/min時,納米乳液達到最穩定的狀態。

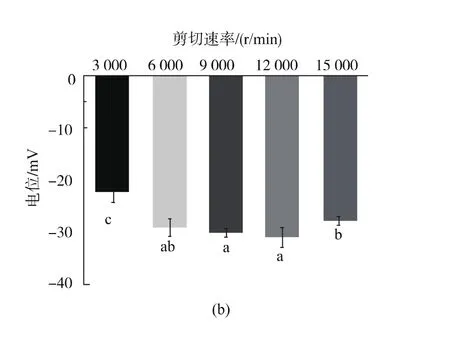
圖4 剪切速率對褚橙精油乳液粒徑和ζ-電位的影響Fig.4 Effect of shear rate on particle size and zeta potential of Chu orang essential oil emulsion
另外,將乳液在4 000 r/min室溫條件下離心30 min,結果見圖 5。 剪切速率為 3 000、6 000、9 000 r/min制備的乳液均有不同程度的明顯分層,隨著剪切速率的增大,分層高度降低,說明剪切速率對納米乳液的穩定性的影響很大。當剪切速率達到12 000 r/min時,乳液未發生分層現象,所以最佳剪切速率選擇12 000 r/min。

圖5 不同剪切速率乳液的離心穩定性Fig.5 Centrifugal stability of emulsions at different shear rates
綜上所述,制備最穩定的褚橙精油納米乳液的優化條件為:表面活性劑選擇Tween 80∶Span 80質量比1∶2、其質量濃度為3 g/dL、剪切速率為12 000 r/min,所得乳液的粒徑為(135±0.76) nm,ζ-電位值為(-30±0.36)mV。
2.2 褚橙精油納米乳的質量評價

圖6 褚橙精油納米乳的微觀形態Fig.6 Microscopic morphology of Chu orange essential oil nanoemulsion
2.2.1 褚橙精油納米乳的微觀形態 通過透射電子顯微鏡(TEM)觀察納米乳形態,結果見圖6。發現褚橙精油納米乳液滴分布均勻,呈圓球形,表明褚橙精油納米乳分散較好。經測量納米乳平均粒徑為96 nm,比動態光散射法測得的稍小一些,由于動態光散射測得的是水合半徑,此結果符合實際規律。
2.2.2 褚橙精油不穩定性分析 限制乳液應用的很大一個原因是乳液在儲存期間不能保持穩定。通常,乳液去穩定化是由3種物理過程引起,即聚結、絮凝或奧斯特瓦爾德熟化和粒子重力遷移[14]。為了探究褚橙精油乳液的不穩定機制,并驗證Tween 80和Span 80復配質量比為1∶2作為復合表面活性劑是否適合于形成褚橙精油納米乳的小粒徑和單峰分布的優質乳液,分別以Tween 80、Tween 80和Span 80復配質量比為1∶2,Span 80為表面活性劑制備了3種乳液,用Turbiscan得到了24 h之內3種乳液的TSI指數和BS的變化,比較3種不同的表面活性劑的穩定性行為,以分析乳液的不穩定性。
3種乳液的常溫下的整體的TSI見圖7。TSI值越大,穩定性越低。可以看到,僅以單一表面活性劑作為乳化劑所制備的乳液的穩定性要低于復配的表面活性劑所制備的乳液。
從圖8可以看出,由于BS強度是位于管的特定高度和粒徑的分散相體積的函數[14],如果粒徑大于入射波長,則BS強度隨粒徑的增加或粒子濃度的下降而降低;反之,BS隨著粒子尺寸的增大而增大。底層中BS的下降表示底部濃度下降代表底部澄清的過程,而頂層中BS的增加則反應顆粒濃度的增加[15]。
從圖8可知,僅以單一表面活性劑Tween 80或者Span 80(即圖8(a)和8(c))為乳化劑的乳液在24 h內BS變化較大。圖8(a)和8(c)的底部BS變化和頂部BS變化均較強烈,這表明乳液底部澄清,乳液發生了嚴重的重力遷移,并且頂部BS增加,即乳液頂層發生油滴上浮現象。此外,以Tween 80為表面活性劑的乳液(圖8(a))的管中間部分BS水平降低,表明由于絮凝或聚結過程導致液滴尺寸增加。而Tween 80 和 Span 80 復配質量比為 1∶2(圖 8(b)),變化最小,底部的BS沒有明顯變化,頂部的BS變化比底部略大。說明樣品的不穩定性主要是由于樣品頂部油滴發生上浮,中間部分BS水平幾乎未發生變化。這些結果表明,褚橙精油乳液的不穩定性是由嚴重的重力分離引起的,其在底部產生澄清,在頂部產生奶油層,且以復配表面活性劑為乳化劑的乳液比以單一表面活性劑制備的乳液穩定性好。

圖7 不同表面活性劑制備的乳液在24 h內TSI指數變化Fig.7 TSI index of emulsions prepared with different surfactants within 24 h
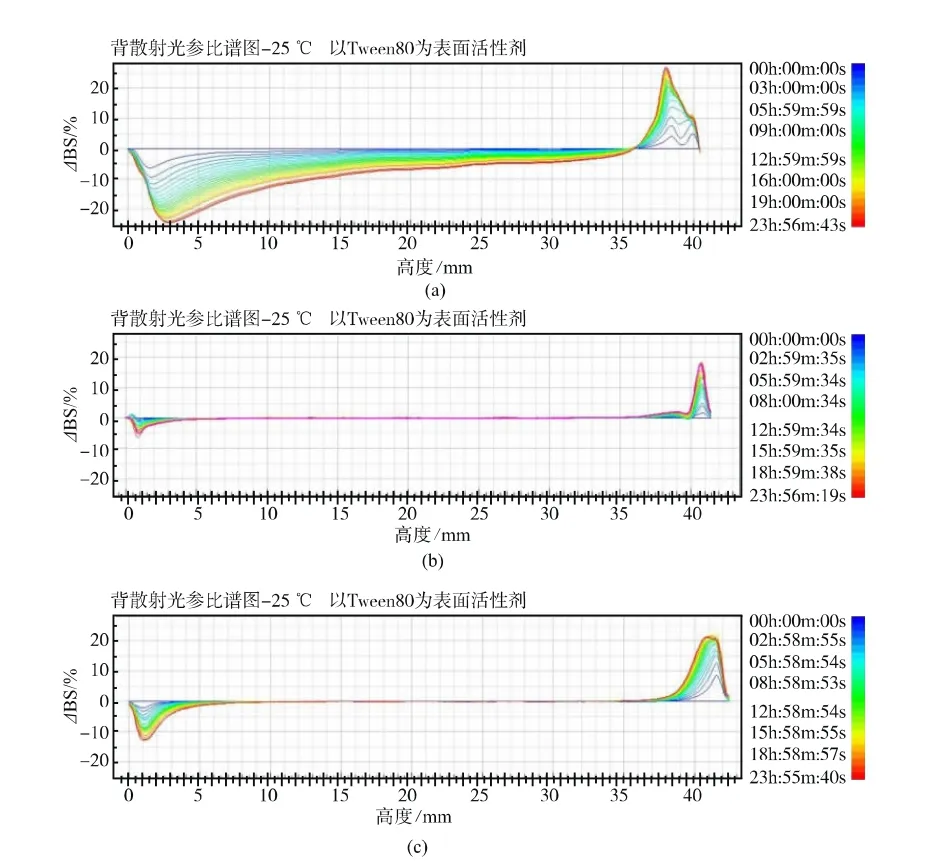
圖8 不同表面活性劑制備的乳液在24 h內的BS變化Fig.8 BS changes in emulsions prepared with different surfactants within 24 h
2.3 褚橙精油抑菌性
2.3.1 GC-MC 通過GC-MS對褚橙精油的成分進行分析,鑒定了精油中的36種化合物,占出峰物質總數的95.41%。定量和定性分析結果見表1。精油的主要化合物是 D-檸檬烯 (52.96%)、β-蒎烯(11.85%)、α-蒎烯(9.19%)和順式-(S)-(-)-檸檬烯氧化物(6.99%)。據報道,D-檸檬烯具有殺菌、抗氧化劑、化學預防和治療活性[16],除此之外,α-蒎烯、β-蒎烯、檸檬烯氧化物等倍半萜烯也具有相似的生物活性,這可能是褚橙精油具有抑菌性的主要原因[17]。
2.3.2 褚橙精油及納米乳的抑菌性 大腸桿菌屬于革蘭氏陰性菌,在一定條件下可以引起人和多種動物發生胃腸道感染或尿道等多種局部組織器官感染。變形桿菌也屬于革蘭氏陰性細菌,通常在食物中繁殖并產生可引起人中毒的毒素,而枯草芽孢桿菌在自然界廣泛存在,屬于革蘭氏陽性細菌。作者研究了精油及乳液對這3種細菌的抗菌性能。

表1 褚橙精油的化學成分分析Table 1 Chemical composition of orange essential oil
如表2所示,褚橙精油納米乳液對大腸桿菌、變形桿菌和枯草芽孢桿菌的抑菌效果比純精油好。這些結果與最近的其他研究一致,這些研究表明,精油轉化為納米乳液可以提高其抗菌活性[1,18]。造成這種現象的原因可能是乳液中的小脂質顆粒能夠將精油帶到細胞膜表面,而純精油由于水溶性低而無法輕易與細胞膜相互作用[18]。
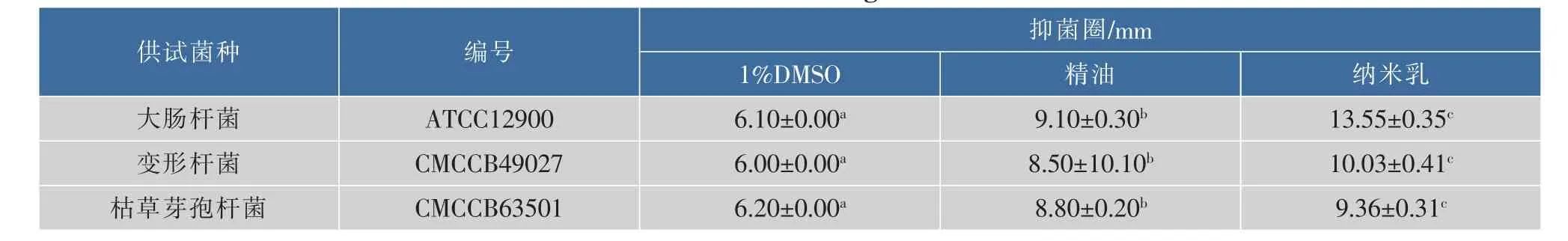
表2 褚橙精油及其納米乳的抑菌效果Table 2 Antibacterial activities of orange oil and its nanoemulsion
3 結 語
本研究對褚橙精油納米乳制備過程中的表面活性劑復配比、濃度以及乳化剪切速率進行了優化,以制備高質量的納米乳液。結果顯示,以Tween 80∶Span 80 質量比 1∶2、質量濃度為 3 g/dL、剪切速率為12 000 r/min時,褚橙精油納米乳液表現出了最小粒徑和最大的穩定性。單一表面活性劑和復配表面活性劑為乳化劑的乳液在24 h內表現出不同程度的不穩定性,褚橙精油納米乳液的不穩定性主要是由嚴重的重力分離引起的,以復合表面活性劑為乳化劑制備的乳液穩定性最好。此外,相比較于純精油,褚橙精油納米乳液表現出更明顯的抑菌效果。該研究為今后褚橙精油在食品或其他領域中的應用提供了依據和參考。

