微生物法制備松仁肽-鋅螯合物及其抗氧化功能的研究
孫家佳 張 智 楊可心 魏 罡 宋希明
(東北林業大學林學院1,哈爾濱 150040) (烏蘭察布市林業和草原局2,烏蘭察布 012000)
我國使用松子已有三千多年的歷史,宋代人們把松子視為延年益壽的“長生果”。由于松仁是美味食物,又是食療佳品,備受歷代醫學家、營養學家推崇。松仁中含有豐富的蛋白質、氨基酸、不飽和脂肪酸、維生素和礦物質等,尤其是人體所必需氨基酸含量較普通植物的高[1]。張智等[2]對于松仁蛋白的利用提出了微生物發酵生產松仁肽,改善了松仁肽的口味[3]的同時達到了蛋白吸收的營養預期。松仁肽具有良好的功能性及生物活性[4, 5],對人體代謝和生理調節功能,如促進免疫、降血壓血脂、抗氧化[6]等作用,是當前國際藥學和食品界熱門的物質和極具發展前景的功能性因子[7]。
鋅存在于眾多的酶系中,如碳酸酐酶、呼吸酶、乳酸脫氫酶、超氧化物歧化酶、堿性磷酸酶、DNA和RNA聚合酶等中,是核酸、蛋白質、碳水化合物的合成和維生素A利用的必需物質。具有促進生長發育,改善味覺的作用。鋅是人體必不可少的微量元素之一[8],在人體生長發育[9]、生殖遺傳等起到至關重要的作用[10]。
多肽-鋅螯合物既具有補鋅作用[10, 11],同時也具有一些特殊的生物活性[12]。張亞麗[13]利用中性蛋白酶水解脫脂豆粕后形成的多肽與微量元素鋅制備多肽螯合鋅,添加多肽螯合鋅的豬油和魚油的過氧化值均低于對照組,說明其是具有抗氧化作用的;將多肽-鋅螯合物喂食小鼠,發現多肽-鋅螯合物具有一定的生物吸收利用率,可以作為食品鋅強化劑。近年來,對活性肽的研究尤為突出,并以其為原料,開發易于身體吸收利用[14]、生理活性強的新型補鋅劑,已成為熱點研究問題[15]。基于螯合物的利用價值較高,并且現有研究僅僅局限化學方法進行螯合,本文主要介紹微生物法螯合,微生物通過自身的生理功能分解蛋白的同時與鋅離子結合,形成螯合物,并對該方法及其抗氧化活性進行研究。
1 實驗材料
1.1 主要原料與試劑
松仁粕,市售;蛋白胨、酵母膏、葡萄糖、1,1-二苯基-2-三硝基苯肼(DPPH)、鐵氰化鉀、三氯乙酸、Fe Cl3、H2O2、水楊酸、Fe SO4、98%硫酸等藥品均為國產分析純級。松仁肽(微生物法制備)。
1.2 儀器與設備
756PC紫外分光光度計;HPG-310培養箱;SW-CJ-IFD超凈臺;離心機LD4-2A等。
1.3 菌種
枯草芽孢桿菌(Bacillussubtilis)ls-45,來源于東北林業大學發酵實驗室。
1.4 培養基
斜面培養基:葡萄糖20 g、牛肉膏1 g、蛋白胨5 g、氯化鈉5 g、瓊脂粉20 g,加熱溶解于1 L水中;種子培養基: 葡萄糖20 g、牛肉膏1 g、蛋白胨5 g、氯化鈉5 g,溶于1 L的水中;發酵培養基:一定量的松仁粉和硫酸鋅溶于水中。
2 實驗方法
松仁粕預處理→發酵加鋅培養基配置→滅菌→接種→發酵→離心→取上層清液→透析→濃縮→冷凍干燥→粗制松仁肽-鋅螯合物
微生物法松仁多肽制備的工藝流程:松仁粕預處理→發酵培養基配置→滅菌→接種→發酵→離心→取上層清液→濃縮→冷凍干燥→粗制松仁肽
2.1 微生物螯合的單因素實驗
2.1.1 螯合單因素實驗設計
固定發酵培養基中松仁粕的量為12%,以螯合率為指標,微生物螯合當中硫酸鋅的添加量、螯合溫度、螯合時間和pH等4個因素5個水平來對微生物法螯合松仁肽與鋅的工藝進行優化。
2.1.2 微生物法螯合條件單因素實驗
生物螯合硫酸鋅添加量的影響:硫酸鋅的添加量為0.1、0.2、0.4、0.6、0.8 g等5個因素水平,微生物螯合時間為50 h溫度為35 ℃,以螯合率作為評價指標,得到最佳添加量。
微生物螯合pH的影響:運用上述實驗得出最佳結果進行下一步,pH設計的值為5、6、7、8、9等5個因素水平,以螯合時間為50 h溫度為35 ℃,螯合率為指標,尋找出最優的pH值進行螯合。
微生物螯合時間的影響:在以上實驗的結果下,設計的時間為20、30、40、50、60 h等。硫酸鋅添加量和pH值采用實驗最佳結果,溫度為35 ℃的條件下進行微生物螯合。指標為螯合率。
微生物螯合溫度的影響:在以上三個因素最優的條件下,溫度設計為33、35、37、39、41 ℃等5個因素水平。以螯合率為評價指標,得出最佳溫度。
2.2 響應面優化實驗
按照中心組合實驗設計原理,以微生物螯合的硫酸鋅添加量、pH、時間、溫度等4個因素為自變量,每個因素3個水平,并以螯合率作為響應值,設計響應面實驗,見表1。實驗重復3次,每次3個平行。

表1 因素水平編碼表
2.3 測定的方法
2.3.1 發酵液中肽含量的測定
對于肽的計算,本實驗以氮的質量來計算。
氨基態氮的測定采用甲醛快速滴定法,氨基態的氮記作A1。
蛋白分解的可溶性氮(TCA)采用國標方法中的凱氏定氮測定法(GB/T 5009.5—1985),測之前用三氯乙酸處理,測得的氮記作Nt。
N(肽的質量以氮計)=Nt-A1
式中:Nt為發酵液中的可溶性氮(TCA)/g;
A1為發酵液中的氨基態的氮/g。
2.3.2 螯合率的測定
吸取處理后的發酵液5 mL裝入透析袋中,以去離子水作為透析液,透析10 h后測透析液中未被螯合上的鋅離子。鋅離子的測定采用國標食品中鋅的測定方法中的二硫腙比色法(GB 5009.14—2017),按標準繪制鋅離子的標準曲線。此法測得的鋅離子量記作M0;加入到發酵培養基的鋅離子的量記作M1。

式中:M0為未被螯合上的鋅離子的質量/μg;M1為加入螯合培養基中鋅離子的質量/mg。
2.3.3 DPPH自由基清除率的測定
取DPPH 3.5 mg,用無水乙醇溶解,轉入10 mL容量瓶,用無水乙醇定容至刻度。取2 mL至100 mL的容量瓶中,搖勻得濃度為0.017 8 mmol/L DPPH儲備液備用。用乙醇將松仁肽-鋅的螯合物稀釋一定濃度,待測。在10 mL比色管中一次加入4 mL DPPH和螯合物的稀釋液,加入乙醇至刻度,混均勻立即在517 nm的波長下測吸光值[16]記為Ai。將待測液在室溫避光的條件下保存30 min后測吸光值。記為Aj。對照試驗為只加DPPH的乙醇溶液,測吸光值為Ac,按下式計算自由基清除率(K)[17]。
2.3.4 還原力的測定
取1 mL三種不同質量濃度的3種待測樣品溶液,分別與 pH為6.6,濃度為0.2 mol/L,2.5 mL的磷酸鈉緩沖液和2.5 mL的鐵氰化鉀混合,在50 ℃,保溫30 min,后迅速冷卻,再加入2.5 mL三氯乙酸后離心3 000 r/min,10 min后取2.5 mL的上清液,加入2.5 mL蒸餾水和0.5 mL氯化鐵溶液,混合均勻[18]。反應10 min,后在700 nm波長下測吸光度,比較3種被測樣品的還原能力,吸光度越大說明還原能力越強[19]。
2.3.5 羥自由基的測定
H2O2與亞鐵離子生成·OH,·OH自由基具有較高的反應活性,因為存活時間較短,加入水楊酸,會與·OH 自由基反應生產紫色絡合物,該有色絡合物在510 nm出有較大的吸收波長,吸光度與·OH 自由基的量成正比[20, 21]。反應體系中含有9 mmol/L乙醇-水楊酸溶液,9 mmol/L硫酸亞,8.8 mmol/L H2O2。比色管中依次加入硫酸亞鐵,水楊酸、去離子水,最后加入H2O2,搖勻,在37 ℃條件下反應30 min,以蒸餾水歸零,在510 nm的波長下測吸光度[22, 23]。
式中:A0空白對照組的吸光度;AX加入樣品后的吸光度;AX0不加顯色劑H2O2樣品溶液本底的吸光度。
3 結果與分析
3.1 微生物螯合的單因素實驗結果
通過實驗得到的數據表明硫酸鋅的添加量對螯合率的影響較大,由圖1可知,當硫酸鋅的添加量為0.6 g時的螯合率最高,這時的螯合物的結合狀態最好,產生的螯合物量較多,綜合的來看,發酵法螯合的硫酸鋅添量為0.6 g最為合適;在pH為7 的條件下螯合率最高,在微生物學當中pH 對微生物來說具有較大的影響,在適宜的pH值下微生物能夠很好地生長,通過微生物生理活性的作用下更能促進蛋白分解為小分子肽,并使多肽與鋅離子更好的結合。所以綜合分析,在微生物法螯合時應選擇pH 7的條件;運用微生物法螯合,要選擇合適的時間,使微生物處于最佳的菌齡,才能更好的發揮微生物的作用,在50 h時螯合率最高,想得到最佳的發酵工藝,使螯合率和螯合物的活性最強,所以選擇發酵螯合時間為50 h;溫度對于微生物的生長和鋅離子的螯合是有著重要的影響,所以對于溫度進行單因素實驗,實驗結果表明,隨著溫度的增加螯合率是呈先增長后下降的趨勢,隨著溫度的增加將會影響微生物的一些生理活性,從而導致微生物的作用減少,影響了螯合率以及螯合物的生物活性,所以綜合分析在運用微生物法螯合時溫度應選擇最為適宜的,該實驗則選擇溫度為37 ℃。

圖1 不同因素對螯合率的影響
3.2 螯合條件響應面優化實驗
在單因素的實驗基礎上,根據表1,采用Box-Behnken設計方法,來對松仁肽與鋅螯合工藝進行優化,響應面方案及結果見表2。
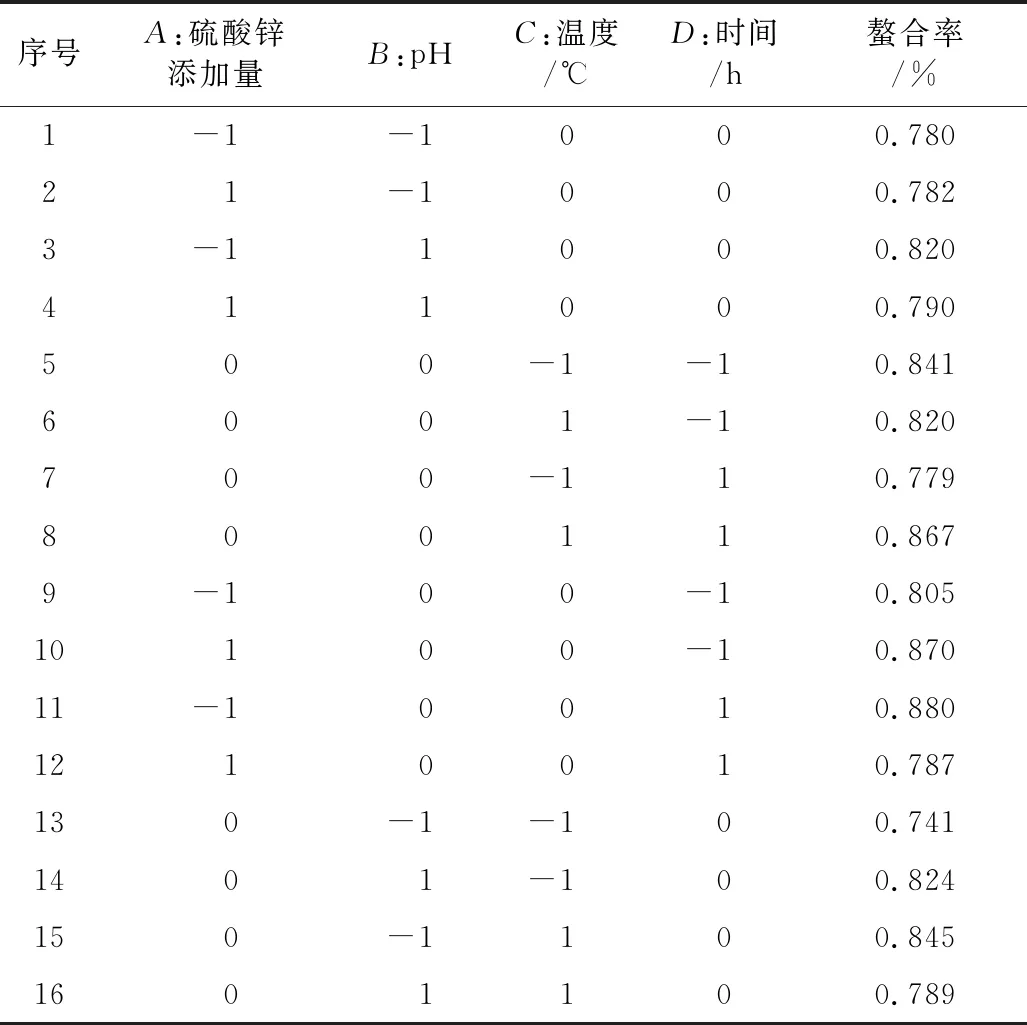
表2 Box-Behnken實驗設計及數據分析

續表2
3.2.1 螯合率分析結果
采用 Design-Expert.8.0.6對實驗數據進行擬合,以螯合率為指標,得到回歸方程如下:Y1=0.938 2-0.006 4A+0.011B+0.019C-0.002 6D-0.038AC-0.039AD-0.035BC-0.022BD+0.027CD-0.071A2-0.068B2-0.072C2-0.033D2
由表3可知,模型中P<0.000 1,R2=0.982 1,表明此模型極其顯著。失擬項P=0.845 8>0.05,影響不顯著,說明結果可靠。由回歸方程的顯著性檢驗可知,模型中C、AC、BC、CD、B2、C2對螯合率的影響極顯著,B、AD、BD對螯合率的影響顯著,其他因子影響不顯著。各因素對螯合率影響的大小依次為:C>B>A>D。
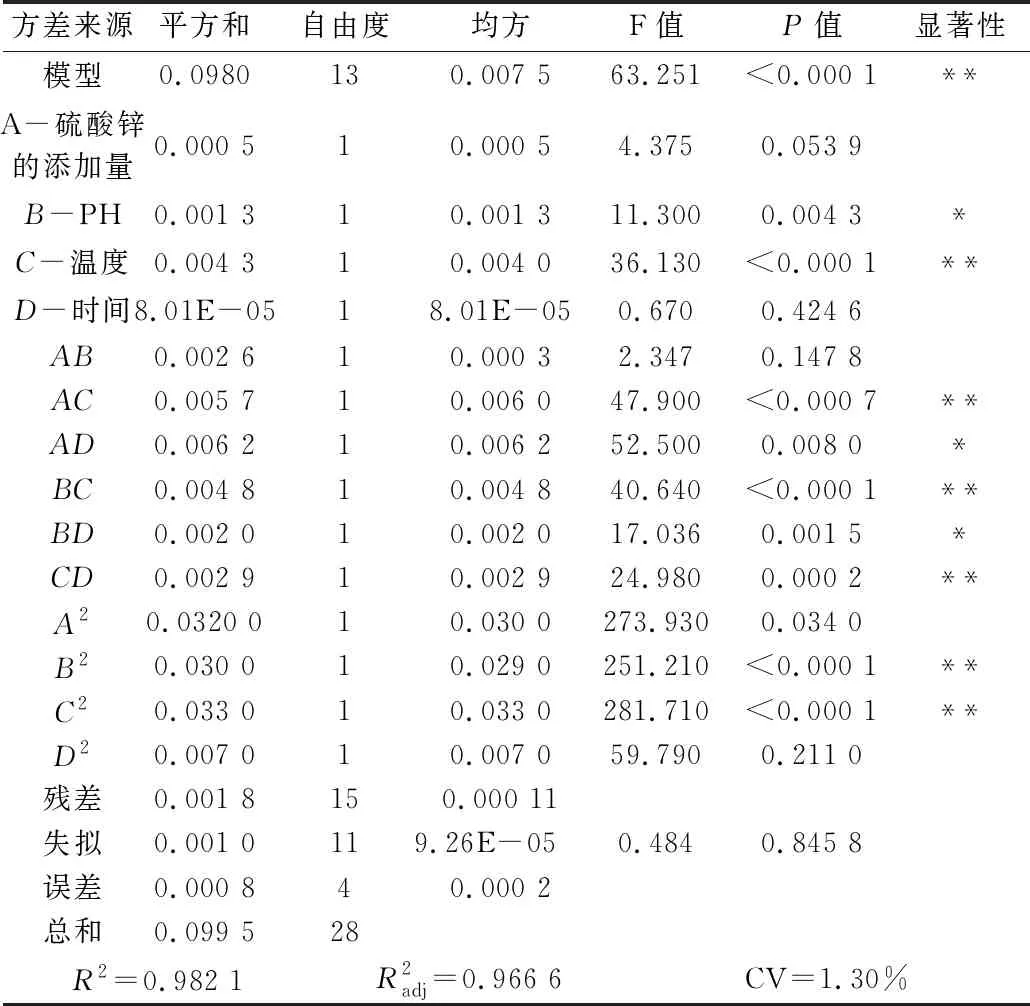
表3 螯合率回歸模型的方差分析
注:“*”在 0.01 水平顯著;“**”在 0.001 水平顯著。
硫酸鋅添加量、pH、時間和溫度中任意2個因素為零水平時,剩下2個因素均可對螯合率產生不同程度的影響。通過面陡峭程度判斷因素對響應值影響的顯著性。結果顯示: pH和溫度對螯合率的影響顯著,隨著這2個因素值的升高,螯合率均先上升后下降,其他兩個因素相比較沒有那么顯著。這與表3中的方差分析的結果一致。
3.2.2 最佳工藝參數及驗證實驗
根據方程計算可得最佳工藝方案為:硫酸鋅的添加量為0.6 g,螯合時間為50.36 h,溫度為38.46 ℃,pH為7.41。螯合率理論值為91.35%。根據實際情況將實驗方案調整為,硫酸鋅的添加量為0.6 g,時間為50 h,溫度為38 ℃,pH值為7,在此條件下,實驗重復三次,最終測得螯合率為90.60%、92.48%。與理論值相差不大,所以經響應面優化的工藝條件是可靠的。
3.3 松仁肽-鋅螯合物的體外抗氧化性質實驗
微生物發酵的松仁肽與松仁肽-鋅螯合物抗氧化能力的對比,并以VC作為對照。
3.3.1 DPPH自由基的測定
由圖2可知,松仁肽和松仁肽-鋅螯合物在不同的濃度下均表現出來很強的DPPH自由基的清除能力,隨濃度的增加,DPPH 自由基清除率也增加,VC對DPPH自由基的半數抑制質量濃度(IC50)為2.123 mg/mL,松仁肽對DPPH自由基的半數抑制質量濃度(IC50)為1.564 3 mg/mL,松仁肽-鋅的螯合物對DPPH自由基的半數抑制質量濃度(IC50)為3.841 mg/mL,在實驗測定的質量濃度范圍內,10mg/mL樣品的清除作用最強,松仁肽的自由基清除率為84.06%,松仁肽-鋅螯合物的自由基清除率為90.31%,VC 的自由基清除率為94.36%。三者質量濃度均與DPPH自由基清除率有顯著的正相關性(松仁肽、松仁肽-鋅螯合物、VC的R2分別為0.941 01、0.922 85、0.918 8)。螯合物的DPPH 自由基清除率均

圖2 不同濃度的螯合物和松仁肽對DPPH自由基的清除能力
高于單純肽,DPPH自由基清除能力是基于DPPH自由基接受抗氧化劑提供的氫原子使奇數電子的氮原子減少從而引起體系中顏色的降低,抗氧化劑清除DPPH自由基效果主要依賴于其供氫的能力[24],由此可推測松仁肽-鋅螯合物在清除自由等一些連鎖反應具有一定的功能,且松仁肽-鋅的螯合物要高于松仁肽,但是兩者均小于陽性對照組VC的清除率。
3.3.2 還原力的測定
由圖3可得,在一定質量濃度范圍內,隨著質量濃度的增大,松仁肽和松仁肽-鋅螯合物的吸光度不斷升高,還原能力不斷增強,說明樣品質量濃度越大,其還原作用越強,兩者存在著明顯的劑量依賴關系。松仁肽和松仁肽-鋅螯合物的還原能力與其質量濃度之間基本上呈直線性關系,陽性對照VC的還原能力與質量濃度呈正相關,也存在劑量依賴關系,并且也是呈直線性關系。三者質量濃度均與還原能力有顯著的正相關性(松仁肽、松仁肽-鋅螯合物、VC的R2分別為0.965 99、0.949 18、0.980 12),但松仁肽的還原能力始終低于同質量濃度的松仁肽-鋅螯合物,二者始終低于同質量濃度的VC。研究表明[25],多肽類物質的抗氧化性質與還原能力之間具有相關性,所以還原能力可以作為一種衡量抗氧化能力的指標。因此松仁肽和松仁肽-鋅的螯合物就有較強的還原能力同時也具有抗氧化性。且松仁肽-鋅螯合物的還原能力更強。

圖3 不同濃度的螯合物和松仁肽的還原能力
3.3.3 羥自由基的測定
由圖4可知,松仁肽和松仁肽-鋅螯合物均表現出較強的清除·OH活性。在一定質量濃度范圍內,對·OH的清除率隨著質量濃度的增加而增加,但二者清除率均低于陽性對照VC。通過清除率-質量濃度回歸曲線可知VC對·OH的IC50為0.513 mg/mL,松仁肽-鋅螯合物對·OH的IC50為1.346 mg/mL,松仁肽對·OH的IC50為1.725 mg/mL,6 mg/mL樣品的清除作用最強,松仁肽清除率達80.56%,松仁肽-鋅螯合物清除率達88.96%,在相同質量濃度下VC對·OH的清除率為92.53%。三者質量濃度均與·OH清除率有顯著的正相關性(松仁肽、松仁肽-鋅螯合物、VC的R2分別為0.988 75、0.976 48、0.993 27)。·OH被認為是引發機體內組織細胞病變,導致疾病與加速衰老最直接的自由基[26],實驗結果證明,松仁肽-鋅螯合物具有較強的·OH清除率,因此推測其具有減少疾病的發生和延緩衰老的作用,且松仁肽-鋅螯合物的清除能力強于松仁肽,但兩者均弱于陽性對照VC。

圖4 不同濃度的螯合物和松仁肽對·OH的清除能力
4 討論
早在十九世紀六十年代中期,研究者就發現肽具有促進鋅吸收的作用。大量的研究結果發現,肽能與鋅離子發生反應,生成化學性質穩定、可溶的肽鋅螯合物。這種螯合物能夠使鋅元素不受胃腸道中植酸等各類物質的影響,并能以肽的吸收模式進入體內,給人體補鋅提供了新的途徑[27]。本實驗研究了微生物法對松仁肽-鋅進行螯合,運用枯草芽孢桿菌將松仁蛋白分解為小分子肽的同時與鋅離子螯合,得出最佳生產工藝參數為:硫酸鋅的添加量為0.6 g,螯合時間為50.36 h,溫度為38.46 ℃,pH值為7.41。影響發酵螯合反應的因素水平溫度最大,其次是pH。優化得到螯合率為90.60%,與理論值相差不大,工藝參數可行。通過對松仁肽和松仁肽-鋅螯合物抗氧化的研究,螯合物的還原能力高于松仁肽且還原能力隨質量濃度升高而增強。二者均可有效的清除DPPH自由基和·OH,螯合物的清除力強于松仁肽。鋅離子與肽形成配合物后呈現出多樣的生物功能活性,如抗氧化、抗菌、免疫調節、抗衰老等生物活性,綜合以上結論,松仁肽與鋅螯合后得到了生物活性高而且毒性低的有機鋅化合物,且能很好的為機體補鋅,松仁肽螯合后的松仁肽-鋅螯合物的抗氧化能力強于螯合前的松仁肽。同時松仁肽的抗氧化活性對于開發松仁肽-鋅螯合物功能性食品提供了方向和理論基礎,具有應用指導意義,但具體的抗氧化功能機理需進一步研究,微生物法制備松仁肽-鋅螯合物的抗氧化功能性需要做體內的實驗進行驗證。

