視神經(jīng)脊髓炎譜系疾病復(fù)發(fā)與外周血免疫細(xì)胞水平相關(guān)性分析
姜 曌,徐 典,李 力△
1.空軍軍醫(yī)大學(xué)西京醫(yī)院神經(jīng)內(nèi)科(西安710032);2.空軍軍醫(yī)大學(xué)口腔醫(yī)院綜合科(西安710032)
視神經(jīng)脊髓炎譜系疾病(Neuromyelitis optica spectrum disorders,NMOSD)是一種中樞神經(jīng)系統(tǒng)的自身免疫性疾病,該病病情兇險(xiǎn)且容易復(fù)發(fā),給患者的神經(jīng)系統(tǒng)造成嚴(yán)重的功能損傷。在NMOSD的治療中,維護(hù)階段的治療尤為重要。有綜述指出,維護(hù)期B細(xì)胞數(shù)量超過總淋巴細(xì)胞計(jì)數(shù)的0.1%時(shí)NMOSD易復(fù)發(fā),推薦以CD20+B細(xì)胞、CD19+/CD27+B細(xì)胞的數(shù)量來判斷NMOSD復(fù)發(fā)的可能性[1]。目前在臨床中使用利妥昔單抗(Rituximab,RTX)來治療NMOSD效果較好。雖然該藥物是CD20+淋巴細(xì)胞的抑制劑,但是在臨床發(fā)現(xiàn)使用該藥物的患者單核細(xì)胞比例、CD19+B細(xì)胞和CD19+/CD27+B細(xì)胞的數(shù)量均會(huì)下降,而這些數(shù)據(jù)被認(rèn)為是NMOSD發(fā)作或復(fù)發(fā)的指標(biāo)。目前在中國(guó)患者人群中,上述免疫細(xì)胞的比值對(duì)于NMOSD發(fā)作的閾值鮮有報(bào)道。本研究旨在回顧NMOSD患者發(fā)病時(shí)上述免疫細(xì)胞的監(jiān)測(cè)數(shù)據(jù)及其隨著利妥昔單抗治療后的變化,以期確定適合中國(guó)人群的NMOSD復(fù)發(fā)指標(biāo)和治療方案。
對(duì)象與方法
1 研究對(duì)象 本研究屬于回顧性隊(duì)列研究,通過西京醫(yī)院電子病例系統(tǒng)查閱、過濾并收集NMOSD復(fù)發(fā)患者的基本信息、影像學(xué)資料、實(shí)驗(yàn)室檢查數(shù)據(jù)、用藥方案、治療效果等臨床資料。本研究已通過西京醫(yī)院倫理委員會(huì)討論并獲準(zhǔn)進(jìn)行。最終共收集到2016年1月至2018年4月在空軍軍醫(yī)大學(xué)西京醫(yī)院神經(jīng)內(nèi)科住院治療的NMOSD復(fù)發(fā)患者18例,其中男性3例,女性15例;年齡16~64歲,復(fù)發(fā)時(shí)發(fā)病時(shí)間≤1周,平均年齡(38.9±14.8)歲。病例納入標(biāo)準(zhǔn):①年齡15~70歲;②臨床表現(xiàn)符合2015版NMOSD診斷共識(shí)[2];③患者及其家屬在充分了解病情、治療方案及可能出現(xiàn)的醫(yī)療結(jié)局的前提下,同意參與研究與并簽署知情同意書;④患者基本資料、各項(xiàng)檢查結(jié)果及治療效果等臨床資料完整。排除標(biāo)準(zhǔn):①患有其他自身免疫疾病;②入院前3個(gè)月內(nèi)已經(jīng)接受糖皮質(zhì)激素、免疫球蛋白或免疫抑制劑治療;③患有重癥肌無力、癲癇、腦血管疾病、顱內(nèi)感染性疾病、神經(jīng)系統(tǒng)腫瘤等。
2 研究方法
2.1 實(shí)驗(yàn)室檢查:入院后清晨采集空腹靜脈血,檢測(cè)分析單核細(xì)胞比例、CD19+B細(xì)胞比例、CD19+/CD27+B細(xì)胞比值。完成腰穿檢查,采用間接免疫熒光法(Indirect immunofluorescence,IIF)試劑盒(德國(guó)歐蒙公司),主要檢查血清及腦脊液水通道蛋白-4抗體(AQP4-IgG)、腦脊液白蛋白/血清白蛋白(Cerebrospinal/serum albuminratio,QALB)、24 h鞘內(nèi)IgG合成率等生化指標(biāo)。
2.2 神經(jīng)影像學(xué)檢查:入院期間接受頭顱、頸椎、腰椎MRI及其增強(qiáng)檢查,完善視覺誘發(fā)電位(Visual evoked potential,VEP)和腦干聽覺誘發(fā)電位(Brain stem auditory evoked potential,BAEP)檢查。
2.3 治療方案:對(duì)癥支持治療的同時(shí)積極進(jìn)行免疫治療,具體方案為:甲強(qiáng)龍1 g/d,連續(xù)5 d;靜脈注射免疫球蛋白(Intravenous immunoglobulin,IVIG)0.4 g/(kg·d),連續(xù)5 d;二線免疫治療方案為:利妥昔單抗(Rituximab,RTX),劑量為每周375 mg/m2,持續(xù)進(jìn)行4周。
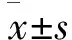
結(jié) 果
1 各項(xiàng)免疫細(xì)胞檢查及分析結(jié)果 患者入院時(shí)進(jìn)行單核細(xì)胞比例、CD19+B細(xì)胞比例和CD19+/CD27+B細(xì)胞比例檢查,見表1。因CD19+B細(xì)胞比例和CD19+/CD27+B細(xì)胞比例差異較大,故采取負(fù)對(duì)數(shù)轉(zhuǎn)換后進(jìn)行95%可信區(qū)間的單尾分析。根據(jù)目前樣本量分析,患者復(fù)發(fā)時(shí)CD19+B細(xì)胞比例的95%可信區(qū)間下限值為0.0060,CD19+/CD27+B細(xì)胞比例的95%可信區(qū)間下限值為0.0115。見表2。
2 實(shí)驗(yàn)室檢查結(jié)果 18例患者中AQP4-IgG陽性患者14例,陰性患者4例,與性別相關(guān)(P=0.043),與年齡分布未發(fā)現(xiàn)統(tǒng)計(jì)學(xué)關(guān)聯(lián)(P=0.307)。72.2% (13/18)的患者腦脊液白細(xì)胞均升高(>5×106/L),其中11.1% ( 2/18) 患者腦脊液白細(xì)胞大于50×106/L。腦脊液蛋白平均56.2 mg/dl(3.2~243 mg /dl)。 9例患者( 9/18,50% ) 24 h鞘內(nèi) IgG合成率升高。在AQP4-IgG陽性患者中,顱內(nèi)MRI檢查異常占78.6%(11/14),脊髓MRI檢查異常者占71.4%(10/14),兩者同時(shí)存在特征性病變者占到50.0%(7/14);AQP4-IgG陰性患者4例,其中MRI檢查顱內(nèi)特征性改變者占50.0%(2/4),脊髓MRI檢查異常占75.0%(3/4),兩者同時(shí)存在特征性病變者占25.0%(1/4),典型影像學(xué)表現(xiàn)見圖1。VEP異常的患者占83.3%(15/18),其中AQP4-IgG陽性患者為92.9%(13/14),陰性患者為50.0%(2/4);BAEP異常患者較少,僅為16.7%(3/18);VEP與BAEP均異常患者僅有1例。見表3。

表1 入組患者入院時(shí)各項(xiàng)免疫細(xì)胞檢查結(jié)果

表2 患者免疫細(xì)胞數(shù)據(jù)分析
注:*CD19+B細(xì)胞比例、CD19+/CD27+B細(xì)胞比例原始數(shù)據(jù)做負(fù)對(duì)數(shù)轉(zhuǎn)換后統(tǒng)計(jì),為單尾95%可信區(qū)間下限值

表3 18例NMOSD復(fù)發(fā)患者臨床特點(diǎn)比較
注:ON:視神經(jīng)炎
3 治療結(jié)果 全部18例患者在對(duì)癥治療和免疫治療的基礎(chǔ)上,均接受RTX治療,劑量為每周375 mg/m2,持續(xù)4周。治療結(jié)束時(shí),有15例患者臨床癥狀明顯改善(15/18,83.3%),3例患者(3/18,16.7%)臨床癥狀得到緩解。
4 隨訪時(shí)接受外周血免疫細(xì)胞細(xì)胞監(jiān)測(cè)結(jié)果 本研究18例患者中,有5例患者出院后接受了隨訪和復(fù)查,并在隨訪時(shí)接受外周血CD19+/CD27+B細(xì)胞檢測(cè)。具體如圖2所示,可見接受利妥昔單抗治療后的15 d內(nèi),患者外周血CD19+/CD27+B細(xì)胞比例顯著降低,治療結(jié)束時(shí)(距復(fù)發(fā)時(shí)1個(gè)月),除1例外,其余患者CD19+/CD27+B細(xì)胞比例均降低至0.005以下;隨訪3個(gè)月時(shí)5例患者外周血CD19+/CD27+B細(xì)胞水平均無升高。

雙側(cè)大腦半球?qū)ΨQ,灰白質(zhì)對(duì)比自然,腦橋背側(cè)見小片狀稍長(zhǎng)T2信號(hào)影,F(xiàn)LAIR序列呈稍高信號(hào),DWI序列呈稍高信號(hào)(A、B、D、E、F中白色箭頭);第4、5頸椎脊髓可見信號(hào)改變(C中白色箭頭)
圖1 典型患者影像學(xué)表現(xiàn)

圖2 隨訪5例患者外周血內(nèi)CD19+/CD27+B細(xì)胞比例變化
討 論
視神經(jīng)脊髓炎(Neuromyelitis optica,NMO)是一種免疫介導(dǎo)的中樞神經(jīng)系統(tǒng)(Central nervous system,CNS)炎性脫髓鞘疾病[3-4]。NMO臨床表現(xiàn)為嚴(yán)重的視神經(jīng)炎(Optic neuritis,ON)和縱向延伸的長(zhǎng)節(jié)段橫貫性脊髓炎(Longitudinally extensive transverse myelitis,LETM),以青壯年女性多發(fā),具有很高復(fù)發(fā)率及致殘率[5]。其病因主要與水通道蛋白4(Water channel aquaporin-4,AQP-4)抗體(AQP4-IgG)相關(guān)[6-7]。隨著臨床研究的深入,NMO的臨床特征不單單局限于視神經(jīng)和脊髓表現(xiàn),而是與室管膜周圍AQP-4高表達(dá)區(qū)域密切相關(guān),呈現(xiàn)一系列中樞神經(jīng)系統(tǒng)脫髓鞘病變疾病譜。國(guó)際NMO診斷小組將NMO相關(guān)的一系列癥候群命名為視神經(jīng)脊髓炎譜系疾病(NMOSD)并制定了相應(yīng)的診斷細(xì)則[2]。本病尚無特效藥物,是神經(jīng)病學(xué)領(lǐng)域的研究重點(diǎn)疾病之一。
本研究采用IIF試劑盒(德國(guó)歐蒙公司),對(duì)患者腦脊液進(jìn)行基于細(xì)胞底物(Cell based assay,CBA)和基于組織底物(Tissue based assay,TBA)聯(lián)合檢測(cè),具有較高的敏感度和特異度,因而廣泛用于腦脊液中相關(guān)生化指標(biāo)和抗體的檢測(cè)[8]。發(fā)現(xiàn)72.2% (13/18)的患者腦脊液白細(xì)胞升高(>5×106/L),與Bergamaschi等[9]報(bào)道79%的腦脊液白細(xì)胞升高率接近,但目前的診療指南認(rèn)為該項(xiàng)指標(biāo)的變化不具備特異性,僅作為臨床參考。本研究77.8%(14/18)的NMOSD患者AQP4-IgG陽性,與Waters等人的研究一致[10]。AQP4-IgG陰性的患者通常被認(rèn)為預(yù)后相對(duì)較好[11]。統(tǒng)計(jì)分析顯示,患者性別分布和VEP陽性檢出率均與AQP4-IgG陽性率呈正相關(guān)(P<0.05),其他臨床特征與AQP4-IgG陽性率未發(fā)現(xiàn)有統(tǒng)計(jì)學(xué)聯(lián)系見表3,可能是因?yàn)楸狙芯恐蠥QP4-IgG陰性的患者數(shù)量太少,不足以說明患者臨床特征的分布規(guī)律。
NMOSD患者的典型MRI表現(xiàn)為病變節(jié)段可大于1/2視神經(jīng)長(zhǎng)度及視交叉。急性期時(shí)視神經(jīng)增粗、強(qiáng)化,視神經(jīng)鞘亦可見強(qiáng)化。慢性期可見視神經(jīng)萎縮,呈現(xiàn)“雙軌征”。脊髓病變典型表現(xiàn)為較長(zhǎng)的、縱向延伸的長(zhǎng)節(jié)段橫貫性損害(超過三個(gè)椎體節(jié)段),矢狀位多表現(xiàn)連續(xù)病變,多累及脊髓后索中央灰質(zhì)和部分白質(zhì)。急性期出現(xiàn)明顯腫脹,呈長(zhǎng)T1長(zhǎng)T2表現(xiàn);慢性期脊髓呈現(xiàn)萎縮、空洞,長(zhǎng)節(jié)段病變可轉(zhuǎn)變?yōu)椴贿B續(xù)的長(zhǎng)T2信號(hào)[12]。張植等[13]研究發(fā)現(xiàn),AQP4-IgG(+)患者中43.9%(43/98)存在顱內(nèi)病灶,且脊髓病變多位于頸段,與Havla等[14]的研究類似。本研究中顱內(nèi)(11/14,78.6%)及脊髓(10/14,71.4%)MRI檢查異常表現(xiàn)與我國(guó)NMOSD臨床診療指南中相關(guān)描述基本符合,但是MRI異常的發(fā)生率均高于上述國(guó)內(nèi)外學(xué)者的研究,可能是由于本研究的對(duì)象均為NMOSD復(fù)發(fā)患者,再次發(fā)病時(shí)神經(jīng)系統(tǒng)的影像學(xué)病變表現(xiàn)更為突出。
VEP可以檢查從視網(wǎng)膜到枕葉皮質(zhì)的視覺神經(jīng)通路的功能,其中P100的潛伏期延長(zhǎng)反映了視神經(jīng)軸突存在脫髓鞘病變,說明視神經(jīng)的傳導(dǎo)速度變慢[15],而波幅的改變反映病變的視神經(jīng)傳導(dǎo)完全阻滯[16]。VEP的P100潛伏期幅度較小被認(rèn)為是NMOSD的典型表現(xiàn)[17]。本研究中納入病例均為NMOSD復(fù)發(fā)病例,故MRI檢查發(fā)現(xiàn)視神經(jīng)異常者,其VEP也均有不同程度的異常變化,并且VEP的異常與AQP4-IgG呈統(tǒng)計(jì)學(xué)關(guān)聯(lián)(P=0.043),即AQP4-IgG陽性患者中VEP異常的比例更高。BAEP可以反映聽覺傳導(dǎo)通路是否完整及評(píng)價(jià)患者的聽力狀況。Ohnari等研究發(fā)現(xiàn)雖然部分NMOSD患者的BAEP正常,但是VEP存在明顯異常,提示VEP與BAEP聯(lián)合檢查有助于NMOSD的診斷[18]。本研究中,BAEP的異常與AQP4-IgG不具有統(tǒng)計(jì)學(xué)關(guān)聯(lián)(P=0.612),BAEP異常的患者僅有3例(3/18,16.7%),但是其中有一例患者AQP4-IgG陰性,MRI僅發(fā)現(xiàn)頸段脊髓連續(xù)病變;但VEP與BAEP同時(shí)出現(xiàn)異常,可能是受到MRI分辨率的限制,無法發(fā)現(xiàn)顱內(nèi)異常,而VEP和BAEP檢查則可能同時(shí)發(fā)現(xiàn)異常,說明VEP聯(lián)合BAEP檢查對(duì)NMOSD的臨床診斷具有鑒別意義。
免疫細(xì)胞的表達(dá)水平對(duì)神經(jīng)系統(tǒng)疾病,特別是對(duì)中樞神經(jīng)系統(tǒng)自身免疫性疾病的嚴(yán)重程度和預(yù)后均有顯著影響[19-20]。所以針對(duì)B細(xì)胞介導(dǎo)的免疫過程,新型靶向免疫抑制藥物越來越多地被用來治療和預(yù)防NMOSD復(fù)發(fā)。RTX是針對(duì)B淋巴細(xì)胞特異性表面抗原CD20研制的人鼠嵌合的IgG1單克隆抗體,于2005年首次應(yīng)用于預(yù)防NMO復(fù)發(fā)并取得良好的臨床效果[21]。但是RTX用于預(yù)防NMOSD復(fù)發(fā)的具體使用方法和用藥指征目前尚無定論[22],主要有如下幾種方案:
第一種:每6~9個(gè)月用藥一次,劑量同初始治療[23]。此方案沒有檢查指標(biāo)作為用藥依據(jù),缺乏循證醫(yī)學(xué)證據(jù)支持,僅憑醫(yī)生經(jīng)驗(yàn)或患者的癥狀確定預(yù)防用藥時(shí)機(jī),主觀性過大。
第二種:以外周血CD19+B細(xì)胞數(shù)量為參考。若CD19+B細(xì)胞比例≥0.01時(shí),重復(fù)輸注RTX 100 mg/周,連續(xù)輸注3周[24];或者發(fā)病時(shí)給予每周100 mg/m2,連用3周,后每2個(gè)月復(fù)查外周血CD19+B細(xì)胞數(shù)量,如超過0.01時(shí),再給予100 mg/m2一次[25]。在本研究中,根據(jù)18例患者復(fù)發(fā)入院時(shí)CD19+B細(xì)胞比例最低值為0.001,經(jīng)過統(tǒng)計(jì)學(xué)分析,復(fù)發(fā)時(shí)CD19+B細(xì)胞比例的95%可信區(qū)間最低為0.0105,與上述學(xué)者的研究結(jié)果相似,說明我國(guó)人群NMOSD患者的CD19+B細(xì)胞比例如果高于0.0105,其復(fù)發(fā)可能性大于95%。
第三種:以外周血CD19+/CD27+記憶性B細(xì)胞數(shù)量為用藥依據(jù)。按 375 mg/m2(體表面積),靜脈滴注,每周1次,連用4周[26]。Kim SH等人對(duì)30例NMOSD復(fù)發(fā)患者進(jìn)行了隨訪觀察:前2年,當(dāng)外周血CD19+/CD27+記憶性B細(xì)胞比例超過0.0005時(shí),給予RTX治療,劑量為375 mg/m2;在此之后,如外周血中CD19+/CD27+記憶性B細(xì)胞比例超過0.001則需要再給予RTX,劑量同前[27]。
本研究采用利妥昔單抗每周375 mg/m2,持續(xù)4周的治療方案。這也是目前被臨床采用較多的治療方案。治療結(jié)束時(shí),有15例患者臨床癥狀明顯改善(15/18,83.3%),3例患者(3/18,16.7%)臨床癥狀得到緩解。有5例患者接受了隨訪并進(jìn)行了外周血CD19+/CD27+B細(xì)胞監(jiān)測(cè)。利妥昔單抗治療后的15 d內(nèi),患者外周血CD19+/CD27+B細(xì)胞比例顯著降低,治療結(jié)束時(shí)(距復(fù)發(fā)時(shí)1個(gè)月),除1例外,其余患者CD19+/CD27+B細(xì)胞比例均降低至0.005以下,隨訪3個(gè)月后,5名患者的CD19+/CD27+B細(xì)胞比例均無升高。雖然本研究采用的RTX治療方案取得相對(duì)良好的治療效果,但是隨訪的患者數(shù)量較小,論證級(jí)別有限,所以目前利妥昔單抗治療 NMOSD 的治療劑量以及防止復(fù)發(fā)的治療時(shí)機(jī)均尚需進(jìn)一步研究證實(shí)[22]。
自身反應(yīng)性記憶性B細(xì)胞激活后產(chǎn)生抗原特異性反應(yīng),這種記憶效應(yīng)可能持續(xù)很長(zhǎng)時(shí)間,從而誘導(dǎo)NMOSD復(fù)發(fā)[28]。因此很多臨床研究關(guān)注于刪除記憶性B細(xì)胞。Kim SH等[29]研究發(fā)現(xiàn),NMOSD復(fù)發(fā)多發(fā)生于CD19+/CD27+記憶性B細(xì)胞回升之后。隨訪5年后,絕對(duì)危險(xiǎn)度降低率(Absolute risk reduction,ARR)由治療前的2.4±1.5下降為治療后的0.3±1.0;18例患者(60%)在5年的隨訪期內(nèi)沒有復(fù)發(fā);28例患者的致殘程度均無加重,且沒有觀察到嚴(yán)重的副作用出現(xiàn)。所以Kim SH等認(rèn)為,在RTX治療中CD19+/CD27+記憶性B細(xì)胞比例可以作為NMOSD復(fù)發(fā)的參考指標(biāo)。經(jīng)過外周血B細(xì)胞刪除治療后,如CD19+/CD27+記憶性B細(xì)胞比例超過0.001,應(yīng)及時(shí)給予RTX治療,以避免復(fù)發(fā)。本研究也以CD19+/CD27+記憶性B細(xì)胞比例作為判斷RTX是否需要重新輸注臨床依據(jù),NMOSD患者復(fù)發(fā)時(shí)CD19+/CD27+B細(xì)胞比例的最低值為0.013,其95%可信區(qū)間的下限值為0.0115,與Kim SH等建議的0.001(即0.1%)差距較大。可能是因?yàn)楸狙芯繉儆诨仡櫺匝芯浚虢M時(shí)患者已經(jīng)出現(xiàn)NMOSD復(fù)發(fā)癥狀,此時(shí)CD19+/CD27+B細(xì)胞比例已經(jīng)上升并超過了Kim SH等建議的0.001警戒值,加之樣本量較小,所以出現(xiàn)了近10倍的差異,但是這也充分說明CD19+/CD27+B細(xì)胞比例作為免疫系統(tǒng)表達(dá)增強(qiáng)的指標(biāo),對(duì)NMOSD復(fù)發(fā)的預(yù)警具有十分重要意義。
NMOSD患者外周血中相關(guān)淋巴細(xì)胞比例是疾病復(fù)發(fā)的重要參考指標(biāo),當(dāng)外周血中CD19+/CD27+B細(xì)胞比例超過0.0115,或CD19+B細(xì)胞比例超過0.006,應(yīng)采取免疫靶向藥物對(duì)相應(yīng)淋巴細(xì)胞進(jìn)行清除治療。以上指標(biāo)可以作為臨床醫(yī)師治療NMOSD和預(yù)防復(fù)發(fā)的參考,使臨床醫(yī)師在制定治療方案時(shí)兼顧NMOSD復(fù)發(fā)的預(yù)防和患者經(jīng)濟(jì)負(fù)擔(dān)的減輕。而目前針對(duì)RTX用于預(yù)防NMOSD復(fù)發(fā)的使用指征目前尚無明確共識(shí),其檢測(cè)指標(biāo)和啟動(dòng)預(yù)防性用藥的閾值均有待于完善設(shè)計(jì)的臨床對(duì)照試驗(yàn)加以論證。

