嗜酸性實(shí)性及囊性腎細(xì)胞癌1例
寇天雷,何 滔,鄭淑芳,何 軒
嗜酸性實(shí)性和囊性腎細(xì)胞癌(eosinophilic solid and cystic renal cell carcinoma, ESC RCC) 是近幾年文獻(xiàn)報(bào)道的一種特殊類型的腎腫瘤,幾乎均發(fā)生在女性患者,伴或不伴有結(jié)節(jié)性硬化癥(tuberous sclerosis complex,TSC)。我科于2019-07發(fā)現(xiàn)1例,現(xiàn)報(bào)道如下。
1 病例報(bào)告
1.1 病例資料 患者,女性,41歲,2019-05因發(fā)現(xiàn)卵巢腫物來我院進(jìn)行腫物切除,術(shù)后病理診斷漿液性乳頭狀癌,行腹部超聲發(fā)現(xiàn)左腎囊性腫物,大小5.3 cm ×4.4 cm ×3.9 cm,MRI示左腎下極囊性占位,符合Bosniak IV級改變,行左腎腫物根治術(shù)。患者發(fā)現(xiàn)腫物以來,無腰痛、尿頻、尿急、血尿等癥狀,本人及家族均無TSC相關(guān)表現(xiàn),皮膚及其他器官均未發(fā)現(xiàn)結(jié)節(jié)。
1.2 標(biāo)本處理 標(biāo)本離體后經(jīng)10% 中性甲醛固定,常規(guī)乙醇梯度脫水,二甲苯透明,常規(guī)石蠟包埋,4 μm厚切片,HE 染色,光鏡下觀察。免疫組織化學(xué)抗體及試劑盒均購自北京中杉金橋生物技術(shù)有限公司。
1.3 病理檢查 (1)大體檢查:楔形切除腎組織,腎臟大小5.0 cm×4.0 cm×1.2 cm,一側(cè)距基底1.3 cm見一囊實(shí)性腫物,大小5.0 cm×5.0 cm×3.5 cm,表面光滑,局部附脂肪,切面多房囊實(shí)性,囊內(nèi)含清亮液體。(2)鏡下觀察:腫瘤與正常腎組織分界較清,局部穿插纖維間質(zhì)生長,血管較豐富,腫瘤細(xì)胞大部分嗜酸,胞質(zhì)可見顆粒,可見異型核,局部可見透明細(xì)胞樣細(xì)胞(圖1A、B)。(3)免疫組化染色:腫瘤細(xì)胞彌漫CK20陽性(圖1C)、Vemintin陽性,PAX-8陽性(圖1D),CD56陽性,部分腫瘤細(xì)胞表達(dá)CK、P504S及CD10。腫瘤細(xì)胞均不表達(dá)EMA、CK7(圖1E)、CD117(圖1F)、SMA、S-100、CgA、Syn、TFE-3、CA IX、HMB-45、Myogenin等。Ki-67 增殖指數(shù)<1%。(4)病理診斷:ESC和RCC。
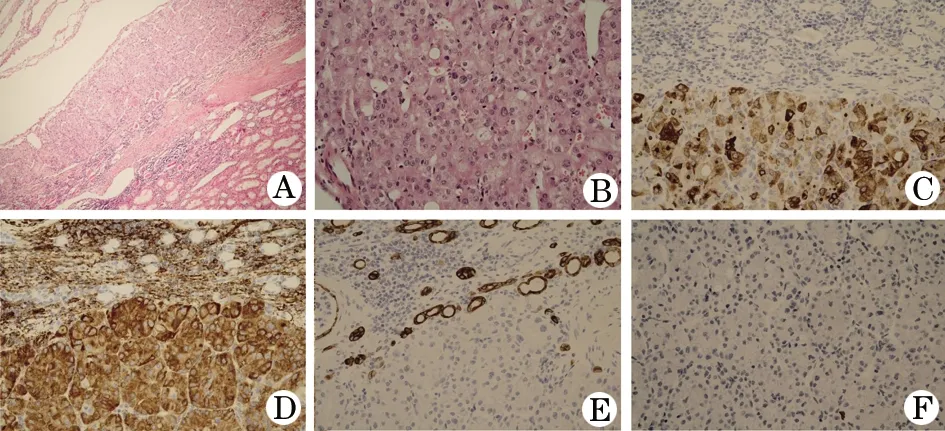
圖1 嗜酸性實(shí)性和囊性腎細(xì)胞癌病理
A.囊實(shí)性,HE×10; B. 腫瘤胞漿嗜酸,HE×40;C. 腫瘤細(xì)胞表達(dá)CK20, IHC×40; D. 腫瘤細(xì)胞表達(dá)Vimentin, IHC×40; E. 腫瘤細(xì)胞不表達(dá)CK7, IHC×40; F. 腫瘤細(xì)胞不表達(dá)CD117, IHC×40
2 討 論
ESC RCC是近幾年新認(rèn)識的一種特殊類型的腎腫瘤[1],最初國外報(bào)道多伴發(fā)TSC,而近來越來越多病例患者未有TSC的臨床表現(xiàn)[2]。
2.1 形態(tài)學(xué) ESC RCC國內(nèi)僅有個(gè)別報(bào)道,如王慧等[3]總結(jié)2例病例,史倩蕓等[4]回顧近10年診斷的嗜酸性腎腫瘤,獲得4例ESC RCC,均為女性,均無TSC病史,臨床均呈惰性,切除后隨訪病例均無復(fù)發(fā)。
國外總結(jié)較多病例,發(fā)現(xiàn)腫瘤多發(fā)生于女性,平均年齡45歲,可有腰背部不適等無特征性的癥狀和體征,影像學(xué)檢查呈囊實(shí)性,臨床低分期,大體腫瘤呈多囊實(shí)性外觀,中位大小3.1 cm。組織學(xué)特征:囊性區(qū)大小不等,上皮可呈鞋釘樣,實(shí)性區(qū)細(xì)胞排列呈腺泡狀或巢狀,可有鈣化及砂礫體,細(xì)胞含有豐富的嗜酸性胞漿,部分呈顆粒狀,核圓形或卵圓形。依據(jù)組織病理學(xué)特征(實(shí)性或囊性優(yōu)勢),影像上也有所不同[5]。
2.2 免疫表型 免疫表型上,ESC RCC一致表達(dá)PAX8,CD10、CA9陽性率高,Trpkov等[6]和Guo等[7]分別報(bào)道了16例和18例TSC相關(guān)的ESC RCC患者,免疫組化顯示腫瘤細(xì)胞均呈CK20+/CK7-表達(dá),且在其他腎腫瘤中表達(dá)均較低,因此,認(rèn)為CK20表達(dá)提示ESC RCC。本例腫瘤細(xì)胞彌漫CK20陽性,Vemintin陽性,PAX-8陽性,CD56陽性,部分腫瘤細(xì)胞表達(dá)CK、P504S及CD10。腫瘤細(xì)胞均不表達(dá)CK7、CD117、EMA、SMA、S-100、CgA、Syn、TFE-3、CA IX、Myogenin,可除外其他嗜酸性腫瘤。Tretiakova[8]報(bào)道了6例形態(tài)學(xué)類似于EAML的ESC RCC腫瘤細(xì)胞表達(dá)HMB-45及Melan-A,提示兩者具有相似的分子基礎(chǔ)。
2.3 鑒別診斷 ESC RCC在形態(tài)上應(yīng)與具有囊實(shí)性結(jié)構(gòu)且胞漿嗜酸的腎腫瘤鑒別,主要包括:(1)透明細(xì)胞腎細(xì)胞癌(clear cell renal cell carcinoma,CCRCC):含有不同比例的透明細(xì)胞,特征性表達(dá)CA9。(2)嗜酸細(xì)胞性嫌色細(xì)胞癌(chromophonbe renal cell carcinoma,CHRCC):具有特征性核周空暈,呈植物細(xì)胞樣,膠體鐵染色陽性。(3)嗜酸性乳頭狀腎細(xì)胞癌(oncocytic papillary renal cell carcinoma,OPRCC):呈乳頭狀,有纖維血管軸心。(4)嗜酸細(xì)胞腺瘤(renal Oncocytoma,RO):邊界清楚無包膜,明顯間質(zhì)水腫,可見異型核,特征表達(dá)CD117。(5)MiT家族相關(guān)性腎細(xì)胞癌(MiTF-RCC):形態(tài)多樣,可有乳頭或菊形團(tuán)樣結(jié)構(gòu),表達(dá)TFE3或TFEB。(6)上皮樣血管平滑肌脂肪瘤(epithelioid angomyolipoma,EAML):含上皮樣細(xì)胞及血管、平滑肌及脂肪等經(jīng)典成分,表達(dá)MelanA及HMB45。(7)琥珀酸脫氫酶缺陷相關(guān)性腎細(xì)胞癌(succinate dehydrogenase-associated renal cell carcinoma,SDH-RCC):細(xì)胞有特征性的絮狀包涵體,琥珀酸脫氫酶B表達(dá)缺失。(8)遺傳性平滑肌瘤病腎癌綜合征相關(guān)性腎細(xì)胞癌(hereditary leiomyomatosis and renal cell carcinoma-associated renal cell carcinoma, HLRCC-RCC):有明確的家族史或平滑肌瘤病史,形態(tài)類似Ⅱ型乳頭狀癌。(9)獲得性囊性腎病相關(guān)腎細(xì)胞癌(acquired cystic disease-associated renal cell carcinoma,Acquired cystic disease-associated RCC):發(fā)生于終末期腎病,經(jīng)過透析,可見草酸鹽沉積。
結(jié)合形態(tài)學(xué)、免疫組化染色、組織化學(xué)染色及熒光原位雜交實(shí)驗(yàn),大多數(shù)嗜酸性腎腫瘤均可鑒別出來,如不能鑒別可定義為未分類[9]。
2.4 分子遺傳學(xué) ESC RCC分子核型分析報(bào)道較少。在TSC的研究基礎(chǔ)上,ESC RCC被假設(shè)為類似于在TSC的RCC亞型,因?yàn)榘l(fā)現(xiàn)其出現(xiàn)TSC1基因的雜合性喪失,并且TSC2基因的復(fù)制數(shù)增加[10]。
Parilla等[11]發(fā)現(xiàn)與TSC無關(guān)的散發(fā)ESC RCC有致病性體細(xì)胞TSC2基因突變,這些突變在與RCC相關(guān)的任何其他基因中都沒有改變。Trpkov等[12]對13例不伴有TSC的ESC RCC患者進(jìn)行了分子核型分析,發(fā)現(xiàn)該腫瘤均有最常見的染色體拷貝數(shù)獲得、拷貝數(shù)缺失及雜合性缺失。Mehra等[13]發(fā)現(xiàn)ESC RCC發(fā)現(xiàn)雷帕霉素rapamycin (mTOR)通路被激活,而TSC1或TSC2基因的雙等位基因缺失是其負(fù)調(diào)節(jié)因子,ESC RCC缺乏與非腫瘤腎實(shí)質(zhì)相匹配的種系TSC畸變,使得ESC RCC與TSC RCC不同。Palsgrove等[14]進(jìn)一步通過測序分析腫瘤TSC1及TSC2基因突變的一致存在,并推測具有乳頭狀結(jié)構(gòu)、缺乏嗜酸性顆粒胞漿及神經(jīng)母細(xì)胞瘤后具有嗜酸性胞漿的腫瘤等形態(tài)學(xué)變異的腫瘤均可能出現(xiàn)TSC分子改變。
結(jié)合免疫組化染色及分子核型研究后發(fā)現(xiàn)ESC RCC 具有共同的基因變化,因此推測ESC RCC應(yīng)為一種獨(dú)立的腫瘤實(shí)體。
2.5 治療及預(yù)后 絕大多數(shù)ESC RCC屬惰性腫瘤,首選手術(shù)切除治療均有良好預(yù)后。個(gè)別病例多發(fā)者可遠(yuǎn)處轉(zhuǎn)移。Tretiakova等[8]報(bào)道的6例形態(tài)上、免疫組化染色均與EAML類似的ESC RCC中有兩例轉(zhuǎn)移至腹膜后、骨及腎上腺。
ESC RCC雖還未被國際泌尿病理學(xué)協(xié)會(ISUP)承認(rèn)[15],并且2016版WHO腎臟腫瘤分類也并未收錄[16],但其已被泌尿病理界所熟知,隨著分子生物學(xué)研究的不斷深入,對該病的認(rèn)識必將不斷加深。

