HPLC法同時測定地西泮直腸凝膠中地西泮、苯甲酸、苯甲醇含量
徐佳雯,李 尚,張彥卓,胡雅君,張 斐*
1 徐州醫(yī)科大學 新藥研究與臨床藥學重點實驗室,徐州221000 2 江蘇恩華藥業(yè)股份有限公司,徐州 221000
小兒癲癇持續(xù)狀態(tài)(status epilepticus,SE)屬于常見急性病的一種,臨床上常使用地西泮、咪達唑侖、丙戊酸鈉靜脈注射方式治療[1],起效快,但作用持續(xù)時間短,且需要醫(yī)務人員操作。而直腸用凝膠可用于急性發(fā)作時的病情控制,操作方便起效快,適合家庭使用。
地西泮直腸凝膠由瓦利安特(Valeant)制藥國際公司研發(fā)并于2005年上市,作為治療癲癇的一種新劑型,它是美國FDA迄今唯一批準可居家安全使用的癲癇急性發(fā)作的治療藥。國內未有同品種上市。
地西泮直腸凝膠在制備和存儲過程中會受到微生物的污染,為保證產品的穩(wěn)定性和安全性,處方中添加了輔料苯甲酸鈉、苯甲酸和苯甲醇作為防腐劑。由于苯甲酸及其鹽類攝入過量會影響人體對鈣的吸收、刺激胃腸道系統(tǒng),并有一定致癌性和細胞毒性[2],需控制其含量;而苯甲醇易被氧化,毒性強,在兒童用藥方面受到限制[3]。ICH Q6a中明確規(guī)定制劑標準中應制定防腐劑含量的可接受標準[4]。因此,防腐劑含量的測定是藥品質量控制中的一項重要指標。
《中國藥典》2015版、歐洲藥典、英國藥典、日本藥典等[5-9]對地西泮注射液和地西泮片中的地西泮含量測定采用高效液相色譜法,方法重現(xiàn)性差,峰形不佳,且無法同時測定苯甲酸和苯甲醇含量。目前尚無同時測定這3個組分的相關文獻報道。本文采用高效液相色譜法(HPLC),同時測定地西泮直腸凝膠中地西泮、苯甲酸、苯甲醇的含量,方法簡便、高效、靈敏度高,為該制劑中主藥及防腐劑含量的控制提供依據(jù)。
1 儀器與藥品、試劑
1.1 儀器
Agilent 1260 infinityⅡ高效液相色譜儀(安捷倫科技有限公司);ME55型、ME204E型電子天平,F(xiàn)E28型pH計(均梅特勒-托利多儀器上海有限公司)。
1.2 藥品與試劑
地西泮原藥(批號:161101,山東信宜制藥有限公司);苯甲酸(批號:20180802-202007,四川樂康藥用輔料有限公司);苯甲酸鈉(批號:20180425-20200424,湖北華日制藥有限公司);苯甲醇(批號:20181001-2020.09,成都華邑藥用輔料制造有限責任公司);無水乙醇(藥用級,批號:P1464903,南京化學試劑股份有限公司);丙二醇(批 號100420181101,湖南爾康制藥股份有限公司);羥丙基纖維素E5(批號:PD229197,上海卡樂康包衣技術有限公司);乙酸銨(色譜純);冰醋酸(分析純);甲醇(色譜純);水為純凈水。
2 方 法
2.1 地西泮直腸凝膠的制備
精密稱定地西泮原藥50 mg,置于100 mL燒杯內,依次加入苯甲酸鈉4.0 g、苯甲酸0.2 g、苯甲醇1.5 g、乙醇10.0 g、丙二醇40.0 g和羧甲基纖維素E5 100 g,攪拌均勻,加水至100.0 g,再次混合均勻后,即得地西泮直腸凝膠樣品,密封靜置備用。
按本方法共制備3批,批號分別為:N19040201、N19040202、N19040203。
2.2 測定方法
2.2.1 色譜條件 色譜柱:Agilent Eclipse Plus C18(4.6 mm×150 mm,3.5 μm);流動相A:0.05 mol·L-1乙酸銨緩沖溶液(稱取乙酸銨3.8 g,加水溶解并稀釋至1000 mL,用冰醋酸調節(jié)pH值至4.0),流動相B:甲醇,按表1進行梯度洗脫;流速:1 mL·min-1;檢測波長:254 nm;柱溫:35 ℃;進樣量:10 μL。
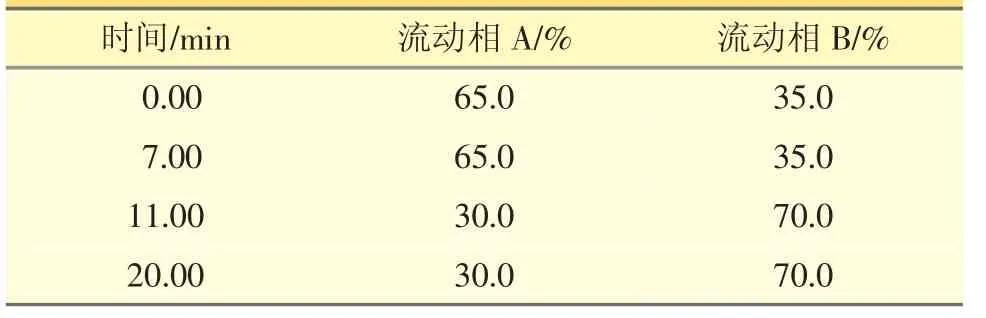
表1 梯度洗脫程序
2.2.2 地西泮對照品溶液配制 精密稱定地西泮原藥50 mg,置于25 mL量瓶中,加稀釋劑(乙酸銨緩沖溶液/甲醇=65∶35)溶解稀釋至刻度,搖勻,作為地西泮對照品儲備液;精密吸取該儲備液2.5 mL至50 mL量瓶中,加稀釋劑稀釋至刻度,搖勻,制成含地西泮0.1 mg·mL-1的對照品溶液。
2.2.3 苯甲酸對照品溶液配制 精密稱定苯甲酸359 mg,置于25 mL量瓶中,加稀釋劑溶解并定容至刻度,搖勻,作為苯甲酸對照品儲備液;精密吸取該儲備液2.5 mL至50 mL量瓶中,加稀釋劑稀釋至刻度,搖勻,制成含苯甲酸718 μg·mL-1的對照品溶液。
2.2.4 苯甲醇對照品溶液配制 精密稱定苯甲醇對照品300 mg,置于50 mL量瓶中,加稀釋劑溶解并定容至刻度,搖勻,作為苯甲醇對照品儲備液;精密吸取該儲備液2.5 mL至50 mL量瓶中,加稀釋劑稀釋至刻度,搖勻,制成含苯甲醇0.3 mg·mL-1的對照品溶液。
2.2.5 混合對照品溶液配制 分別精密吸取地西泮對照品儲備液、苯甲醇對照品儲備液、苯甲酸對照品儲備液各1.0 mL,置于20 mL量瓶中,加稀釋劑稀釋至刻度,搖勻,即為混合對照品溶液。
2.2.6 供試品溶液配制 精密稱定地西泮直腸凝膠樣品(批號為19040201)1.0 g至50 mL量瓶中,加稀釋劑溶解并定容至刻度,搖勻,即為供試品溶液。
3 結果
3.1 系統(tǒng)適用性及專屬性考察
分別精密量取地西泮對照品溶液、苯甲酸對照品溶液、苯甲醇對照品溶液、混合對照品溶液、稀釋劑各10 μL,按“2.2.1”項下色譜條件分別進樣。
結果表明,地西泮、苯甲酸和苯甲醇的分離度均大于1.5,達到基線分離。理論塔板數(shù)均大于15 000。見圖1。
3.2 線性關系考察
精密量取地西泮對照品溶液、苯甲酸對照品溶液、苯甲醇對照品溶液各0.1、0.2、0.5、0.8、1.0、1.5、2.0 mL,分別置于50 mL量瓶中,加稀釋劑稀釋成一系列不同濃度的對照品溶液,按“2.2.1”項下色譜條件分別進樣10 μL。以峰面積(Y),濃度(X,μg·mL-1)進行線性回歸,得地西泮、苯甲酸和苯甲醇回歸方程與線性范圍,見表2。結果表明,地西泮、苯甲酸和苯甲醇線性關系均良好,r2均≥0.999 8。
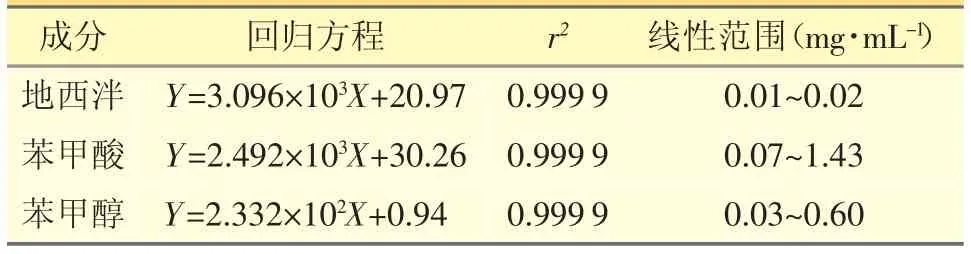
表2 線性關系考察結果
3.3 定量限設定
取“2.2.5”項下混合對照品溶液,逐級稀釋后進樣測定,按峰高為噪音10倍測得量為定量限。結果表明地西泮、苯甲酸、苯甲醇的定量限分別為0.10、0.18、1.00 μg·mL-1。
3.4 進樣精密度試驗
精密吸取同一混合對照品溶液10μL,按“2.2.1”項下色譜條件重復進樣6次,記錄峰面積,測得地西泮、苯甲酸、苯甲醇峰面積的RSD分別為0.02%、0.03%、0.04%(n=6)。表明精密度均良好。
3.5 穩(wěn)定性試驗
精密吸取“2.2.6”項下的供試品溶液10 μL,按“2.2.1”項下色譜條件,分別在0、1、2、4、6、12、24 h進樣測定,記錄峰面積,測得地西泮、苯甲酸、苯甲醇峰面積的RSD分別為0.11%、0.32%、0.19%,表明供試品溶液在24 h內穩(wěn)定。
3.6 重復性試驗
稱取同一批地西泮直腸凝膠樣品(批號N19040201),按“2.2.6”項下制備方法平行制備供試品溶液6份,按“2.2.1”項下色譜條件,進樣測定,分別記錄每份供試品溶液中地西泮、苯甲酸、苯甲醇的峰面積,地西泮、苯甲酸、苯甲醇的平均含量的RSD分別為1.92%、1.50%、1.37%。表明該方法重復性良好。
3.7 加樣回收率試驗
稱取同一批已知含量的地西泮直腸凝膠(批號N19040201)9份,每份1.0 g,分別置于25 mL量瓶中,精密量取地西泮、苯甲酸、苯甲醇對照品溶液3.5、2.5、1.5 mL各3份,加入上述量瓶內(加入水平依次為80%、100%、120%),加稀釋劑溶解并稀釋至刻度,搖勻;精密量取上述溶液5 mL,分別置于20 mL量瓶中,加稀釋劑溶解并定容至刻度,搖勻,按“2.2.1”項下色譜條件分別進樣10 μL,記錄峰面積,以外標法計算3種成分的含量及回收率,結果見表3。地西泮、苯甲酸和苯甲醇的平均回收率均在98%~101%,RSD均小于2.0%(n=9)。表明該方法回收率符合要求。
3.8 耐用性檢測
取同一批供試品溶液(批號N19040201),分別在pH值3.8、4.0、4.2,流速0.8、1.0、1.2 mL·min-1,柱溫30 ℃、35 ℃、40 ℃條件下進樣,記錄峰面積,并考察各成分峰之間的分離情況,結果見表4。地西泮、苯甲酸、苯甲醇的分離度均大于1.5,理論塔板數(shù)均大于15 000,各成分含量測定值的RSD值均在限定范圍內(≤2.00%),本方法耐用性良好。
3.9 樣品測定
精密稱定不同批號樣品2.0 g,各2份,按“2.2.6”項下方法制備供試品溶液,依照“2.2.1”項下色譜條件進樣測定,記錄峰面積,以外標一點法分別計算地西泮、苯甲酸、苯甲醇的含量,結果見表5。
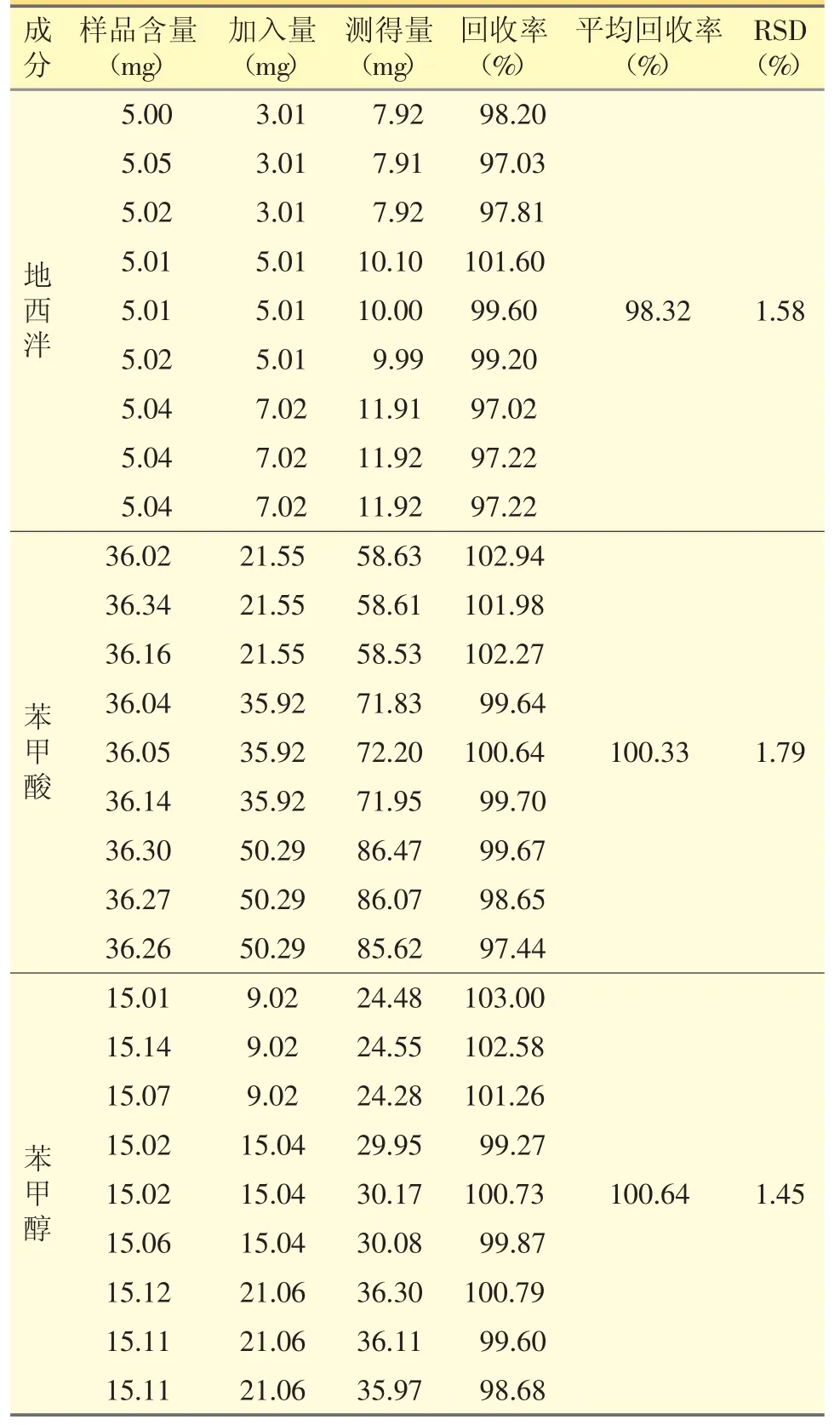
表3 加樣回收率試驗結果(n=9)
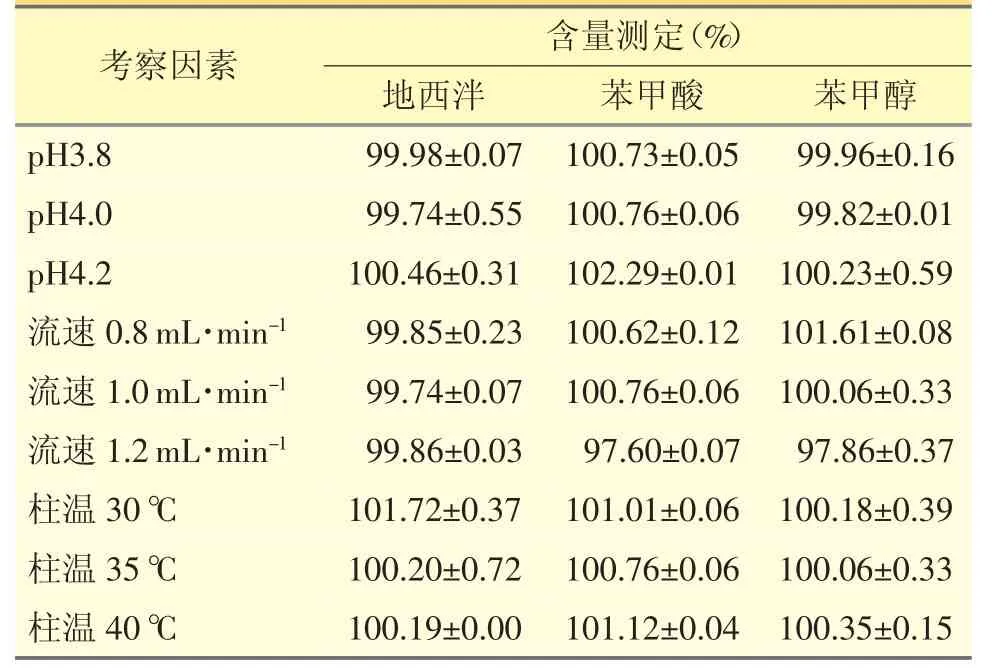
表4 耐用性考察因素及實驗結果(n=2)
4 討論
4.1 流動相pH值的選擇
本實驗選擇乙酸鹽緩沖液作為流動相和稀釋劑,其pH值是4.0,苯甲酸鈉在此條件下可完全轉化成苯甲酸。
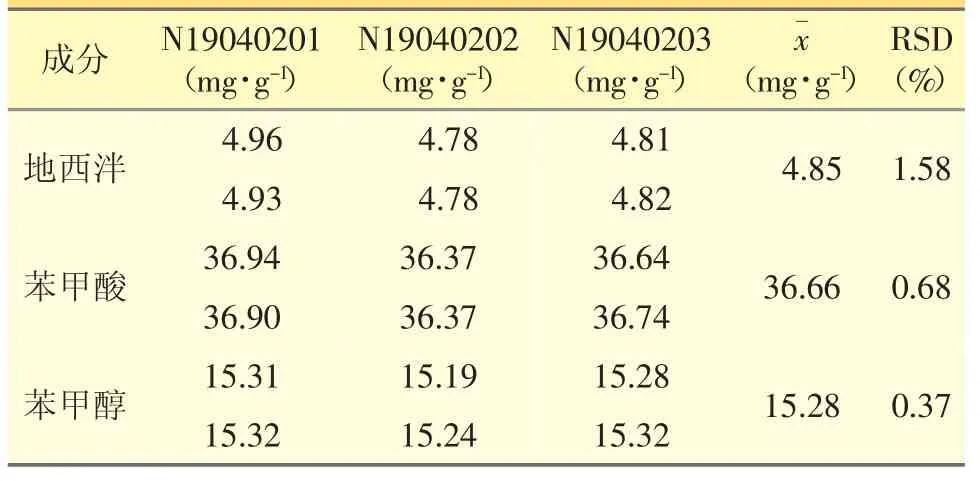
表5 3批地西泮直腸凝膠中地西泮、苯甲酸、苯甲醇含量檢測結果(n=2)
4.2 流動相比例的選擇
苯甲酸和苯甲醇需要在高比例水相下出峰,地西泮需要在高比例有機相下出峰,本方法結合3種成分的出峰位置和峰形,選用梯度洗脫程序。本法選用的梯度洗脫程序可同時用于地西泮直腸凝膠有關物質的檢測,在地西泮峰和苯甲酸峰相隔時間內可檢測到其他雜質峰。如果只用于含量檢測,可通過進一步優(yōu)化,縮短檢測時間。
本實驗可在同一色譜條件下,同時測定地西泮直腸凝膠中地西泮、苯甲酸、苯甲醇的含量,方法簡便準確,為有效控制地西泮等成分的含量提供了科學依據(jù)。

