人星狀病毒核酸檢測方法的建立及應用
桑筱筱,操燕明,楊艾玲,王敬,杜松云
(武漢華夏理工學院,湖北武漢 430223)
人星狀病毒(human astrovirus,HAstV)是導致嬰幼兒、老年人以及免疫功能缺陷者腹瀉的重要病原體之一[1-2]。Madeley等人在1975年首次從腹瀉嬰兒糞便中分離得到球形、直徑為28~35 nm、無包膜、電鏡下表面結構呈星形且表面有5~6個星狀突起的病毒顆粒,因此命名為星狀病毒[3]。HAstV感染率僅次于輪狀病毒和諾如病毒,檢出率在2%~10%[4]。HAstV是無包膜單股正鏈RNA病毒,基因組全長約 7 kb,包含 3個開放讀碼框(ORFla、ORFlb、ORF2),其中ORFla和ORFlb編碼非結構蛋白,ORF2編碼衣殼蛋白。根據ORF2的348 bp核苷酸片段差異可將人星狀病毒劃分HAstV 1~8基因型,與其血清型的劃分是一致的[5-6]。人星狀病毒起初在實驗室的診斷主要利用電鏡鑒定以及免疫學方法,但準確度不夠,這些檢測方法在一定程度上限制了為腹瀉患者提供最佳的初始診斷和后續的治療。因此,需要一種可靠、快速的診斷工具。實時逆轉錄聚合酶鏈反應(RT-qPCR)已經取代了病毒培養和血清學等不敏感和耗時的技術,用于診斷病毒性胃腸道疾病。目前,HAstV的診斷依賴于分子診斷,用RT-PCR方法檢測病毒RNA。因此,開發一種經濟有效的RT-qPCR方法,用于檢測臨床標本中的HAstV,這對優化臨床管理至關重要,可以減少不必要的抗生素使用,并允許在適當情況下使用抗病毒藥物。
1 材料和方法
1.1 臨床標本
研究采用的高溫滅活人星狀病毒上清液來源于武漢大學病毒國家重點實驗室,共計12份;對象為2018年12月—2019年6月就診的腹瀉感染患兒195例,均為急性腸胃炎感染患者。
1.2 病毒核酸的提取
提取試劑為德國Qiagen公司的QIAamp min Elute virus spin kit,根據試劑盒的說明書操作,用200 μL臨床標本提取病毒核酸,用100 μL洗脫液洗脫,如24 h內未檢測,放-80 ℃保存。
1.3 引物及探針設計
根據GenBank上公布的HAstV全基因組序列,選取基因組中比較保守的ORF2基因保守序列設計引物和探針,上游引物為5’-TCAACGTGTCCGTAA MATTGTCA-3’,下游引物為5’-TGCWGGTTTTGGTCC TGTG A-3’;探針為FAM-CAACTCAGGAAACARGMGB-BHQ-1。引物和探針合成由上海生工生物技術有限公司完成。
1.4 構建陽性質控品
PCR擴增HAstV ORF2基因,反應體系為25 μL,反應條件為42 ℃,30 min;95 ℃,5 min,95 ℃,3 min,60 ℃,1 min,共35個循環。擴增產物為88 bp。PCR產物回收后與pGEM-T載體進行連接,轉化大腸桿菌,藍白篩選后,獲得重組陽性質粒pGEMT-ORF2。
1.5 建立標準曲線
計算出重組質粒pGEMT-ORF2初始拷貝數,10倍倍比稀釋,分別稀釋為1×106copies/L、1×105copies/L、1×104copies/L 以及1×103copies/L,實時RT-qPCR,獲取標準曲線,進而確定線性范圍。
1.6 準確度試驗
對12份人星狀病毒上清液進行準確度試驗,測試擴增反應準確性。
1.7 特異性試驗
分別取臨床上可見的消化道病毒,如輪狀病毒、諾如病毒、腸腺病毒、札如病毒、腸道病毒和致病性大腸桿菌,測試擴增反應特異性。
1.8 RT-qPCR擴增
利用RT-qPCR方法對收集到的195份臨床標本進行檢測。反應體系:10×Buffer(含Mg2+)5.0 μL,dNTP Mix(每管 2.5 mmol)4.0 μL,上下游引物終濃度均為0.4 μmol/L,TaqMan探針0.2 μmol/L,Taq DNA聚合酶4.0 μL,M-MLV逆轉錄酶1.0 μL,RNA酶抑制劑0.5 μL,模板10 μL,加純水至終體積50 μL。RT-qPCR反應條件為:42 ℃,30 min;95 ℃ ,3 min,95 ℃,10 s;60℃,3 min,共 40 個循環。
2 結果與分析
2.1 pGEMT-Easy-ORF2目的基因普通PCR檢測結果
對pGEMT-Easy-ORF2進行擴增,凝膠電泳檢測為單一條帶,大小在130 bp左右,與對照條帶127 bp相符(見圖1),表明重組質粒pGEMT-Easy-ORF2構建成功。
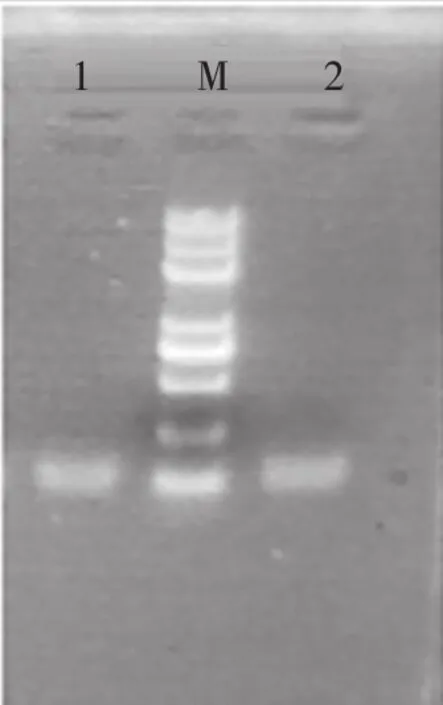
圖1 pGEMT-Easy-ORF2目的基因普通PCR檢測結果
2.2 實時熒光定量PCR的標準曲線的建立
圖2為人星狀病毒靈敏度試驗結果。當標準品濃度為1×106~1×103copies/L時,拷貝數與其對應的CT值之間呈現良好的線性關系,相關系數R2為0.999,線性關系為y=-4.166x+39.37,可對未知濃度的HAstV進行定量。
2.3 實時熒光定量PCR的準確性試驗結果
如圖3所示,對來源于武漢大學病毒國家重點實驗室的高溫滅活的人星狀病毒上清液,共計12份進行準確度試驗,準確度達100%。

圖2 人星狀病毒靈敏度試驗
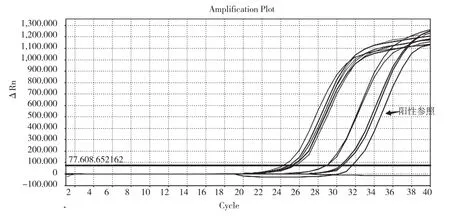
圖3 人星狀病毒上清液準確性試驗
2.4 實時熒光定量PCR的特異性試驗結果
如圖4所示,對HAstV和消化道病毒如輪狀病毒、諾如病毒、腸腺病毒、札如病毒、腸道病毒、致病性大腸桿菌進行特異性檢測,檢驗結果無交叉反應。
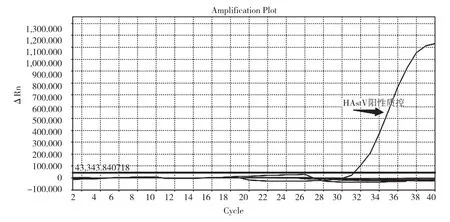
圖4 特異性試驗
2.5 RT-qPCR檢測結果
如圖5所示,應用RT-qPCR方法對195份臨床樣本進行檢測,檢測陽性標本15份,陽性率為7.7%。
3 討論與結論
目前,研究HAstV的主要方法是傳統PCR等技術[7-8]。上述方法存在操作復雜繁瑣,特異性較差、靈敏度不高等缺點,大大限制了對人星狀病毒檢測的臨床研究。為了實現對人星狀病毒操作簡易、時間快速、特異性高的檢測,本論文建立了人星狀病毒進RT-qPCR檢測研究方法。選取人星狀病毒ORF2基因保守片段設計引物和探針,對常見消化道病原體如輪狀病毒、諾如病毒、腸腺病毒、札如病毒、腸道病毒、致病性大腸桿菌等進行特異性檢測;對195份樣本進行檢測,15份樣本陽性,陽性率占比7.7%,由于樣本量較少,靈敏度還需進一步加以研究和證實。

圖5 臨床應用檢測
綜上所述,本研究成功建立了人星狀病毒RT-qPCR檢測技術手段,實現了對臨床樣本中人星狀病毒的檢測,具有快速、靈敏度高、特異性強等優點,為人星狀病毒感染的臨床診斷提供了一個輔助方法。

