膽胰分流并十二指腸轉位術治療胃袖狀切除術后復胖個案報告并文獻復習
張 鵬,陳麗華,黃曉娜,伍 雯,章 雄,朱萍芳
(1.首都醫科大學附屬北京友誼醫院普通外科中心,北京,100050;2.復旦大學附屬浦東醫院糖尿病與肥胖外科;3.復旦大學附屬浦東醫院手術室)
近年,我國肥胖癥的流行趨勢呈現兩個特點,一是發病率持續攀高,二是肥胖程度越來越嚴重。對于重度肥胖癥及病理性肥胖癥,代謝與減重手術是最有效的治療方法,一方面可快速大量減輕體重,另一方面可快速緩解肥胖相關合并癥,包括2型糖尿病(type 2 diabetes mellitus,T2DM)、高血壓、高脂血癥、非酒精性脂肪性肝炎、睡眠呼吸暫停綜合征等。代謝與減重手術按照作用機制通常可分為三類,第一類:以減少攝食量為主的手術,如胃袖狀切除術(sleeve gastrectomy,SG)、可調節胃綁帶術(adjustable gastric banding,AGB);第二類:以減少營養在小腸吸收為主的術式,如膽胰分流并十二指腸轉位術(biliopancreatic diversion with duodenal switch,BPD/DS);第三類:同時減少營養攝入與吸收的術式,如Roux-en-Y胃旁路術(Roux-en-Y gastric bypass,RYGB)。目前全球范圍內及我國施行最多的減重手術為SG與RYGB,此外,AGB、BPD/DS也是國際專業學會的推薦術式,由于AGB術后綁帶相關并發癥發生率較高,目前施行數量越來越少,而BPD/DS由于技術難度、患者管理問題,施行量一直不多,且僅限于少數一些中心。整體而言,各種手術有各自的適應證,臨床結局各有利弊,按照減重與肥胖相關代謝病的臨床治療效果,從高到低依次為BPD/DS>RYGB>SG>AGB,而手術難度、風險及遠期營養并發癥的發生率由高到低也同樣為BPD/DS>RYGB>SG>AGB[1]。標準的BPD/DS由兩部分組成,包括一個較大胃囊的SG及較長長度的小腸旁路曠置。全球范圍內的薈萃研究結果表明,BPD/DS術后,遠期多余體重減輕率平均為70%,T2DM、高脂血癥與高血壓的臨床緩解率分別為99%、99%與83%[2],因此從治療肥胖與相關代謝紊亂性疾病方面看,BPD/DS是目前各種代謝與減重手術中最為有效且臨床結局最為確切的術式。
目前,BPD/DS手術越來越受到關注,一方面是因為對于超級肥胖癥和/或病史較長的糖尿病,BPD/DS作為初次手術具有較其他手術方式更優的臨床結局,另一方面,隨著越來越多的SG與RYGB手術后遠期復胖與T2DM復發而面臨需要再次修正手術的問題,BPD/DS是最有效的術式,因而在全球范圍內其數量有增加趨勢,以美國為例,2017年,BPD/DS占減重手術總數量的0.7%,約1 600例。根據國際肥胖及相關代謝病外科聯合會估算,全球范圍內,BPD/DS占比為1%~2%[3]。2015年10月筆者為一例女性肥胖合并T2DM患者施行腹腔鏡胃袖狀切除術(laparoscopic sleeve gastrectomy,LSG),術后3年因復胖、T2DM復發,經多學科討論,再次行腹腔鏡BPD/DS術,現將其病例資料作一總結匯報,并對BPD/DS作為SG術后復胖的修正手術進行討論。
1 資料與方法
1.1 首次SG時的病例資料 患者女,51歲,身高162 cm,體重111 kg,身體質量指數(body mass index,BMI)42.3 kg/m2,腰圍142 cm,臀圍132 cm,同時患有T2DM,病史10年。應用優泌林,按早24單位、中午8單位、晚20單位的方案皮下注射,血糖依然控制不佳,空腹血糖(fasting plasma glucose,FPG)12.7 mmol/L,糖化血紅蛋白(hemoglobin A1c,HbA1c)10.5%。此外,患者有慢性阻塞性肺病與哮喘病史10余年,8年前曾患腦梗塞,并有“冠心病”、慢性胃竇炎,10余年前曾行膽囊切除術、闌尾切除術,兩年前曾因“肺結節”行肺結節切除術,術后病理報告提示為良性炎癥,此外,患者對頭孢類、青霉素類藥物過敏。經過多學科評估討論,經過積極改善呼吸功能后,于2015年10月14日在全麻下行LSG,充分游離胃大彎、胃底部,經口置入36Fr胃定標管至胃幽門,距胃幽門環近端約4 cm處起始,應用直線切割閉合器沿胃定標管進行袖狀胃切除術,直至胃底部距His角約1 cm處,應用可吸收縫線全層連續加固縫合胃切緣,術中胃鏡檢查無吻合緣漏、袖狀胃無梗阻、胃腔內無出血后,取出被切除的部分胃,關腹,術畢。初次LSG術后3個月,體重降至95 kg,BMI為36.2 kg/m2,停用胰島素治療,改為口服二甲雙胍1 000 mg/d,FPG降至8.7 mmol/L,HbA1c 7.6%;術后1年,體重降至85 kg,BMI 32.4 kg/m2,繼續維持口服二甲雙胍治療,FPG 10.5 mmol/L,HbA1c 8.9%;術后2年,體重反升至99.5 kg,BMI 37.9 kg/m2,FPG 6.6 mmol/L,HbA1c 9.1%,重新啟動胰島素治療,外加口服二甲雙胍1 000 mg/d;術后3年,體重進一步反升至105.6 kg,BMI 40.2 kg/m2,腰圍129 cm,臀圍110 cm,胰島素51 IU/d,HbA1c為10%。因為體重反彈至重度肥胖水平、糖尿病進展及患者意愿,經多學科討論,決定再次行修正手術,鑒于患者T2DM病史較長,且個人飲食依從性較差,難以控制食量,因此決定于2018年10月9日行腹腔鏡下BPD/DS術。
1.2 BPD/DS手術方法 全麻,經臍部建立氣腹,患者取頭高腳低平臥位,首先腹腔探查,見肝臟邊緣圓鈍,脂肪浸潤,原袖狀胃有所擴大,可順利置入60Fr胃定標管,右側膽囊窩及十二指腸與周圍組織、網膜粘連致密,左右下腹腸管與腹壁多處粘連,腹腔內未見明顯占位病灶。PD/DS術按照標準的手術參數設計進行,見圖1。沿胃大彎向遠側游離十二指腸球部,于幽門遠側2~3 cm處建立十二指腸球部后壁隧道,置入60 mm藍色直線切割閉合器橫斷十二指腸。調整體位,確認回盲部,由此處起沿回腸向近端測量100 cm,以3-0藍色縫線標記,然后繼續向近端測量150 cm,再次標記,將此處向右上腹部上提,與十二指腸近端切緣以雙層連續縫合方式行端側吻合。貼著吻合口,在吻合口近端以60 mm白色直線切割閉合器將小腸橫斷,近側斷端在距回盲瓣100 cm標志處與回腸進行側側吻合,這樣食物支長度為150 cm,共同支長度為100 cm,其余均為膽胰支。關閉小腸離斷與轉位所形成的腸系膜缺損,胃鏡檢查十二指腸回腸吻合口通暢,無吻合口漏、出血,關腹術畢。手術操作見圖2~圖5。

圖1 BPD/DS手術示意圖
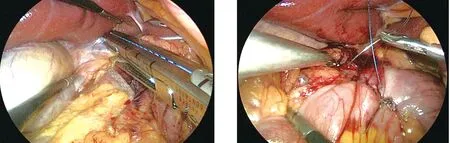
圖2 分離并切斷閉合十二指腸球部 圖3 十二指腸-回腸端側吻合,雙層連續縫合,吻合口距回盲瓣250 cm

圖4 在十二指腸-回腸吻合口輸入襻側切斷回腸,近側 圖5 以連續縫合方式關閉回腸切斷所形成的系膜裂孔斷端距回盲瓣100 cm處行回腸-回腸側側吻合
2 結 果
BPD/DS手術順利完成,用時185 min,術中出血120 mL,術后無發熱、消化道出血,術后第2天行上消化道造影,造影劑下行順利,未見梗阻或消化道瘺。術后經驗性停用胰島素治療。BPD/DS術后1個月,體重降至102 kg,術后3個月,降為99.5 kg,BMI 39.9 kg/m2,FPG 6.79 mmol/L,HbA1c 8.9%(圖6),恢復正常進食,排便次數3~4次/d,質軟,無特殊不適。
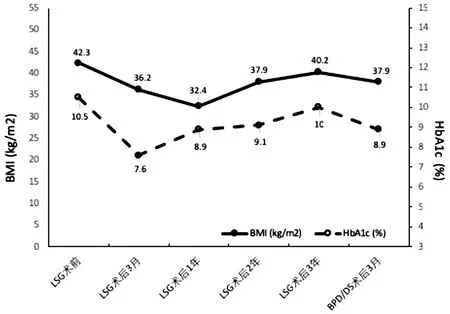
圖6 兩次手術前后BMI與HbA1c的變化
3 討 論
本例是較常見的初次LSG術后體重與血糖反彈的病例,在初次LSG前,其特點是BMI>40 kg/m2,腰圍142 cm,T2DM病史較長,大于10年,基礎疾病較多,包括心腦血管疾病、呼吸系統疾病;LSG術后,體重、血糖短期均有較明顯的下降,但術后飲食與鍛煉依從性不強,喜食高脂肪、高碳水化合物食物,1年后,體重、血糖達到最低后即開始反彈,并持續升高。術后第3年,患者BMI再次達到重度肥胖癥水平,應用胰島素,血糖控制依然不佳,經多學科討論,認為患者已施行過以縮小胃容積為主的LSG,再次LSG預期效果不佳,于是決定以減少營養吸收為主的BPD/DS作為修正術式,以期達到最佳效果,并盡可能小地影響患者的生活習慣。術后3個月,體重下降6.1 kg,停止胰島素治療,HbA1c較前也有明顯下降。
BPD/DS已有40年的歷史,1979年意大利的Scopinaro醫生首先報道了膽胰分流手術[4-5],胃小囊的制作方式是在胃體部中上三分之一處橫斷胃,并建立回腸與胃囊的Roux-en-Y式吻合,膽汁胰液直接輸入至回腸遠端,與食物支形成約120 cm的共同通道,為現代版的BPD/DS奠定了基礎。Scopinaro的膽胰分流手術盡管減重效果優異,但傾倒綜合征、邊緣性潰瘍發生率較高;1998年Hess等[6]、Marceau等[7]分別報道了Scopinaro手術加十二指腸轉位手術,即將小胃囊的制作方式改為SG,再行十二指腸轉位術,成為現代版BPD/DS的雛形,由于胃幽門的保留,傾倒綜合征、膽汁反流、邊緣性潰瘍的發生明顯減少。1999年Gagner等率先完成了腹腔鏡BPD/DS術[8],即應用60Fr的胃定標管做一個較大的SG,橫斷十二指腸球部,進行Roux-en-Y式的十二指腸轉位,最終形成150 cm的食物腸襻與50~100 cm的共同腸襻,這個方式成為目前標準版的BPD/DS。2000年Sudan率先應用手術機器人成功完成BPD/DS,由于機器手在十二指腸區域的精巧操作,手術時間顯著縮短,從而進一步提升了手術安全性,并使其學習曲線降為50例[9]。一直以來,BPD/DS被專業學會認可為一種標準的減重術式,它屬于以減少營養物質在小腸吸收為主的術式,同時輕度縮小胃容積,不論是作為重度肥胖癥和/或病史較長T2DM治療的一期手術,抑或其他減重手術后體重反彈、糖尿病復發的修正手術,尤其作為LSG術后的修正手術,BPD/DS均具有確切的優于其他現有減重手術的治療效果[10]。但術后遠期營養相關并發癥,尤其低蛋白血癥、脂肪性痢疾發生率較高,因而對術后患者管理也有較高要求。與Roux-en-Y胃旁路術相比,BPD/DS胃小囊通常較大,約為250 mL,胃幽門依然存在,因而BPD/DS術后進食習慣基本不受影響,傾倒綜合征較罕見,由于胃腔內壓力無明顯增高,較少惡心、嘔吐等。與RYGB手術相比,在營養管理方面,RYGB術后水溶性B族維生素、尤其B12缺乏較為常見,而BPD/DS手術后脂溶性維生素包括維生素A、D的缺乏較為常見,因而需要注意脂溶性維生素的補充,而且脂溶性維生素的補充應以水溶性制劑為主。此外BPD/DS術后草酸鹽結晶較多見,因而通常建議同步切除膽囊,此外,由于脂肪吸收顯著減少,因而排便次數增加,通常2~3次/d,并有脂肪吸收不全引起的惡臭味。
LSG是目前施行數量最多的減重術式,然而長期病例隨訪報道,LSG術后需再次修正的患者比例多于Roux-en-Y胃旁路術,有報道LSG術后10年修正率可達33%,修正手術患者中約66%是因為體重復胖[11]。LSG術后因復胖而需行修正手術的術式有再次SG、Roux-en-Y胃旁路術、BPD/DS術,或新近興起的“袖狀胃加”手術,選擇哪種術式進行修正一直是個有爭議的話題。LSG是以限制攝食量為主的減重術式,肥胖患者經歷一次限制攝食量的治療后由于機體保護機制的產生,再次行減少胃容積的手術,減重效果明顯差于首次手術;而以Roux-en-Y修正LSG,再次減重效果亦不理想,其原因可能與生活行為習慣較差相關,生理方面與小腸的適應能力、胃小囊出口缺乏括約肌功能相關,進食后食物較快進入空腸。而以減少食物在小腸吸收為主的BPD/DS,是LSG術后體重與血糖反彈最有效的手術,其優勢是多數情況下不必再次建立過小的胃囊,在首次LSG的基礎上只需進行十二指腸轉位即可,不影響患者已經形成的、難以改變的進食習慣,且再次減重與控制血糖的效果最佳,因而作為LSG術后的修正手術具有合理性。
此外,作為BPD/DS的簡化手術,新興的單吻合口十二指腸回腸旁路手術(single anastomosis duodeno-ileal bypass,SADI)[12-13]省去了標準BPD/DS的最后兩個步驟,即回腸輸入襻的離斷及回腸-回腸吻合,從手術技術層面而言,尤其因為省掉了回腸-回腸吻合,手術難度、所需時間均顯著下降;從手術相關并發癥而言,由于回腸離斷、再次吻合所帶來的吻合口梗阻及系膜缺損導致的內疝發生率也顯著降低;從手術效果來講,減重程度及對肥胖相關代謝性疾病的治療均接近BPD/DS,因而值得關注[14]。在本病例修正手術決策方面,MDT團隊曾反復斟酌采用SADI抑或BPD/DS,最終決定采用BPD/DS的原因主要是其為減重手術的標準術式,而SADI依然處于早期階段,臨床病例積累還不多[15]。隨著SADI手術臨床證據及經驗的不斷積累,未來甚至可能成為替代BPD/DS的術式。
綜上所述,LSG盡管是目前施行量最大的減重手術,然而術后遠期相當多的患者因為體重和/或血糖反彈而需行再次修正手術,整體而言,修正手術對體重、血糖的減輕及控制效果差于初次減重手術,因而BPD/DS是針對此類患者更為確切的術式。BPD/DS手術難度較大,且術后營養管理較為復雜,需要密切隨訪。新興起的SADI可能成為BPD/DS的替代手術之一,因而值得關注。

