太子參抗心肌缺血作用機制的網絡藥理學研究*
高 源,彭丹冰,方 燦,范東生
(1. 貴州省食品檢驗檢測所 貴陽 550004;2. 貴陽中醫藥大學第一附屬醫院 貴陽 550001)
心肌缺血是指心臟的血液灌注減少,導致心臟的供氧減少,心肌能量代謝不正常,不能支持心臟正常工作的一種病理狀態。心肌缺血引發的心肌梗死是患者死亡的重要原因。心肌缺血可致氧自由基大量增加,氧化應激又可進一步加重心肌缺血性損傷;而心肌梗死后的心室重塑及纖維化更是導致心功能下降的主要病理基礎。因此,尋找安全有效的防治心肌缺血損傷藥物具有重要意義[1]。
太子參為石竹科植物孩兒參Pseudostellariaheterophylla(Miq.)Pax ex Pax et Hoffm.的干燥塊根;甘、微苦,平;歸脾、肺經;益氣健脾,生津潤肺。用于脾虛體倦,食欲不振,病后虛弱,氣陰不足,自汗口渴,肺燥干咳[2]。太子參始載于《本草從新》,又名孩兒參、童參、雙批七、四葉參、米參,是傳統中成藥復方太子參口服液等品種主要原料;廣泛用于太子參黃精膠囊等各類保健食品方面。現代研究表明,太子參主要含有多糖類、皂苷類、環肽類、揮發油類等化學成分,文獻報道可知,這些成分具有:抗心肌缺血、提高免疫功能、抗氧化、抗癌、降血糖降脂等藥理作用[3-9]。
近年來,有關太子參抗心肌缺血的研究報道較多,如劉湘湘等,利用心肌缺血大鼠模型,以太子參多糖為給藥組,硝酸異山梨酯片作為對照組進行試驗,發現太子參對心肌缺血大鼠模型有保護作用;孫弼等,利用缺血再灌注損傷模型大鼠,顯示太子參多糖能顯著減輕心肌缺血再灌注損傷模型大鼠的心肌組織損傷,并抑制心肌細胞凋亡;吳靈群等通過大鼠心肌缺血模型,以太子參水提物進行灌胃,顯示其具有修復心梗大鼠促進缺血心肌組織的功效,通過研究太子參水提物對COCl2 誘導缺氧EA.hy926 細胞的修復作用,提示太子參水提物針對EA.hy926細胞損傷具有細胞增殖、遷移及小管形成作用[10-12]。
太子參在中醫臨床中多采用復方形式進行治療,如陳東等通過定心湯加太子參、合歡皮針對氣血兩虛型心臟神經癥進行臨床觀察,總有效率為77.5%,顯效人數為10人,占25%,采用定心湯合太子參、合歡皮治療心臟神經癥,可以有效地緩解患者心悸、胸痛、氣短、乏力等癥狀的發作程度,發作頻率及持續時間,提高患者的生活質量。在曹玉山教授辯治冠心病的臨床經驗一文中,作者采用自擬通冠湯為基礎方,采用黃芪、當歸、太子參等8 味藥材用于臨床治療冠心病,取得很好的療效,并且文中也提到,曹玉山教授在臨床中遇到氣血兩虛的冠心病患者,也會用太子參代替黨參使用,可見太子參在臨床治療中確有療效[13,14]。
雖然目前已有眾多學者針對太子參抗心肌缺血進行了全面研究,但從細胞及分子水平進行系統全面的揭示太子參是通過何種途徑發揮抗心肌缺血的作用機制鮮見報道,亟待進一步加強。傳統中醫藥研究,往往缺乏分子藥理表征,難以與現代科學有機的融合[15];而網絡藥理學在系統藥理學基礎上建立,利用生物醫藥領域數據的迅速增加與計算能力與實驗手段的快速進步,通過觀察藥物的整體性、系統性、與中醫藥傳統理論的特點不謀而合,為中醫藥復雜系統的研究提供了新的視角和思路[16-18]。因此,本研究利用網絡生物信息數據庫,初步預測太子參活性成分抗心肌缺血的作用靶點及信號通路,為揭示太子參抗心肌缺血的作用機制和太子參的深入研究及開發利用提供參考依據,技術路線見圖1。
1 方法
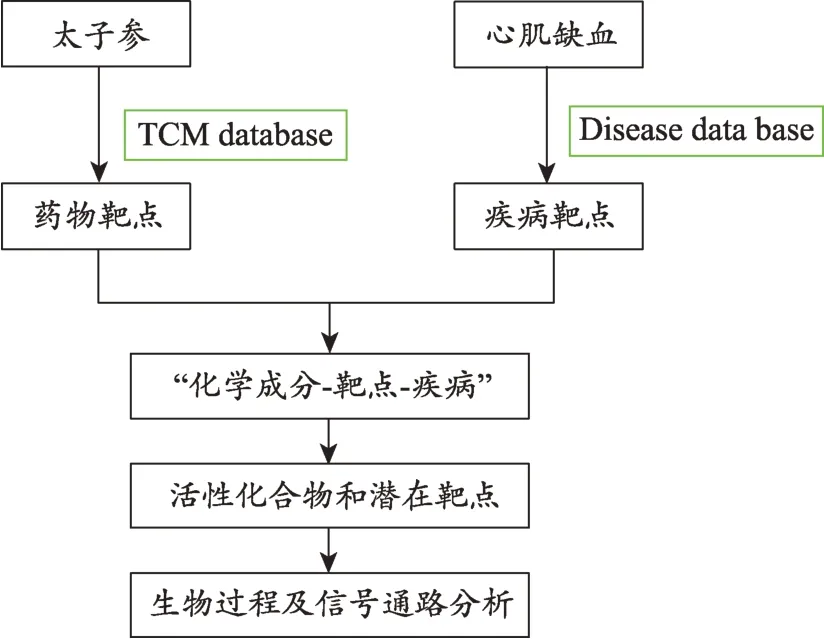
圖1 太子參抗心肌缺血作用機制的網絡藥理學技術路線圖
1.1 化學成分的建立
中醫藥綜合數據庫(Traditional Chinese Medicine Integrated Database,TCMID)和中藥系統藥理學分析平臺(Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform,TCMSP)檢索太子參的化學成分。
TCMID 數據庫收集了約 47000 個處方,8159 個中藥以及它們包含的25210 個主要成分,并且通過主要成分將它們與3791 個疾病,6828 個藥物和17521 個疾病相關的蛋白質關聯起來。其中中藥相關的數據以及中藥與西藥關聯的數據主要來源于現存的數據庫,以及通過人工文本挖掘的方法從發表的文章及書籍中獲得;西藥相關數據主要來在PubMed、OMIM、DrugBank、Uniprot等數據庫。
TCMSP 包括中國藥典注冊的499 種中藥,含29384 種成分,3311 個靶標和837 個相關疾病。該數據庫采用的是HIT 數據庫預測算法SysDT 來獲得藥物靶點之間的關系。該數據庫中的疾病信息來自TTD數據庫和PharmGKB 數據庫。這些信息可以在該數據庫中查詢和下載。該數據庫特別的價值在于,它為每種化合物提供了藥物藥代動力學信息,如成藥相似性(drug-likeness,DL)、口服生物利用度(oral bioavailability,OB)、血腦屏障(blood-brain barrier,BBB)、腸上皮通透性(Caco-2)、脂水分配系數(ALogP)和 H 鍵供體/受體(Hdon/Hacc)的數量。因此,通過這2 個數據庫,用戶可以較為全面,準確的搜索藥物化合物和作用靶點用于進一步研究。
1.2 活性成分的篩選
將太子參查詢所得的化學成分,根據藥物動力學(ADME)參數(OB ≥ 30%和DL ≥ 0.18)設置,進行活性化合物篩選。再通過PubChem 數據庫,查找活性化學成分的結構式。
1.3 藥物靶點與疾病靶點的建立
通過TCMSP 數據庫和SwissTargetPrediction 數據庫,查找太子參活性成分作用靶點,建立靶點數據集。通過人類基因和基因表型綜合數據庫(OMIM)、DrugBank 數據庫和TTD 數據庫查找對心肌缺血有治療預防作用的相關基因和蛋白靶點,建立抗心肌缺血的靶點數據集。
1.4 網絡構建與分析
通過蛋白互作(protein protein interaction,PPI)網絡分析,將太子參活性成分與心肌缺血相關聯的靶點蛋白,通過Cytoscape 3.6.1 軟件構建可視化的“活性成分-作用靶點-疾病”網絡,并得到每個節點的Degree、Betweenness centrality、Closeness centrality 三個拓撲參數,選擇以上3 個拓撲參數值均大于所有點中位數值的靶點,作為太子參抗心肌缺血的潛在作用靶點。
1.5 生物過程分析
將篩選出的關鍵靶點使用生物學信息注釋數據庫(Database for Annotation, Visualization and Integrated Discovery,DAVID)數據庫進行KEGG 通路分析和GO生物學過程分析。然后再利用STRING 對篩選出的潛在靶點進行蛋白互作關系分析。
1.6 構建太子參心肌缺血作用的通路圖
利用KEGG 信號通路數據庫,將與心肌缺血最為密切的靶點在信號通路上標注出來,驗證太子參抗心肌缺血作用的主要信號通路。
2 結果
2.1 活性成分的篩選
通過TCMSP 數據庫和TCMID 數據庫,共查找得到太子參25 個化學成分,以ADME 參數(OB ≥30%和DL ≥0.18)為標準,共篩選得到8個活性化合物及結構式,包括Supraene(角鯊烯)、Acacetin(刺槐素)、Linarin(蒙花苷)、Beta-sitosterol(β-谷甾醇)、Luteolin(木犀草素)、Taraxerol(蒲公英賽醇)、Schottenol(仙人掌甾醇)、1-Monolinolein(1-亞油酸甘油單酯),具體結果見表1。
2.2 藥物靶點和疾病靶點數據的篩選
通過TCMSP 數據庫和SwissTargetPrediction 數據庫,剔除重復靶點后,共篩選得到858個太子參活性化學成分的作用靶點,結果見表1。通過疾病靶點數據庫,查找得到418 個心肌缺血相關的靶點。通過PPI網絡分析,將靶點導入數據庫,篩選出54個交互蛋白,構建蛋白互作網絡,可直觀的看出活性化學成分與疾病靶點之間的網絡關系,結果見圖2。其中,黃色方形與黃色圓點分別代表最重要的靶點蛋白和作用靶點;紅色三角形代表活性化學成分;藍色圓點為活性化學成分的作用靶點;紫色圓點代表連接活性化學成分與疾病靶點的交互蛋白。
2.3 太子參抗心肌缺血作用的靶點拓撲參數分析
將太子參活性成分與心肌缺血相關聯的靶點蛋白,通過Cytoscape 3.6.1 構建活性成分-作用靶點網絡,并對這些靶點蛋白進行拓撲參數計算。得到中位數均值為 Degree:4.0、Betweenness centrality:0.002 6、Closeness centrality:0.241 6。根據中位數值,篩選出12 個靶點,結果見表2。將12 個潛在靶點蛋白進行蛋白互作關系分析,結果見圖3。蛋白互作關系分析說明太子參抗心肌缺血的潛在靶點蛋白相互關聯且彼此調節。
2.4 GO生物學功能分析
將太子參心肌缺血疾病與活性成分匹配得到的12 個潛在靶點,映射到 DAVID 數據庫中,利用 GO 生物學功能富集分析,太子參抗心肌缺血所涉及的生物過程共富集得到116 條,其中P≤0.001 的生物過程共有25條,結果見表3。結果表明,太子參抗心肌缺血與多個生物過程的調控相關,其中最為密切的生物過程包括內皮細胞增殖的正調節、細胞對缺氧的反應、細胞對血管內皮生長因子刺激的反應、一氧化氮生物合成過程的積極調節、肽基絲氨酸磷酸化的正調節、血管內皮生長因子受體信號通路的正調節、血管生成的積極調節、血管生成、血管內皮生長因子受體信號通路等。說明太子參抗心肌缺血可能主要是通過調節血管內皮生長因子而發揮治療作用。
2.5 KEGG通路分析
將太子參心肌缺血疾病與活性成分匹配得到的12 個潛在靶點,映射到DAVID 數據庫中,通過KEGG通路富集得到34 條信號通路,其中22 條信號通路(P≤0.01),結果見表4;其中與太子參抗心肌缺血作用機制密切相關的主要信號通路包括HIF-1 信號通路、PI3K-Akt信號通路、細胞凋亡、甲狀腺激素信號通路、肌萎縮側索硬化癥(amyotrophic laternal sclerosis,ALS)、mTOR 信號通路、Rap1 信號通路、VEGF 信號通路等。同時利用KEGG 信號通路數據庫中的KEGG Mapper 功能將12 個潛在靶點蛋白,在PI3K-Akt 信號通路上標注出來,結果顯示有7 個靶點蛋白參與PI3K-Akt信號通路的相關調控,結果見圖4。
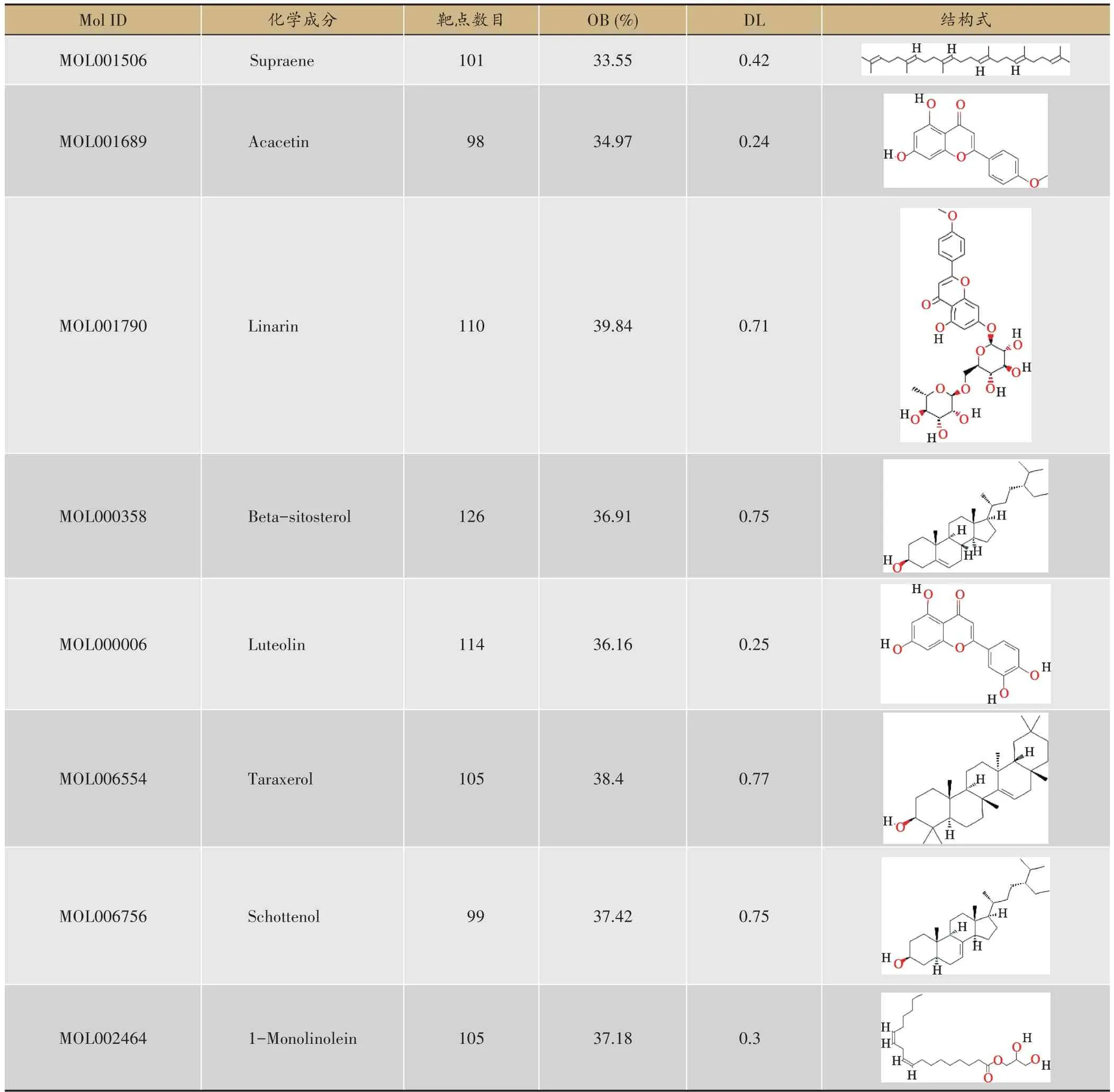
表1 太子參活性化合物及靶標數
3 討論
太子參在我國具有悠久的歷史,同時也具有豐富的資源。目前,太子參被廣泛應用于保健食品和藥品等方面;但由于太子參所含的化學成分的非常復雜,難以系統全面的揭示其藥效物質基礎和作用機制,不利于太子參進一步研究。通過網絡藥理學方法進行分析,構建“成分-靶點-疾病”關系,為中藥藥效物質基礎和作用機制的研究提供了新的思路和方法,進一步推動了中醫藥的快速發展。
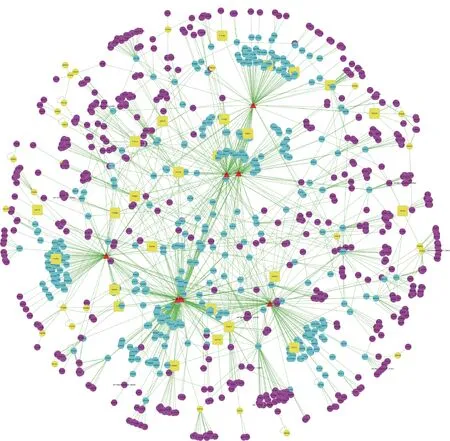
圖2 太子參抗心肌缺血的“成分-靶點-疾病”交互網絡

表2 太子參活性成分抗心肌缺血的潛在靶點相關拓撲參數
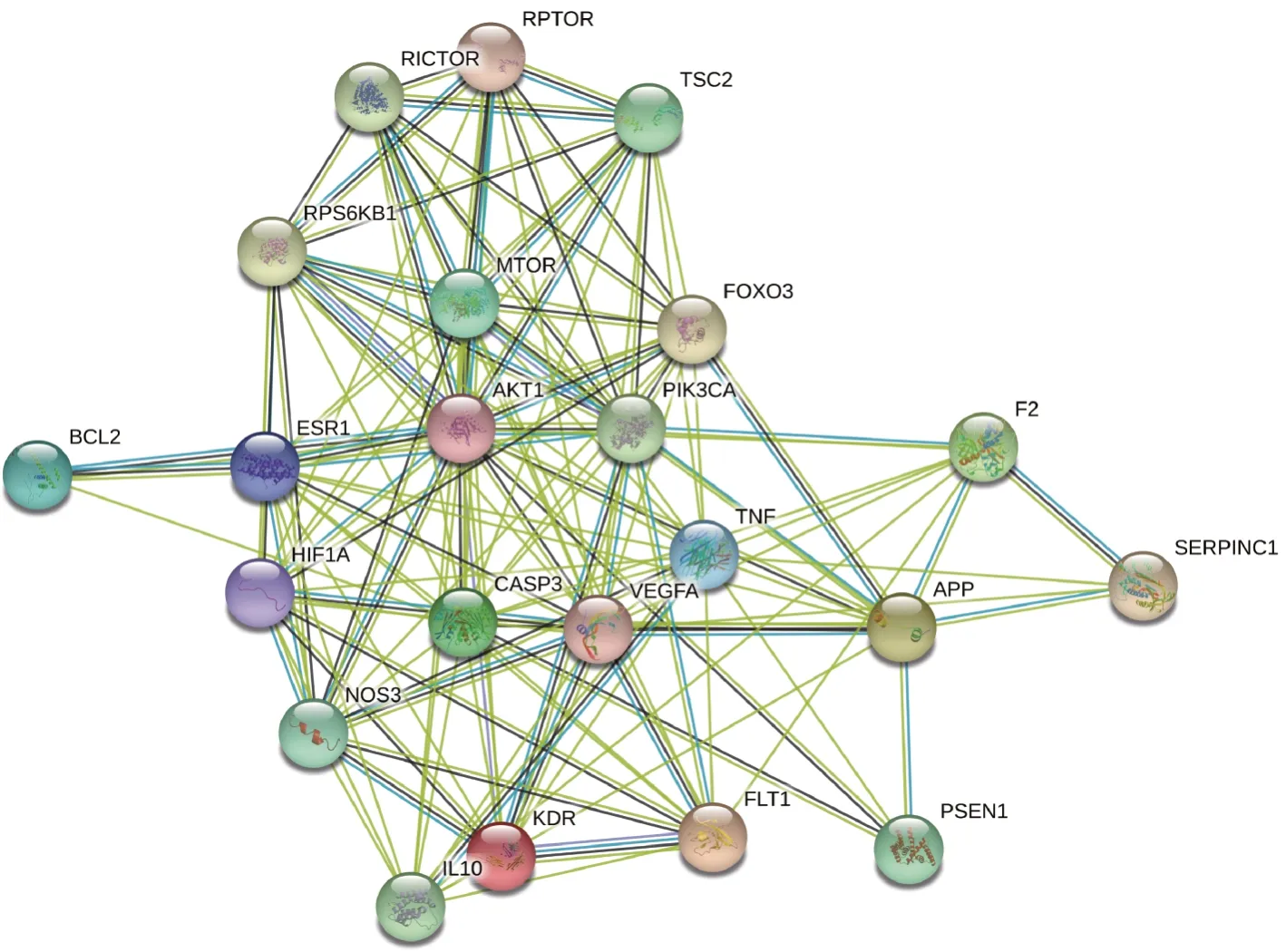
圖3 太子參抗心肌缺血作用的靶點蛋白互作關系圖

表3 太子參抗心肌缺血的GO生物學功能富集分析結果
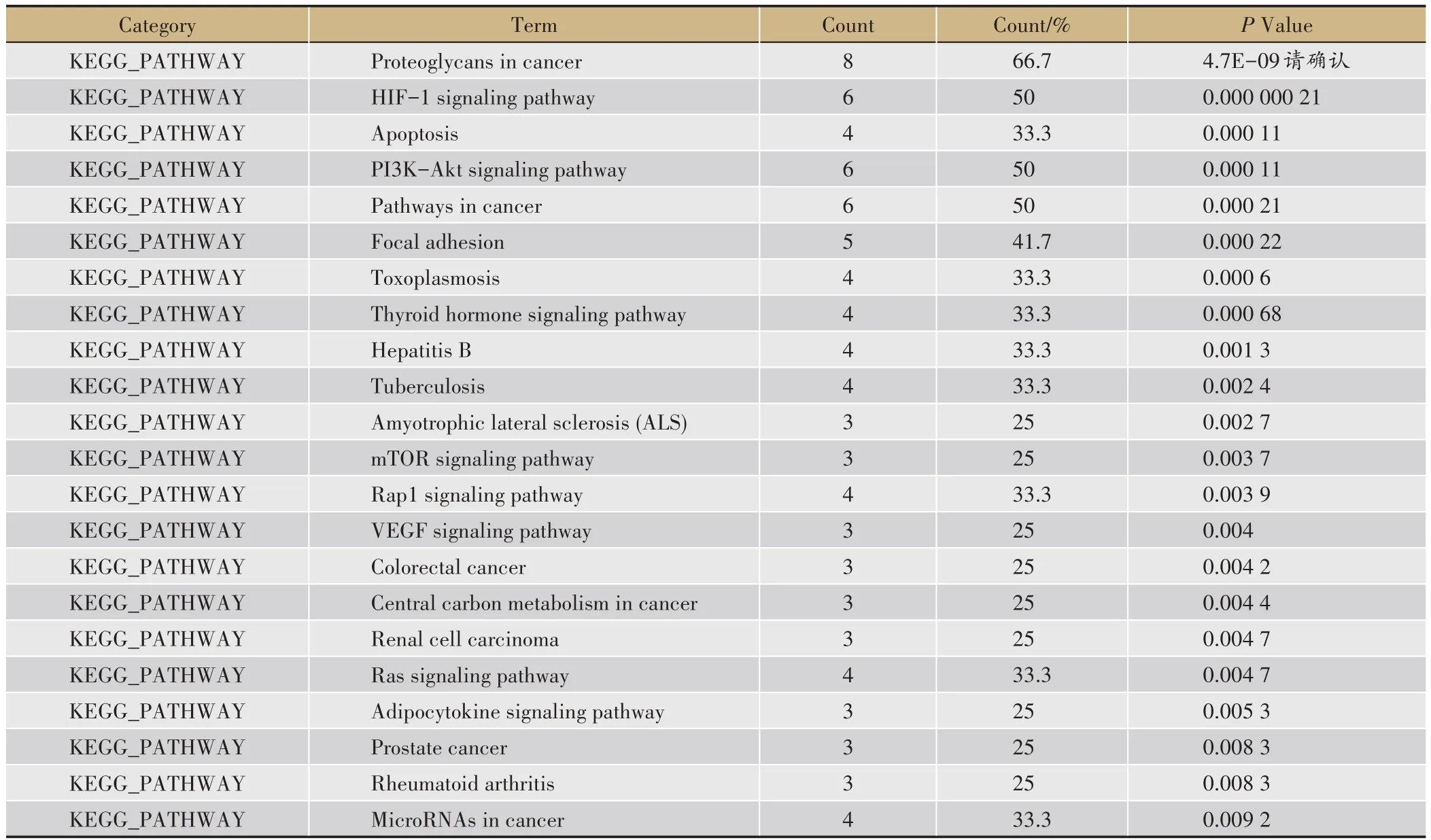
表4 太子參抗心肌缺血的KEGG通路富集分析結果

圖4 太子參活性成分潛在靶點在PI3K-Akt信號通路上的標注圖
本研究通過網絡藥理學方法,利用TCMSP、TCMID、TCMIP、BATMAN-TCM 數據庫,篩選得到了8個太子參活性化學成分以及與太子參抗心肌缺血直接相關的12 個潛在作用靶點,根據文獻報道,戴宇翔等通過臨床收集冠狀動脈完全閉塞病變患者,觀察VEGFA、HIF-1α對心肌缺血影響,結果表明,慢性持續缺血、缺氧所導致的HIF-1α和VEGF 表達增加在促進冠狀動脈側枝循環的建立、增加心肌血供給、改善預后、減少臨床心功能不全的發生率方面具有重要意義,張宏如等學者通過電針干預心肌缺血再灌注損傷大鼠心肌組織,發現電針干預對心肌保護效應,是通過提高Bcl-2 表達、降低Beclin1 表達以抑制再灌注期的過度自噬而實現的。叢濱海在博士論文中發現雌激素對SGK 表達的調節,并探討了雌激素、UCNs-CRHR2、SGK 之間的關系,發現雌激素可以通過UCNs-CRHR2系統間接上調心肌細胞SGK 表達,這可能是雌激素在心肌缺血時增強心肌對缺血損傷抵抗力的一種重要分子機制[19-21]。利用GO 生物富集和KEGG 通路注釋分析功能,發現34 條信號通路及116個生物過程參與太子參的抗心肌缺血作用,其中與太子參抗心肌缺血作用機制密切相關的主要信號通路包括HIF-1 信號通路、PI3K-Akt 信號通路、細胞凋亡、甲狀腺激素信號通路、ALS、mTOR信號通路、Rap1信號通路、VEGF信號通路。韋皓等[22,23]學者通過研究HIF-1α抗心肌缺血作用機制,可能通過抑制TLR4/NF-κB信號通路抑制炎癥因子的釋放,降低機體炎癥因子水平,改善MIRI心肌損傷,葉楨干等學者[24-26]運用PI3K-Akt信號通路,研究不同藥物抗心肌缺血再灌注損傷機制。獲得較好的實驗結果。刁思幃[27]等通過研究三氟淫羊藿素(ICTF)對大鼠心肌缺血再灌注損傷的治療作用,發現其機制可能與調控mTOR信號通路抑制細胞過度自噬有關。本文首次運用網絡藥理學挖掘和篩選,太子參的活性成分,并對其作用靶點與機制進行初步的篩選與分析,以期為太子參的保健食用價值提供科學依據,也為太子參的深入研究及開發利用提供參考。

