硫唑嘌呤不良反應文獻分析*
楊 霞,肖 敏,吳 斌,吳逢波
(四川大學華西醫院,四川 成都610041)
硫唑嘌呤(azathioprine,AZA)為甲基咪唑替代6-巰基嘌呤(6-MP)結構中的氫原子和硫原子所形成的非特異免疫抑制劑,在體內通過抑制淋巴細胞的增殖,發揮免疫抑制作用[1],廣泛應用于移植術后的免疫抑制治療及各類免疫性疾病如系統性紅斑狼瘡、炎癥性腸病、類風濕關節炎等。硫唑嘌呤常與糖皮質激素和(或)其他免疫抑制藥物聯用,但隨其廣泛應用,相關藥品不良反應(ADR)報道也逐漸增多。本研究中基于文獻報道分析了硫唑嘌呤的ADR,旨在為臨床合理用藥提供參考。
1 資料與方法
1.1 文獻檢索策略
以“硫唑嘌呤”和“不良反應”或“不良事件”或“安全性”為主題詞,對中國期刊全文數據庫(CNKI)、萬方數據庫和中文科技期刊全文數據庫(VIP)進行檢索,各數據庫檢索時限均為建庫至2019年7月。
1.2 納入與排除標準
納入標準:主要干預措施為硫唑嘌呤,包括ADR報告(A類)和臨床研究(B類),其中B類包括隨機對照試驗、非隨機對照研究及病例觀察報告。
排除標準:干預措施雖以硫唑嘌呤為受試藥物,但合并使用其他藥物,無法判斷ADR歸屬;單一分析硫唑嘌呤引起某一特定ADR;因ADR分析不能提供足夠信息以供評價。
1.3 文獻篩選與數據提取
文獻篩選和數據提取均由2位研究人員獨立進行,交叉復核,必要時聯系原文作者核實相關信息。若存在爭議則協商結局或由第3位研究員仲裁。按事先設計好的資料提取表格提取納入文獻資料,主要包括患者原患疾病,硫唑嘌呤用藥情況,ADR患者的性別、年齡及有無過敏史等情況,ADR出現時間、類型、處理及轉歸等。
2 結果
2.1 檢索結果
共檢索到相關文獻627篇,剔除重復文獻158篇,通過閱讀題目、摘要及全文,根據納入和排除標準,最終納入98篇文獻。其中A類42篇,B類56篇(病例觀察報告13篇,對照研究43篇)。
2.2ADR情況
ADR例數:98篇文獻共有2 464例患者,ADR821例。其中A類(42篇)文獻共有患者55例,發生ADR 55例;B類(56篇)文獻共有2 409例,發生ADR 766例(31.78%)[1];其中43篇對照研究共報道449例ADR,13篇回顧性研究共報道317例ADR。
ADR患者性別、年齡分布:結果見表1。因B類文獻僅提供受試對象的性別和年齡分布,未提供發生ADR患者的性別和年齡分布,故僅分析納入A類文獻患者年齡和性別分布。A類文獻(42篇)中,有1篇文獻未提及患者的性別和年齡,其余文獻中ADR患者男24例,女30例,男女比例為1∶1.25;年齡10~78歲,最多發生于31~49歲。硫唑嘌呤主要用于治療各種免疫相關疾病,B類(56篇)文獻中提及平均年齡分布的文獻43篇,平均年齡為31~59歲的文獻35篇(81.40%),提示應更重視硫唑嘌呤在此年齡段患者應用中的監測。
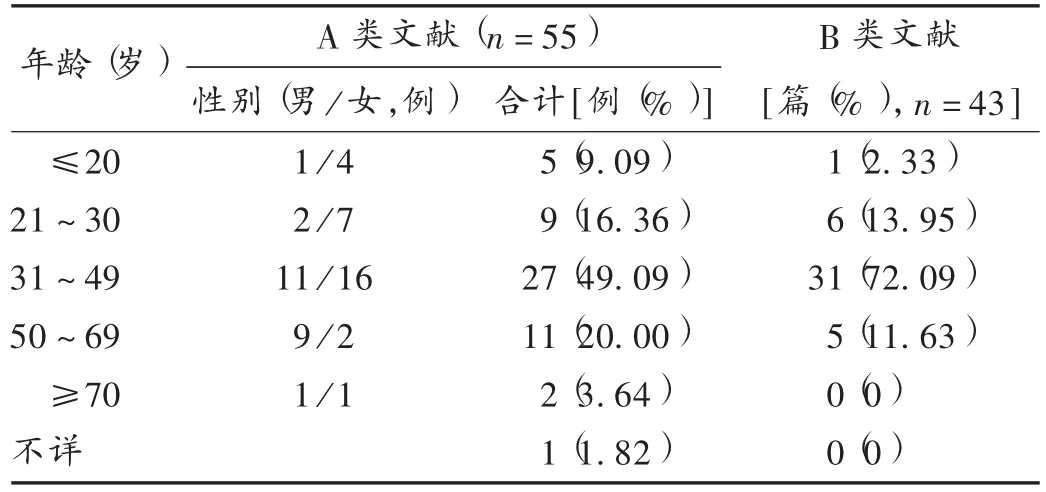
表1 硫唑嘌呤不同年齡段ADR患者分布
ADR涉及系統:硫唑嘌呤ADR涉及全身多個系統/器官,詳見表2。A類文獻報道的ADR主要集中于血液系統(骨髓抑制、粒細胞缺乏、白細胞減少、再生障礙性貧血)、皮膚(脫發)。B類文獻報道的ADR主要集中在消化系統(胃腸道反應如惡心、嘔吐、肝功能異常、胰腺炎)、血液系統(白細胞減少、粒細胞減少、骨髓抑制)、全身反應(頭暈頭痛、發熱、感染),以及皮膚(脫發、皮疹、過敏反應)。A類文獻報道的ADR涉及系統相對較窄,主要與硫唑嘌呤最易引發的血液系統相關,該類ADR相對較嚴重,臨床醫師較重視且易判定。提示將來硫唑嘌呤臨床使用過程中,不應局限于監測血液系統相關的ADR。
因ADR死亡患者情況:A類文獻55例ADR中,有13例死亡(23.64%),包括因白細胞減少引起感染、粒細胞缺乏致感染各2例,急性白血病導致死亡1例,骨髓抑制引起嚴重感染3例,再生障礙性貧血引起死亡5例。詳見表3。
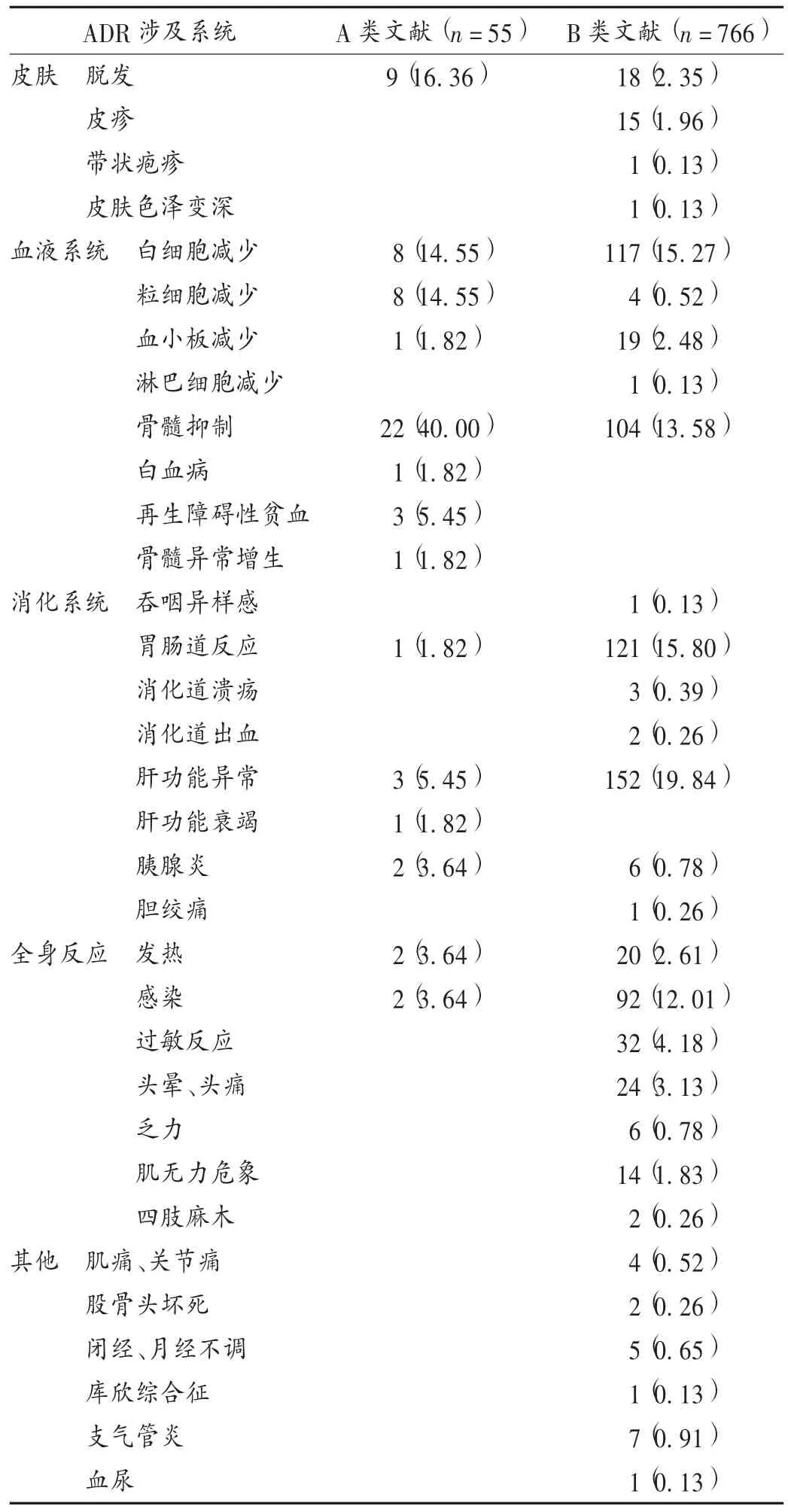
表2 硫唑嘌呤片ADR涉及系統[例(%)]
2.3 發生ADR患者基礎疾病分布
結果見表4。A類文獻報道的ADR患者中,原患疾病最多的為腎病綜合征,其次為系統性紅斑狼瘡、潰瘍性結腸炎、重癥肌無力、天皰瘡。B類文獻所報道的ADR患者中,排前5位的原患疾病依次為炎癥性腸病、克羅恩病、視神經性脊髓炎、潰瘍性結腸炎、重癥肌無力。

表4ADR患者基礎疾病分類[例(%)]
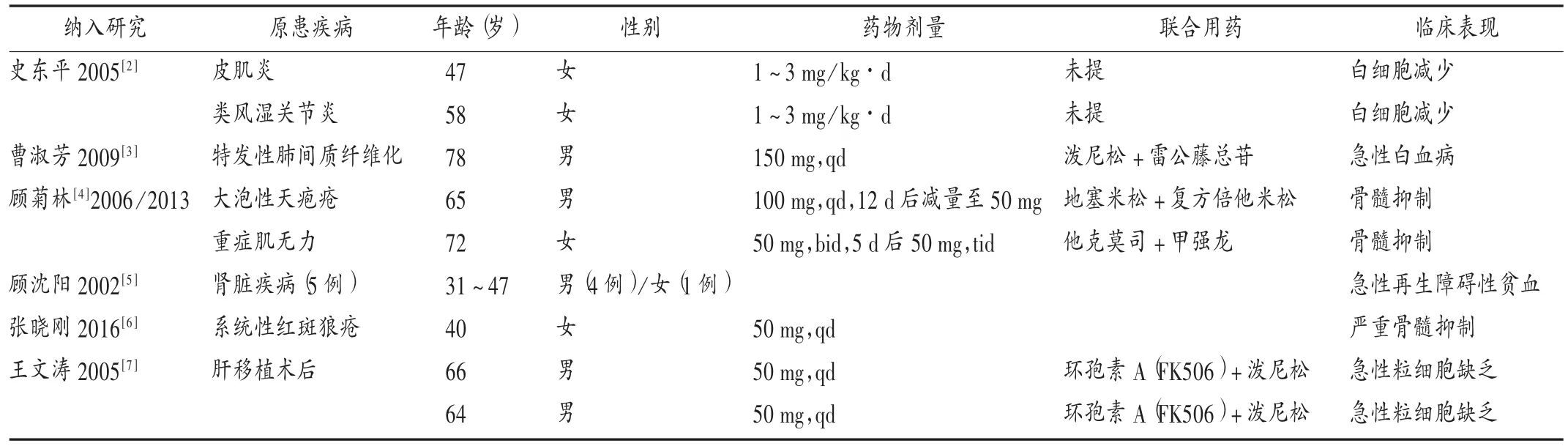
表3 硫唑嘌呤ADR死亡患者情況
3 討論
硫唑嘌呤為臨床常用免疫抑制劑,通過干擾嘌呤代謝的所有環節,抑制嘌呤核苷酸的合成,進而抑制細胞DNA和RNA及蛋白質的合成。硫唑嘌呤主要應用于急性淋巴細胞白血病、器官移植、炎癥性腸病及自身免疫性疾病,尤其在炎癥性腸炎的藥物治療中,硫唑嘌呤不可替代,其合理使用備受關注[8]。
硫唑嘌呤所致ADR種類繁多,輕重程度不一,導致患者停藥的概率高達9%~40%[9-10],其中常見類型包括血液系統損傷、肝損傷、胃腸道功能紊亂、感染等。硫唑嘌呤ADR主要與硫代嘌呤甲基轉移酶(TPMT)的活性和遺傳多樣性有關[11-12]。TPMT是硫唑嘌呤/6-MP代謝的關鍵酶,可將6-MP及硫唑嘌呤甲基化為無活性的代謝產物6-甲基巰基嘌呤(6-MMP),同時也能影響6-硫鳥嘌呤核苷酸(6-TGNs)等活性代謝產物的生成[13]。當TPMP活性降低,6-TGNs主要通過次黃嘌呤鳥嘌呤磷酸核糖基轉移酶途徑代謝生成,將明顯增加ADR發生[14]。當TPMT活性過高時,6-TGNs生成減少,不能達到藥物治療目的[15],且增加6-甲基巰嘌呤核糖核酸(6-MMPR)的生成,引發肝臟毒性反應[16]。硫唑嘌呤治療前行TPMT活性檢測能減少血液學毒性反應的發生風險[17],英國皮膚學會推薦所有患者接受硫唑嘌呤治療前進行TPMT活性測定[18]。故臨床患者使用硫唑嘌呤前可考慮檢測TPMT活性,根據基因檢測結果選擇最佳用藥方案。
硫唑嘌呤ADR死亡病例多因骨髓抑制且免疫力低下引起全身感染治療無效而死亡。臨床患者在接受硫唑嘌呤單獨治療或聯用其他免疫抑制藥物(如糖皮質激素類),由于機體處于免疫抑制狀態,因此對于細菌、真菌和病毒感染的易感性增加[18]。這類患者多合并骨髓抑制狀態,白細胞、粒細胞等顯著降低。一旦引起感染,患者治療難度增加,住院時間顯著延長且預后較差,嚴重情況可引起死亡。硫唑嘌呤引起的骨髓抑制通常可逆,故臨床應密切監測血常規,患者一旦出現白細胞降低、粒細胞減少應及時停藥并給予對癥治療。
本研究也存在局限性。由于本研究是二次研究,原始研究文獻未對ADR的嚴重情況進行分析,同時硫唑嘌呤應按體質量給藥但原始文獻中未描述患者體質量;本研究僅檢索了中文數據庫,未對國外數據庫進行檢索分析;硫唑嘌呤臨床多與其他藥物聯用,其他藥物可能影響ADR的判斷。因此建議,臨床研究過程中應加強ADR監測,應充分報道ADR情況;硫唑嘌呤在臨床使用前可考慮進行TMTP基因檢測,醫護人員在用藥全過程應密切觀察,一旦發生ADR,應立即采取措施;構建硫唑嘌呤ADR信號檢測和預警模型。

