熱量限制的低碳水化合物飲食和膳食纖維對非酒精性脂肪肝影響的研究進展
盛佳智1,弓臘梅
(1.四川文理學院體育學院,運動與健康促進實驗室,四川達州 635000;2.四川文理學院康養產業學院,四川達州 635000)
非酒精性脂肪肝(nonalcoholic fatty liver disease,NAFLD)是脂肪在肝臟內過多堆積的一種病理狀態,是代謝綜合征的一部分[1],Day等[2]在1998年提出經典的“二次打擊學說”認為活性氧導致脂質過氧化損傷及其相關事件,引起脂肪性肝炎;脂肪性肝炎持續存在(炎癥-壞死循環:ECM),ECM合成大于降解,形成進展性肝纖維化。較新的理論認為NAFLD發生的機制是“多重打擊學說”,該學說認為初次打擊主要是胰島素拮抗,二次打擊是各種原因引起的氧化應激或脂質過氧化損傷,引起脂肪性肝炎,脂肪性肝炎和胰島素拮抗的持續性存在引發第三次打擊,導致肝臟細胞外有害機制合成大于降解,形成進展性肝臟纖維化[3]。隨著人們生活水平提高和西式飲食頻率增加,過多攝入能量導致了NAFLD的發生和發展[4]。生活方式的改變,比如久坐行為的增加和體力活動嚴重不足,加劇肥胖率的同時,增加了NAFLD的發生。臨床實驗方面,國內學者研究發現適宜的有氧運動可以有效治療NAFLD,但是其研究中沒有報道具體的飲食情況,這似乎在強調運動的重要性[5]。有氧運動干預對NAFLD影響的分析表明,有氧運動可以顯著降低患者肝臟脂肪水平,然而對ALT(alanine aminotransfease,谷丙轉氨酶)、AST(aspartate transaminase,谷草轉氨酶)、TG(triglyceride,甘油三酯)、HDL(high-density lipoprotein,高密度脂蛋白膽固醇)和LDL(low-density lipoprotein,低密度脂蛋白膽固醇)水平均沒有發現顯著變化,提示生活方式的改變更重要[6]。有氧運動可以通過提高血清脂聯素水平,激活肝臟組織PPARα蛋白的表達[7]和改變肝臟細胞PPARαRNA的表達[8]發揮預防NAFLD的作用。有氧運動調節NAFLD的機制通過調節活性氧來降低肝臟氧化應激,借助抑制促炎癥因子來降低肝臟炎癥[9]。甚至有學者[10]認為有氧運動改善NAFLD的功能比節食有效。運動治療NAFLD的研究雖然很多,但是還處于初級階段,許多問題還需要解決,闡明其中的機制,可能為NAFLD的治療提供新的方向[11]。然而發表在英國運動醫學雜志上的系統評論表明,僅僅依靠運動,并不能實現減肥或者管理體重的效果,提出熱量限制的飲食干預可能在管理體重或者減肥上更有效[12],并且提出如果繼續使用高碳水化合物飲食,在未來的10年,胰島素拮抗將更加糟糕。
日本學者在比較和評估日本NAFLD和II型糖尿病患者的膳食攝入量研究中,發現相對于II型糖尿病患者,NAFLD患者中蔬菜的攝入量低,NAFLD患者更有可能具有促進體內脂肪堆積的飲食習慣[13]。而伊朗學者對159例患者和158個健康對照研究發現,患者組的腰圍和體重指數均高于對照組,健康個體的體力活動水平高于NAFLD患者,NAFLD患者的膳食攝入飽和脂肪酸和糖含量顯著高于健康人。健康人攝入總膳食纖維、葉酸、維生素D的比例顯著高于NAFLD患者[14],提示增加體力活動和膳食纖維的重要性。一項隨機對照臨床試驗在60名超重的NAFLD和肥胖個體中進行為期8周的飲食干預,兩種飲食(普通中等碳水化合物飲食和DASH飲食)都含有52%~55%的碳水化合物(中等碳水化合物飲食),16%~18%的蛋白質和30%的總脂肪,然而DASH飲食(Dietary Approaches to Stop Hypertension;DASH)的設計富含水果、蔬菜、全谷物和低脂乳制品,且飽和脂肪、膽固醇和精制谷物含量低;與對照組飲食相比,堅持DASH進食模式,體重、BMI、ALT、胰島素水平、評估的胰島素抵抗的均衡模型顯著降低,DASH飲食導致血清甘油三酯和總膽固醇/HDL比率顯著降低;NAFLD患者服用DASH飲食8周對體重、BMI、ALT、TG、胰島素代謝標志物、炎癥標志物均有益[15],表明攝入膳食纖維在改善NAFLD患者肝臟功能的重要性。限制熱量的低碳水化合物飲食和高膳食纖維飲食可能是治療NAFLD的有效手段[16]。為探究飲食結構和比例對肝臟功能的影響,本研究從低碳水化合物和高膳食纖維對NAFLD影響的研究進展進行系統綜述,以期為理解預防或者治療NAFLD提供幫助。
1 低碳水化合物飲食對NAFLD的影響
1.1 低碳水化合物飲食對NAFLD患者體重和BMI的影響
低碳水化合物飲食是在飲食結構中降低碳水化合物比例的飲食風格,尤其是限制熱量的低碳水化合物飲食,近年來其在健康領域被廣泛關注。不限制熱量的極低碳水化合物飲食聯合生酮飲食干預不但顯著降低了患者的體重和BMI,而且顯著降低了肝臟脂肪變性程度[17]。然而針對58例NAFLD患者使用中等(27人)和低碳(31人)水化合物飲食比較發現,6周的飲食干預,兩組之間腰圍和體重沒有顯著差異,但是低碳水化合物干預顯著降低了其AST、ALT、LDL、TG水平,改善了肝臟功能[18]。
限制熱量的低碳水化合物飲食顯著降低了NAFLD患者(肥胖)(9女5男)的體重和BMI[19]。國內學者[20]的研究也發現了相似的結論,然而此研究中沒有具體報道碳水化合物的比例。盡管受試者只有8人,但8周的限制熱量的低碳水化合物飲食干預顯著降低了患者的內臟脂肪和肝臟脂肪面積[21]。研究還發現飲食干預顯著降低了患者內臟脂肪、身體脂肪和腰圍等指標[22]。對肥胖的NAFLD患者熱量限制飲食聯合運動干預3個月發現,不論是男性還是女性,極低碳水化合物飲食干預顯著降低了其腰圍、臀圍、腰臀比和內臟脂肪以及體脂[23](見表1)。以上的研究大多限制熱量,表明限制熱量的低碳水化合物飲食干預在此方面效果較好。
1.2 低碳水化合物飲食對NAFLD患者肝臟功能和脂質代謝的影響
臨床上評價肝臟代謝情況的生物化學指標主要是ALT和AST,低碳水化合物飲食對ALT的影響結論不一致。其中國內的研究[18,22]認為限制熱量飲食顯著降低了ALT水平,而另外的兩項研究[17,19]沒有發現顯著變化。限制熱量飲食對AST的影響比較一致,國內兩項研究[18,22]和國外兩項研究[17,19]均證實干預產生了顯著的影響,即使一項研究[17]僅有5個樣本,AST下降幅度為23.2 U/L。基于上述的研究,熱量限制飲食干預對NAFLD患者肝臟功能的改善是有效的。
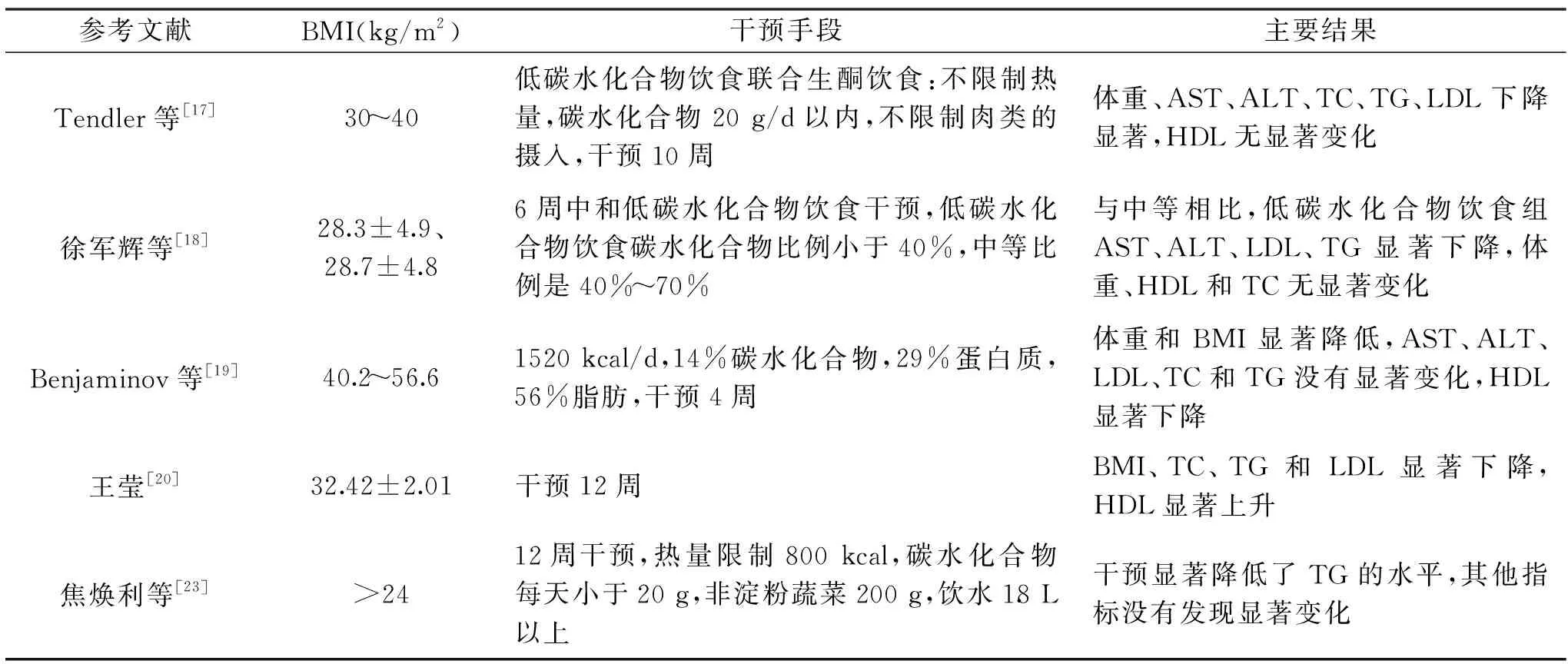
表1 低碳水化合物飲食對NAFLD的影響Table 1 Effect of low carbohydrate diet on NAFLD
評價肝臟脂質代謝情況的血液生化指標主要有總膽固醇(Total Cholesterol,TC)、TG、HDL和LDL,學者[17,19-20,22]認為飲食干預對TC的降低是有效的,也有研究沒有發現顯著改變[18,23]。干預顯著降低了TG水平[17,22],因此干預在這個指標上是值得深入研究的。而只有一項研究被證明干預顯著提升了HDL水平(5個樣本)[17],而大多研究沒有發現這個趨勢[18,21-23],還有一項研究發現低碳水化合物飲食干預顯著降低了HDL水平[19]。干預對LDL的影響大多顯著降低[17-20,22],也有兩項研究認為效果不顯著[21,23](具體見表1)。以上的研究除一項研究[11]沒有詳細介紹具體的飲食結構比例,其他六項研究均描述了飲食結構。其中三項研究嚴格限制了總熱量,就目前的研究來看,熱量限制的低碳水化合物飲食在改善肥胖的NAFLD患者的肝臟功能是有效的。
低碳水化合物干預通過熱量控制減輕體重和降低肥胖程度,促進脂肪酸氧化分解,改善血脂水平[24];通過限制糖類攝入,減少外周血循環中游離脂肪酸的含量,提高胰島素的敏感性,減少肝臟細胞的脂肪堆積及肝細胞損傷[25]。
2 膳食纖維干預對非酒精性脂肪肝的影響
膳食纖維一詞來源于1972年H.c.t.orwe提出,定義為食物中不被人吸收和消化的植物成分。膳食纖維具有很高的持水力,并可以改變腸道微生物的構成,從而預防疾病[26]。
2.1 肝臟橫斷面研究
通過對70名肥胖個體標準化方法分析膳食記錄,經過6個月的能量限制性營養干預后,回歸模型證明了肝臟狀態與水果纖維之間的關系[27]。通過對比NAFLD患者和健康的對照組發現,NAFLD患者脂肪攝入量顯著高于對照組,總能量攝入顯著高于對照組,TG、ALT、AST 顯著高于對照組,TC兩組沒有區別,提示限制熱量的高膳食纖維飲食是改善肝臟功能的有效手段[28]。
2.2 膳食纖維素干預研究
2.2.1 動物模型影響研究 通過低脂肪高膳食纖維飲食(纖維來自麩皮和大白菜,相當于普通飼料熱量的60%)對昆明小鼠干預12周,發現低脂肪高膳食纖維組小鼠體重及體脂率明顯降低,肝臟組織中TC、TG、LDL含量明顯降低,HDL含量明顯升高,提示低脂肪高膳食纖維飲食具有顯著降低小鼠體重、體脂率的作用[29]。探討不同谷物膳食纖維對高脂高膽固醇膳食喂養誘導的C57BL/6J小鼠體重控制和脂肪分解的機制,發現干預24周,谷物膳食纖維小鼠體重、血脂和游離脂肪酸水平顯著下降,脂肪細胞體積變小,且燕麥和全小麥膳食纖維顯著上調了脂肪分解蛋白的表達,在體重控制和脂肪分解能力上,全麥膳食纖維優于燕麥膳食纖維。主要因為全麥膳食纖維對動物脂肪分解的限速酶ATGL(脂肪甘油三酯脂肪酶)和HSL(激素敏感脂肪酶)升高的作用更加明顯,這兩種限速酶可以分解游離脂肪酸供給能量[30]。
2.2.2 補充膳食纖維干預對患者的影響 通過低熱量、高膳食纖維干預脂肪肝患者發現,干預顯著降低了TC、TG和ALT水平,認為干預有效改善了脂肪肝[16]。對肥胖代謝綜合征的患者進行每天12~18 g的大豆膳食纖維為期3.3個月的干預,發現膳食纖維干預顯著降低了其腰圍、臀圍、體重和BMI[31]。此研究報道了早期的反應脂質代謝指標的TC、TG、HDL、LDL,但是沒有報道干預之后這些指標的變化,導致研究結論的說服力不足。研究進行了為期6個月的飲食干預,發現在干預期間,膳食纖維攝入量從19 g/d增加到29 g/d,伴隨著膳食纖維消耗頻率的增加。所有減肥的患者的血清AST、ALT均顯著降低,研究提示增加營養纖維可能通過降低腸道通透性改善脂質代謝的狀況,增加膳食纖維的水平應該納入NAFLD患者的飲食指南[32](具體見表2)。

表2 膳食纖維素干預對NAFLD的影響Table 2 Effect of dietary fiber intervention on NAFLD
NAFLD是一種多因素疾病,涉及遺傳、飲食和生活方式之間的復雜相互作用,所有這些都結合形成NAFLD表型[13]。膳食纖維干預可以提高PPAR-αmRNA的表達水平,改善脂質代謝異常和胰島素抵抗,以及一些炎癥水平[33],PPAR-α的配體非諾貝特降低TG,增加HDL的水平,使載脂蛋白增加[34]。其還可以提高肝臟中胰島素的敏感性,減少內臟脂肪,增加脂肪酸氧化酶的水平,增加脂肪的消耗。膳食纖維可以改變腸道的通透性[32],減少膽固醇吸收,促進膽固醇的排泄,降低血漿中膽固醇水平,增加食物在腸道的時間,延緩胃排空,減緩脂肪吸收,從而降低血漿中的甘油三酯[35]。膳食纖維經腸道生態系統調節脂質代謝,促進益生菌生長,抑制有害菌生長;改變腸道擬桿菌門與厚壁菌門的比值,增加腸道微生物的多樣性[36]。膳食纖維通過腸道菌群發酵產生的短鏈脂肪酸,可增強肝臟對胰島素的敏感性,改善機體胰島素抵抗,進而防止脂肪在肝臟堆積[37]。調節腸道短鏈脂肪酸水平調節脂質代謝,短鏈脂肪酸一旦與腸粘膜上皮細胞吸收就能被轉運到肝臟和脂肪組織,參與膽固醇、甘油三酯和脂肪酸的代謝過程。總之,通過調整腸道菌群[38],改善腸-肝軸功能紊亂是治療NAFLD的新策略[39]。
3 結論與局限性
低碳水化合物飲食會產生一系列不良適應,早期1~2周表現為頭暈、虛弱和便秘等,一般癥狀會在3~4周自行消失[40]。當然這也是一些受試者退出實驗的重要原因[19]。先前的關于低碳水化合物干預對肝臟功能影響的研究存在諸多待完善之處,比如低碳水化合物飲食并不等于低熱量飲食,且缺少受試者體力活動和久坐等相關信息的描述,這些重要的信息均會影響研究結論的可靠性。而實施膳食纖維素干預的研究,因膳食纖維的類別較多,而且缺乏明確的劑量-效應關系,未來的研究可能需要在這些方面深入探究。而著眼運動聯合高膳食纖維飲食對NAFLD的影響將成為此領域的重要視角。
久坐行為、低體力活動、不良飲食行為是導致NAFLD發生和惡化的主要原因。臨床證據強烈支持改變生活方式作為NAFLD管理的主要治療方法[41]。在控制碳水化合物的同時,增加膳食纖維的比例,有助于增加飽腹感,減少熱量的攝入,對NAFLD的控制和逆轉起到積極的效果[24]。建立合理地膳食結構,倡導健康的生活方式是預防NAFLD發生和發展的重要措施[42-43]。不良的膳食成分是NAFLD發展的重要因素,大多數NAFLD患者遵循飲食過量消耗簡單的碳水化合物,總脂肪和飽和脂肪,減少攝入膳食纖維和富含ω-3的食物。雖然包括減肥和運動在內的生活方式改變仍然是NAFLD管理的基石,但改變飲食成分或限制卡路里的飲食也可能是NAFLD治療的可行和可持續的策略[44]。

