鐵錳復合陰極MFC-EF耦合系統產電及降解RhB效能
史 珂,趙慶良,王維業,王 琨
(1.城市水資源與水環境國家重點實驗室(哈爾濱工業大學),哈爾濱 150090; 2.哈爾濱工業大學 環境學院,哈爾濱 150090)
微生物燃料電池(MFC)能夠在微生物的催化作用下將化學能轉化為電能,同時實現產電與污染物的處理,已成為環境工程領域的一項重要技術[1-2].但由于輸出功率低下,MFC在污染物處理的應用中受到一定限制.有研究將MFC與其他工藝結合,如MBR-MFC[3]、CW-MFC[4]和MFC-SBR[5]等,拓寬了MFC的應用范圍.電芬頓(EF)技術利用·OH的無選擇性強氧化能力,在處理難降解污染物中表現優秀[6],也因其可以原位產生H2O2,解決了傳統Fenton法中H2O2的運輸和儲存難題,降低了藥劑成本[7].然而,EF技術需要外部電能輸入,此部分成本的投入也在一定程度上限制其工業化應用.將MFC與EF技術耦合構成生物電芬頓系統(MFC-EF),利用MFC原位產生的電能驅動EF反應降解有機污染物,在實現電能原位利用的同時,保證EF的優勢,進一步降低污染物處理能耗,具有良好的發展前景[8-9].
目前對MFC-EF的研究已經初見成效.Fu等[10-12]將MFC與EF結合,通過外加鐵源作為EF催化劑,實現了對莧菜紅、對硝基苯酚等物質的降解.Zhuang等[13-15]則是在MFC-EF的陰極上負載了不同類型的鐵氧化物,在對染料、TPTC等物質的降解中也取得良好效果.通過外加鐵離子催化Fenton反應的常規均相EF技術,嚴格限制了酸性pH范圍,還會產生大量的金屬沉淀,增加了后續處理的難度.引入其他具有類芬頓(Fenton-like)催化性能的金屬與鐵共同作用,組建非均相催化體系,可以解決上述問題[16].
錳作為一種Fenton-like催化劑能夠促進H2O2生成·OH[17],有研究[18]制備了含有鐵錳雙金屬的催化劑用于Fenton-like系統中,污染物降解效果良好,但目前將鐵錳雙金屬催化劑直接做成陰極材料,并應用于MFC-EF系統的研究很少.因此,本研究聚焦MFC微電的原位利用,結合EF的優勢,構建MFC-EF耦合系統,并制備非均相催化電極材料——鐵錳復合陰極,以同類研究中常用的、具有代表性的染料羅丹明B(RhB)為目標污染物,與碳纖維(CF)無負載電極以及較為經典的Fe&Fe2O3/CF復合電極[19]對比,探究MFC-EF耦合系統的產電性能和污染物降解效果.本研究旨在實現資源的再生及利用,提高MFC-EF耦合系統的性能及應用范圍,并為實際廢水的處理提供新的思路.
1 實 驗
1.1 反應器的構建及運行
MFC-EF耦合系統采用雙室反應器構型(圖1),反應器壁均采用有機玻璃板制成,兩反應室間由PEM膜分隔.反應器的陽極室為密閉式圓柱體型,規格為φ85 mm×100 mm,容積550 mL;陰極室為長方體型,規格為60 mm×60 mm×100 mm,容積360 mL.陽極室中設Ag/AgCl參比電極(+0.195 V vs. SHE),陽極室底物為哈爾濱文昌污水處理廠的剩余污泥.陽極材料是由鈦絲和碳纖維絲(T700,日本東麗)擰制而成的碳纖維刷,規格為φ90 mm×100 mm,陽極和陰極之間通過導線連接外電阻(啟動階段為1 000 Ω).系統運行時保證陽極處于厭氧環境,定期補充更換陽極污泥,以維持反應器的良性運行.啟動階段陰極室電解液為K3[Fe(CN)6](65.8 g/L)與KH2PO4(27.2 g/L)的混合液,每48 h更換一次;啟動成功后正式實驗時將陰極液換成RhB(30 mg/L)與Na2SO4(0.10 mol/L)的混合液,以上溶液均由蒸餾水配制而成.
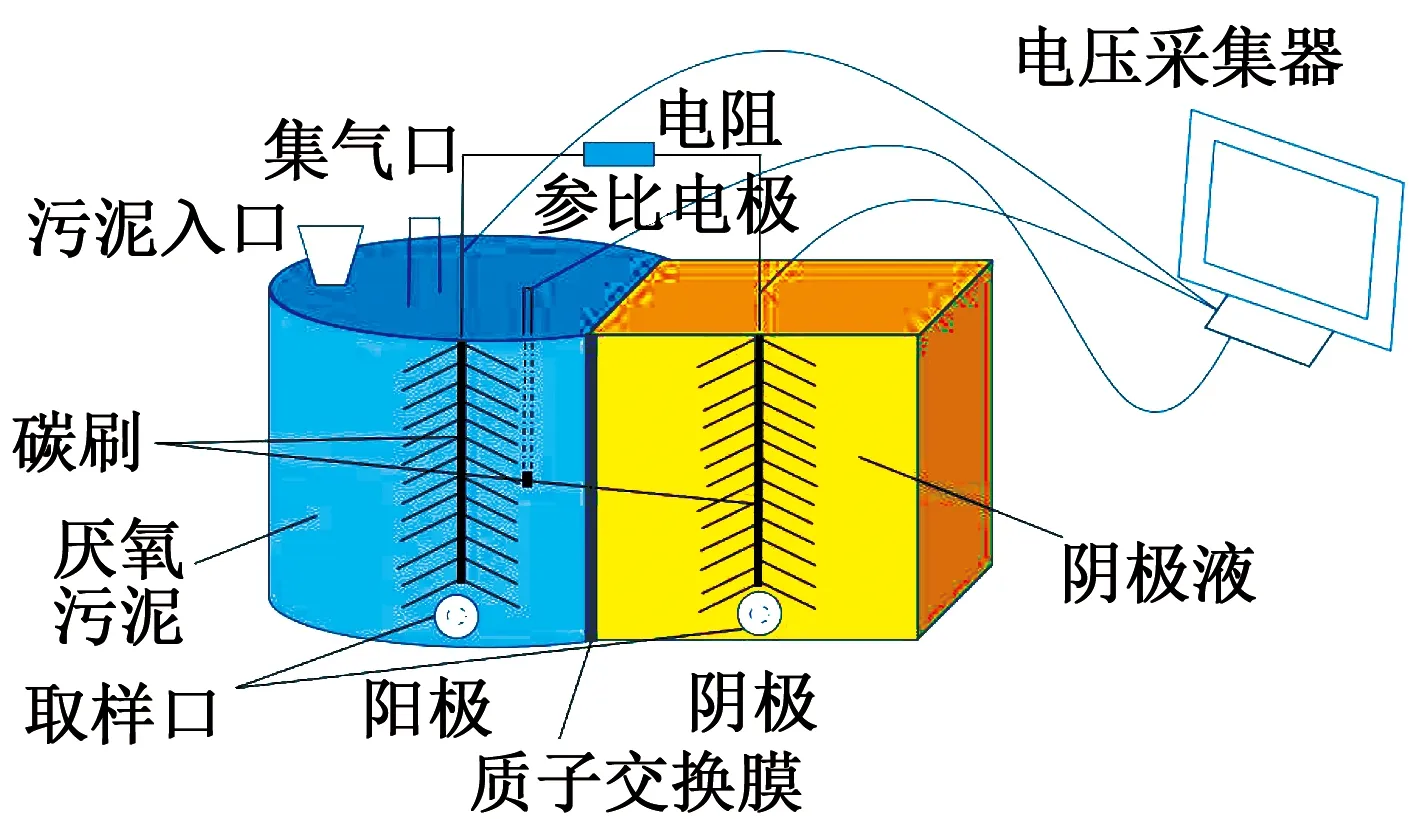
圖1 MFC-EF耦合系統反應器構型
Fig.1 Configuration diagram of the reactor of MFC-EF coupling system
1.2 陰極材料的制備及表征
陰極材料制備時均采用與陽極相同的CF作為基底材料,CF使用前需進行預處理:先用無水乙醇浸泡超聲作用1 h,隨后分別用1.0 mol/L HCl和1.0 mol/L NaOH浸泡處理4 h,用去離子水沖洗數次,置于80 ℃干燥箱中烘干.預處理后的CF可直接作為CF無負載電極.
Fe&Fe2O3/CF復合電極的制備方法:將2.7 g FeCl3·6H2O和3.6 g NaBH4分別溶解在200和80 mL的去離子水中,將預處理后的CF置于FeCl3溶液中超聲20 min,然后將NaBH4緩慢加入其中,之后用去離子水清洗,在N2中干燥.
FeMnOx/CF復合電極的制備方法:將高錳酸鉀(KMnO4,3.0 g)、硫酸亞鐵(FeSO4·7H2O,15.6 g)分別溶于250 mL去離子水中.將預處理后的CF浸沒于KMnO4溶液中,在劇烈的磁力攪拌下,向KMnO4溶液中緩慢加入FeSO4溶液,同時加入5.0 mol/L NaOH溶液,使溶液的pH保持在7和8之間.加入后,將形成的懸浮液連續攪拌1 h,室溫下老化12 h,然后用去離子水將CF進行反復洗滌,在105 ℃下干燥4 h.
采用掃描電子顯微鏡(SEM,SIGMA300,ZEISS)對電極材料的表面形貌進行分析,用XPS(PHI 5700 ESCA System,美國物理電子公司)確定復合陰極材料中的元素及元素價態.
1.3 電化學性能評價
1.3.1 工作電壓
MFC-EF耦合系統的工作電壓通過多通道電壓采集器PISO-813的采集卡(12 bit A/D conversion chips, US)實時測量并記錄.
1.3.2 極化曲線和功率密度曲線
在MFC-EF耦合系統穩定運行狀態下,先將系統開路運行12 h,得到開路電壓;然后將反應電路外電阻從9 kΩ逐級減少到10 Ω,記錄各級外電阻下穩定的系統總電壓,計算電流密度和功率密度,繪制極化曲線和功率密度曲線.
1.4 測試分析方法
1.4.1 H2O2濃度
H2O2濃度采用I3-分光光度法進行測定,具體操作方法為:取水樣2 mL,分別加入1 mL碘試劑(0.40 mol/L KI, 0.06 mol/L NaOH,10-4mol/L(NH4)2MoO4)和1 mL(0.10 mol/L)鄰苯二甲酸氫鉀,靜置顯色,采用紫外分光光度計測352 nm處的吸光度.
1.4.2 電流效率(EC)
H2O2的電流效率是電極反應產生H2O2所消耗的電量與反應系統的總電量的比值,即
(1)
式中:n為H2O2氧還原轉移的電子數,F為法拉第常數(96 485 C/mol),c為反應生成的H2O2濃度(mol/L),V為溶液的體積(L),I為電流(A),t為時間(s).
1.4.3 RhB去除率
由紫外分光光度計測定554 nm下的吸光度,RhB去除率R計算公式為
(2)
式中:A1為RhB的初始吸光度,A2為處理后RhB的吸光度.
1.4.4 TOC
采用TOC測定儀(TOC-VCPN,日本Shimadzu有限公司)測定陰極液TOC,并計算去除率.
2 結果與討論
2.1 電極材料表征
2.1.1 電極材料表面形貌分析
通過SEM分析電極材料的表面形貌,結果見圖2.CF無負載電極是普通的碳纖維,根據相關文獻[20]及經驗,易知其表面是整體光滑的,而Fe&Fe2O3/CF復合電極(圖2(a)、(b))的碳纖維上可以明顯看到負載物,粗糙度增加.大部分負載呈現鱗片狀結構,但分布不均勻,有團聚現象出現.負載物的團聚不利于與污染物進行充分接觸,會影響負載電極的處理效率.FeMnOx/CF復合電極(圖2(c)、(d))的碳纖維上同樣擁有豐富的負載,而且負載量更大,包覆性更好,團聚現象消失;除了鱗片狀結構的負載,還出現了絮狀負載物,有利于增加接觸面積和傳質效率,提高電極的產電和污染物處理效率.

圖2 不同電極SEM圖
2.1.2 元素及其價態分析
為確定復合陰極材料中的元素及其價態,進行XPS測試和分析,結果如圖3,4所示.除了C、O元素,Fe&Fe2O3/CF和FeMnOx/CF復合電極表面還分別檢測出Fe、Fe和Mn元素(圖3),證明了相關元素的成功負載.
CF無負載電極在結合能為531.7 eV處出現O1s特征峰(圖4(a)),此峰可能是由預處理過程吸附在碳纖維表面的·OH、H2O和碳酸鹽類物質形成的[21],而Fe&Fe2O3/CF復合電極的O1s譜圖中,還增加了結合能為530.0 eV的峰,此峰則是金屬氧化物中O1s的特征峰[22];Fe&Fe2O3/CF復合電極Fe2p譜圖(圖4(c))中峰的位置出現在709.86 eV、722.88 eV、707.94 eV和717.33 eV,分別對應于文獻[22]報道的Fe2O3的Fe2p3/2、Fe2p1/2和Fe0的Fe2p3/2、Fe2p1/2軌道峰.由此說明Fe&Fe2O3/CF復合電極上成功負載了Fe和Fe2O3.
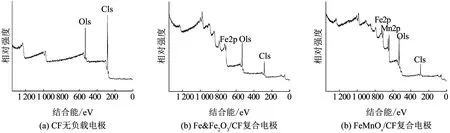
圖3 不同電極材料的XPS全譜圖
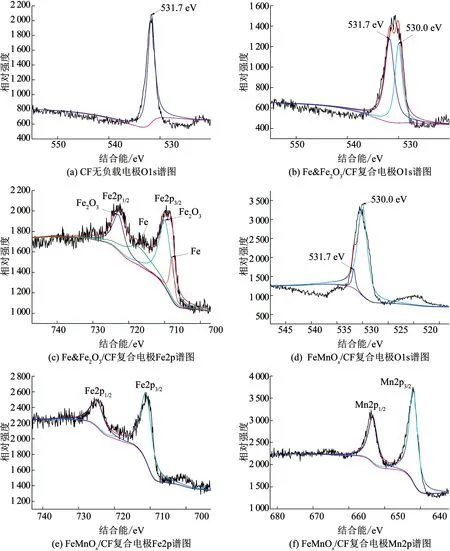
圖4 不同電極材料元素的高分辨率譜圖
類似地,FeMnOx/CF復合電極中的O也主要來自金屬氧化物,Fe2p3/2和Fe2p1/2的軌道峰位置說明FeMnOx/CF復合電極中Fe為3價;Mn2p3/2和Mn 2p1/2軌道峰分別在642.08 eV 和653.68 eV,與文獻[23]報道的4價Mn相符,說明FeMnOx/CF復合電極中Mn為4價.綜上,FeMnOx/CF復合電極上成功負載了Fe(Ⅲ)和Mn(Ⅳ)的二元金屬氧化物.
2.2 不同陰極材料所在MFC-EF耦合系統的產電效能分析
參考相關文獻[24-26],設置陰極染料RhB的初始質量濃度為30 mg/L,支持電解質溶液Na2SO4濃度為0.1 mol/L,初始pH為3,曝氣速率為200 mL/min,在上述陰極環境下,測試了FeMnOx/CF復合電極、Fe&Fe2O3/CF復合電極及CF無負載電極在MFC-EF耦合系統中的電化學性能.
2.2.1 工作電壓
圖5為外電阻為1 000 Ω時不同電極的工作電壓情況.3種電極在MFC-EF耦合系統的工作電壓存在顯著差異,FeMnOx/CF復合電極所在耦合系統的工作電壓最高,平均值達0.956 V,比Fe&Fe2O3/CF復合電極(0.559 V)提高了71.14%,比CF無負載電極(0.401 V)提高了138.48%.說明FeMnOx/CF復合電極對MFC-EF耦合系統的工作電壓有提升效果,鐵、錳雙金屬的加入比單一的鐵負載對耦合系統工作電壓的提升作用更加顯著.
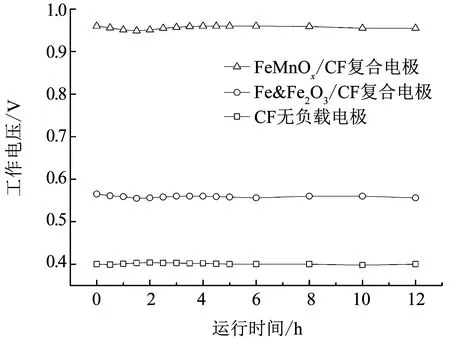
圖5 不同電極所在MFC-EF耦合系統的工作電壓
Fig.5 Working voltages of MFC-EF coupling system with different electrodes
2.2.2 極化曲線和功率密度曲線
根據極化曲線和功率密度曲線量化MFC-EF耦合系統的產電效能,結果如圖6所示.經計算得到的FeMnOx/CF復合電極下MFC-EF耦合系統最大功率密度為5.47 W/m3, Fe&Fe2O3/CF復合電極和CF無負載電極下MFC-EF耦合系統最大功率密度分別為2.63和0.52 W/m3.可見,FeMnOx/CF復合電極下MFC-EF耦合系統的最大功率密度有了顯著提高.由Rint=-ΔE/ΔI計算得到FeMnOx/CF復合電極、Fe&Fe2O3/CF復合電極和CF無負載電極所在耦合系統的內阻分別為109.00,115.06和262.80 Ω.
FeMnOx/CF復合電極與Fe&Fe2O3/CF復合電極、CF無負載電極相比,內阻降低,這是由于鐵、錳元素對氧還原反應均有催化作用,鐵和錳的負載提供了更多的氧還原催化活性中心,提高了氧還原反應活性;而且鐵和錳的共同作用比單一的鐵對氧還原反應的催化作用更強,可以更有效地降低陰極反應阻力[27].錳元素在催化過程中通過不同價態之間的轉換,加速電子的傳遞速率,降低了氧還原反應的超電勢,從而提高了電池的輸出功率[28],改善了耦合系統的產電效能,有利于為陰極的電芬頓反應提供更多的電能,實現電能的原位利用及污染物的降解.
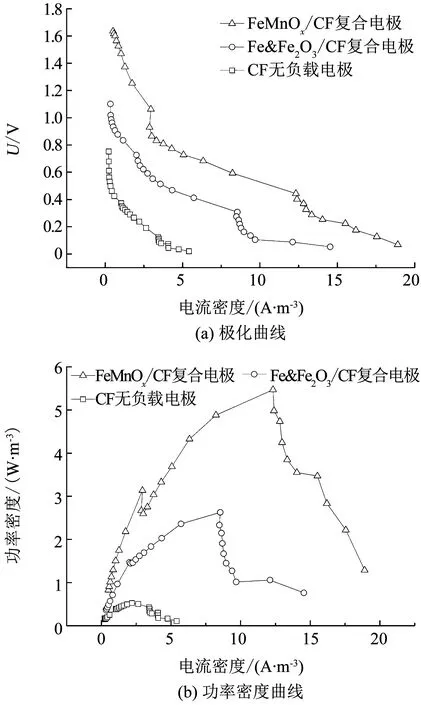
圖6 不同電極所在MFC-EF耦合系統的極化曲線和功率密度曲線
Fig.6 Polarization curve and power density curve of MFC-EF coupling system with different electrodes
2.3 不同陰極材料所在MFC-EF耦合系統對RhB的降解效果分析
在與2.2相同的陰極環境下,將外電阻設為100 Ω(接近電池內阻),運行不同陰極材料下的MFC-EF耦合系統,間隔一定時間取樣,測定不同陰極下H2O2的產生量及電流效率、RhB去除率和TOC等指標,評價不同陰極對污染物的降解能力.
2.3.1 H2O2的產生量及電流效率
不同電極下MFC-EF耦合系統H2O2的產量及電流效率如圖7所示.FeMnOx/CF復合電極下耦合系統的H2O2產率具有明顯優勢,0.5 h產生的H2O2質量濃度即可達3.69 mg/L,比另外兩電極運行5 h產生的H2O2質量濃度還高,且在5 h時達15.82 mg/L.由此說明,MFC-EF耦合系統實現了H2O2的原位產生,并且FeMnOx/CF復合電極極大提高了MFC-EF耦合系統的H2O2產生量.
根據式(1)可計算得到不同電極產H2O2的電流效率(圖7(b)).3種電極下產H2O2的電流利用效率均在系統運行最初時最高,并隨著反應進行會有所降低,這與H2O2的伴生反應有關[29].FeMnOx/CF復合電極的H2O2電流效率在三者中最高,反應5 h時為40.44%,比同時刻的Fe&Fe2O3/CF復合電極(11.79%)提高了242.94%,進一步證明了金屬錳的加入促進了O2的二電子轉移過程[30],提高了產H2O2的電子利用率,從而提高了H2O2的產生效率;同時也說明FeMnOx/CF復合電極使MFC-EF耦合系統中的電能得到了更有效的利用,提高了微電的利用率.
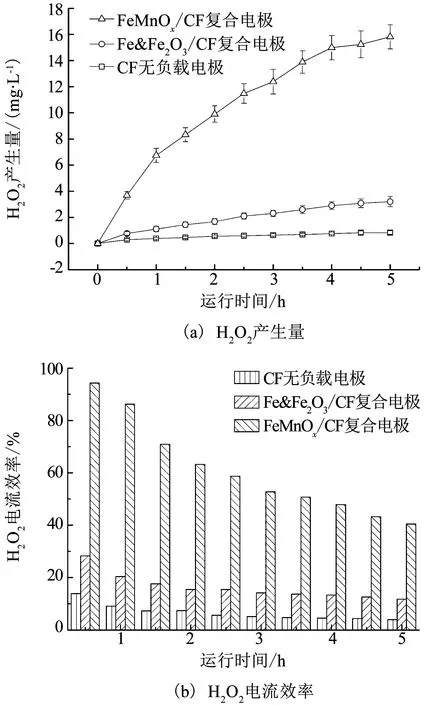
圖7 不同電極所在MFC-EF耦合系統的H2O2產量及電流效率
Fig.7 Production and current efficiency of hydrogen dioxide in MFC-EF coupling system with different electrodes
2.3.2 RhB的去除率及礦化率
測定MFC-EF耦合系統對RhB的去除率,評價不同陰極材料的性能,結果如圖8(a)所示.CF無負載電極、Fe&Fe2O3/CF復合電極和FeMnOx/CF復合電極在5 h的RhB去除率分別為72.27%、82.27%和91.60%,FeMnOx/CF復合電極最高.為了進一步探究CF本身對染料的吸附作用,在保證其他條件相同的情況下,進行斷路狀態下CF無負載電極對RhB的去除實驗(圖8(a)中CF無負載電極-不通電),結果表明,在單純的CF吸附作用下,運行5 h對RhB的去除率為47.96%.
除去CF的吸附以及原位產生的H2O2對RhB的氧化降解,Fe&Fe2O3/CF和FeMnOx/CF復合電極在RhB去除率上表現出的優勢則是通過EF過程生成·OH等活性氧基團對RhB的氧化.而FeMnOx/CF復合電極對RhB的去除效果比Fe&Fe2O3/CF復合電極有提高,是由于金屬錳和鐵的協同作用比單一的金屬鐵對電芬頓反應的催化效果更好,Fe在催化H2O2產生·OH的同時,Mn也在發揮類芬頓催化作用,重要的是,在催化過程中Fe(Ⅱ)和Mn(Ⅲ)會發生反應生成Fe(Ⅲ)和Mn(Ⅱ),這一過程加速了Fe(Ⅲ)/ Fe(Ⅱ)和Mn(Ⅲ)/ Mn(Ⅱ)的氧化還原循環,從而促進了·OH的產生,增強對有機物的氧化降解.協同作用發生的具體過程為[31-32]:
Fe(Ⅲ)+H2O2→Fe(Ⅱ)+·OOH+H+,
(3)
Fe(Ⅱ)+H2O2→Fe(Ⅲ)+·OH+OH-,
(4)
Mn(Ⅲ)+H2O2→Mn(Ⅱ)+·OOH+H+,
(5)
Mn(Ⅱ)+H2O2→Mn(Ⅲ)+·OH+OH-,
(6)
Fe(Ⅱ)+Mn(Ⅲ)→Fe(Ⅲ)+Mn(Ⅱ).
(7)
為了進一步說明耦合系統對RhB的礦化效果,測定了陰極污染物的TOC隨時間變化情況,結果如圖8(b)所示.通電條件下,3種電極的TOC呈現隨時間下降的趨勢,FeMnOx/CF復合電極的礦化效果最好,5 h的TOC去除率達30.84%,比CF無負載電極和Fe&Fe2O3/CF復合電極分別提高了212.88%和23.92%;而不通電狀態下CF無負載電極的陰極液TOC基本保持水平,無下降趨勢.由此進一步說明,MFC-EF耦合系統對RhB的礦化主要依賴于EF過程,由于FeMnOx/CF復合電極可以更有效地催化EF反應,對RhB的礦化程度最高,降解效果最為徹底.同時說明本研究利用MFC產生的微電成功實現了對污染物RhB的降解,對解決MFC的應用和RhB相關染料廢水的處理等問題均有重要意義.
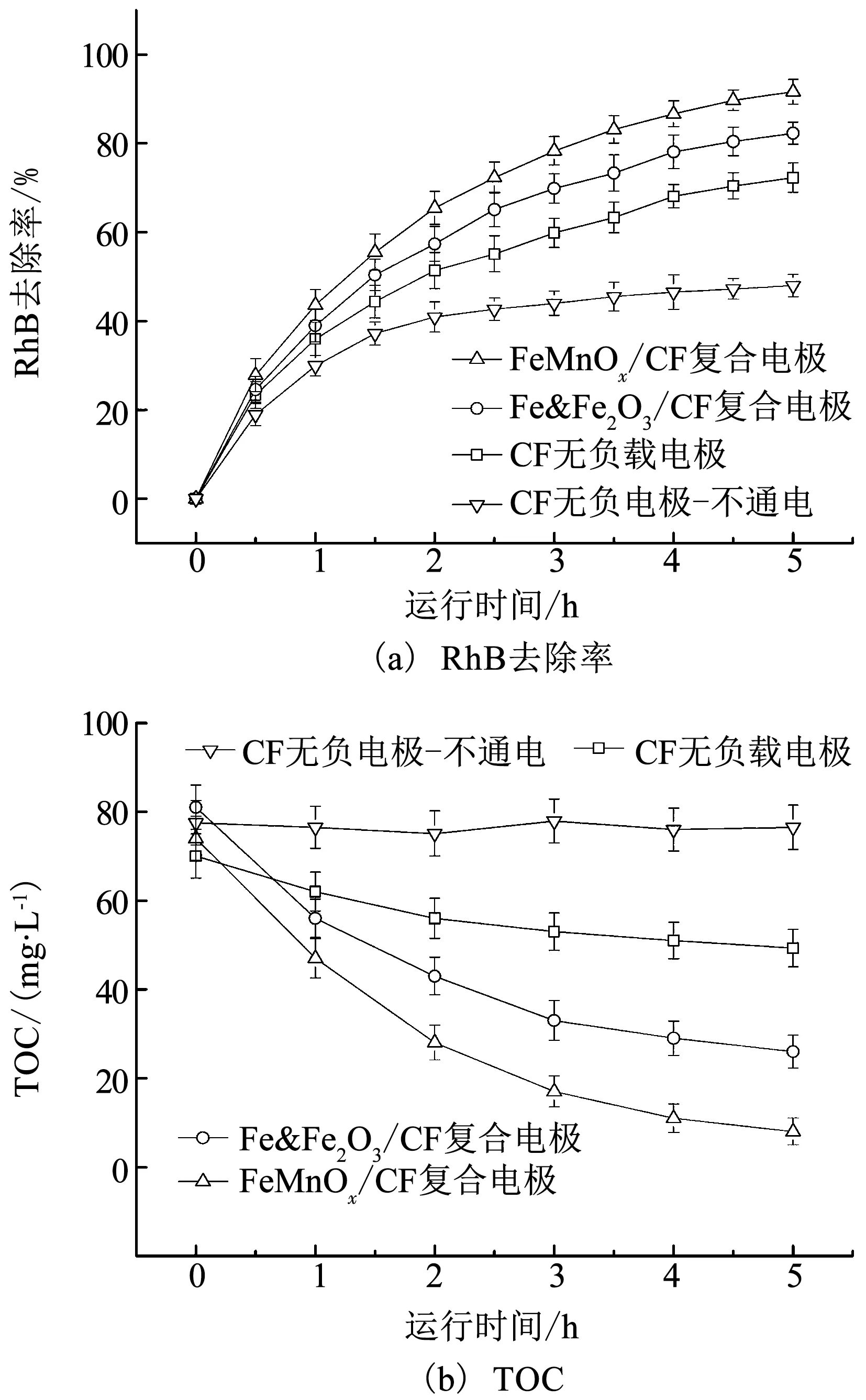
圖8 不同電極所在MFC-EF耦合系統RhB去除率及TOC
Fig.8 Removal rates of RhB and TOC in MFC-EF coupling system with different electrodes
2.4 陰極液初始pH對MFC-EF耦合系統產電性能及污染物去除效率的影響
保持其他條件與2.3相同,分析陰極液初始pH對Fe&Fe2O3/CF和FeMnOx/CF復合電極所在MFC-EF耦合系統的工作電壓和RhB去除率的影響.
2.4.1 陰極液初始pH對工作電壓的影響
圖9(a)、(b)分別為Fe&Fe2O3/CF和FeMnOx/CF復合電極在不同陰極液初始pH下的工作電壓.pH在3~7,兩種電極所在耦合系統的工作電壓均隨pH的升高而降低,但Fe&Fe2O3/CF復合電極對pH變化的響應更為明顯,工作電壓下降幅度更大,尤其當pH由3升至4時,工作電壓平均值下降了47.04%;而FeMnOx/CF復合電極對pH的包容性更強,工作電壓下降幅度很小,pH由3升至7時,工作電壓平均值僅下降了21.61%,且FeMnOx/CF復合電極在pH=7時的工作電壓比Fe&Fe2O3/CF復合電極pH=3時的工作電壓還要高出46.90%.由此說明,如要維持Fe&Fe2O3/CF復合電極下MFC-EF耦合系統的工作電壓較高,需要將pH嚴格限定在3附近,而FeMnOx/CF復合電極在pH=3~7內均能保證耦合系統的工作電壓處于較高水平.
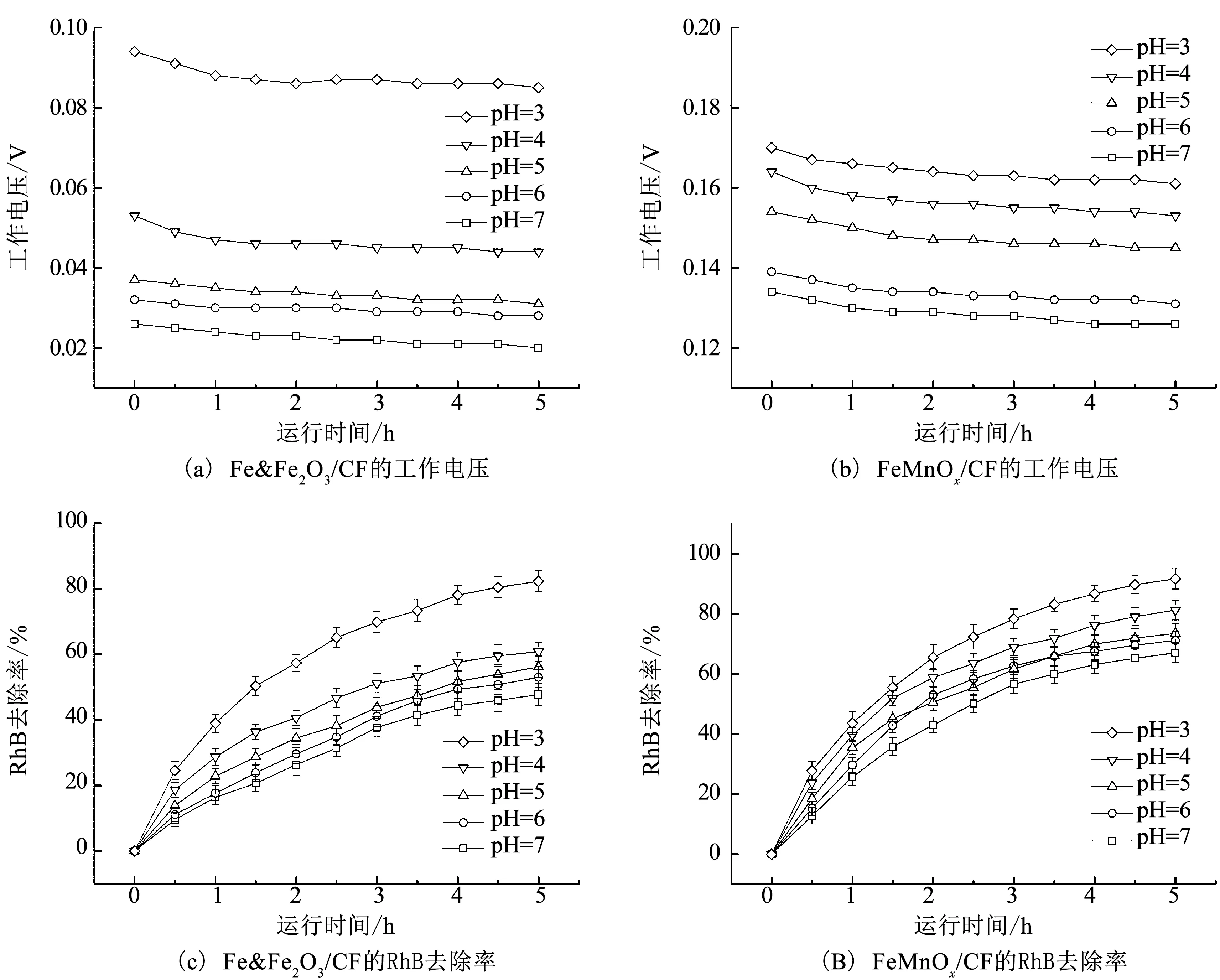
圖9 陰極液初始pH對不同電極所在MFC-EF耦合系統工作電壓及RhB去除率的影響
2.4.2 陰極液初始pH對RhB去除率的影響
圖9(c)、(d)分別為不同陰極液初始pH下Fe&Fe2O3/CF和FeMnOx/CF復合電極所在耦合系統對RhB的去除率.與電壓變化規律相同,pH在3~7,兩種電極對RhB的去除依然呈現隨pH升高而降低的趨勢.Fe&Fe2O3/CF復合電極的降低幅度更大,pH=7時5 h的RhB去除率比pH=3時下降了41.99%;FeMnOx/CF復合電極的降低幅度相對較小,pH=7時5 h的RhB去除率比pH=3時僅下降了26.86%.
按照傳統Fenton反應的原理,當溶液的pH較低時,H2O2分解生成羥基自由基較多,RhB的去除率較高;另有研究[33]表明,工作電流是影響生物電芬頓體系中H2O2生成的關鍵因素.綜合考慮pH對工作電壓的影響,推斷本研究中陰極液初始pH對MFC-EF耦合系統RhB去除率的影響機制,除去pH影響Fenton反應速率以外,也與pH影響耦合系統的工作電流有關.
實驗還證明了FeMnOx/CF復合電極可擺脫常規Fenton體系對陰極液pH的嚴格限制,擴大了MFC-EF耦合系統的陰極液pH范圍,解決了均相電芬頓催化的一大弊端,有望促進MFC-EF耦合工藝的實際應用.
2.5 穩定性實驗
電極材料的穩定性和重復利用性能是影響其應用的重要指標.圖10給出了FeMnOx/CF復合電極在MFC-EF耦合系統中循環使用6次時RhB的去除率.可以看出,循環使用過程中RhB的去除率略有下降,當重復使用6次時,FeMnOx/CF復合電極所在耦合系統對RhB的去除率由第1次的91.59%降至81.74%,說明FeMnOx/CF復合電極穩定性良好,能重復使用,同時也有提升空間,在后續研究中可以嘗試通過改變材料的制備條件進一步增強其穩定性.
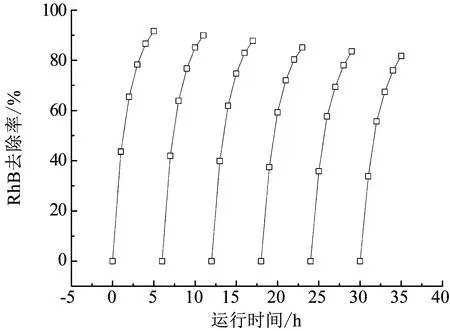
圖10 FeMnOx/CF復合電極的穩定性實驗結果
3 結 語
FeMnOx/CF復合電極作為MFC-EF耦合系統的一種陰極材料,可以在耦合系統中同時實現電能、H2O2、芬頓反應催化劑(鐵離子和錳離子)的原位產生和利用,并達到降解、礦化污染物的目的.與Fe&Fe2O3/CF復合電極、CF無負載電極相比,FeMnOx/CF復合電極所在MFC-EF耦合系統的產電性能和污染物去除效率均有所提升.此外,FeMnOx/CF復合電極擴大了常規Fenton體系嚴格的陰極液pH范圍,并具有良好的穩定性.本研究有望促進MFC-EF耦合工藝的應用,并為染料廢水的處理提供新的思路.

