404 Not Found
404 Not Found
非天然手性氨基酸合成的研究進展
吳法浩
(南京紅杉生物科技有限公司,江蘇南京 210000)
非天然氨基酸是指自然界無法直接獲得的一類非蛋白光學性氨基酸。這類氨基酸通常無法通過發酵獲得,只能通過化學合成或者構建工程菌發酵產酶,進行酶催化合成。合成工藝在日本起步較早,而中國是在20世紀90年代才開始研究開發。早期的非天然氨基酸大部分以進口為主,價格較高,例如在2004年前后,D-半胱氨酸鹽酸鹽,D-色氨酸,D-苯丙氨酸等系列非天然氨基酸的價格都在3 000~5 000元/kg不等。隨后,國內公司逐漸開始了非天然氨基酸的合成研發,比較早實現工業化的國內公司有南京紅杉生科技有限公司、上海瀚鴻化工科技有限公司、湖南福來格生物技術科技有限公司以及洛陽華榮生物科技有限公司等。隨著技術的進步,國內合成非天然氨基酸的技術水平得到了很大的提高,成本和價格均大幅下降,目前非天然氨基酸的價格基本都維持在在1 000元/kg以內,甚至一些技術已經領先日本等國家。非天然氨基酸的結構通式如圖1所示。
在該通式中,R基團代表烷基、芳香基等各種取代基團,構成了具有特殊手性中心的手性化合物。這個結構上的羧基又可以通過不同的方式進行還原、酯化等保護,形成不同的手性化合物。氨基也可以進行叔丁氧羰基(Boc)、芐氧羰基(Cbz)以及笏甲氧羰基(Fmoc)等各種基團的保護,形成手性化合物進入手性藥物的側鏈。傳統手性藥物的手性中心,大部分通過不對稱催化或者拆分實現,這種方法效率和手性純度不高,極大地限制了手性藥物的發展。所以解決非天然氨基酸的合成問題對手性藥物的發展具有重要意義。
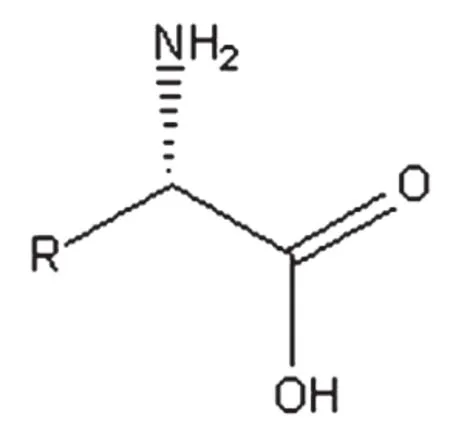
圖1 非天然氨基酸的結構通式
1 非天然氨基酸性質及功能
1.1 非天然氨基酸性質
非天然氨基酸和天然氨基酸的結構相似,只是手性方向不同,大部分水溶性較好,熔點較高,一般都在200 ℃以上,游離狀態比較穩定,以內鹽形式存在。非天然氨基酸都有氨基和羧基,且比較活潑,在后期的基團轉變中有著較大的天然優勢。比較常見且用途廣泛的非天然氨基酸如圖2所示。
1.2 非天然氨基酸功能
圖2中各種非天然氨基酸在醫藥領域用途廣泛,具體功能如下。
D-丙氨酸可以合成D-丙氨醇,向下合成R-3-甲基嗎啉[1],成為阿爾茲海默癥藥物的中間體。
L-2-氨基丁酸可以合成L-2-氨基丁酰胺鹽酸鹽,是合成左乙拉西坦的關鍵中間體[2]。左乙拉西坦是比利時優時比制藥公司(UCB)研發的具有全新抗癲癇機制藥物,屬于吡咯烷酮類西坦類,是神經系統主要用藥系列之一,具有不良反應較少且輕、耐受性好等優點;主要用于成人以及4歲以上兒童癲癇患者部分性發作的治療;此外,還具有一定的抗炎、鎮痛和抗抑郁等作用。
L-正纈氨酸是合成培哚普利的主要中間體[3],培哚普利(Perindopril)為第三代血管緊張素轉換酶抑制劑,服后6 h降壓效果最好,作用持續時間長。培垛普利可擴張大、小動脈,減少血容量,降低系統血管阻力、左室充盈壓和肺毛細血管楔壓,增加心排血量和每搏輸出量,增加心臟指數而不改變心率,提高患者運動耐量,減輕左室心肌肥厚,改善血流動力學。本品耐受性好,不會引起高血糖,對血脂亦無不良影響。培哚普利服后對血管緊張素轉換酶(ACE)的抑制較其他抑制劑起效慢,但對ACE的抑制率達90%以上。
D-纈氨酸是鹽酸沃尼妙林的中間體[4],沃尼妙林(Valnemulin,VA)是新一代廣譜的截短側耳素類半合成抗生素,屬二萜烯類,是動物專用抗生素。
D-苯丙氨酸是合成那格列奈的中間體[5],那格列奈(Nateglinide)為硬膠囊劑,內容物為類白色,是D-苯丙氨酸衍生物,屬于非磺酰脲類降血糖藥。其作用機理主要為通過與胰島B細胞上磺酰脲受體相結合,阻滯胰島細胞ATP敏感鉀通道的開放,導致細胞膜去極化,引起鈣通道開放,促進胰島素分泌。那格列奈是一種新型餐時血糖調節劑,能有效控制餐后血糖水平,具有起效快、作用時間短、引起心血管副作用和低血糖發生率低等特點。
D-色氨酸是合成他達那非的主要中間體,他達那非可以治療男性勃起功能障礙(ED)。作用原理和西地那非、伐地那非相同,都是依靠磷酸二酯酶抑制劑(PDE-5)通過抑制環磷鳥苷(cGMP)的分解來提高NO的血管擴張作用,使ED病人重新獲得陰莖勃起的能力,他達那非服用后通過腸胃吸收。
D-酪氨酸是抗心衰藥物沙庫必曲的關鍵中間體[6],entresto是結合sacubitril,一腦啡肽酶抑制劑,和纈沙坦,血管緊張素Ⅱ受體阻斷劑,以減少風險心力衰竭患者的心血管死亡及住院治療慢性心力衰竭(NYHAII-IV級)和射血分數降低。
D-絲氨酸是拉科酰胺的中間體[7],拉科酰胺是治療癲癇和神經性疼痛的藥物。
D-半胱氨酸是合成頭孢米諾鈉的中間體[8],頭孢米諾鈉,別名美士靈、Cefminox、meicilin,為頭霉素衍生物,由半合成法制取,其作用性質與第三代頭孢菌素相近,制成品為七水合物。常用其鈉鹽,為白色或微黃白色結晶性粉末,溶于水,其作用性質與第三代頭孢菌素相近。
D-蘇氨酸是合成頭孢拉宗的中間體。頭孢拉宗(Cefbuperazone)是一種固體化學品,別名頭孢布宗、頭孢羥哌嗪鈉、乙氧哌甲氧頭孢菌素、克波阿宗、頭孢布哌拉唑、Cefobutazine、Keiperazon、Tomiporan、BMY-25182。分子式為 C22H29N9O9S2,分子量627.651,熔點118~120 ℃。臨床上用于大腸桿菌、沙雷菌屬、普通及奇異變形菌、流感嗜血菌、肺炎球菌等敏感菌引起的敗血病、慢性支氣管炎、肺炎、肺化膿性疾病、心內膜炎、膽囊炎、腹膜炎、膀胱炎等。
L-叔亮氨酸是合成抗病毒藥物阿扎那韋的關鍵側鏈[9],阿扎那韋以商品名Reyataz銷售的阿扎那韋是蛋白酶抑制劑(PI)類的抗逆轉錄病毒藥物。與其他抗逆轉錄病毒一樣,可用于治療人類免疫缺陷病毒(HIV)的感染。阿扎那韋與其他PI的區別在于,可以每天給予1次(而不是每天需要多次劑量),且對患者的脂質分布(血液中膽固醇和其他脂肪物質的量)具有較小的影響。與其他蛋白酶抑制劑一樣,阿扎那韋僅與其他HIV藥物組合使用。美國食品和藥物管理局(FDA)于2003年6月20日批準阿扎那韋,這是被批準用于每日1次給藥的第1個PI,且引起脂肪營養不良和膽固醇升高等副作用的可能性較小,可以不與其他PI交叉耐藥。當用利托那韋加強時,會降低阿扎那韋的代謝優勢,但其與洛匹那韋的效力等效,可以用于具有一定程度耐藥性患者的補救治療,是世界衛生組織基本藥物清單上和基本衛生系統所需的重要藥物之一。
D-脯氨酸是合成依來曲普坦的中間體[10],依來曲普坦可用于治療偏頭疼,該藥物原研發自美國Pfizer公司,在2001年上市。
2 非天然氨基酸的合成方法
2.1 化學拆分劑拆分法
如圖3所示,以混旋的DL-非天然氨基酸為底物,用酒石酸、DBTA、樟腦磺酸、扁桃酸等手性拆分劑進行拆分分離[11]。這種拆分劑化學拆分會有天然的弊病,拆分效率只能達到50%,對工藝結晶條件比較苛刻,控制不好,手性容易超標,達到99%以上的手性純度相對比較困難。
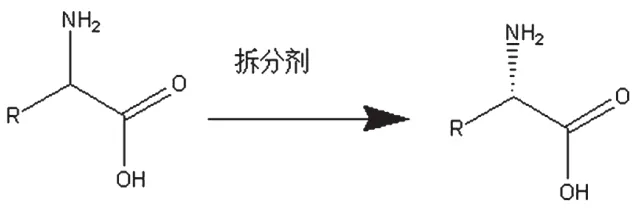
圖3 化學拆分劑拆分機理
2.2 酰化水解酶拆分
如圖4所示,以N-乙酰-DL-氨基酸為底物,用L-酰化水解酶或者D-酰化水解酶[12]通過化學手段水解或者分離得到非天然氨基酸。酰化水解酶拆分氨基酸中,D-酰化水解酶普遍性不好,很多非天然氨基酸只能用L-酰化水解酶,而L-酰化水解酶需要再通過化學手段酸解來實現D-氨基酸的合成,酸解時對氨基酸會造成破壞,導致整體收率不高,因此工業價值越來越低。
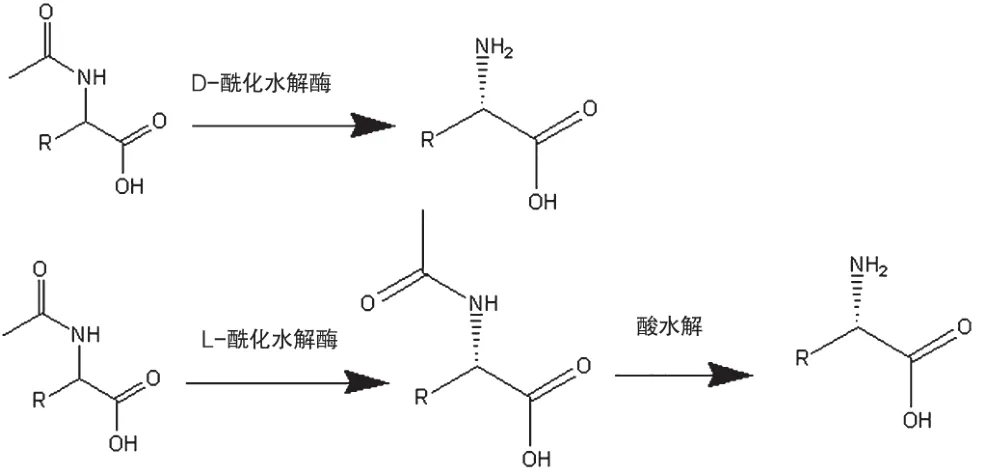
圖4 酰化水解酶拆分機理
2.3 不對稱轉化法
如圖5所示,不對稱轉化法是以單一構型氨基酸為原料,以有機酸為溶劑,醛類為消旋劑,添加手性拆分劑,通過溶解度差異形成動態拆分的過程[13]。該方法目前在工業中應用較多,但是非天然氨基酸是大類產品,每個產品復鹽的溶解度不盡相同,所以在特殊的產品上也無法應用。
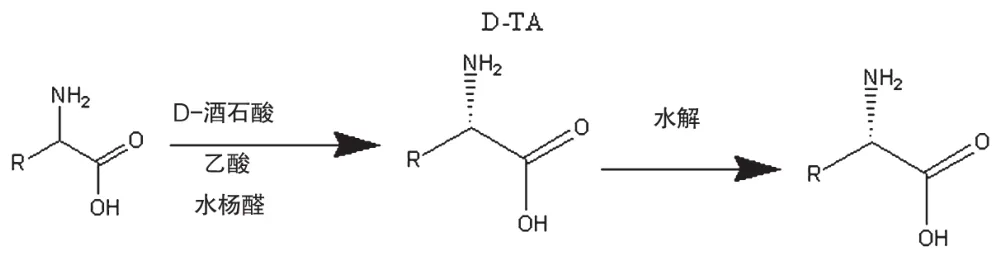
圖5 不對稱轉化法動態拆分機理
2.4 化學合成
如圖6所示,化學合成是以一個手性化合物為底物,采用化學手段進行合成[14]。R1可以是鹵素系列(圖6b),這個路線也只能針對少數產品的合成,因為手性前體比較難獲得,導致這個路線不能大規模應用,而且在氨化過程中存在手性翻轉,得到的手性氨基酸容易出現手性純度不夠。

圖6 化學拆分劑拆分機理
2.5 脫氫酶法
脫氫酶法是通過酮底物利用轉氨酶或氨基酸脫氫酶,提供合適的氨供體,加入輔酶NAD,進行酶催化得到手性非天然氨基酸,L-氨基丁酸[15]和L-叔亮氨酸[16]的合成都是用該方法合成。
2.6 海因法
海因法最早應用在對羥基苯甘氨酸的合成上,包括合成氨基酸海因前體,韋萍[17]通過海因酶和氨甲酰水解酶的共同作用,實現了非天然氨基酸的合成,并提出了氨基酸海因自發消旋的動力學原理。隨后,南京紅杉生物科技有限公司等也開始研究海因法合成氨基酸。海因法合成氨基酸的原理如圖7所示。
海因法比較好地實現了非天然氨基酸的合成,收率和轉化率都達到了比較高的水平,每個取代海因的性質不同,海因底物的自發消旋的動力也不盡相同,而海因酶的溫度耐受度是有限的,這也就導致了海因酶法無法實現個別氨基酸轉化水解的合成目的。因此,有學者研究了海因消旋酶,完整地解決了海因法合成非天然氨基酸的難題[18]。
2.7 誘導拆分法
如圖7所示,以混旋的非天然氨基酸為底物,通過過飽和溶液,加入晶種,控制降溫速度和攪拌速度,緩慢結晶,通過溶解度差異,達到拆分分離的過程。母液可以重復套用,富集到一定程度則不能再使用,可濃縮結晶回收另外一半非天然氨基酸。D-谷氨酸[19]和D-蘇氨酸[20]就是用這種方式合成獲得。
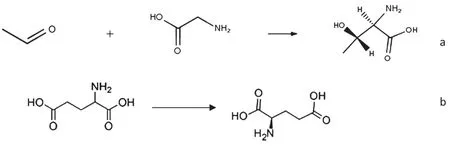
圖7 誘導拆分法機理
2.8 氧化酶法
氧化酶法是以混旋的非天然氨基酸為底物,通過工程菌氨基酸氧化酶,根據需要把L-氨基酸或D-氨基酸氧化為酮酸,保留需要的L-氨基酸或D-氨基酸,從來獲得需要的手性非天然氨基酸產物[21]。
3 結論與討論
合成非天然氨基酸的方法還有很多種,包括膜分離方法、電泳法、層析法等。這些方法無法滿足現有工業化條件,意義不大。文中詳細論述的幾種路線都是可以工業化的路線,也是非天然氨基酸發展史上使用過的方法,其中在工業生產中主要采用不對稱轉化法、脫氫酶法和海因法3種方法,其他方法因成本問題或拆分弊端而無法實現高手性純度非天然氨基酸的合成。其中不對稱轉化法是化學法合成的典型特例,脫氫酶法和海因法是合成非天然氨基酸的生物方法典型特例。
隨著社會的發展和環保意識的加強,化學法的壓力越來越大,未來生物法合成非天然氨基酸必然取代化學法,而生物法要想長久發展,也需要減少排放和發酵體量,降低COD的處理難度。因此,應將固定化酶生物轉化作為現有基礎上新的研究方向,或者獲得更高效率的工程菌來減少酶的用量。
非天然氨基酸作為非蛋白氨基酸,發展較晚,在人體內也并未發現,前期重視不夠,國內合成非天然氨基酸的起步也較晚。但是隨著手性藥物的發展,研究人員也越來越重視非天然氨基酸的合成。分子生物學的突飛猛進,使得人類基因組計劃、定向進化、合成生物學等各學科得到了發展,為非天然氨基酸的合成奠定了強有力的基礎。目前,國內非天然氨基酸的市場缺口還很大,隨著技術的進步,這類手性氨基酸必將在醫藥、食品等行業發揮巨大的作用。
