個性化方案治療惡性青光眼的療效分析
陳曉莉,賓 莉,徐智科
0引言
惡性青光眼的概念首先由Von Graefe于1869年提出,惡性青光眼也稱為睫狀環阻滯性青光眼或房水迷流綜合征[1],目前普遍可接受的定義是:原發性閉角型青光眼術后和其他眼前段手術之后,在有明確虹膜周邊切除孔的情況下,出現淺前房、高眼壓,使用縮瞳劑可使病情加重,睫狀肌麻痹劑可使之緩解,常規手術治療無效[2]。本研究通過對惡性青光眼患者的臨床資料進行回顧性分析,探討惡性青光眼的個性化治療方案。
1對象和方法
1.1對象回顧分析2016-01/2018-10在我院眼科接受治療的惡性青光眼患者19例19眼的臨床資料。其中女11例,男8例,年齡30~75(平均53.4±10.2)歲,發病時間為1~14d,術前LogMAR視力0.1~1.7(平均0.71±0.25),眼壓25~61(平均31.25±5.19)mmHg,經UBM測得前房深度0.25~1.79(平均0.69±0.57)mm,眼軸長度20.33~22.57(平均21.24±0.53)mm。惡性青光眼診斷標準:抗青光眼或其他內眼術后前房變淺或消失,眼壓升高,睫狀肌麻痹劑治療有效,虹膜周邊切除孔通暢,無濾過泡滲漏、睫狀體脈絡膜脫離及脈絡膜出血等眼后節改變。19例19眼患者中小梁切除術后11 眼,小梁切除聯合白內障超聲乳化吸出+人工晶狀體植入術后7眼,小梁切除聯合白內障超聲乳化吸出術中1眼。所有治療方案的優缺點均告知患者,尊重患者意愿,患者充分理解病情后作出選擇,簽署手術同意書。
1.2方法所有惡性青光眼患者初期均先采用藥物治療方案,用藥情況相同,藥物不能緩解病情再根據患者不同的眼部情況選擇不同的手術方案。
1.2.1藥物治療睫狀肌麻痹劑:硫酸阿托品眼膏2次/d;糖皮質激素:妥布霉素地塞米松眼液2h一次,妥布霉素地塞米松眼膏每晚一次,球周注射20mg曲安奈德。局部降眼壓藥物:噻嗎洛爾眼液2次/d,布林佐胺眼液3次/d,溴莫尼定眼液2次/d。全身用藥:20%甘露醇注射液250mL,30min內輸注完畢。7眼(37%)經藥物治療后眼壓下降、前房恢復。
1.2.2手術方法(1)3眼(16%,小梁切除聯合白內障超聲乳化吸出+人工晶狀體植入術后)采取YAG激光虹膜周邊切除+后囊膜切開+玻璃體前界膜切開,選擇下方6∶00位進行,后續以上述抗炎及麻痹睫狀肌藥物治療,眼部炎癥完全消退后停藥。(2)2眼(11%,小梁切除聯合白內障超聲乳化吸出+人工晶狀體植入術后)采取前部玻璃體切除+后囊膜切除,采用后入路,通過瞳孔窺及玻璃體切割頭后行前段玻璃體以及大小約4~5mm左右的晶狀體后囊膜切除,術后予以局部抗炎治療。(3)5眼(26%,小梁切除術后)采取白內障超乳化+人工晶狀體植入+前部玻璃體切除+后囊膜切除術,術中先采用后入路,透過瞳孔區可見玻璃體切除頭后切除部分玻璃體軟化眼球,在黏彈劑注入前房并分離周邊前粘連虹膜,完成超聲乳化白內障+后房型人工晶狀體植入,再用玻璃體切割頭切除中央后囊膜及前段玻璃體,術后予以局部抗炎治療。(4)1眼(5%,小梁切除術后)30歲年輕女性不愿喪失自身眼調節能力的患者采取單純標準25G玻璃體三通道玻璃切除術,術后需一直使用阿托品眼膏維持治療。(5)1眼(5%)在擬行小梁切除+白內障超聲乳化術中于透明角膜緣穿刺前房注入黏彈劑時發現前房難以維持,虹膜至穿刺口脫出,指測眼壓T+2,在排除爆發性脈絡膜上腔出血可能性后,考慮發生術中惡性青光眼,在顳下方角膜緣后3.5mm處用1mL空針行玻璃體腔穿刺抽液,約0.4mL,再完成超聲乳化晶狀體核,抽吸干凈皮質,前房注入黏彈劑,行上方小梁切除,水密縫合鞏膜瓣4針(其中2針為可調整縫線),抽吸干凈黏彈劑后水密切口形成前房,指測眼壓Tn。所有患者隨訪6~18(平均9.2±3.5)mo,觀察治療前后最佳矯正視力、眼壓,UBM檢查的前房深度及術后并發癥。
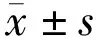
2結果
2.1治療前后最佳矯正視力比較最后一次隨訪時最佳矯正視力(LogMAR)為0~1.2(平均0.34±0.19),與治療前0.1~1.7(0.71±0.25),差異有統計學意義(t=3.26,P<0.01)。
2.2治療前后眼壓比較隨后一次隨訪眼壓為8~21(平均14.43±3.46)mmHg,與治療前(31.25±5.19mmHg)相比,差異具有統計學意義(t=12.6,P<0.01)。
2.3治療前后前房深度比較最后一次隨訪時UBM測前房深度1.95~3.57(平均2.64±0.47)mm,與治療前(0.69±0.57mm)相比,差異具有統計學意義,(t=14.73,P=<0.01)。
2.4手術并發癥情況所有患者手術后局部基本都有輕度角膜水腫和無菌炎癥反應,予以妥布霉素地塞米松眼液點眼治療, 2wk左右前房無菌炎癥基本完全消退。1眼出現低眼壓、脈絡膜脫離,給予抗炎、麻痹睫狀肌治療后脈絡膜脫離治愈,眼壓恢復正常。無其他如角膜內皮失代償、感染、出血、視網膜脫離等并發癥,術后結膜濾過泡形態基本無改變。
3討論
惡性青光眼可見于各種眼科術后,抗青光眼術后發生率較高,劉春義等[3]報道閉角型青光眼術后惡性青光眼的發病率為2.79%。目前研究發現,惡性青光眼可能是在異常眼部解剖結構(睫狀環縮小、房角窄,眼軸短等)的基礎上,多個致病因素和發病機制共同參與的病變過程[4]。目前多認為與以下機制相關:(1)房水后潴留,如睫狀體-晶狀體或睫狀體-玻璃體阻滯,或是前玻璃體阻滯。(2)晶狀體懸韌帶松弛造成晶狀體-虹膜隔前移,房水向前排出受阻,逆流-潴留在玻璃體腔的惡性循環過程。
惡性青光眼發生后首選藥物治療,包括局部應用睫狀肌麻痹劑,睫狀肌松弛,睫狀環阻滯緩解,晶狀體懸韌帶緊張,使晶狀體-虹膜隔后移,前房恢復,眼壓下降;房水生成抑制劑,降低眼壓和減少玻璃體內水袋的房水;高滲劑使玻璃體脫水;眼局部及全身使用糖皮質激素,減輕炎癥反應和睫狀體水腫等[5]。我們的研究中藥物治療的有效率為僅有37%,但患者術后早期炎癥反應重,再次手術創傷大,部分患者不愿短時間內接受再次手術,藥物治療在一定程度上可緩解患者的經濟、精神壓力,部分患者甚至通過藥物治療獲得痊愈,所以惡性青光眼發生后應首選藥物治療。但藥物效果不佳者或者反復發作的惡性青光眼患者,則需通過手術治療重構患眼前后節房水循環通道,逐次解除各個解剖阻滯節點[6]。
當人工晶狀體眼發生惡性青光眼時,樊寧等[7]認為可試行Nd∶YAG 激光經虹膜周邊切除口打斷睫狀突、懸韌帶周圍的滲出物、粘連組織(包括周邊的晶狀體囊膜和玻璃體前界膜),達到溝通前后房,糾正房水逆流的目的。本研究中有3眼人工晶狀體眼發生惡性青光眼的患者通過Nd∶YAG激光行虹膜周邊切除+后囊膜切開+玻璃體前界膜切開,激光治療瞬間可見房水涌進前房,前房立刻加深。該組患者年齡偏大,視力相對較差,對再次手術有顧慮,與患者溝通病情后選擇相對保守的激光治療,但也收獲了良好的效果。有報道對于白內障超聲乳化術后發生惡性青光眼采取YAG激光后囊膜切開有效率超過80%[8]。而對于囊袋內植入囊膜黏附性好的人工晶狀體的情況下,僅做中央部后囊膜和玻璃體前界膜切開是不夠的;而對于睫狀溝固定的人工晶狀體,有可能人工晶狀體(包括襻)與囊膜沒有形成緊密的屏障,中央部激光切開可能有效。該治療方案中需特別注意周邊前后房的溝通:包括虹膜周邊切口及其后面的晶狀體囊膜、懸韌帶、前段玻璃體和粘連組織的清除,才能充分溝通前后房,恢復房水流出通道[9]。本研究中另有2眼人工晶狀體眼經藥物治療無效的惡性青光眼患者,術前視力較好,對再次手術易于接受,選擇了后入路的前段玻璃體切除+后囊膜切開,該方案較YAG激光行后囊膜切開+玻璃體前界膜打開更為徹底的糾正了睫狀環-玻璃體、睫狀環-人工晶狀體阻滯,避免了YAG激光后玻璃體再次嵌頓阻塞后囊膜切開口及虹膜周邊切除口,導致后房水不能流入前房,眼壓再次升高。但該方案為再次手術,需注意切口滲漏、眼內炎、術后低眼壓和脈絡膜脫離、人工晶狀體偏位、視網膜脫離等風險。孫建軍[10]報道采用23G微創玻璃體切割術治療青光眼術后惡性青光眼效果明確,患者術后最佳矯正視力得到改善。隨著微創玻璃體切除手術的發展,特別是25G+微創玻璃體手術的開展,多能安全有效地完成前部玻璃體切除聯合晶狀體后囊膜切開,并且創傷較輕[11]。
本研究中有5眼行小梁切除術后發生惡性青光眼的患者,前房極淺,選擇了行白內障超聲乳化+人工晶狀體植入+前部玻璃體切除+后囊膜切開術,超聲乳化白內障+后囊膜切開能夠在一定程度上改善玻璃體腔內液體向前房流動受阻的狀態,一方面晶狀體體積減小降低了瞳孔阻滯力,另一方面晶狀體囊膜在白內障術后發生收縮,晶狀體直徑減小,加寬了晶狀體睫狀體間隙,使玻璃體腔內液體向前房流動的面積增加從而增加流量[12]。如果晶狀體-虹膜隔前移壓力主要來自玻璃體腔,那么單純的白內障手術不能有效解決房水的迷流,需同時行前段玻璃體切除打破玻璃體前界膜完整性,同時切透至玻璃體水囊,有效預防玻璃體液體聚集而導致的玻璃體腔高壓力狀態[13]。該術式中需注意切除干凈前段周邊玻璃體特別是虹膜周邊切除口后的玻璃體,徹底打破晶狀體囊膜和囊袋內固定的人工晶狀體復合體及玻璃體囊韌帶的阻隔,傅婷等[14]在白內障超聲乳化聯合前段玻璃體切除術治療惡性青光眼治療效果欠佳的病例中再次手術時采用了周邊虹膜及周邊晶狀體囊膜、前段周邊玻璃體切除,術后患者眼壓、前房恢復理想。
本研究中還有1例小梁切除術后惡性青光眼患者為30歲年輕女性,術前裸眼小數視力0.8,患者因擔心白內障術后喪失眼調節能力,不能視近,不愿摘除自身晶狀體,采用單純玻璃體切除術,術后輔以阿托品麻痹睫狀肌治療,1wk內眼壓控制好,前房深度恢復,后停用阿托品眼膏,患者再次出現前房變淺,眼壓升高,目前一直處于阿托品依賴狀態。還有1例老年男性患者在小梁切除+白內障超聲乳化吸出術中出現前房不能形成,眼壓增高,行玻璃體腔水囊穿刺抽液后完成手術,術后患者前房形成好,眼壓控制,該例患者術前視神經損傷重、視野極晚期,手術目的僅為降低眼壓保持眼球外觀,同時患者經濟條件差,術中發生惡性青光眼后我們選擇了花費相對較小的玻璃體腔穿刺,而不是選擇進一步行前段玻璃體切除。
充分把握惡性青光眼的特點和發病規律,診治及時果斷,先藥物治療,若藥物不能緩解采用創傷小的手術干預,若仍不能緩解,采用徹底手術治療[15]。惡性青光眼患者病情復雜,手術風險大,具體手術方案應根據患者自身眼部狀態、經濟承受能力以及各醫療機構自身的診療水平等多因素綜合考慮,以對眼球最小的侵襲達到最佳療效,為患者制定個性化安全有效的治療方案。

