Paternò-Büchi(PB)反應與串聯質譜結合實現不飽和脂質精確結構解析
馬瀟瀟,胡清源,瑕 瑜
(1.清華大學 精密儀器系 精密測試技術及儀器國家重點實驗室,北京 100084;2.清華大學 化學系,北京 100084)
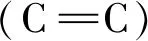


本文主要介紹基于PB反應的脂質分析的基本原理,以及適用于脂質衍生化的電噴霧質譜(ESI-MS)實驗設置。以不同類型脂質(如甘油磷脂、脂肪酸和膽固醇酯)為例,介紹了脂質結構解析和定量分析的基本方法。該方法既可直接用于鳥槍脂質組學分析,也可與液相色譜聯用。本衍生方法無需對質譜儀器做改造,通過紫外光源即可在離子源處實現脂質快速衍生化,裝置簡單,譜圖易解,有望在各類脂質分析中獲得廣泛應用。
1 Paternò-Büchi反應

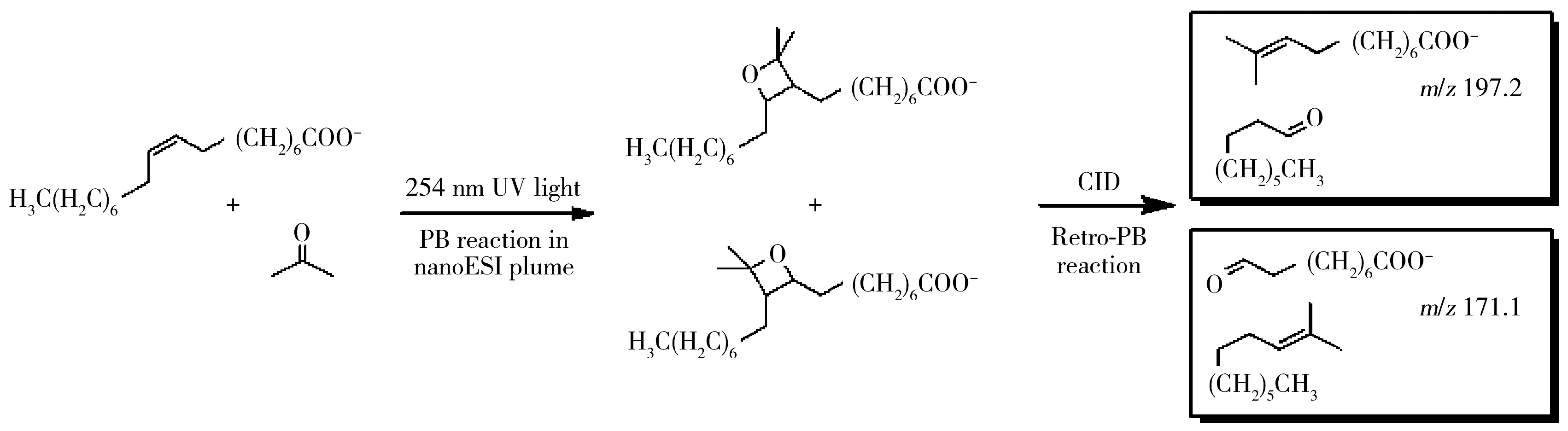
圖1 油酸和丙酮間的PB及逆反應
2 PB反應與ESI-MS聯用
2.1 光化學反應器
常規用于有機合成的PB反應體系通常體積較大[28-32],量子產率也較低(0.01~0.1),因此需要高濃度的反應試劑(mmol/L到mol/L)、較長的反應時間(3~24 h)和非極性溶劑條件[33]。然而,這些反應條件與電噴霧離子化不兼容。為將PB反應與ESI-MS聯用,本課題組發展了流式微反應器和nanoESI在線反應兩種分析模式。
2.1.1 流式微反應器發展流式微反應器(Flow microreactor)主要目的是使光衍生反應時間可調,使其能與常規ESI分析聯用。流式微反應器采用內徑 <1 mm的毛細管作為流道,可實現對UV照射時間的準確控制以及較高的光子效率,并可減少由過度或不均勻UV照射導致的副產物的生成。經過不斷優化,目前一般采用可透過UV輻射的熔融石英毛細管作為反應流道(外徑363 μm,內徑100 μm)。該裝置的流速可調范圍較大:從亞μL/min到亞mL/min[34-35]。將毛細管以0.5 cm間距繞在UV燈上(反應時間>10 s),或與UV燈距離0.5 cm保持平行(圖2A)。UV照射5 s后,PC 16∶0/18∶1(9Z)(5 μmol/L,在70∶30丙酮/水溶液中,1%乙酸)衍生化產物的離子強度基本與底物相當,轉化率約為50%。這種反應裝置可以提供比體相反應更高的產率,并顯著減少副反應。在該類型的反應器中,UV照射5 s后,反應即基本達到平衡。反應器的流速范圍(100 nL/min~50 μL/min)恰好與常規ESI-MS進樣的流速相當,因而兩者可以很好地聯用。
2.1.2 nanoESI在線反應在nanoESI在線模式下,衍生化反應在nanoESI噴針中進行。反應前,將5~10 μL不飽和脂質溶液(溶劑:50∶50丙酮/水,體積比)加入噴針中。采用發射波長254 nm的低壓汞燈作為激發光源。反應裝置示意圖如圖2B所示。盡管硼硅酸鹽玻璃對254 nm的UV光不透明,但噴針的尖端玻璃壁厚已降至μm水平,透光率大大增加,因而使得反應可在此處發生。丙酮既作為PB試劑,也作為nanoESI溶劑。以PC 16∶0/18∶1(9Z)(10 μmol/L,溶于50∶50 丙酮/水中,1%乙酸)為例,UV照射1~2 min后,在 +58 Da的位置清晰檢測到光衍生化產物(m/z818.6)。從提取離子流圖(XIC)可見,反應在1 min內即達到穩態。除PB產物外,一般還會檢測到少量由丙酮的諾里斯類型1斷裂和后續氧化所產生的副產物。nanoESI硼硅酸鹽玻璃噴針的使用大大簡化了實驗裝置的設計,實現了反應裝置和離子源一體化。但由于nanoESI噴針中的脂質溶液受電滲流驅動,因此該裝置僅對較小的流速范圍(20 ~100 nL/min)適用[36]。
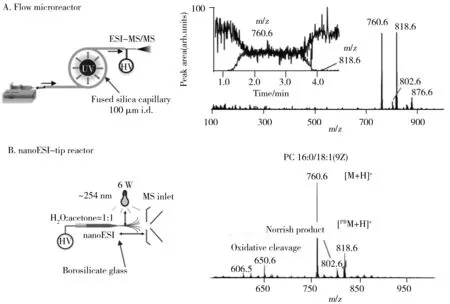
圖2 兩種反應器的脂質衍生化產率及反應動力學效果比較
在常規有機反應中PB反應通常需在mL級的有機溶劑中反應數小時,無法直接與ESI-MS聯用。使用nanoESI-噴針反應器或者流式微反應器極大地提高了PB 反應和分析的速度。PB反應和在線MS分析在20~30 s即可完成,僅需數μL脂質溶液。丙酮作為PB反應試劑具有與大部分溶劑混溶、廉價易得、可直接作為電噴霧溶劑等優點。而與nanoESI-噴針反應器相比,流式微反應器的優點是反應動力學可精確控制、產率高、副反應少。更重要的是,后者能在較寬的流速范圍內與ESI-MS及LC-MS聯用[37]。
2.2 溶 劑
選擇合適的溶劑對脂質的高效PB衍生化非常關鍵。合適的溶劑應該至少具備溶解性好和對紫外光呈惰性兩個特點。例如,對脂肪酸和極性脂質(甘油磷脂(GPs)和鞘磷脂(SMs)等)而言,丙酮/水是最佳的溶劑體系。在丙酮/水中,PB反應的產率較高,同時丙酮/水也是良好的電噴霧溶劑。在溶解性方面,濃度在~100 μmol/L的脂質均可溶于丙酮/水。而對非極性脂質(如糖脂和固醇酯)而言,丙酮/水并非最佳的溶劑體系。例如,用于膽固醇酯(CE)在線衍生化的最佳溶劑體系是含有100 μmol/L LiOH的丙酮/甲醇/二氯甲烷/水(40∶30∶20∶10,體積比)體系[38]。
2.3 副反應
254 nm UV輻射會導致丙酮發生諾里斯類型1斷裂[39-40],產生乙酰基(·C(O)CH3)和甲基(·CH3)。這些自由基會從脂肪酰/烷鏈中捕獲丙基氫,產生脂質自由基。脂質自由基會繼續與甲基或乙酰基結合,產生穩定取代產物。為了有效減少諾里斯類型1副反應對脂質分析的不利影響,可適當減少紫外光照射時間。盡管反應產率會有所下降,卻可以大大降低副反應的干擾。此外實驗發現,如果在溶劑體系中加入乙醇等醇類物質,也會在降低PB反應產率的同時,提高反應的選擇性,這對于多不飽和脂質的分析往往是有利的。但要注意醇類物質也會被自由基奪氫,并繼續與不飽和脂質反應。導致副產物生成的另一個因素是氧氣。一般而言,PB反應需在無氧條件下進行。如果存在氧氣,反應過程中所產生的脂質自由基會迅速與氧氣反應,生成過氧化產物[41],其在抑制PB反應的同時會降低分析靈敏度。
2.4 典型PB反應規律

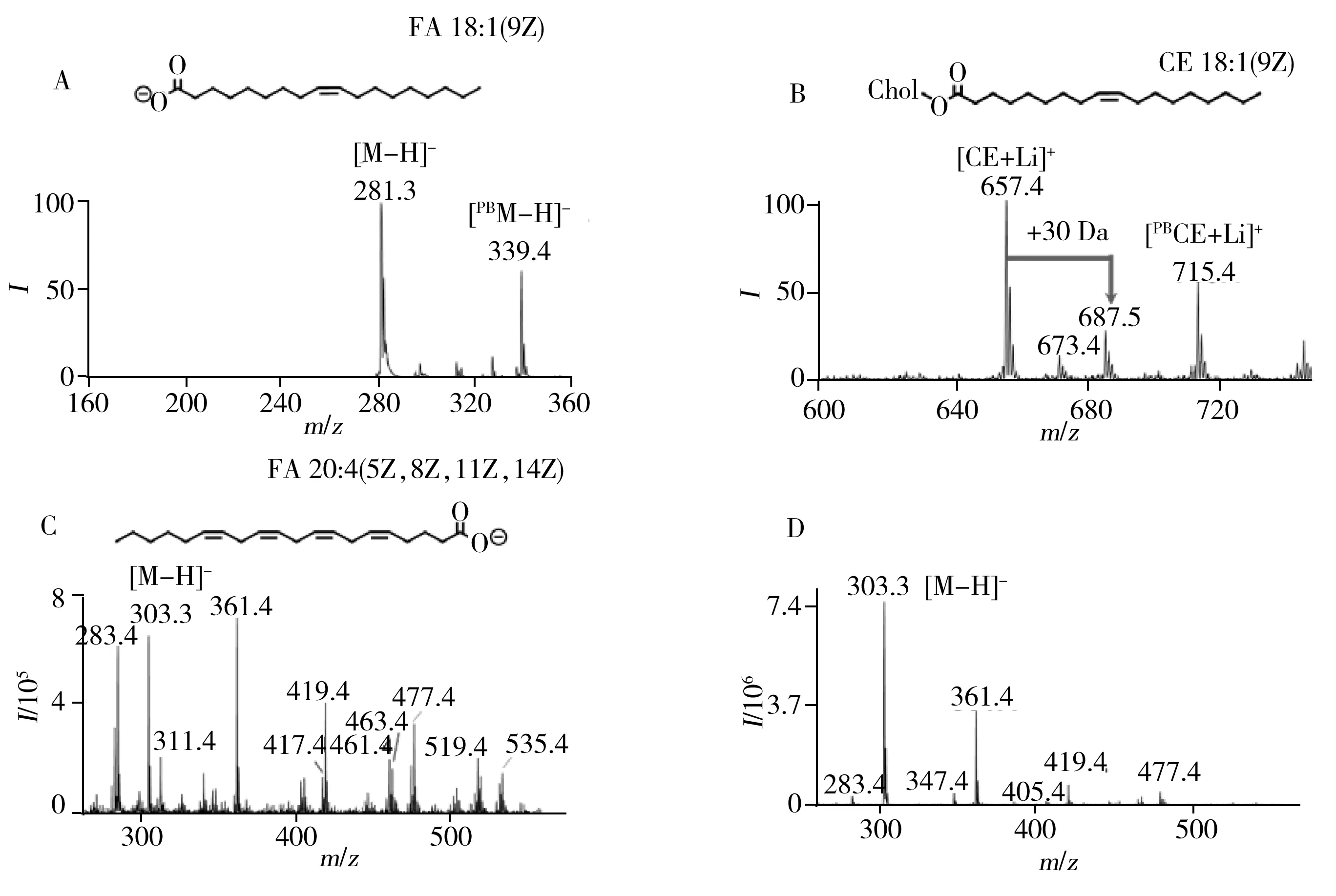
圖3 幾種典型脂質的衍生質譜圖
3 利用PB-MS/MS分析不同類型脂質的結構

3.1 脂肪酸的分析

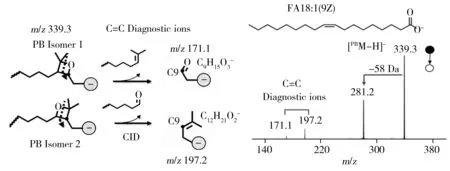
圖4 油酸(FA 18∶1(9Z))PB產物的碎裂規律及特征離子結構
3.2 不飽和甘油磷脂的分析


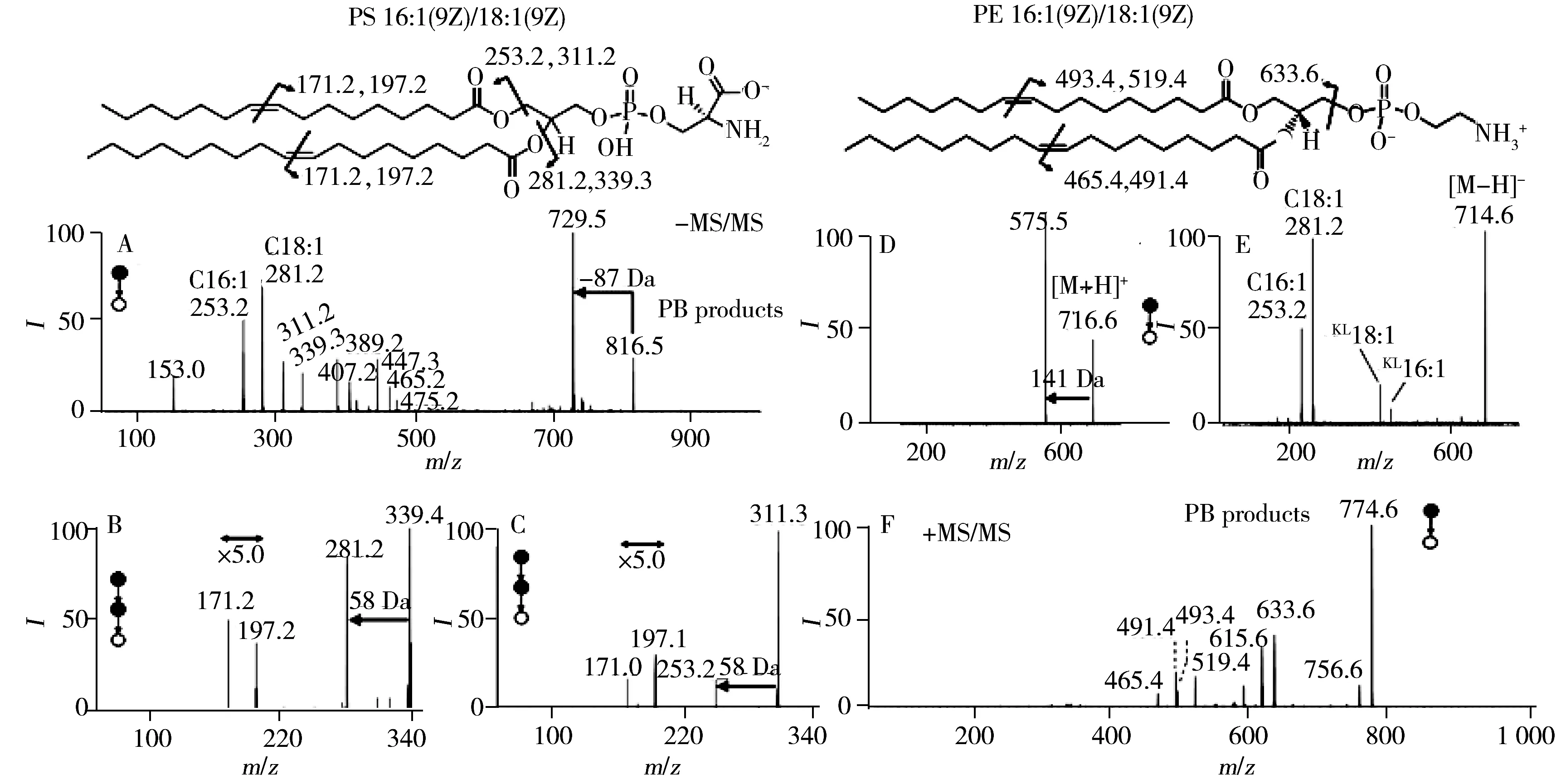
圖5 脂質結構解析的一般流程:PS 16∶1/18∶1在負離子模式下的PB-MS/MS譜圖(A),A中m/z 339.3處對應離子的MS3譜圖(B),A中m/z 311.2處對應離子的MS3譜圖(C),PE 16∶1/18∶1的MS/MS譜圖(D),在m/z 714.6處的去質子PE 16∶1/18∶1的MS/MS譜圖(E),PE 16∶1/18∶1在正離子模式下的PB-MS/MS譜圖(F)
3.3 膽固醇酯的分析
3.4 脂質位置異構體的定量分析
4 鳥槍脂質分析法
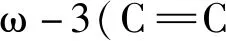
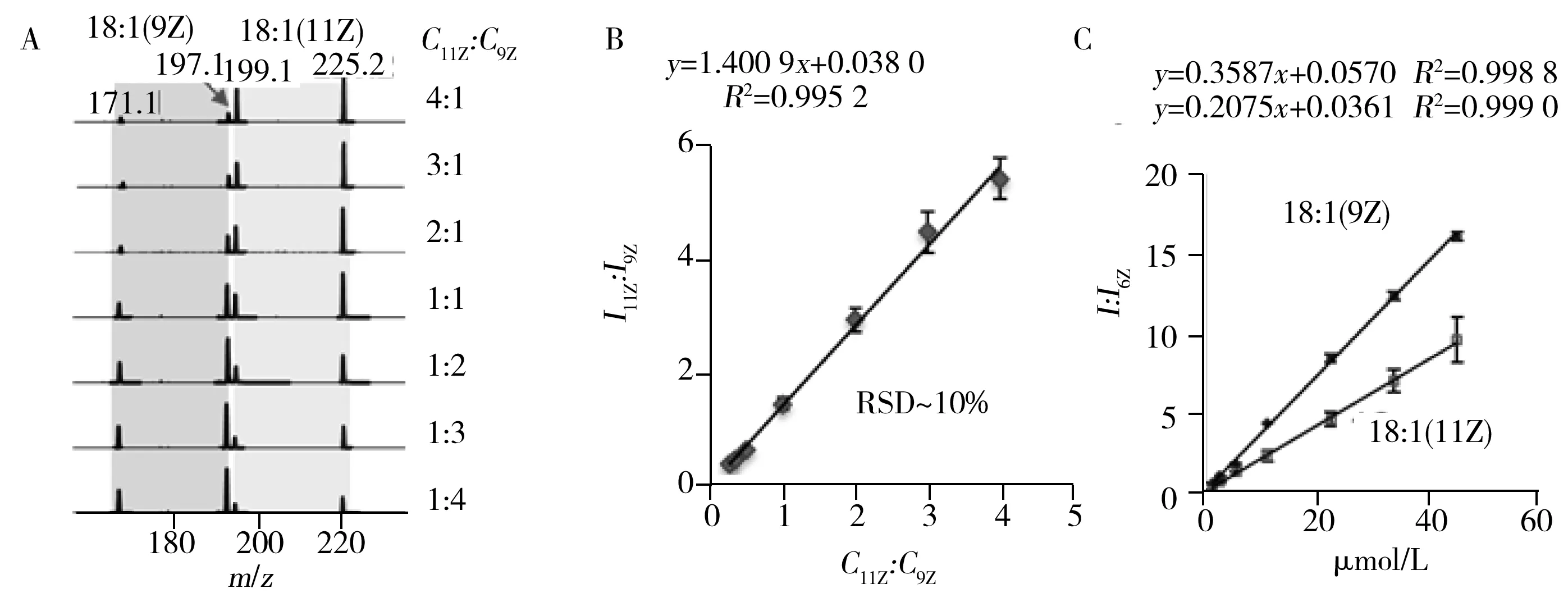
圖6 通過PB-MS/MS對脂質異構體進行定性和定量分析:不同摩爾比例(在右邊指出)的FA 18∶1的Δ9和Δ11混合物的PB-MS/MS分析(A);建立在FA 18∶1的Δ9和Δ11異構體的診斷離子比例(I11Z/I9Z)和摩爾比例(C11Z/C9Z)間的線性關系(B);以FA 18∶1(6Z)作為內標定量FA 18∶1的Δ9和Δ11異構體的標定曲線(C)
5 PB反應與質譜成像



6 結論與展望




