茶葉內含物質與外源污染物在沖泡過程中的浸出規律
陳紅平,劉新,魯成銀*,邱靜
茶葉內含物質與外源污染物在沖泡過程中的浸出規律
陳紅平1,2,3,劉新2,魯成銀2*,邱靜1*
1. 中國農業科學院農業質量標準與檢測技術研究所,北京 100081;2. 中國農業科學院茶葉研究所農業部茶葉產品質量安全風險評估實驗室,農業部茶葉質量安全控制重點實驗室,浙江 杭州 310008;3. 中國農業科學院研究生院,北京 100081
在收集相關文獻的基礎上,總結分析茶葉內含物質、農藥殘留與金屬元素在茶湯中的浸出規律。化合物的理化性質和茶葉沖泡方法是影響浸出率的內因和外因,其中內因起著決定性作用。茶湯中化合物浸出率與水溶解度呈正相關,與辛醇-水分配系數(辛醇/水)呈負相關。沖泡水溫升高能顯著提高茶葉內含物質與外源污染物的浸出率及其在茶湯中的濃度,沖泡時間與化合物浸出速率呈負相關,但隨著時間增加,茶湯中化合物的濃度顯著提高。新煙堿類農藥和氨基甲酸酯類農藥浸出率較高,大部分農藥浸出率高于60%。金屬元素在茶湯中的浸出率研究結果相差較大,氟、鎳、鈷在茶湯中浸出率較高,達到50%以上,鉛的浸出率在20%~50%。基于質譜分析代謝組學技術將在茶葉沖泡過程的化學物質浸出規律研究中發揮重要作用,熱力學理論基礎和傳質動力學模型將有利于更深層面認識外源有害物質在茶湯中的浸出行為。
茶葉沖泡;內含物質;農藥殘留;重金屬;浸出規律
茶葉的色、香、味等品質是茶葉沖泡過程中內含物質在茶湯中溶解、釋放的體現。茶多酚、咖啡堿、茶多糖、氨基酸、茶色素等特征成分溶解于茶湯中,形成茶葉獨特的香氣與滋味[1-2]。茶多酚是一類多酚化合物,主要有兒茶素、黃酮和黃酮類、酚酸及縮酚酸等。茶多酚易溶于熱水,是構成茶湯品質的基礎,一定程度上決定了茶湯的滋味及顏色。盡管咖啡堿呈苦味,但是咖啡堿與茶葉中的其他物質在茶湯溫度下降后形成絡合物,從而呈現鮮爽滋味。茶氨酸是茶葉游離氨基酸主要成分,占氨基酸總量50%~60%,具有焦糖香和鮮爽味,增加茶湯甜味和鮮味。茶葉呈香物質主要包括醇類、醛類、酸類、酯類、酮類、萜烯類,盡管呈香物質在茶湯中的溶解度差異較大,但茶葉沖泡過程中,呈香物質的釋放通常與時間、水溫及沖泡次數等因素密切相關。因此,茶葉內含物質在茶湯中溶解與釋放是茶葉滋味與香氣的化學物質基礎,是茶葉品質的決定性條件。
茶湯既是茶葉特征成分的載體,同時也是茶葉中外源有害物質被人體吸收的主要途徑之一。與其他農產品或食品不同,茶葉中外源有害物質在飲茶時并非完全進入人體,只有當有害物質溶解于茶湯后才被人體吸收,從而對人體構成潛在的健康風險。因此,有害物質在茶湯中的浸出率是茶葉中有害物質風險評估的關鍵參數。
本文在收集相關文獻基礎上,分別從茶葉特征成分、農藥殘留與金屬元素(重金屬)等三方面,總結分析茶葉內含物質和外源污染物在茶湯中的溶解、釋放與轉化規律,旨在探尋茶葉沖泡過程中物質遷移轉化的基礎規律,從而為茶葉品質調控、感官審評以及茶葉質量安全風險評估研究提供線索。
1 茶葉沖泡條件對內含物質浸出率的影響
多酚、咖啡堿、氨基酸、多糖、色素等特征成分在茶湯中的溶解與釋放不僅與化合物的理化性質相關,而且與茶葉的種類、形狀、水質、水溫、茶水比、沖泡時間、沖泡次數等相關[3-5]。我國將茶葉分為綠茶、紅茶、青茶(烏龍茶)、白茶、黃茶和黑茶,它們之間的差異不僅體現在茶葉品種、工藝和外形上,而且在沖泡方式和方法上也存在差異,從而體現茶葉品質特點。
1.1 沖泡溫度對內含物特征成分的影響
茶葉中內含物質的浸出是溶質分子(浸出物)在固相(茶葉)與液相(水相)之間的分配,并逐漸達到平衡狀態。浸出過程包括:水相進入茶葉固體內并溶解茶葉內含物,隨后溶質從茶葉內部液體中擴散而達到茶葉表面,最后溶質從茶葉表面通過液膜擴散而達到外部水相的主體。在此過程中,水溫是影響茶葉內含物浸出速度的關鍵影響因子之一。
茶葉沖泡溫度不同,內含物在茶湯中的溶解度和溶解速率不同,從而影響茶湯中可溶性成分含量,形成不同口感,影響茶湯品質[6-8]。Jin等[9]采用非靶向UPLC-QTOF/MS結合組學分析,通過主成分分析(PCA)和正交偏最小二乘判別分析(OPLS-DA),發現60℃與90℃水溫沖泡下的茶湯中內含物含量存在顯著差異。李再兵[10]研究發現,綠茶沖泡時水溫從60℃上升至100℃時,茶多酚、咖啡堿和氨基酸的浸出率均呈上升趨勢,浸出率分別提高70.22%、59.30%和46.34%(圖1)。金恩惠[11]研究發現,烏龍茶和普洱茶沖泡過程中可溶性物質的浸出量呈先上升至飽和濃度,再趨于平緩的趨勢。通過溫度對茶葉特征成分的影響分析,結合感官審評,烏龍茶與普洱茶的沖泡溫度推薦為100℃。劉曉莎[12]利用核磁共振技術,發現烏龍茶沖泡過程中,隨著水溫的增加,水浸出物、茶多酚、可溶性糖、游離氨基酸和生物堿均顯著增加(圖2)。Kelebek[13]研究發現,隨著水溫提高(從80℃上升到100℃),茶湯顏色發生顯著變化,抗氧化能力下降15.5%~36.6%,茶多酚、沒食子酸衍生物、黃烷-3-醇、羥基肉桂酸酯、茶黃素、咖啡堿含量分別上升17.2%、30.1%、45.5%、7.5%、18.1%和17.3%。Pérez-Burilloa等[14]研究發現,茶葉沖泡水溫60℃上升到98℃時,兒茶素和咖啡堿呈上升趨勢,尤其在70℃~90℃區間,上升更為明顯,同時茶湯抗氧化能力也顯著上升。兒茶素在高溫下(高于95℃)發生差向異構反應,由表沒食子兒茶素沒食子酸酯(EGCG)、表沒食子兒茶素(EGC)轉化為沒食子兒茶素沒食子酸酯(GCG)、沒食子兒茶素(GC)。因此當水溫從75℃上升到85℃時,茶湯中EGCG和EGC呈上升趨勢,而水溫從85℃上升到95℃時,EGCG和EGC呈下降趨勢[15]。
由此可見,茶葉內含特征物質隨著沖泡水溫提高,在茶湯中的浸出率增加。水溫增加,有助于提高化合物在水中的溶解度以及水對茶葉組織的滲透能力;同時水溫提高,加速茶葉組織破壞,增加茶葉組織間的空隙,從而有利于茶葉內含物質的溶出。
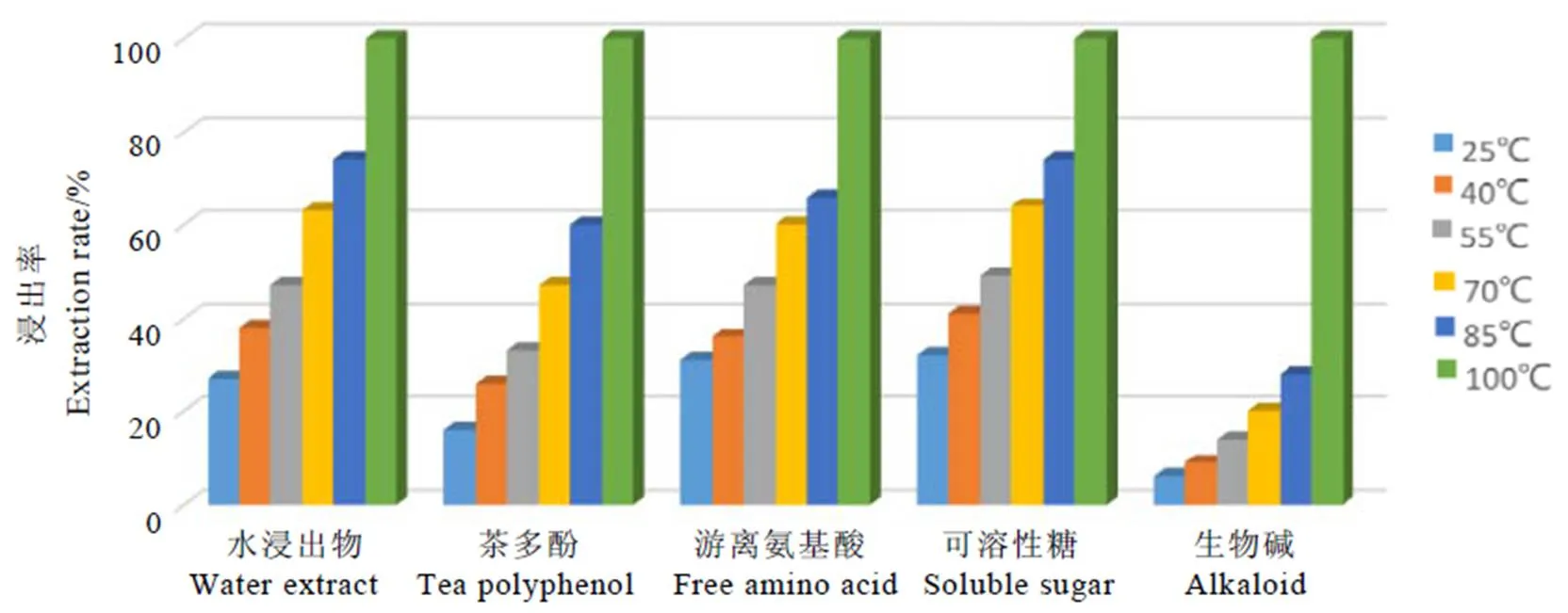
注:浸泡時間5?min,茶葉∶水=3?g∶150?mL Note: infusion time for 5?min and tea∶water=3?g∶150?mL
1.2 沖泡時間對內含物特征成分的影響
茶葉中內含物在茶湯中的浸出過程是一個動態平衡過程,但不是簡單的溶質分子在水相中快速達到平衡狀態,而是溶質分子從固相(茶葉)到液相(茶湯)中溶解、擴散和傳質的過程。在這個動態平衡過程中,時間是影響溶質分子在水相(茶湯)中含量的關鍵因素,在一定范圍內符合一級動力學方程。李再兵[10]發現綠茶中氨基酸的浸出率和沖泡時間符合一級動力學方程,如公式(1):
=7.504ln()+18.708(2=0.993)·······························(1)
式中為每100?mL的含量(mg),為時間(min)。
?lyaso?lu等[16]采用響應面統計軟件分析了沖泡時間和溫度對茶葉抗壞血酸、茶多酚的影響,并建立了數學模型(2)和(3),用于預測抗壞血酸和茶多酚在茶湯中的浸出率。
=3.229+0.002-0.1292+0.100-0.0542·······························(2)
=61.411+1.835-2.0112+1.358-2.5212·······························(3)
式中為每100?mL的含量(mg),為時間(min),為溫度(℃)
Jin等[9]研究發現,水溫為60℃時,在60?min內,茶湯中兒茶素總量隨溫度升高而增加,主要是由于GC、C、GCG和CG在茶湯中含量上升;在90℃時,茶湯中兒茶素總量在10?min內迅速上升,然后在10~30?min內呈下降趨勢,其主要原因是EGC、EC、EGCG和ECG向對應的差向異構體轉化。Gani等[17]采用273?nm波長作為HPLC-UV檢測波長,考查了監測信號與茶葉沖泡時間的關系,結果表明信號強度與沖泡時間呈正相關,由此說明,茶湯中內含物質隨沖泡時間延長而增加。Nikniaz等[18]發現散裝紅茶和袋泡紅茶隨著沖泡時間延長,茶湯中的多酚含量增加,抗氧化能力提升。Zhang等[19]研究了沖泡參數對白茶品質的影響,在沖泡6?min后,兒茶素、咖啡堿和茶氨酸均呈上升趨勢,但在第7分鐘,EGCG、EC、ECG和咖啡堿有所下降,結合茶湯特征成分分析和感官審評,白茶推薦沖泡參數為沖泡時間7?min,溫度100℃,料液比1∶30或1∶40,沖泡2次。Gan等[20]考查了泡時間對不同茶葉茶湯中多酚物質與抗氧化能力的影響,結果表明,10?min內多酚物質和抗氧化能力均上升,并推薦紅茶、綠茶沖泡2次,但袋泡茶只沖泡1次。
由此可見,沖泡時間與茶湯中內含物質濃度呈正相關,與單位時間浸出量呈負相關。沖泡時間越長,茶湯中內含物質濃度越高,但單位時間浸出量降低。茶葉沖泡起始階段(1~2?min),茶多酚、氨基酸、咖啡堿、水溶性多糖等內含物質迅速溶解于茶湯中,茶湯中內含物質濃度比例與茶葉中內含物質比例相近。當沖泡時間延長時,茶湯中茶多酚、咖啡堿等高含量內質成分浸出濃度高于氨基酸,從而導致酚氨比增大,苦澀味更為明顯。
1.3 水質對茶葉內含物質浸出的影響
水質對茶葉品質的影響包括兩方面,一方面水中有機物質和無機物質添加到茶湯中,不與茶葉內含物作用,由于添加物質本身的物理化學屬性,從而改變茶湯滋味、湯色和香氣等;另一方面,水中有機物或無機物與茶葉內含物質相互作用,產生新的化合物,從而改變茶湯滋味、湯色和香氣等品質特征。對茶葉品質及其化學成分影響的水質因子主要包括金屬離子、礦物質離子、pH、水中氣體分子等[21-23]。大量研究表明,Ca2+、Fe3+/Fe2+、Al3+等金屬離子是影響茶湯品質關鍵因子之一,其原因是金屬離子與茶葉內含物相互作用,形成絡合物從而改變茶湯滋味、湯色或香氣[24-27]。由于茶葉富含多酚、氨基酸等弱酸性物質,茶湯具有較強的緩沖能力,pH范圍明顯窄于飲用水pH范圍,因而水中pH對茶葉內含物浸出的影響并不顯著[28-29]。
2 茶葉中農藥殘留在茶湯中的浸出規律
農藥殘留是茶葉外源污染物,茶樹鮮葉吸附農藥后,經過茶葉加工滲透到茶葉組織內,或與茶葉內含物質相互作用。農藥在茶葉中的分布包括葉表面、組織間和組織內。因此,農藥在茶湯中的溶出規律與茶葉內含物浸出規律存在較大差異。
2.1 農藥在茶湯中的浸出率
目前,國內外針對在茶葉中使用的農藥進行了浸出規律研究,已查明60種農藥在茶湯中的浸出率,包括有機磷農藥(15種)、新煙堿類農藥(5種)、擬除蟲菊酯農藥(7種)、苯甲酰脲類(7種)、有機氯類農藥(5種)、氨基甲酸酯類(3種)和其他農藥(18種)(表1)。總體上,新煙堿類農藥和氨基甲酸酯類農藥浸出率較高,大部分浸出率高于60%。有機氯農藥、擬除蟲菊酯農藥和苯甲酰脲類農藥浸出率較低,均低于10.5%,部分浸出率為0。有機磷農藥浸出率差異較大,甲胺磷、乙酰甲胺磷和樂果的浸出率高于80%,三唑磷、水胺硫磷、殺撲磷和磷銨浸出率為27%~65%,其他有機磷農藥浸出率較低。另外,多菌靈和噻苯唑農藥浸出率較高,均高于80%。
2.2 影響農藥浸出率的主要因素
農藥在茶湯中的浸出率取決于農藥理化性質(內因)和沖泡方法、茶葉屬性及其農藥殘留量等(外因)。農藥的浸出率與水溶解度、辛醇/水比和蒸汽壓密切相關,水溶解度越大、辛醇/水比越小、蒸汽壓越小,農藥浸出率就越大[31,42,45]。圖3與圖4說明了19種農藥的水溶解度和辛醇/水比與浸出率的關系,農藥浸出率隨著其在水中的溶解度增加而提高,當在水中的溶解度低于20?mg·L-1時,農藥浸出率低于15%;當在水中的溶解度從35?mg·L-1(三唑磷)上升到4?100?mg·L-1(噻蟲嗪)時,農藥浸出率從22.6%上升到90.6%。因此,在水中的溶解度20?mg·L-1可能是農藥浸出率的關鍵參數。農藥浸出率與辛醇/水比成負相關,辛醇/水比越低,浸出率就越高。當辛醇/水比(Logow)從1.52(多菌靈)上升到2.48(水胺硫磷)時,農藥浸出率從80%下降到30%。由此可見,辛醇/水比Logow=2可能是農藥浸出率的閾值[31]。Wan等[55]研究表明,水溶解度低于10?mg·L-1或高于179?mg·L-1時,農藥浸出率與水溶解度相關性不顯著,農藥浸出率分別在1%~4%和大于90%范圍;但水溶解度為10~150?mg·L-1時,農藥浸出率與水溶解度幾乎呈線性上升關系。Hou等[37]比較了3種新煙堿類農藥在茶湯中的浸出率,吡蟲啉、噻蟲嗪和啶蟲脒的水溶解度分別為0.51、4.10?g·L-1和4.25?g·L-1,3種農藥在茶湯中平均浸出率為63.1%、80.5%和78.3%。盡管農藥浸出率與農藥理化性質和沖泡方法相關,但Wang等[56]認為水溶解度是影響浸出率最主要的因素,浸出率符合熱力學行為,并建立了浸出率(Log)與水溶解度(Log)數學預測模型,用于預測農藥在茶湯中的浸出率。
茶葉沖泡方法,包括水溫、沖泡時間和沖泡次數等外因對農藥浸出率起到重要影響。浸泡水溫升高,有助于提高農藥的水溶解度,加大水對茶葉基質的滲透能力,加快農藥的溶出速率。因此,沖泡溫度升高,農藥在茶湯中浸出率顯著提升[56-57]。甲氰菊酯、氯氰菊酯、氰戊菊酯和三氟氯氰菊酯隨著沖泡水溫度從60℃提高到100℃時,浸出率分別從0.76%、0、0.72%和0上升到5.82%、5.58%、4.87%和3.96%[42]。
沖泡時間對農藥浸出率的影響取決于農藥的溶出速率、揮發速率和其在茶湯中的穩定性。沖泡時間延長會提高農藥的浸出率,尤其對于水溶解度低的農藥影響更大。在2、5、10、20、30?min內,甲氰菊酯、氯氰菊酯、氰戊菊酯和三氟氯氰菊酯在浸泡10?min時浸出率最大,比2?min時的浸出率提高了6.5倍以上[42]。Ozbey等[58]發現隨著浸出時間的延長,殺螟硫磷、毒死蜱、樂果、馬拉硫磷和乙基嘧啶磷等有機磷農藥后期的浸出速率呈下降趨勢,在10?min下降不明顯,但在20?min后,殺螟硫磷、毒死蜱、樂果、馬拉硫磷和乙基嘧啶磷分別下降了28.5%、35.4%、12.6%、39.8%和39.1%。噻蟲嗪和噻蟲啉在茶湯中的浸出率隨著時間延長而增加,并在20?min達到最大值[38]。

圖3 農藥水溶解度與浸出率的關系[31]
Fig 3. Relationship of water solubility and extraction rate of pesticides during tea brewing[31]

圖4 農藥辛醇/水比(LogKow)與浸出率的關系[31]
Fig 4. Relationship of octanol/water ratio (Logow) and extraction rate of pesticides during tea brewing[31]
茶葉一般沖泡2~3次,每次沖泡過程中農藥浸出率存在顯著差異,一般第一次沖泡農藥浸出率大于第二次。Chen等[31]研究發現,當農藥總浸出率大于20%時(沖泡2次),第一泡和第二泡農藥浸出率比例為(2∶1)~(5∶1);當農藥總浸出率小于10%時,第一泡和第二泡農藥浸出率相當。這一結果與茶葉中鄰苯二甲酸酯在茶湯中的浸出率相近[59]。Fang等[38]研究發現,噻蟲嗪在第一泡和第二泡中的浸出率分別為30.7%和3.8%,噻蟲啉在第一泡和第二泡中的浸出率分別為12.5%和2.8%,在第三泡中均未檢出兩種農藥。一般來講,農藥浸出率與茶水比呈負相關,茶水比越大,浸出率越小[42]。然而,當茶水比(g∶mL)從1∶30上升到1∶100時,噻蟲嗪和噻蟲啉農藥浸出率分別從8.8%上升到31.5%和4.8%上升到16.5%[42]。同時,沖泡器具密閉或敞開對茶湯中農藥含量有一定影響,與茶杯密閉相比,茶杯無蓋時,噻蟲嗪和噻蟲啉浸出率分別下降3.1%和2.5%[42]。
茶葉種類及其殘留量對農藥浸出率的影響不明顯[31,37]。Chen等[31]研究發現,茶葉中農藥殘留量與浸出率無顯著關系,但Kumar等[51]研究發現,茶葉中已唑醇在茶湯中浸出率與其殘留量呈正相關,濃度越高,浸出率越大。
Gao等[60]為了查明茶葉淋洗對農藥去除效果,考察了8種農藥(樂果、馬拉硫磷、啶蟲脒、吡蟲啉、噻蟲嗪、聯苯菊酯、氯氰菊酯和氰戊菊酯)在不同時間(5、10、20、30?s)內在綠茶、紅茶和烏龍茶中的浸出規律。結果表明,在5~30?s,樂果、馬拉硫磷、啶蟲脒、吡蟲啉、噻蟲嗪等5種農藥在綠茶中的浸出率分別為10.8%~16.7%、8.4%~12.6%、7.1%~13.3%、7.8%~10.5%和3.8%~5.6%,紅茶浸出率結果與綠茶相近,但烏龍茶中5種農藥浸出率與綠茶、紅茶不一致,農藥浸出率與沖泡時間關系不顯著。另外,短時間內聯苯菊酯、氯氰菊酯和氰戊菊酯等3種農藥浸出率幾乎為0。由此推測,茶葉飲用前,沸水洗茶棄去后重新泡茶,可以減少水溶解度較高的農藥對人體的暴露水平。
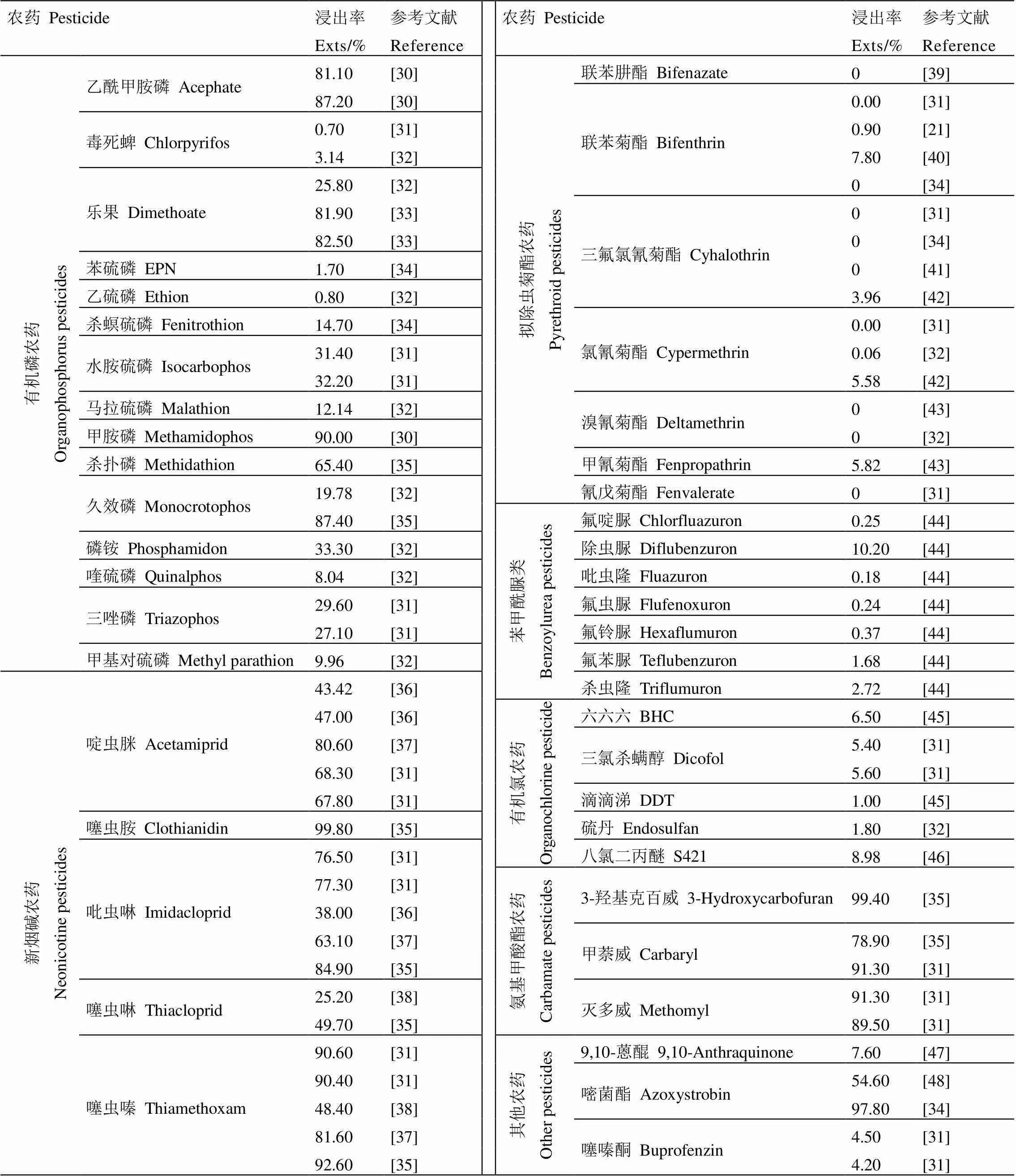
表1 農藥在茶湯中的浸出率
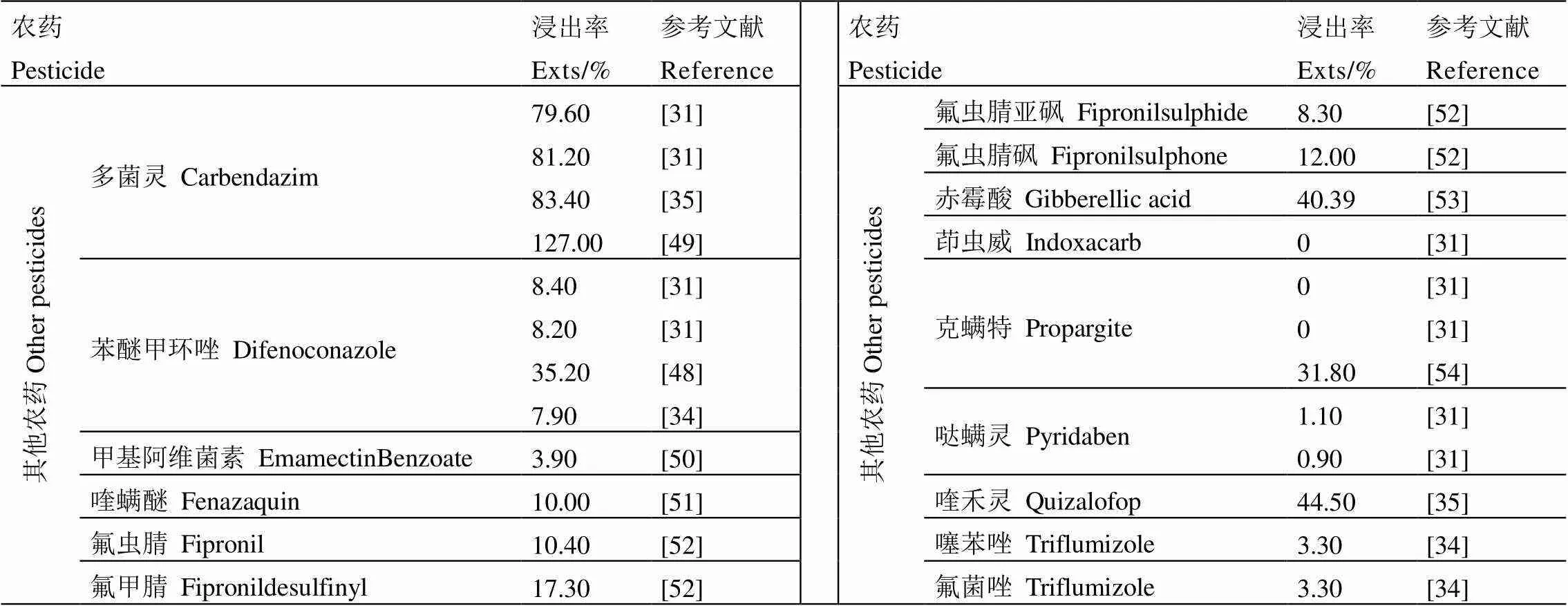
續表1
由此可見,農藥在茶湯中的浸出率取決于農藥的理化性質(內因)和沖泡方法(外因)。水溶解度和辛醇/水比是影響農藥浸出率最主要因素,農藥浸出率與水溶解度呈正相關,與辛醇/水比呈負相關。農藥浸出率與茶葉沖泡溫度、時間在一定范圍內呈正相關,但與茶葉種類、茶葉農藥殘留量的相關性較小。
3 茶葉中金屬元素與氟在茶湯中的溶解規律
金屬元素與氟作為茶葉外源污染物之一,主要通過土壤-根系或大氣-茶樹鮮葉之間的吸附、轉化與累積作用,導致不同化學形態的金屬元素與氟在茶樹新梢中累積。因此,與茶葉內含物和農藥在茶湯中的浸出規律不同,影響金屬元素或氟在茶湯中的浸出率內因主要是金屬元素或氟的存在形態,而不僅是無機態金屬元素或氟的溶解度。然而,茶葉中金屬元素的化學形態研究集中于土壤-茶樹系統間吸附、轉運、累積作用以及茶葉中含量測定等方面研究,浸出規律以總量計算,尚未有不同化學形態的金屬元素在茶湯中浸出規律研究[61-63]。目前,茶湯中金屬元素的浸出規律主要集中在沖泡溫度、時間、沖泡次數等外因的影響。茶葉中氟的存在形式包括無機氟離子、有機氟和氟化物。Zhang等[64]調查了19個中國生產的茶葉樣品中氟含量及其存在形態,結果表明,茶葉中氟主要以無機氟離子存在,有機氟僅有0.023%~0.41%,且50%~99%的氟化物是短鏈化合物,碳原子的數量不多于6,而大部分有機氟尚未鑒定出是何種化合物。
金屬元素(重金屬)與氟在茶湯中的浸出率差異非常大,不僅表現在不同金屬元素(重金屬)之間,而且同一種元素在不同茶葉中或不同分析方法中差異也很大(表2)。總體來看,氟在茶湯中的浸出率較高,達到60%~98.8%,其次是鎳(51.13%~82.4%)和鈷(31.04%~74.48%)。茶湯中氟含量差異較大,浸出率分布范圍也非常廣。Das等[76]調查了中草藥、紅茶、綠茶、烏龍茶、白茶和普洱茶沖泡后茶湯中氟含量,分別為0.06~0.69、1.47~5.45、2.43~6.94、3.08~5.63、5.39?mg·L-1和2.87~4.96?mg·L-1,平均浸出率為57.6%、60%、72.8%、76.2%、98.9%和65.9%。鉛的浸出率分布范圍很廣,達到1.17%~49.76%,其主要原因除了茶葉中鉛含量差異、分析方法差異等因素外,鉛在茶葉中的化學形態也是導致浸出率差異極大的主要原因之一。
劉銳[80]研究發現,茶葉中各元素在不同溫度沖泡下,浸出率差異較大。其中As、Cd、Mn、Ni、Pb、Ti和Zn的浸出率隨溫度升高而增加,Cu呈下降趨勢,而Cr和Fe變化不大。傅仙玉等[81]研究了不同溫度(60、80、100℃)對水仙和肉桂兩種烏龍茶中氟浸出率的影響,隨著溫度升高,水仙茶湯中氟的含量分別為0.752、1.106?mg·L-1和1.681?mg·L-1,而肉桂茶湯中氟含量分別為1.095、1.388?mg·L-1和1.761?mg·L-1。
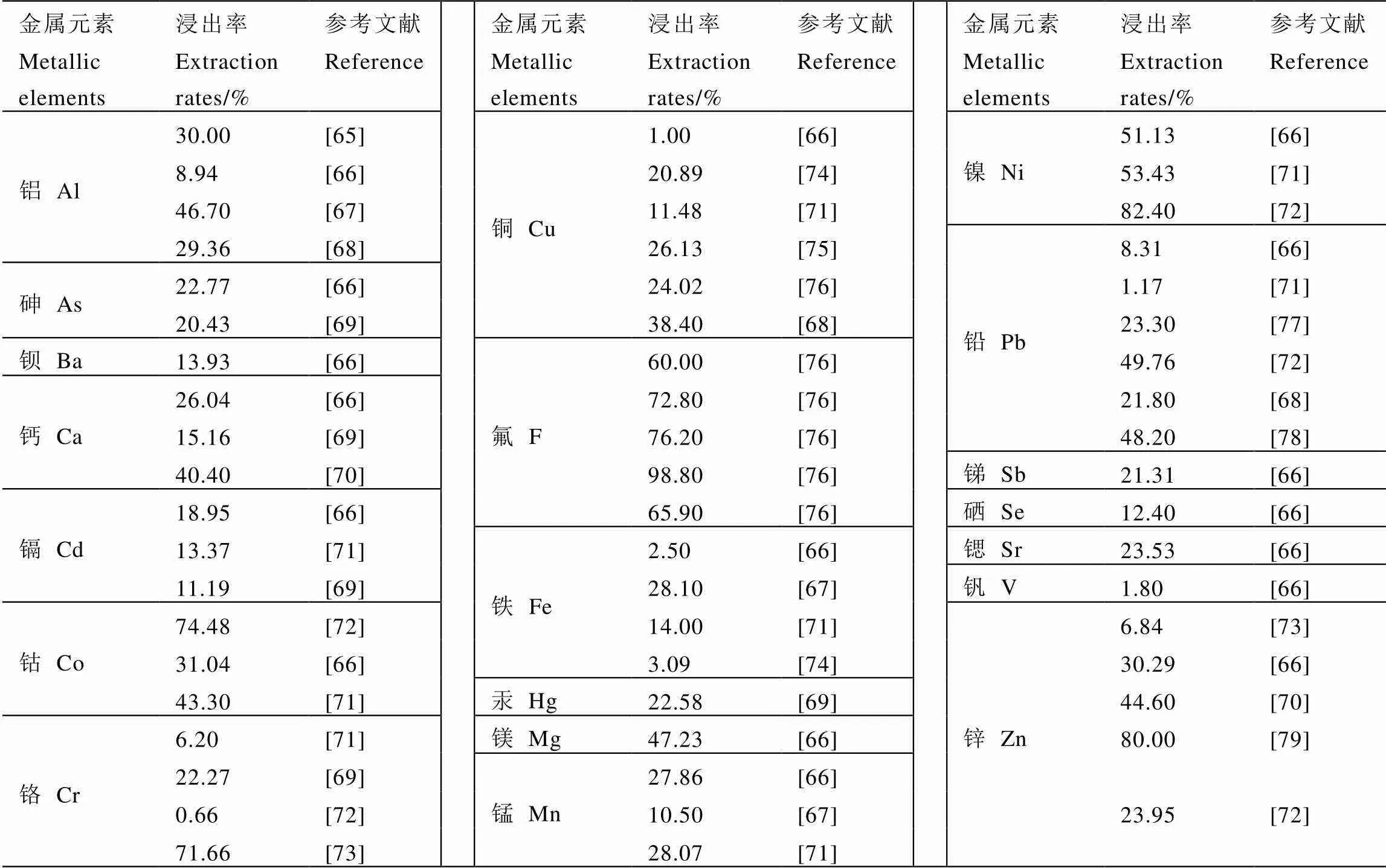
表2 屬元素(重金屬)與氟在茶湯中的浸出率
沖泡時間對茶中金屬元素(重金屬)的浸出率提取有著顯著影響。研究表明,碧螺春、金駿眉和鐵觀音中Cu和Zn在3、5、7、10?min內浸出率幾乎呈倍數增加,但10?min后(10~120?min)浸出率呈平穩水平[82]。Miri等[83]研究發現,沖泡時間在5、10?min和15?min時,肯尼亞紅茶、綠茶、伊朗茶中氟的浸出率隨沖泡時間延長而增加,以綠茶為例,5、10、15?min沖泡后,茶湯中氟含量分別為1.35、1.80、1.98?mg·L-1,10?min后分別提高了33.3%和46.7%。傅仙玉等[81]發現隨著沖泡時間延長(5、15、30?s),烏龍茶中氟的浸出量與時間呈正相關,且肉桂中浸出量高于水仙。緊壓茶通常采用煮沸形式飲用,但煮茶時間(5、10、20?min)對氟的浸出量影響不大,未達到極顯著差異[77]。
沖泡次數對烏龍茶中氟的浸出量影響呈先升后降的趨勢,第二泡中氟的浸出量最高,而第一泡和第三泡中氟的含量相當[81]。但在緊壓茶中,鉛的浸出率隨著沖泡次數增加而顯著降低,在第一泡、第二泡和第三泡中鉛的浸出率分別為15.9%、5.4%和2.0%[78]。茶水比的提高,有助于增大鉛在茶湯中的浸出率[77]。
金屬元素與氟在茶湯中浸出規律相對復雜,浸出率不僅與金屬元素的理化性質相關,而且與金屬元素在茶葉組織中的位置、金屬元素的形態與價態相關。因此,金屬元素在茶湯中的浸出率研究結果相差較大。總體來看,氟、鎳、鈷在茶湯中浸出率較高,達到50%以上,鉛的浸出率在20%~50%。
4 總結與展望
化合物的理化性質和茶葉沖泡方法是影響浸出率的內因和外因,前者起決定性作用,后者對茶葉內含物質浸出率的影響更突出。茶多酚、咖啡堿、氨基酸酸、可溶性多糖等茶葉內含物質由于分子量小,水溶解度高,因而在茶湯中浸出速率高,且濃度隨著沖泡溫度提高與沖泡時間延長而增加,直至飽和呈平穩狀態。農藥在茶湯中浸出率差異較大,新煙堿類農藥、氨基甲酸酯類農藥由于水溶解高,因而在茶湯中的浸出率高,但有機氯農藥和擬除蟲菊酯農藥浸出率極低。由于分析方法、金屬元素存在形式等方面的差異,金屬元素(含重金屬)與氟在茶湯中浸出率研究結果差異較大,氟、鎳和鈷的浸出率較大,鉛次之,其他金屬元素(重金屬)大部分低于30%。
茶葉品質是一個系統物質基礎,不僅僅是由幾類特征成分的疊加反應決定的。因此,茶葉沖泡過程中全組分分析(或大數據分析)則更能反應沖泡方法對茶湯浸出物質的變化規律,更全面揭示沖泡溫度、沖泡時間和沖泡次數對茶葉品質的影響。由此可見,基于質譜分析技術,尤其是高分辨質譜分析技術,結合大數據軟件分析系統,將成為茶葉-茶湯品質化學研究的有力工具。茶湯是茶葉農藥殘留、重金屬等外源污染物暴露人體最主要的途徑之一,其浸出率是評價外源有害物質安全性的關鍵參數。從熱力學理論基礎和傳質動力學模型解析茶湯中外源有害物質浸出機理,預測外源有害物質在茶湯中的浸出率,將有利于更深層面認識外源有害物質在茶湯中的浸出行為,從而為制定茶葉中最大殘留限量標準提供基礎數據和理論依據。
[1] Liang Y, Lu J, Zhang L, et al. Estimation of black tea quality by analysis of chemical composition and colour difference of tea infusions [J]. Food Chemistry, 2003, 80(2): 283-290.
[2] Liang Y, Lu J, Zhang L, et al. Estimation of tea quality by infusion colour difference analysis [J]. Journal of the Science of Food and Agriculture, 2005, 85(2): 286-292.
[3] 余澤恩, 頂仕華, 梁青青, 等. 綠茶“陜茶1號”中主要品質成分的溶出規律研究[J]. 西南農業學報, 2018, 31(8): 1682-1689. Yu Z E, Ding S H, Liang Q Q, et al. Study on dissolving rules of main quality components in green tea ‘Shanchayihao’ [J]. Southwest China Journal of Agricultural Sciences, 2018, 31(8): 1682-1689.
[4] Li J, Joung H J, Lee W, et al. The influence of different water types and brewing durations on the colloidal properties of green tea infusion [J]. International Journal of Food Science & Technology, 2015, 50(11): 2483-2489.
[5] Astill C, Birch M R, Dacombe C, et al. Factors affecting the caffeine and polyphenol contents of black and green tea infusions [J]. Journal of Agricultural and Food Chemsitry, 2001, 49(11): 5340-5347.
[6] Sharpe E, Hua F, Schuckers S, et al. Effects of brewing conditions on the antioxidant capacity of twenty-four commercial green tea varieties [J]. Food Chemistry, 2016, 192: 380-387.
[7] Liu Y, Luo L, Liao C, et al. Effects of brewing conditions on the phytochemical composition, sensory qualities and antioxidant activity of green tea infusion: A study using response surface methodology [J]. Food Chemistry, 2018, 269: 24-34.
[8] Fernando C D, Soysa P. Extraction Kinetics of phytochemicals and antioxidant activity during black tea (L.) brewing [J]. Fernando and Soysa Nutrition Journal, 2015, 14: 74. doi: 10.1186/s12937-015-0060-x.
[9] Jin Y, Zhao J, Kim E M, et al. comprehensive investigation of the effects of brewing conditions in sample preparation of green tea infusions [J]. Molecules, 2019, 24(9): 1735. doi:10.3390/molecules24091735.
[10] 李再兵. 綠茶主要品質成分的浸出動態及其與滋味感官評分的相關性研究[D]. 杭州: 浙江大學, 2002. Li Z B. Studies on the dynamic changes of the main quality components in green tea during brewing and the correlation between the components and the organolepeic evaluation [D]. Hangzhou: Zhejiang University, 2002.
[11] 金恩惠. 沖泡條件對鐵觀音和普洱茶的浸出規律和感官品質影響[D]. 杭州: 浙江大學, 2012. Jin E H. Effect of extraction and sensory evaluation of pu'er tea and tieguanyin in different brewing condition [D]. Hangzhou: Zhejiang University, 2012.
[12] 劉曉莎. 核磁共振技術應用于鐵觀音茶湯水浸出物溶出規律的研究[D]. 廈門: 廈門大學, 2016. Liu X S. The application of NMR techniques in studying the water extracting behavior of Tie-guanyin tea [D]. Xiamen: Xiamen University, 2016.
[13] Kelebek H. LC-DAD–ESI-MS/MS characterization of phenolic constituents in Turkish black tea: Effect of infusion time and temperature [J]. Food Chemistry, 2016, 204: 227-238.
[14] Pérez-Burilloa S, Giménez R, Rufián-Henares J A, et al. Effect of brewing time and temperature on antioxidant capacity and phenols of white tea: Relationship with sensory properties [J]. Food Chemistry, 2018, 248: 111-118.
[15] Saklar S, Ertas E, Ozdemir I S. Effects of different brewing conditions on catechin content and sensory acceptance in Turkish green tea infusions [J]. Journal of Food Science and Technology, 2015, 52(10): 6639-6646.
[16] ?lyaso?lu H, Arpa T E. Effect of brewing conditions on antioxidant properties of rosehip tea beverage: study by response surface methodology [J]. Journal of Food Science and Technology, 2017, 54(11): 3737-3743.
[17] Gani A, Prasad K, Ahmad M, et al. Time-dependent extraction kinetics of infused components of different Indian black tea types using UV spectroscopy [J]. Cogent Food & Agriculture, 2016, 2(1): 1137157. doi: 10.1080/23311932.2015.1137157.
[18] Nikniaz Z, Mahdavi R, Ghaemmaghami S J, et al. Effect of different brewing times on antioxidant activity and polyphenol content of loosely packed and bagged black teas (L.) [J]. Aviecnna Journal of Phytomedicine, 2016, 6(3): 313-321.
[19] Zhang H, Li Y, Lv Y, et al. Influence of brewing conditions on taste components in Fuding white tea infusions [J]. Journal of Science and Food Agriculture, 2017, 97(9): 2826-2833.
[20] Gan P T, Ting A S Y. Our tea-drinking habits: effects of brewing cycles and infusion time on total phenol content and antioxidants of common teas [J]. Journal of Culinary Science & Technology, 2019, 17(2): 170-183.
[21] 何靚. 水質和沖泡方式對綠茶茶湯及其抗氧化性能的影響[D]. 杭州: 浙江大學, 2016. He J. Effect of water quality and brewing menthods on the quality and antioxidant ability of green tea infusion [D]. Hangzhou: Zhejiang University, 2016.
[22] Franks M, Lawrence P, Abbaspourrad A, et al. The influence of water composition on flavor and nutrient extraction in green and black tea [J]. Nutrients, 2019, 11(1): 80-93.
[23] Murugesh C S, Manoj J B, Haware D J, et al. Influence of water quality on nutritional and sensory characteristics of green tea infusion [J]. Journal of Food Process Engineering, 2017, 40(5): 1-10.
[24] Xu Y, Zou C, Gao Y, et al. Effect of the type of brewing water on the chemical composition, sensory quality and antioxidant capacity of Chinese teas [J]. Food Chemistry, 2017, 236: 142-151.
[25] Xu Y, Hu X, Tang P, et al. The major factors influencing the formation of sediments in reconstituted green tea infusion [J]. Food Chemistry, 2015, 172: 831-835.
[26] Karak T, Kutu F R, Nath J R, et al. Micronutrients (B, Co, Cu, Fe, Mn, Mo, and Zn) content in made tea (L.) and tea infusion with health prospect: A critical review [J]. Critical Reviews in Food Scinece and Nutrition, 2017, 57(14): 2996-3004.
[27] Koch W, Kukula-Koch W, Komsta ?, et al. Green tea quality evaluation based on its catechins and metals composition in combination with chemometric analysis [J]. Molecules, 2018, 23(7): 1689. doi: 10.3390/molecules23071689.
[28] 尹軍峰. 水質對龍井茶風味品質的影響及其機制[D]. 杭州: 浙江工商大學, 2015. Yin J F. Effect of water quality on flavor quality of Longjing tea infusion and its mechanism [D]. Hangzhou: Zhejiang Gongshang University, 2015.
[29] 鄭少燕. 不同水質對白茶內含物溶釋及茶湯品質風味的影響[D]. 福州: 福建農林大學, 2016. Zheng S Y. Effects of brewing water on the components dissolution and infusion quality of white tea [D]. Fuzhou: Fujian Agriculture and Forestry University, 2016.
[30] Pan R, Chen H, Wang C, et al. Enantioselective dissipation of acephate and its metabolite, methamidophos, during tea cultivation, manufacturing, and infusion [J]. Journal of Agricultural and Food Chemistry, 2015, 63(4): 1300-1308.
[31] Chen H, Pan M, Pan R, et al. Transfer rates of 19 typical pesticides and the relationship with their physicochemical property [J]. Journal of Agricultural and Food Chemistry, 2015, 63(2): 723-730.
[32] Jaggi S, Sood C, Kumar V, et al. Leaching of pesticides in tea brew [J]. Journal of Agricultural and Food Chemistry, 2001, 49(11): 5479-5483.
[33] Pan R, Chen H, Zhang M, et al. Dissipation pattern, processing factors, and safety evaluation for dimethoate and its metabolite (Omethoate) in tea () [J]. Plos One, 2015, 10(9): e0138309. doi: 10.1371/journal.pone.0138309.
[34] Cho S, El-Aty A M A, Rahman M M, et al. Simultaneous multi-determination and transfer of eight pesticide residues from green tea leaves to infusion using gas chromatography [J]. Food Chemistry, 2014, 165: 532-539.
[35] Wang J, Cheung W, Leung D. Determination of pesticide residue transfer rates (percent) from dried tea leaves to brewed tea [J]. Journal of Agricultural and Food Chemistry, 2014, 62(4): 966-983.
[36] Gupta M, Shanker A. Persistence of acetamiprid in tea and its transfer from made tea to infusion [J]. Food Chemistry, 2008, 111(4): 805-810.
[37] Hou R, Hu J, Qian X, et al. Comparison of the dissipation behaviour of three neonicotinoid insecticides in tea [J]. Food Additives & Contaminants: Part A, 2013, 30(10): 1761-1769.
[38] Fang Q, Shi Y, Cao H, et al. Degradation dynamics and dietary risk assessments of two neonicotinoid insecticides duringplanting, drying, and tea brewing processes [J]. Journal of Agricultural and Food Chemistry, 2017, 65(8): 1483-1488.
[39] Satheshkumar A, Senthurpandian V K, Shanmugaselvan V A. Dissipation kinetics of bifenazate in tea under tropical conditions [J]. Food Chemistry, 2014, 145: 1092-1096.
[40] Tewary D K, Kumar V, Ravindranath S D, et al. Dissipation behavior of bifenthrin residues in tea and its brew [J]. Food Control, 2005, 16(3): 231-237.
[41] Seenivasan S, Muraleedharan N N. Residues of lambda-cyhalothrin in tea [J]. Food and Chemical Toxicology, 2009, 47(2): 502-505.
[42] Xiao J, Li Y, Fang Q, et al. Factors affecting transfer of pyrethroidresiduesfrom herbal teas to infusion and influence of physicochemical properties of pesticides [J]. International Journal of Environmental Research and Public Health, 2017, 14(10): 1157. doi: 10.3390/ijerph14101157.
[43] Paramasivam M, Chandrasekaran S. Persistence behaviour of deltamethrin on tea and its transfer from processed tea to infusion [J]. Chemosphere, 2014, 111: 291-295.
[44] Chen L, Chen J, Guo Y, et al. Study on the simultaneous determination of seven benzoylurea pesticides in Oolong tea and their leaching characteristics during infusing process by HPLC–MS/MS [J]. Food Chemistry, 2014, 143: 405-410.
[45] Chen Z, Wan H. Factors affecting residues of pesticides in tea [J]. Pesticides Science, 1988, 23(2): 109-118.
[46] Liao M, Shi Y, Cao H, et al. Dissipation behavior of octachlorodipropyl ether residues during tea planting and brewing process [J]. Environmental and Monitoring Assessment, 2016, 188: 551. doi: 10.1007/s10661-016-5573-z.
[47] Wang X, Zhou L, Luo F, et al. 9,10-Anthraquinone deposit in tea plantation might be one of the reasons for contamination in tea [J]. Food Chemistry, 2018, 244: 254-259.
[48] Xue J, Li H, Liu F, et al. Transfer of difenoconazole and azoxystrobin residues from chrysanthemum flower tea to its infusion [J]. Food Additives & Contaminants: Part A, 2014, 31(4): 666-675.
[49] Zhou L, Jiang Y, Lin Q, et al. Residue transfer and risk assessment of carbendazim in tea [J]. Journal of Science of Food and Agricuture, 2018, 98(4): 5329-5334.
[50] Zhou L, Luo F, Zhang X, et al. Dissipation, transfer and safety evaluation of emamectin benzoate in tea [J]. Food Chemistry, 2016, 202: 199-204.
[51] Kumar V, Tewary D K, Ravindranath S D, et al. Investigation in tea on fate of fenazaquin residue and its transfer in brew [J]. Food and Chemical Toxicology, 2004, 42(3): 423-428.
[52] Chen H, Gao G, Liu P, et al. Development and validation of an ultra performance liquid chromatography Q-ExactiveOrbitrap mass spectrometry for the determination of fipronil and its metabolites in tea and chrysanthemum [J]. Food Chemistry, 2018, 246: 328-334.
[53] Chen H, Liu X, Yang D, et al. Degradation pattern of gibberellic acid during the whole process of tea production [J]. Food Chemistry, 2013, 138(2/3): 976-981.
[54] Kumar V, Sood C, Jaggi S, et al. Dissipation behavior of propargite––an acaricide residues in soil, apple () and tea()[J]. Chemosphere, 2005, 58(6): 837-843.
[55] Wan H, Xia H, Chen Z. Extraction of pesticide residues in tea by water during the infusion process [J]. Food Additives & Contaminants, 1991, 8(4): 497-500.
[56] Wang X, Zhou L, Zhang X, et al. Transfer of pesticide residue during tea brewing: Understanding the effects of pesticide's physico-chemical parameters on its transfer behavior [J]. Food Research International, 2019, 121: 776-784.
[57] Chen H, Pan M, Liu X, et al. Evaluation of transfer rates of multi pesticides from green tea into infusion using water as pressurized liquid extraction solvent and ultra-performance liquid chromatography tandem mass spectrometry [J]. Food Chemistry, 2017, 216: 1-9.
[58] Ozbey A, Uygun U. Behaviour of some organophosphorus pesticide residues in peppermint tea during the infusion process [J]. Food Chemistry, 2007, 104(1): 237-241.
[59] Liu P, Chen H, Gao G, et al. Occurrence and residue pattern of phthalate esters in fresh tea leaves and during tea manufacturing and brewing [J]. Journal of Agricultural and Food Chemistry, 2016, 64(46): 8909-8917.
[60] Gao W, Yan M, Xiao Y, et al. Rinsing tea before brewing decreases pesticide residues in tea infusion [J]. Journal of Agricultural and Food Chemistry, 2019, 67(19): 5384-5393.
[61] Fred-Ahmadu O H, Adedapo A E, Oloyede M O, et al. Chemical speciation and characterization of trace metals in dryand herbal tea marketed in Nigeria [J]. Journal of Health and Pollution, 2018, 8(19): 180912. doi: 10.5696/2156-9614-8.19.180912.
[62] Wen B, Duan Y, Zhang Y, et al. Zn, Ni, Mn, Cr, Pb and Cu in soil-tea ecosystem: The concentrations, spatial relationship and potential control [J]. Chemosphere, 2018, 204: 92-100.
[63] Brzezicha-Cirocka J, Grembecka M, Szefer P. Monitoring of essential and heavy metals in green tea from different geographical origins [J]. Environmental and Monitoring Assessment, 2016, 188: 183. doi: 10.1007/s10661-016-5157-y.
[64] Zhang R, Zhang H, Chen Q, et al. Composition, distribution and risk of total fluorine, extractable organofluorine and perfluorinated compounds in Chinese teas [J]. Food Chemistry, 2019, 219: 496-502.
[65] Malik J, Frankova A, Drabek O, et al. Aluminium and other elements in selected herbal tea plant species and their infusions [J]. Food Chemistry, 2013, 139: 728-734.
[66] Nookabkaew S, Rangkadilok N, Satayavivad J. Determination of trace elements in herbal tea products and their infusions consumed in Thailand [J]. Journal of Agricultural and Food Chemistry, 2006, 54(18): 6939-6944.
[67] 屈艷琴, 何焱, 劉芷君, 等. 白茶中鋁、鐵、錳元素的測定及溶出特征分析[J]. 茶葉學報, 2018, 59(4): 211-214. Qu Y Q, He Y, Liu Z J, et al. Determination and leaching at brewing of aluminum, iron and manganese in white tea [J]. Acta Tea Sinica, 2018, 59(4): 211-214.
[68] Schulzki, G, Nü?lein B, Sievers, H. Transition rates of selected metals determined in various types of teas (L.) and herbal/fruit infusions [J]. Food Chemistry, 2017, 215: 22-30.
[69] 張清海, 龍章波, 林紹霞, 等. 貴州云霧茶園土壤高含量重金屬和砷在茶葉中的積累與浸出特征[J]. 食品科學, 2013, 34(8): 212-215. Zhang Q H, Long Z B, Lin S X, et al. Distribution of heavy metals in soil and tea from Yunwu tea area in Guizhou province and diffusion characteristics of heavy metals in tea infusion [J]. Food Science, 2013, 34(8): 212-215.
[70] Klink A, Dambiec M, Polechońska L, et al. Evalution of macroelements and fluorine in leaf and bagged black teas [J]. Food Measure, 2017, 12(1): 488-496.
[71] 楊欽沾, 陳孟君, 溫恒, 等. 茶葉中10種重金屬浸出率[J]. 福建農業學報, 2015, 30(4): 406-410. Yang Q Z, Chen M J, Wen H, et al. Leaching rates of ten heavy metals in tea [J]. Fujian Journal of Agricultural Sciences, 2015, 30(4): 406-410.
[72] Li L, Fu Q, Achal C, et al. A comparison of the potential health risk of aluminum and heavy metals in tea leaves and tea infusion of commercially available green tea in Jiangxi, China [J]. Environmental and Monitoring Assessment, 2015, 187: 228. doi: 10.1007/s10661-015-4445-2.
[73] Chand P, Sharma R, Prasad R, et al. Determination of essential & toxic metals and its transversal pattern from soil to tea brew [J]. Food and Nutrition Sciences, 2011, 2: 1160-1165.
[74] Karak T, Paul R K, Kutu F R, et al. Comparative assessment of copper, iron, and zinc contents in selected Indian (Assam) and South African (Thohoyandou) tea (L.) samples and their infusion: a quest for health risks to consumer [J]. Biological Trace Element Research, 2016, 175(2): 475-487.
[75] 徐潔, 葉芝祥, 張麗, 等. 茶葉中重金屬浸出規律的研究[J]. 化學分析計量, 2007(1): 23-25. Xu J, Ye Z X, Zhang L, et al. Study on the law of heavy metal leaching in tea [J]. Chemical Analysis and Meterage, 2007(1): 23-25.
[76] Das S, Oliveira L M, Silva F, et al. Fluoride concentrations in traditional and herbal teas: Health risk assessment [J]. Environmental Pollution, 2017, 231: 779-784.
[77] 陳利燕, 劉新, 劉汀. 緊壓茶中鉛的浸出規律研究[J]. 中國茶葉加工, 2010(4): 10-12. Chen Y L, Liu X, Liu T. Study on the leaching law of lead in pressed tea [J]. China Tea Processing, 2010(4): 10-12.
[78] Zazouli M A, Bankper A M. Determination of cadmium and lead contents in black tea and tea liquor from Iran [J]. Asian Journal of Chemistry, 2010, 22(2): 1387-1393.
[79] 毛清黎, 王星飛, 朱旗, 等. 富鋅茶的鋅浸出率及其飲用安全性研究[J]. 食品科學, 2003(8): 137-139. Mao Q L, Wang X F, Zhu Q, et al. Study on zinc leaching rate and drinking safety of Zn-enriched tea [J]. Food Science, 2003(8): 137-139.
[80] 劉銳. 浸泡溫度對不同茶葉中重金屬浸出的影響分析[J].昆明學院學報, 2017, 39(3): 43-48. Liu R. Effects of immersion temperatures on dissolving of metal elements in different tea infusions [J]. Journal of Kunming University, 2017, 39(3): 43-48.
[81] 傅仙玉, 鐘智霞, 武廣珩, 等. 武夷巖茶水仙和肉桂中氟離子的浸出規律研究[J]. 阜陽師范學院學報(自然科學版), 2019, 36(1): 40-44. Fu X Y, Zhong Z X, Wu G H, et al. Study on fluorine ion leaching of Shuixian and Rougui in Wuyi rock tea [J]. Journal of Fuyang Normal University (Natural Science), 2019, 36(1): 40-44.
[82] 宋曼銅, 王歡, 葉麗杰, 等. 火焰原子吸收光譜法測定茶水中銅、鋅元素的含量及沖泡時間對其浸出量的影響[J]. 沈陽醫學院學報, 2016, 18(6): 459-461. Song M T, Wang H, Ye L J, et al. Determination on the content of copper and zinc in tea by flame atomic absorption spectrophotometry [J]. Journal of Shenyang Medical College, 2016, 18(6): 459-461.
[83] Miri M, Bhatnagar A, Mahdavi Y, et al. Probabilistic risk assessment of exposure to fluoride in most consumed brands of tea in the Middle East [J]. Food and Chemical Toxicology, 2018, 115: 267-272.
《茶葉科學》第八屆編輯委員會副主任委員劉仲華教授當選中國工程院院士
11月22日,中國工程院公布了2019年院士增選結果,我刊第八屆編輯委員會副主任劉仲華教授當選中國工程院院士。繼陳宗懋院士之后,我刊迎來了第二位中國工程院院士編委。
劉仲華,湖南農業大學教授、博士生導師、學術委員會副主任、茶學學科帶頭人,浙江大學兼職教授。現任國家植物功能成分利用工程技術研究中心主任、國家茶葉產業技術體系加工研究室主任、國家農產品加工技術研發中心茶葉分中心(湖南)主任。兼任國務院學位委員會園藝學科評審組成員、教育部科技委農林學部委員、中國茶葉學會監事、中國茶葉流通協會副會長、中國國際茶文化研究會副會長、國家茶葉標準化技術委員會顧問兼黑茶工作組和茯茶工作組組長、湖南省茶葉學會名譽理事長、湖南省大湘西茶業發展促進會會長等職。
劉仲華教授長期從事茶葉深加工與功能成分利用、茶葉加工理論與技術、飲茶與健康等領域的研究與教學,致力于創新茶葉加工理論技術、提高茶葉資源利用率和產業綜合效益。創新黑茶加工和茶葉深加工理論與技術體系,揭示了黑茶加工品質風味形成機理及黑茶健康屬性,創建了黑茶優質高效安全加工關鍵技術體系,強力推進了我國黑茶產業提質增效與快速發展;揭示了茶葉功能成分的生物活性及作用機制,創制的茶葉提取物制品催生了一批國際主流健康產品,引領我國茶葉深加工從追蹤日本和歐美發達國家到領先國際同行。為我國茶葉科技進步、茶葉產業提質增效與轉型升級做出了突出貢獻。
劉仲華教授先后主持國家和部省級項目30多項,以第一完成人獲國家科技進步二等獎2項、湖南省科技進步一等獎3項、湖南省科技進步二等獎1項,并榮獲首屆湖南省十大科技創新獎、湖南省光召科技獎、國際茶葉科技創新杰出貢獻獎等榮譽;先后在國內外學術刊物發表論文400多篇,其中SCI收錄60多篇,授權發明專利60多件。2019年獲得了“何梁何利基金”科學與技術進步獎(農學獎)。
Leaching Pattern of Internal Substances and Xenobiotic Pollutants during Tea Brewing
CHEN Hongping1,2,3, LIU Xin2, LU Chengyin2*, QIU Jing1*
1. Institute of Quality Standard and Testing Technology for Agro-Products of Chinese Academy of Agricultural Sciences, Beijing 100081, China; 2. Tea Research Institute, Chinese Academy of Agricultural Sciences, Tea Quality and Supervision Testing Center, Key Laboratory ofTea Quality and Safety & Risk Assessment, Ministry of Agriculture, Ministry of Agriculture R. P. China, Hangzhou, 310008, China; 3. Graduate School of Chinese Academy of Agricultural Sciences, Beijing 100081, China
Based on the recent literatures, the dissolving, releasing and transformation patterns of tea internal compounds and exogenous contaminants were summarized and discussed in this study. Physicochemical properties of chemicals and tea brewing methods are the internal and external cause affecting extraction rates of chemicals during tea brewing. Internal cause plays a crucial role in extraction rates, while external cause is more prominent for the leaching of tea internal substances. Water solubility of chemicals is positively correlated with extraction rates, while octanol-water partition is negatively correlated with extraction rates. Increasing water temperature is helpful for increasing extraction rates of chemicals and their concentrations in tea infusion. Brewing time is negatively correlated with extraction rates in a period of time, while the concentrations of chemicals in tea infusion increase with the brewing time. Compared with other pesticides, most of neonicotine pesticides and carbamate pesticides have higher extraction rates over 60%. The results of extraction rates of metal elements in tea infusion are quite different, and extraction rates of fluorine, nickel and cobalt have high extraction rates over 50%, while extraction rates of lead range from 20% to 50%. Metabonomic analysis based-high resolution mass spectrometry technique is a promising and powerful method for profiling extracting pattern of chemicals during tea brewing. Meanwhile, extracting behavior of toxic compounds during tea brewing will be deeply understood by using thermodynamic theory and kinetic model of mass extraction.
tea brewing, internal substance, pesticide residues, heavy metals, leaching pattern
S571.1;TS201.6
A
1000-369X(2020)01-063-14
2019-06-27
2019-07-25
中國農業科學院創新團隊茶葉質量與風險評估團隊(CAAS-ASTIP-2014-TRICAAS-06)、浙江省公益應用項目(2017C32059)、現代農業產業技術體系建設專項基金資助項目(nycytx-26)、國家自然科學基金(31671941)
陳紅平,男,副研究員,主要從事茶葉質量安全檢測與研究方面的研究。
lchy@mail.tricaas.com,qiujing@caas.cn

