老年2型糖尿病患者25(OH)D與尿白蛋白肌酐比值的相關性研究
吳麗娟
福建省立醫院干部特診一科,福建省福州市 350001
隨著經濟快速發展和生活方式的變化,2型糖尿病(T2DM)已日益增長為全球流行病,嚴重威脅人類健康。糖尿病腎病是最常見的微血管并發癥,是慢性腎臟病和終末期腎臟病的主要原因。早期干預糖尿病腎病對老年患者延緩終末期腎病的發生發展具有重要意義。維生素D是類固醇激素,有助于調節鈣和磷的代謝,并在維持骨骼健康方面發揮重要作用[1]。25(OH)D在血清中含量高、半衰期長,可用作評估體內維生素D狀態的指標。研究表明腎內腎素—血管緊張素系統(RAS)的激活在糖尿病腎病進展中起關鍵作用[2]。維生素D通過其對腎素—血管緊張素—醛固酮系統的負調節作用,抑制RAS的活化,防止微量白蛋白尿導致的腎臟內皮損傷,從而在糖尿病腎病中起保護作用。研究發現隨著維生素D水平的降低,微量白蛋白尿的患病率有所增加[3]。微量白蛋白尿對于診斷早期糖尿病腎病有重要意義。本研究的目的是探討老年T2DM患者25(OH)D與ACR值的相關性,為糖尿病腎病的早期干預提供途徑,提高老年患者生活質量及生存壽命。
1 資料與方法
1.1 一般資料 收集2017年9月—2019年6月在我院內分泌科住院的年齡≥60歲的T2DM患者98例,其中男54例,女44例。參照2012 年美國糖尿病學會糖尿病診療指南推薦,根據尿白蛋白/肌酐比值(ACR)將 T2DM 患者分為三組。(1)正常蛋白尿組(ACR<30mg/g)44例,男21例,女23例,平均年齡(68.68±7.61)歲;(2)微量蛋白尿組(30mg/g≤ACR<300mg/g )28例,男16例,女12例,平均年齡(69.32±7.47)歲;(3)大量蛋白尿組(ACR≥300mg/g) 26例,男17例,女9例,平均年齡(68.62±7.23)歲。T2DM診斷標準:參照1999年 WHO糖尿病診斷及分型標準,典型糖尿病癥狀(多飲、多尿、多食、體重下降)加上隨機血糖檢測≥11.1mmol/L,或加上空腹血糖檢測≥7.0mmol/L,或加上葡萄糖負荷后2h血糖檢測≥11.1mmol/L。無糖尿病癥狀者,需改日重復檢查。排除1型糖尿病、其他特殊類型糖尿病、妊娠糖尿病。排除標準:糖尿病酮癥酸中毒、高滲性昏迷等急性并發癥;嚴重感染;惡性腫瘤;慢性腎炎及其他腎臟疾病;肝功能不全;骨質疏松癥;甲狀旁腺功能亢進;自身免疫病;近期服用影響骨代謝藥物者。
1.2 研究方法 對所有研究對象進行詳細的病史采集、體格檢查,收集性別、年齡、病程、身高、體重、收縮壓(Systolic blood pressure,SBP)、舒張壓(Diastolic blood pressure,DBP)指標,計算體質量指數(Body mass index,BMI)= 體重/身高2(kg/m2)。所有對象空腹狀態(8~12h)并在次日上午 6—8時采集靜脈血,采用全自動生化儀檢測空腹血糖(FBG)、甘油三酯(TG)、總膽固醇(CHOL)、高密度脂蛋白膽固醇(HDL-C)、低密度脂蛋白膽固醇(LDL-C)、血尿酸、血肌酐、血尿素氮、血鈣、血磷、尿肌酐、尿微量白蛋白,計算尿白蛋白/肌酐比值(ACR)。采用全自動糖化血紅蛋白分析儀測定糖化血紅蛋白(HbA1c)。采用電化學發光法檢測25(OH)D、甲狀旁腺激素(PTH),羅氏診斷試劑盒檢測。

2 結果
2.1 三組一般資料和生化指標比較 對各指標進行的單因素方差分析結果顯示:25(OH)D在三組間有顯著性差異(P=0.000<0.05):進行兩兩比較,微量蛋白尿組、大量蛋白尿組的25(OH)D均顯著低于正常蛋白尿組(P<0.05),大量蛋白尿組25(OH)D顯著低于微量蛋白尿組(P<0.05)。見表1。
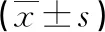
表1 三組一般資料和生化指標比較
注:與正常蛋白尿組比較,*P<0.05;與微量蛋白尿組比較,ΔP<0.05。1mmHg=0.133kPa。
2.2 各指標與25(OH)D的相關性分析 經Pearson相關分析,25(OH)D與ACR、收縮壓、CHOL、TG、LDL-C、尿酸、尿素氮、血肌酐、FBG、HbA1c、PTH呈負相關(P<0.05),與血鈣呈正相關(P<0.001),而與病程、BMI、舒張壓、HDL-C、血磷無明顯相關性。見表2。

表2 各指標與25(OH)D的相關性分析
3 討論
我國已進入老齡化社會,60歲以上老年人口數量達2.41億,占總人口17.3%,預計到2050年前后,我國老年人口數將達到峰值4.87億。2017年,全世界估計有4.51億人患有糖尿病,預計到2045年將增加到6.93億[4],直接影響微血管并發癥的患病率。糖尿病是老年人高發的慢性病,糖尿病腎病是常見的微血管并發癥,是終末期腎病的最主要原因,致死率高,嚴重影響老年人生活質量和預期壽命。早發現、早干預,可以阻止和延緩其進一步進展為終末期腎病。
維生素D缺乏癥是一種全球性的健康問題,與幾種癌癥(如前列腺癌和結腸癌)、糖尿病、心血管疾病、高血壓、骨折和代謝綜合征的高風險之間存在關聯,近年來受到人們的特別關注。維生素D可在肝臟中羥基化為25(OH)D,然后通過腎近端小管中的1α-羥化酶進一步羥基化為1,25-二羥基維生素D,這是維生素D的生物活性形式[4]。25(OH)D是維生素D的一種形式,用于儲存和運輸,在骨代謝中起重要作用,通常用作評估體內維生素D狀態的指標。維生素D被認為通過刺激胰島素合成和分泌,降低胰島素抵抗以及其經典作用,在葡萄糖代謝中發揮重要作用[5]。有大量證據表明維生素D缺乏與T2DM發病率增加之間存在關聯,補充維生素D有助于優化T2DM患者的葡萄糖穩態,可改善T2DM患者的血糖控制和胰島素抵抗[6]。
本研究發現空腹血糖、HbA1c與25(OH)D呈負相關,表明維生素D水平可能通過促進胰島素分泌和胰島素受體的刺激影響T2DM患者的血糖控制,或者糖尿病控制可能影響維生素D代謝[7]。需要進一步的研究來測試維生素D替代對糖尿病血糖控制的治療效果。在評估血壓時,發現25(OH)D與收縮壓呈負相關,維生素D水平與高血壓之間存在密切關系。對照研究和薈萃分析顯示,高血壓風險增加與低維生素D水平相關[8]。在Forman等人[9]的一項為期4年的前瞻性研究中,與血漿25(OH)D水平>30ng/ml的患者相比,血漿25(OH)D水平<15ng/ml的患者高血壓發生的相對風險增加3.18倍,血漿25(OH)D水平與高血壓發病風險呈負相關。
糖尿病腎病的病理特征最初是腎小球和腎小管上皮肥大,基底膜增厚和過量的細胞外基質沉積,最終導致腎小球硬化和腎小管間質纖維化。糖尿病腎病的主要臨床表現是進行性白蛋白尿和腎功能下降[10]。一些實驗研究表明25(OH)D濃度可能對糖尿病腎病的進展產生不利影響。與糖尿病野生型小鼠相比,敲除糖尿病小鼠維生素D受體基因后,因腎小球基底膜增厚和足細胞滲出而出現更嚴重的蛋白尿和腎小球硬化,觀察到25(OH)D可抑制高糖(HG)誘導的系膜及腎小球旁細胞RAS和TGF-β的激活[11]。另一項研究表明,25(OH)D部分拮抗晚期糖基化終產物(AGEs)介導的小鼠足細胞中NFκB活化[12]。維生素D受體的腎臟保護作用機制包括抑制腎素—血管緊張素系統、抗炎癥、抑制腎纖維化形成、恢復線粒體功能、抑制自身免疫和腎細胞凋亡、減少蛋白尿等[13]。維生素D及其類似物治療可顯著改善腎功能,并為糖尿病腎病患者帶來顯著的生存優勢。
ACR的增加是糖尿病腎病的主要臨床表現,可反映T2DM患者早期腎臟的變化[14]。在第三次健康和營養檢查調查(NHANES Ⅲ)隊列中,維生素D缺乏與白蛋白尿和腎功能衰竭的風險增加有關[15]。腎功能不全可影響血清25(OH)D水平,研究證實慢性腎病患者血清25(OH)D水平較低[16]。還發現慢性腎病患者用維生素D治療可改善腎功能,降低ACR和改善估計腎小球濾過率(eGFR)[17]。近年來,多項國內外研究闡明,血清25(OH)D水平與糖尿病腎病密切相關,維生素 D 缺乏是糖尿病腎病的獨立危險因素[18-20]。本研究中,發現血清25(OH)D與ACR值具有顯著的負相關性,微量蛋白尿組、大量蛋白尿組的25(OH)D均顯著低于正常蛋白尿組,大量蛋白尿組25(OH)D顯著低于微量蛋白尿組,隨著糖尿病腎病的嚴重程度不同以及ACR值的增加,T2DM患者的25(OH)D依次降低。與之前研究結果一致,說明血清25(OH)D水平與糖尿病腎病密切相關,可能可以反映糖尿病腎病的嚴重程度。且25(OH)D與腎功能指標血肌酐、尿酸、尿素氮呈負相關,提示維生素 D 缺乏在糖尿病腎病的發生發展中發揮一定作用。
綜上所述,25(OH)D水平與老年糖尿病患者的ACR值呈負相關,25(OH)D 水平可能可以反映糖尿病腎病的嚴重程度。低維生素D水平可能是糖尿病腎病可改變的危險因素,臨床上應密切監測老年患者的25(OH)D水平變化,通過補充維生素D來保護胰島功能、降低糖尿病發生風險、早期干預糖尿病腎病、延緩糖尿病腎病進展,降低終末期腎病發生率,提高老年患者的生活質量。然而,維生素D缺乏與糖尿病腎病之間的因果關系以及維生素D治療能否延緩糖尿病腎病進展仍存在爭議,需要更多的其他后續研究來證實。

