燈盞花素TPGS聚合物膠束的制備工藝研究*
李云貴,軒貴平,姚海倫,鄒 柳
(1 湖南環(huán)境生物職業(yè)技術(shù)學(xué)院,湖南 衡陽 421001;2 柳州市婦幼保健院,廣西 柳州 454001)
燈盞花素(breviscapine)又叫燈盞細(xì)辛,是菊科植物短葶飛蓬(Erigeron breviscapus(Vant.)Hand-Mazz)的干燥全草,其中主要成分是燈盞花乙素(又叫野黃芩苷),另還含少量燈盞花甲素,其中燈盞乙素的含量占95%以上,為燈盞花素的主要有效成分[1]。現(xiàn)代醫(yī)學(xué)研究表明:燈盞花素可以改善心腦微循環(huán)、增加血流量、抗氧化、抗炎及拮抗心機(jī)缺血再灌注損傷等藥理作用[2-6],其中最顯著的作用是保護(hù)心腦血管[7-9]。目前上市的燈盞花素制劑中依然存在著生物利用度低,體內(nèi)消除迅速,半衰期短等缺點(diǎn)。
為此,針對(duì)燈盞花素水溶性和脂溶性均差的特性,本實(shí)驗(yàn)選用以經(jīng)SFDA認(rèn)證的安全高分子材料聚乙二醇1000維生素E琥珀酸酯為聚合物脂質(zhì)體載體材料包載燈盞花素,制備燈盞花素聚合物脂質(zhì)體。
1 材 料
1.1 儀 器
KQ-250DE型超聲儀,昆山市超聲儀器公司;UV-1750紫外分光光度儀,島津公司;Nano-ZS粒度測(cè)定儀,英國Malvern公司;XW-80A旋渦混合器,上海醫(yī)科大學(xué)儀器廠;AG285型電子分析天平,瑞士METTLER公司;EM-1200EX透射電子顯微鏡,日本電子公司;X-射線衍射儀,日本Rigaku公司。
1.2 試 藥
燈盞乙素標(biāo)準(zhǔn)品,中國藥品生物制品檢驗(yàn)所(批號(hào):201707);燈盞花素原料藥,湖南恒生制藥有限公司(批號(hào):20180506);聚乙二醇1000維生素E琥珀酸酯,阿拉丁試劑有限公司(批號(hào):20180323);其他試劑均為分析純。
2 方 法
2.1 燈盞花素儲(chǔ)備液的制備
精密稱取50 mg燈盞花素原料藥,置棕色容量瓶中,加入適量甲醇使其完全溶解后定容,最終得到1 mg/mL的燈盞花素儲(chǔ)備液,置4 ℃冰箱中保存、備用。
2.2 聚乙二醇1000維生素E琥珀酸酯儲(chǔ)備液的制備
精密稱取聚乙二醇1000維生素E琥珀酸酯2.00 g,放入容量瓶中,加入適量甲醇進(jìn)行溶解,稀釋、定容至刻度,制得20 mg/mL的聚乙二醇1000維生素E琥珀酸酯儲(chǔ)備液,置4 ℃冰箱中保存、備用。
2.3 建立UV法測(cè)定Bre/TPGS脂質(zhì)體的含量
2.3.1 檢測(cè)波長(zhǎng)的確定
取適量燈盞花素儲(chǔ)備液,放入棕色容量瓶中,加入適量的甲醇溶液進(jìn)行稀釋、定容至刻度處,輕輕搖晃均勻,配制成0.04 mg/mL 的燈盞花素溶液,以甲醇溶液為空白參比,用UV法進(jìn)行紫外吸收波長(zhǎng)掃描來確定其最大吸收波長(zhǎng)。
2.3.2 標(biāo)準(zhǔn)曲線的繪制
精密稱取50 mg燈盞乙素標(biāo)準(zhǔn)品,置棕色容量瓶中,加入適量甲醇待其完全溶解后定容,搖勻,即得100 μg/mL的燈盞乙素標(biāo)準(zhǔn)品溶液。再用甲醇稀釋定容至刻度,制備成濃度分別為4.00、6.00、8.00、10.00、12.00和14.00 μg/mL的一系列燈盞乙素標(biāo)準(zhǔn)品溶液。按照UV法確定的燈盞花素最適吸收波長(zhǎng)處對(duì)這一系列標(biāo)準(zhǔn)品溶液進(jìn)行測(cè)定,得系列標(biāo)準(zhǔn)品溶液的吸光度值(A),以吸光度值對(duì)質(zhì)量濃度(C)進(jìn)行線性回歸,繪制標(biāo)準(zhǔn)曲線。
2.3.3 精密度考察
分別配制低(4μg/mL)、中(8 μg/mL)、高(12 μg/mL)三種不同濃度的燈盞乙素標(biāo)準(zhǔn)品溶液,每個(gè)濃度設(shè)置三個(gè)平行組,按照UV法確定的最適宜的吸收波長(zhǎng)在同一天內(nèi)測(cè)定5次吸光度值A(chǔ),考察其日內(nèi)精密度,計(jì)算RSD。同法,用上述樣品每天測(cè)定1次連續(xù)測(cè)定3 天吸光度值A(chǔ),考察其日間精密度,計(jì)算RSD。
2.3.4 方法回收率
分別配制低(4 μg/mL)、中(8 μg/mL)、高(12 μg/mL)三種不同濃度的燈盞乙素標(biāo)準(zhǔn)品溶液,每個(gè)濃度設(shè)置三個(gè)平行組,按照UV法確定的最適吸收波長(zhǎng)的吸光度值(A),根據(jù)繪制的標(biāo)準(zhǔn)曲線方程,計(jì)算出燈盞乙素的實(shí)際測(cè)定濃度,可得出其方法回收率,即實(shí)際濃度/理論濃度×100%。
2.4 Bre/TPGS脂質(zhì)體的制備
精密吸取5.00 mL的聚乙二醇1000維生素E琥珀酸酯儲(chǔ)備液(20 mg/mL),置茄型瓶中,加入7.00 mL的燈盞花素儲(chǔ)備液(1 mg/mL),攪拌混勻后,用減壓旋轉(zhuǎn)蒸發(fā)回收甲醇,然后再加入蒸餾水10 mL,于37 ℃磁力攪拌2 h,再加甲醇溶解、攪拌,減壓回收甲醇,用微孔濾膜過濾,即得Bre/TPGS脂質(zhì)體。同上述方法,不加入燈盞花素即制得空白脂質(zhì)體。
2.5 脂質(zhì)體包封率及載藥量的測(cè)定
精密吸取1.00 mL 的Bre/TPGS脂質(zhì)體溶液,置10 mL容量瓶中,加甲醇稀釋、定容到刻度,再從上述溶液中精密吸取3.00 mL溶液,置25 mL容量瓶中,加甲醇稀釋、定容到刻度,超聲10 min。測(cè)定脂質(zhì)體中燈盞花素的含量,計(jì)算其的包封率(EE%)和載藥量(DL%)。
包封率=M0/M1×100%
載藥量=M0/M ×100%
式中:M為所制備的聚乙二醇1000維生素E琥珀酸酯與燈盞花素總投入的量;M0為脂質(zhì)體中燈盞花素的量;Ml為脂質(zhì)體前投入燈盞花素的量。
2.6 單因素法篩選Bre/TPGS的制備工藝
在實(shí)驗(yàn)過程影響聚合物脂質(zhì)體形成的因素有很多,根據(jù)預(yù)實(shí)驗(yàn)基礎(chǔ),選取了水化溫度、水化時(shí)間和藥物與載體藥物比等三個(gè)單因素進(jìn)行考察,為下一步實(shí)驗(yàn)設(shè)計(jì)提供依據(jù)。
2.6.1 水化溫度對(duì)Bre/TPGS脂質(zhì)體的影響
精密吸取5.00 mL的Bre/TPGS脂質(zhì)體儲(chǔ)備液(20 mg/mL),放入茄型瓶中,加入5.00 mL的燈盞花素儲(chǔ)備液(1 mg/mL),磁力攪拌混勻后,減壓回收甲醇,然后再加入蒸餾水10 mL,于水化溫度為37、50、60 ℃溫度條件下磁力攪拌3 h,再加甲醇溶解、攪拌,減壓回收甲醇,用微孔濾膜過濾,即為Bre/TPGS脂質(zhì)體。
2.6.2 水化時(shí)間對(duì)Bre/TPGS脂質(zhì)體的影響
精密吸取5.00 mL的聚乙二醇1000維生素E琥珀酸酯儲(chǔ)備液(20 mg/mL),置茄型瓶中,加入5.00 mL的燈盞花素儲(chǔ)備液(1 mg/mL),磁力攪拌混勻后,用減壓回收甲醇,然后再加入蒸餾水10 mL,于水化溫度為37 ℃下磁力攪拌1、2、3、4、5 h,再加甲醇溶解、攪拌,減壓回收甲醇,用微孔濾膜過濾,即為Bre/TPGS脂質(zhì)體。
2.6.3 藥物與載體藥物比對(duì)Bre/TPGS脂質(zhì)體的影響
精密吸取5.00 mL的聚乙二醇1000維生素E琥珀酸酯儲(chǔ)備液(20 mg/mL),置茄型瓶中,加入不同體積的燈盞花素儲(chǔ)備液(1 mg/mL),磁力攪拌混勻后,減壓回收甲醇,然后再加入蒸餾水10 mL,于水化溫度為37 ℃下磁力攪拌3 h,再加甲醇溶解、攪拌,減壓回收甲醇,用微孔濾膜過濾,即為Bre/TPGS脂質(zhì)體。
2.7 正交實(shí)驗(yàn)優(yōu)化Bre/TPGS脂質(zhì)體的制備工藝
通過正交實(shí)驗(yàn)來進(jìn)一步優(yōu)化Bre/TPGS脂質(zhì)體的制備工藝,選擇包封率為考察指標(biāo),考察了藥物與載藥量的比值(A)、水化溫度(B)、水化時(shí)間(C)對(duì)脂質(zhì)體包封率的影響,每個(gè)因素考察 3 個(gè)水平。設(shè)計(jì)L9(33)正交設(shè)計(jì)表,進(jìn)行三因素、三水平正交實(shí)驗(yàn),篩選出制備Bre/TPGS脂質(zhì)體的最佳工藝。正交實(shí)驗(yàn)水平見表1。
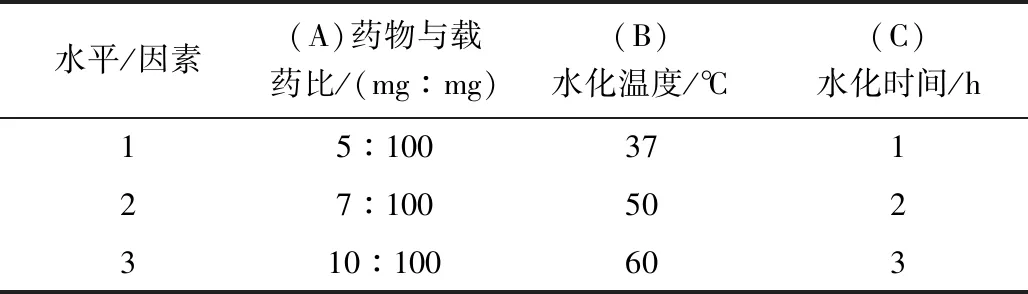
表1 正交設(shè)計(jì)因素水平表
3 結(jié)果與討論
3.1 Bre/TPGS脂質(zhì)體的含量測(cè)定結(jié)果
3.1.1 檢測(cè)波長(zhǎng)的確定
分別取燈盞花素甲醇溶液和聚乙二醇1000維生素E琥珀酸酯甲醇溶液進(jìn)行紫外掃描,確定燈盞花素檢測(cè)波長(zhǎng)為335 nm。
3.1.2 標(biāo)準(zhǔn)曲線的繪制
采用UV法在335 nm 處分別測(cè)定已配置好一系列濃度的燈盞乙素標(biāo)準(zhǔn)品溶液的吸光度(A),測(cè)定的數(shù)據(jù)結(jié)果見表2。其線性方程為:Y=0.0564X-0.0054,R2=0.9998。用于Bre/TPGS脂質(zhì)體的含量測(cè)定。

表2 燈盞花素標(biāo)準(zhǔn)溶液標(biāo)吸光度值A(chǔ)
3.1.3 精密度試驗(yàn)
低、中、高三種不同濃度燈盞乙素標(biāo)準(zhǔn)溶液的日內(nèi)精密度實(shí)驗(yàn)結(jié)果見表3,日間精密度實(shí)驗(yàn)結(jié)果見表4。日內(nèi)和日間精密度良好,RSD均小于3%,符合樣品含量測(cè)定要求。
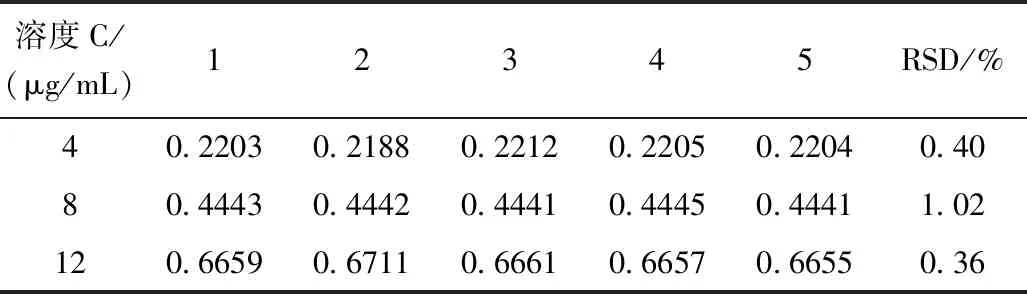
表3 燈盞花素日內(nèi)精密度實(shí)驗(yàn)結(jié)果
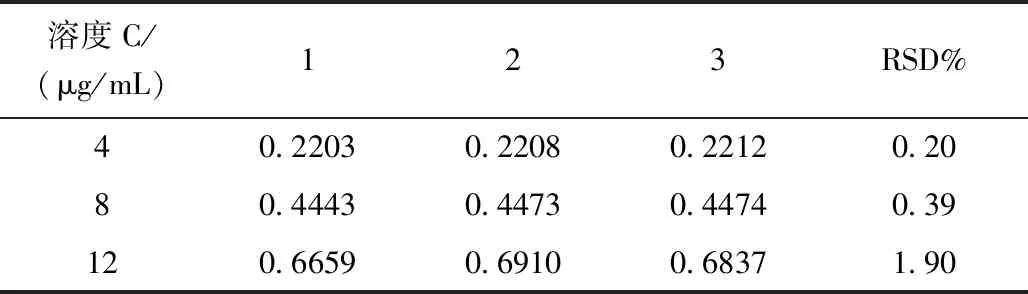
表4 燈盞花素日間精密度實(shí)驗(yàn)結(jié)果
3.1.4 方法回收率試驗(yàn)
低、中、高三種不同濃度的燈盞乙素溶液的方法回收率實(shí)驗(yàn)結(jié)果見表5,RSD小于3%,表明此測(cè)定方法符合含量測(cè)定要求。
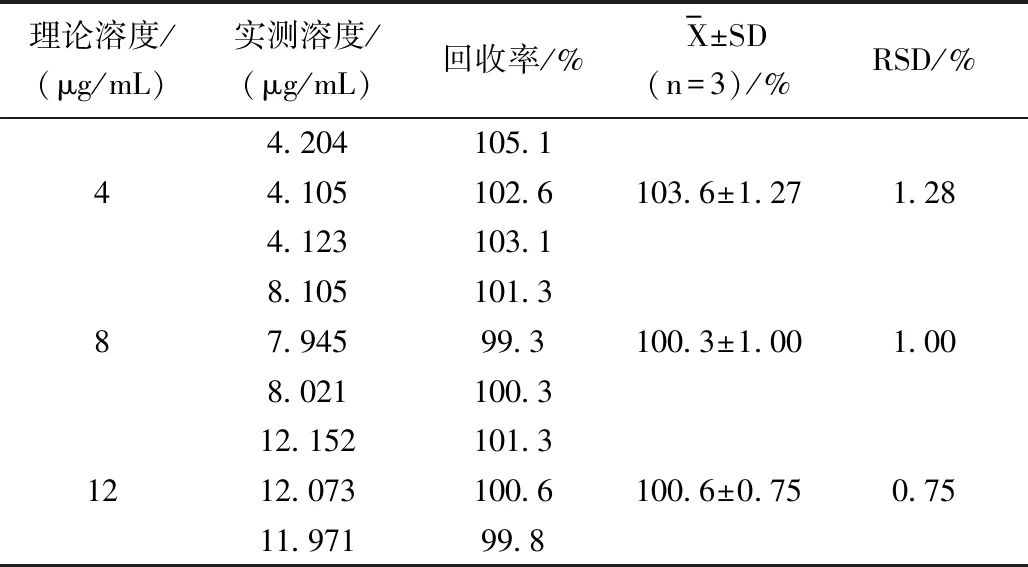
表5 燈盞花素方法回收率實(shí)驗(yàn)結(jié)果(n=3)
3.2 Bre/TPGS脂質(zhì)體的制備工藝篩選結(jié)果
3.2.1 水化溫度對(duì)Bre/TPGS脂質(zhì)體的影響
固定藥物與載體比例與水化時(shí)間,在制備過程中考察水化溫度對(duì)脂質(zhì)體的粒徑、包封率和載藥量的影響。從表6可知水化溫度對(duì)聚合物的粒徑影響較小,37 ℃時(shí)制備的聚合物脂質(zhì)體的包封率和載藥量較高。

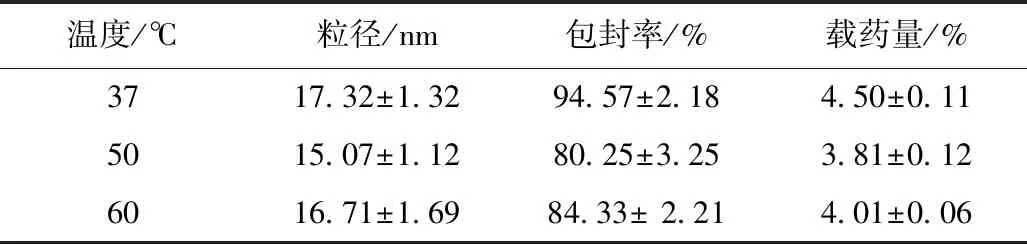
溫度/℃粒徑/nm包封率/%載藥量/%3717.32±1.3294.57±2.184.50±0.115015.07±1.1280.25±3.253.81±0.126016.71±1.6984.33± 2.214.01±0.06
3.2.2 水化時(shí)間對(duì)Bre/TPGS脂質(zhì)體的影響
固定藥物與載體比例與水化溫度,在制備過程中考察水化時(shí)間對(duì)脂質(zhì)體的粒徑、包封率和載藥量的影響。從表7中可知,脂質(zhì)體的粒徑受水化時(shí)間的影響變化不大,在3 h時(shí)藥物的包封率達(dá)到94.57%。

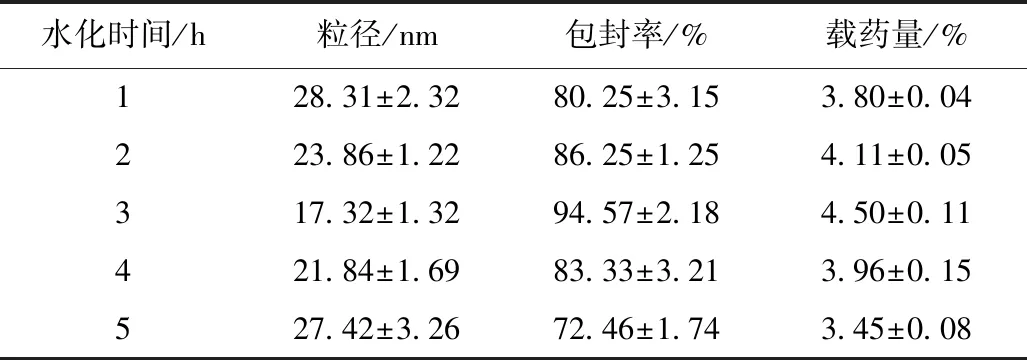
水化時(shí)間/h粒徑/nm包封率/%載藥量/%128.31±2.3280.25±3.153.80±0.04223.86±1.2286.25±1.254.11±0.05317.32±1.3294.57±2.184.50±0.11421.84±1.6983.33±3.213.96±0.15527.42±3.2672.46±1.743.45±0.08
3.2.3 藥物與載體比例對(duì)Bre/TPGS脂質(zhì)體的影響
從表8中數(shù)據(jù)可知,固定水化溫度與水化時(shí)間,在制備過程選取6個(gè)不同藥物與載體比考察其對(duì)脂質(zhì)體的粒徑、包封率和載藥量的影響。
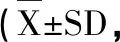
表8 不同藥物與載體比例對(duì)Bre/TPGS脂質(zhì)體的影響n=3)
3.3 Bre/TPGS脂質(zhì)體的制備工藝優(yōu)化結(jié)果
通過正交實(shí)驗(yàn)來進(jìn)一步優(yōu)化Bre/TPGS脂質(zhì)體的制備工藝,選擇包封率作為考察指標(biāo),考察藥物與載藥量的比值(A)、水化溫度(B)、水化時(shí)間(C)對(duì)脂質(zhì)體包封率的影響。根據(jù)L9(33)正交設(shè)計(jì)表,進(jìn)行三因素、三水平正交實(shí)驗(yàn),篩選出制備Bre/TPGS脂質(zhì)體最佳工藝。
3.4 正交實(shí)驗(yàn)最佳制備工藝的驗(yàn)證
精密稱取100 mg聚乙二醇1000維生素E琥珀酸酯,置茄型瓶中,加入7.00 mL燈盞花素甲醇溶液(1 mg/mL),攪拌混勻后,減壓回收甲醇,然后再加入蒸餾水10 mL,在37 ℃水化溫度,磁力攪拌水化2 h,再加甲醇溶解,減壓回收甲醇,用微孔濾膜過濾,按照此最優(yōu)方法制備3批Bre/TPGS脂質(zhì)體。 Bre/TPGS脂質(zhì)體的包封率為90%±2.62%(n=3),RSD為2.36%。該結(jié)果表明,A2B1C2實(shí)驗(yàn)方案的實(shí)驗(yàn)結(jié)果重現(xiàn)性良好,即制備的Bre/TPGS脂質(zhì)體具有良好的穩(wěn)定性。
4 討 論
燈盞花素在波長(zhǎng)335 nm處有最大吸收峰,且載體藥物聚乙二醇1000維生素E琥珀酸酯在此波長(zhǎng)處不干擾藥物的含量測(cè)定,具有良好專屬性和精密度。實(shí)驗(yàn)證明,采用薄膜溶劑揮發(fā)法制備Bre/TPGS脂質(zhì)體,包封率與載藥量有較大提高。實(shí)驗(yàn)的過程中,選擇對(duì)載藥量和包封率影響較大的單因素,進(jìn)行L9(33)正交設(shè)計(jì)實(shí)驗(yàn)來優(yōu)選Bre/TPGS脂質(zhì)體的制備工藝。通過該法制備聚乙二醇1000維生素E琥珀酸酯脂質(zhì)體工藝簡(jiǎn)單,其粒徑、包封率、載藥量均可控,并具有一定的緩釋作用,為進(jìn)一步臨床應(yīng)用提供參考。

