艾葉揮發油化學成分和藥理作用研究進展
趙秀玲,黨亞麗
1黃山學院生命與環境科學學院, 黃山 245021;2寧波大學海洋學院, 寧波 315211
艾葉為菊科植物艾(ArtemisiaargyiLevi.et Vant)的干燥葉,性溫,味苦、辛,歸肝、脾、腎經,具有散寒止痛、溫經止血、鎮咳平喘、殺蟲止癢及安胎的作用[1]。艾葉富含多種生物活性成分,其中揮發油是艾葉的主要有效成分群[2],艾葉揮發油含量為1.23%,并且艾葉揮發油已成為當階段的研究熱點[3]。艾葉揮發油具有抗菌、抗炎、消毒驅蟲、美白、止血、平嗜、抗過敏、鎮嚏、止癢等功效[4- 9],是食品、香料及化學工業的重要原料。現對近幾年艾葉揮發油的提取方法、化學成分、藥理作用、臨床應用及安全性做一概述,為艾葉揮發油的進一步開發利用提供借鑒。
1 艾葉揮發油的提取
有效的提取方法和工藝是揮發油質量和臨床療效的保證,艾葉揮發油的研究主要從提取工藝的比較及其成分鑒別方面展開,對于艾葉資源的開發利用也具有重要意義。艾葉揮發油的提取方法可分為水蒸汽蒸餾法、微波輔助法、超臨界流體萃取法、超聲波輔助法、溶劑法、壓榨法、半仿生法、活性離子水法、酶法、荷電法等[10- 12]。
其中以水蒸汽蒸餾法提取應用較多,提取所得揮發油中化學成分種類較少,能特征性的反映艾葉的種屬特性,但揮發油得率低。在水蒸汽蒸餾的基礎上添加了超聲、微波協同水蒸氣蒸餾純化的裝置,使用水作為溶劑。酶法提取則在溫和的條件下使有效成分充分溶解、混懸于溶劑中從而達到提高提取率。Bao[13]采用微波輔助水蒸汽蒸餾法提取艾葉揮發油,具有綠色、環保、操作便捷和節省時間等優點[14,15],還提高了艾葉揮發油的商業價值。Xie等[16]利用半仿生法提取艾葉揮發油,與水蒸氣蒸餾法相比盡管提取率提高了43.84%,但還需改進提取工藝條件以提高提取率和避免活性組分進一步轉化。Wang[17]優選CO2超臨界萃取法提取艾葉揮發油的工藝(比水蒸氣蒸餾法[18]提取的得率提高了97.67%),此法對有效成分進行選擇性提取及分離純化,但所得揮發油并不純凈,導致處理過程揮發油易損失。Liang等[19]、Zhang等[20]建立了HS- SPME- GC- MS法測定艾葉揮發性成分,此法簡單、快捷、所需樣品量小,能全面快速獲得樣品中揮發性物質的組成信息等。
2 艾葉揮發油的化學成分
艾葉具有濃烈香氣,揮發性成分較復雜,由于環境、氣候條件的差異,不同產地、不同品種、不同提取方法的艾葉揮發油化學成分的類型與種類及其相對百分含量都有較大差異。工業化生產時應充分考慮這個因素。現將不同條件下艾葉揮發油的成分特點綜述如下。
2.1 不同提取方法所得艾葉揮發油成分
不同提取方法艾葉揮發油成分特點如下表。
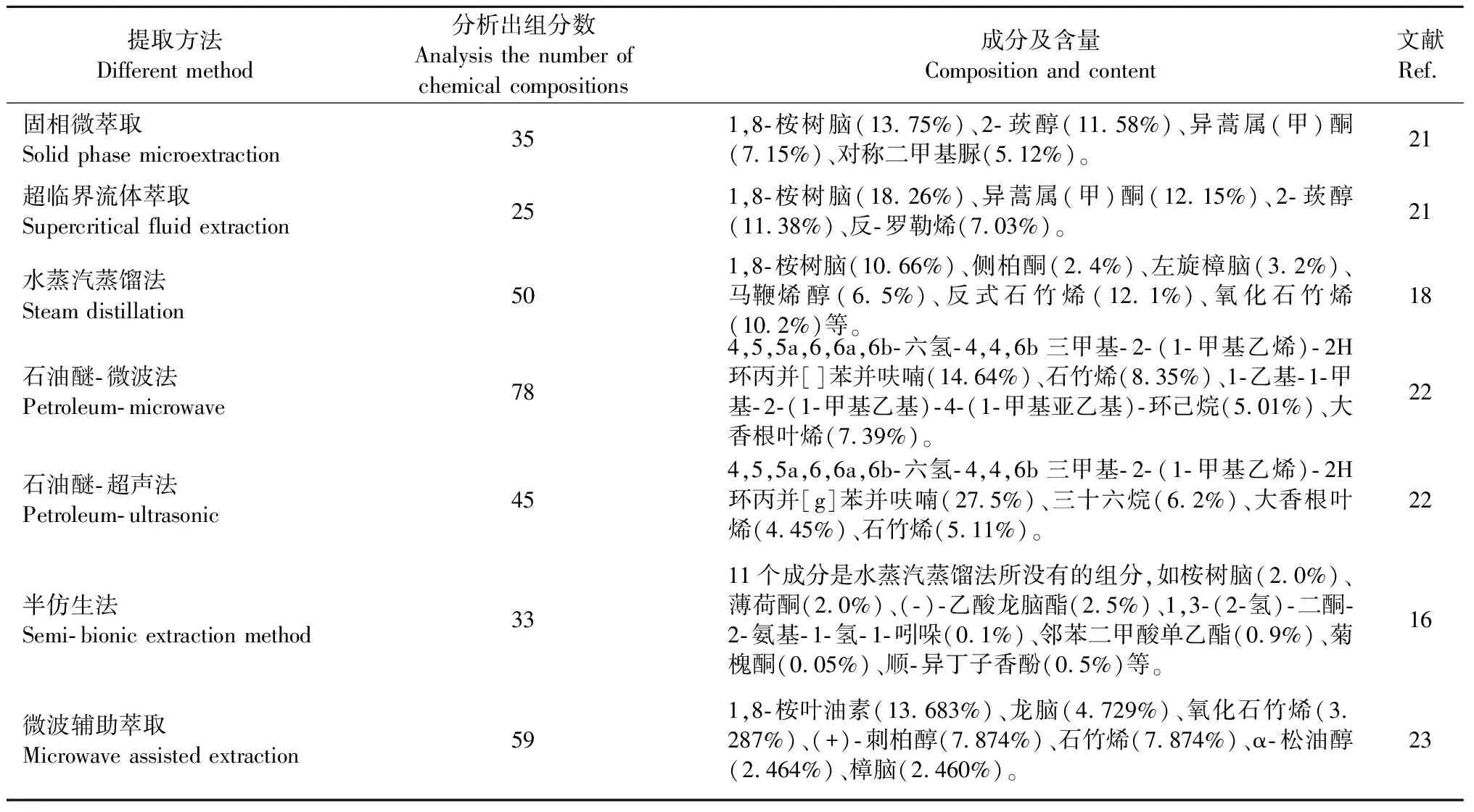
表1 不同提取方法艾葉揮發油中的化學成分
超臨界CO2萃取法所得成分較少,且以酮類和醇類居多,而水蒸氣蒸餾法得到的成分以醇類和烯類居多。石油醚對植物的細胞壁滲透性較差,超聲法雖然能夠破損一部分細胞,但是還是不能很好的提取化合物,而用微波法卻能比較好的對植物的細胞壁破損從而提取得到比較全的化合物。半仿生法實驗時間較早,且選擇考察的指標成分和設備陳舊,其實驗結果對艾葉揮發油制備工藝工業化生產有一定的局限性。
2.2 不同產地艾葉揮發油的化學成分
通過對產自湖北、湖南、廣東、甘肅、河北、山西等12個不同產地的品種及移栽品種的艾葉揮發油的GC- MS分析得知:各產地艾葉揮發油主要共有成分為樟腦、桉油精、松油醇、龍腦、側柏酮、石竹烯等;樟腦、側柏酮等毒性成分較低的為安徽六安、甘肅蘭州及山西五城的五月艾的艾葉揮發油;蘄春移栽至山西的艾葉揮發油含量(1.25%)、化學成分種類(37個)及毒性成分(樟腦和側柏酮比均較低)在含量均優于Jin[24]。Zhao[25]試驗結果表明艾葉揮發油中主要含有醇類、烯類、醛酮類、酯類等化合物,與文獻報道中用GC- MS方法分析中的艾葉揮發油所的成分相一致。設定相關系數閾值0.950 0以區分河南產地與其它產地艾葉藥材。因此,植物生長環境如海拔高度、溫度、濕度、日照等,都直接影響揮發油的化學成分,不同產地的艾葉揮發油成分也存在明顯差異[26],在其使用上需要注意產地因素。此后應進一步開展該藥材的規范化種植、化學成分與質量標準研究,以指導艾葉在不同領域的合理應用。
2.3 不同采摘時間艾葉揮發油的化學成分
由于植物處于不同的生長期,生物合成與代謝的累積受各種生物酶、光照、溫度、水分、不同土壤肥力以及植物個體差異、大田等因素影響,使得成分種類和含量不斷發生變化。采集艾葉樣本時間的變化規律同揮發性組分主成分含量累積表現呈現正向的相關性[27]。不同采集時間構成艾葉揮發性主要的特征性成分(R)- 4- 甲基- 1- (1- 異丙基)- 3- 環己烯- 1- 醇、莰烯、1- 甲基- 3- (1- 異丙基- 苯)、C- 松油烯、龍腦、桉油精等成份含量較高,其中前14種成分具有明顯的上升趨勢,最后兩種則呈現相對波動下降的趨勢。可見艾葉最佳采摘時間為端午節前后1~2周[27]。此結論與Hong[28]的研究結果大致一致。
2.4 陳化或炮制前后艾葉揮發油的化學成分
研究發現艾葉陳化前后其揮發油成分的種類及含量會發生比較明顯的變化,還有新的成分出現[29]。如陳化后β- 蒎烯、乙酸菊烯酯、4,4′- 二甲基聯苯、澳白檀醇等成分的色譜峰增加;桉油精、1- 甲基萘、2,5,8- 三甲基萘酚等色譜峰降低;順- 松油醇、沉香醇、側柏醇等為新鮮艾葉沒有的色譜峰,而陳化后艾葉出現了這些色譜峰[29]。Song[30]將生艾葉炮制成醋艾炭后,發現揮發油含量由0.35%(生艾葉)降為0.015%(醋艾炭),艾葉揮發油莰烯、鄰異丙基甲苯等成分消失,α- 蒎烯絕對含量降低了8倍,合成右旋龍腦含量由7.95%降至0.38%,桉樹腦由18.22%降至0.82%,這可能與艾葉炮制后刺激性、毒性降低有關。
2.5 存儲條件對艾葉揮發油的化學成分的影響
Miao[31]對儲存條件對艾葉揮發油成分影響的研究,結果表明影響艾葉儲存效果的因素主次排序為:儲存溫度>儲存濕度>儲存時間,艾葉在最佳儲存條件下(儲存溫度40 ℃,儲存濕度40%,儲存時間為8個月)艾葉揮發油的香氣特征豐富、明顯,主要成分為桉葉油醇(31.54%)、右旋龍腦(8.94%)、左旋樟腦(6.12%)和石竹烯(6.09%),可見由于受不同生長環境及儲藏條件等因素影響,其有效成分含量及功效均存在一定差異。
3 艾葉揮發油的藥理作用
3.1 抗病毒和抑菌作用
Feng等[32]研究結果表明艾葉揮發油及納米結構脂質載體(Naostructured lipid carrier,NLC)均對鴨肝組織中乙肝病毒有抑制作用,高劑量抑制作用更明顯,且艾葉揮發油做成NLC制劑后抑制作用比原料藥更加顯著。原因可能是艾葉揮發油NLC納米粒粒子較小,比表面積較大,增加了艾葉揮發油的溶解,利于吸收;艾葉揮發油NLC延長在體內的滯留時間,可增強與體內粘膜組織的黏附性,進而發揮更強的藥性[33]。
艾葉的抑菌實驗表明,艾葉揮發油對金黃色葡萄球菌、沙門氏菌、大腸桿菌的抑菌效果都很好[18],作用機理可能是由于破壞了細胞膜的通透性從而阻礙了細菌的呼吸作用[34]。Yang等[35]采用三聚氰胺甲醛包裹艾葉揮發油,運用傅里葉變換紅外光譜和熱重分析鑒定,評估了微膠囊的抗菌活性,結果表明包裹物性能良好,為開發新的具殼結構找到一種新方法。Shi等[36]研究艾葉揮發油誘導白念珠菌凋亡的活性,結果顯示艾葉揮發油對白念珠菌SC5314的MIC為0.5 mL/L,大于0.5 mL/L的艾葉揮發油干預后,白念珠菌SC5314細胞內活性氧水平顯著升高、線粒體膜電位顯著降低、凋亡比例顯著增加、metacaspase活性顯著升高、細胞核固縮,為艾葉揮發油治療皮膚常見真菌感染的作用機制研究提供了重要的實驗基礎。
3.2 平喘作用
Wang等[37]研究艾葉油的平喘作用,艾葉油具有舒張支氣管平滑肌的作用,所以能明顯舒緩氯化鋇引起的離體豚鼠氣管平滑肌的痙攣;通過霧化給藥能明顯延長豚鼠的引喘潛伏期,對乙酰膽堿和組胺誘發的豚鼠哮喘具有抑制作用。Wei等[38]研究艾葉油的平喘活性,結果艾葉油高劑量組對卵蛋白引起的小鼠哮喘,能明顯減少BAL下中白細胞總數(P<0.05)和嗜酸性粒細胞計數(P<0.01),得出艾葉油具有平喘作用的結論。艾葉揮發油中含有α- 萜品烯醇,此成分能夠作用于中樞,通過調節氣管達到祛痰、平喘、鎮咳的作用,從而治療藥物性哮喘,使組胺和乙酰膽堿引起哮喘的潛伏期延長,從而減少抽搐。
3.3 抗炎作用
Zhao等[39]探討艾葉油對小鼠耳腫脹急性炎癥的抗炎作用,結果表明,艾葉揮發油高劑量、低劑量組對二甲苯致炎的小鼠腫脹均有顯著的抑制作用,當艾葉揮發油10 mL/kg劑量時,對小鼠耳腫脹急性炎癥發揮較強的抗炎活性;二甲苯的最佳作用時間為40 min左右。Tian[40]研究艾葉提取組分艾葉輕油(揮發油類成分占60%)的抗炎作用。在體內實驗中,觀察到在熒光顯微鏡下斑馬魚炎癥模型中經熒光標記的巨噬細胞和中性粒細胞都有一定數量減少,證明了其具有一定的抗炎作用。Real- time PCR 方法檢測發現提取組分能有效降低RAW 264.7細胞在LPS刺激后IL- 6、JL- lβ和TNF- α炎癥因子的表達和分泌。Griess方法檢測發現艾葉提取物能顯著減少在LPS刺激下巨噬細胞NO的釋放量,并呈濃度依賴性降低。因此,艾葉提取物可以作為有效治療炎癥疾病的有效藥物。
3.4 鎮痛鎮靜作用
Fu等[41]探討了艾葉溫經儀(結構中間是艾葉揮發油層,用以保存艾葉揮發油)在治療痛經中的療效,結果艾葉溫經儀具有行氣消瘀,散寒止痛的功效,對治療痛經有良好的效果。Sun等[42]的研究結果表明艾葉揮發油發揮鎮痛作用主要與降低血中PGE2含量,調節體內SOD、MDA、NO水平有關,而且艾葉揮發油功效的發揮與揮發油劑量、用藥時間密切相關,呈現一定的劑量依賴關系。有研究發現將艾葉油從低到高一系列濃度對家兔腹腔注射,觀察艾葉油對小鼠戊巴比妥鈉睡眠時間的影響,研究發現艾葉油可以延長小鼠的睡眠時間;同時家兔表現出從鎮靜到呼吸減慢最后死亡的不同階段反應,表明艾葉油具有鎮靜作用。
3.5 對藥物透皮吸收的促滲作用
采用天然產物中的有效成分作為滲透促進劑是目前透皮領域研究的熱點之一。Pan[43]研究艾葉揮發油對雙氯芬酸鈉透皮吸收的促進作用。結果在完整皮膚中,艾葉油對雙氯芬酸鈉有促透作用,滲透作用比氯酮的強(P<0.05);在去角質層皮膚中,氯酮對雙氯芬酸鈉12 h促透作用顯著,與艾葉油差異無統計學意義(P>0.05)。這是因為艾葉中含有較多烯萜類化合物能夠改變角質層細胞內的角蛋白構象、性質、松弛角蛋白之間的結合力,形成微孔通道,增加藥物通過細胞內途徑的滲透性[44]。Gao[45]的研究結果表明0.8%的艾葉揮發油的β- 環糊精包合物對鹽酸環丙沙星有顯著的透皮吸收促進作用。
3.6 其他作用
He等[46]的研究結果表明艾葉揮發油能夠刺激紅細胞的生成,具有抗自由基損傷的作用,可以提高血液中吞噬細胞的活性的作用,從而提高機體抗感染作用,促進機體免疫保護功能。用艾葉油給卵蛋白致敏的鼠灌胃后,對再次因卵蛋白引起的過敏性休克有顯著的保護作用,能有效抑制組胺及慢反應物質的釋放[47]。
4 臨床應用
臨床上,艾葉揮發油主要用于治療瘡瘍、鼻炎、肩背腰部軟組織疼痛,可用于有效抑制室內空氣中的細菌生長,還可用于治療慢性支氣管炎和哮喘等癥疾。目前,臨床使用的艾葉揮發油的劑型包括乳膏劑、油劑、膠囊、氣霧、注射劑等。艾葉資源豐富,價值低廉,是菊科多年生草本植物艾的干燥葉,揮發油的提取制作方便,值得大范圍推廣應用。
5 艾葉揮發油的安全性
研究者對艾葉揮發油毒性認識和研究結論不一致,在臨床應用時要引起重視。Huang等[48]研究艾葉水提組分和揮發油對小鼠肝毒性“量- 時- 毒”關系,結果二者均可造成明顯的肝毒性損傷,并且肝毒性作用程度揮發油>水提組分。Wang等[49]研究艾葉油霧化吸入對大鼠的長期毒性研究表明艾葉油連續給藥3個月后和6個月及停藥1個月后,提示艾葉油長期霧化吸入給藥無明顯毒性,是安全的。Liu等[22]分析不同提取方法得到的揮發油的急性肝毒性并進行比較,結果表明:水蒸汽蒸餾法(小分子萜類、部分苯類物質為主)的急性肝毒性最大,超臨界CO2提取法的(以長鏈酯類化合物為主)為輕,石油醚法(以芳香族化合物為主)的未顯示明顯毒性。艾葉揮發性組分是其功效和毒性大小的重要物質組成,可以將毒性成分如側柏酮、樟腦、丁子香酚含量的降低作為艾葉采摘的主要依據[27]。現代實驗方法中艾葉是生艾葉沒經過任何預處理,而且用量是臨床應用的十幾倍甚至幾百倍。而臨床應用艾葉揮發油應該將艾葉配伍、炮制(甚至蒸煮煎炸),嚴把用藥劑量,正確針對適應癥,控制煎煮時間。應用艾葉揮發油時還應注意揮發油的提取方法,肝毒性是其物質基礎,避免采用水蒸汽蒸餾法提取,宜采用有機溶劑法提取(如石油醚),這樣就避開了有急毒性或亞毒性的物質被萃取出來。
6 結論
艾葉揮發油的藥理作用廣泛,其作用機制的研究已深入到分子和細胞水平,是當今的研究熱點,并在其提取工藝、化學成分、藥理作用、臨床應用及其安全性方面進行了較為系統的研究,證實了艾葉揮發油具有抗菌譜廣、抗菌活性強、臨床療效好、不良反應少而輕微的一種的天然抗菌藥物,但進一步開拓市場還需解決一系列問題。首先,艾葉揮發油易揮發,且易受外界影響而改變成分,在一般制劑中性質不穩定、不易溶于水、配制成水溶液濃度低,降低了藥效。因此,后續研究中,需要運用新技術(如包合技術)研究出新劑型并注重其構效關系,提高血藥濃度,充分發揮其藥效及易于給藥的途徑。其次,需加強對艾葉揮發油化學成分質量控制的研究,針對艾葉揮發油中有活性的化學成分開發出新的劑型與高效低毒的新藥,以充分發揮艾葉揮發油的市場潛力與應用潛力,將會產生重大的社會意義與經濟效益。

