小鼠局部淋巴結實驗在紅花注射液致敏性研究中的應用
徐小玲,鄔姍,潘望平,呂曉君,吳森,何開勇
(湖北省藥品監督檢驗研究院,武漢 430064)
隨著中藥注射劑在臨床的廣泛應用,與其相關的變態反應的報道也日益增多。紅花注射液是由中藥紅花經提取制成的滅菌溶液,主要成分大多為相對分子質量較小的化合物,主要含有色素、黃酮類化合物、酚酸、脂肪酸、揮發油及多炔等[1-2],臨床上用于閉塞性腦血管、冠心病和脈管炎等疾病的治療。近年來,紅花注射液在臨床使用中引起的不良反應特別是變態反應日趨增多[3],已逐漸引起人們的重視。目前國內對藥物的致敏性評價主要通過主動過敏實驗、被動過敏實驗,以及應用于Ⅵ型超敏反應的豚鼠最大化實驗(guinea-pig maximization test,GPMT)和局部封閉涂皮實驗(buehler test,BT)[4-5],而該類實驗主要針對的是大分子蛋白質類引起的變態反應,對小分子化合物容易出現假陰性結果。對于小分子化學藥物,尤其是變態反應居高不下的中藥注射劑,亟需要建立一種靈敏、特異、簡便和可靠的非臨床安全性實驗方法來評價其致敏潛在風險。局部淋巴結實驗(local lymph node assay,LLNA)是目前惟一可靠的篩選和評價藥物超敏反應的實驗方法,主要依據是腘窩淋巴結(popliteal lymph node,PLN)是足趾部注射外源化學物質發生免疫應答的第一部位和惟一引流淋巴結,因此,在足趾引入的致敏物質勢必首先導致腘窩淋巴結及其相關免疫細胞的變化[6-9]。本研究旨在建立小鼠LLNA的方法,以替代傳統的豚鼠全身主動過敏實驗(active systemic anaphylaxis,ASA)檢測方法,對中藥紅花注射液的致敏性進行檢測,探討紅花注射液引起變態反應的可能機制,并與豚鼠全身主動過敏實驗進行比較。
1 材料與方法
1.1試藥 供試品1~5:紅花注射液(批號:150411301,14091912,140914,141002020,10314122-32);陰性對照:磷酸鹽緩沖液(PBS,pH值7.2),氯化鈉注射液;陽性對照:鏈脲佐菌素(streptozotocin,STZ)、2,4,6-三硝基苯磺酸(2,4,6-trinitrobenzene-sulfonic acid sol,TNBS)、D-青霉胺(D-penicillamine,D-PEN)。anti-mouse B220抗體、anti-mouse CD3抗體、anti-mouse CD4抗體、anti-mouse CD8抗體、anti-mouse CD69抗體(美國eBioscience公司和BD公司)。
1.2實驗動物 無特定病原體(SPF)級Balb/c小鼠,雌性,6~8周齡,體質量18~22 g,由武漢生物制品研究所有限責任公司提供,動物生產許可證號:SCXK(鄂) 2017-0013。小鼠適應性飼養l周后開始實驗。自由飲水攝食,溫度(23±1) ℃,相對濕度45%~55%,12 h明暗交替。豚鼠,健康合格,體質量250~350 g,雌雄各半,由武漢生物制品研究所有限責任公司提供,動物生產許可證號:SCXK(鄂) 2017-0013,適應性喂養l周后開始實驗。動物使用許可證號:SYXK(鄂) 2014-0009。
1.3儀器 Navios流式細胞儀(貝克曼庫爾特商貿有限公司);TC20細胞計數儀(美國BIO-RAD公司);高速冷凍離心機(貝克曼庫爾特公司)。
1.4豚鼠全身主動變態反應 按《中華人民共和國藥典》2015年版四部進行。豚鼠隨機分為6組,每組6只。第1組為氯化鈉注射液對照組,第2~6組為供試品1~5。各組動物分別腹腔注射氯化鈉注射液和供試品溶液0.5 mL,隔日致敏1次,共3次。在注射后第14,21 天,分別從耳靜脈注射氯化鈉注射液和供試品溶液1 mL,觀察激發后30 min內豚鼠的反應。
1.5小鼠局部淋巴結實驗
1.5.1劑量與分組 實驗設9個組別,隨機分為陰性對照組(PBS)、STZ組、TNBS組、D-PEN組、供試品組1~5,每組10只小鼠。將STZ溶于PBS。
1.5.2免疫動物 固定小鼠,以乙醇棉球消毒左后側(處理側)足趾部,一次性無菌胰島素注射器皮下注射給藥,進針方向由足跟指向足尖,各組給藥體積均為50 μL,對照組給予PBS,對側不做處理。
1.5.3PLN質量指數和PLN細胞指數測定 注射7 d后,處死小鼠,將其雙側腘窩淋巴結與周圍組織分離取出,分別用分析天平稱質量。計算 PLN質量指數(WI),PLN質量指數=左側PLN質量/右側PLN質量。
PLN細胞指數測定,分別取小鼠雙側腘窩淋巴結,用載玻片壓碎,加入PBS溶液(pH 值7.4)2 mL,制成單細胞懸液,用細胞計數儀計數。計算PLN細胞指數(CI),PLN細胞指數=左側PLN細胞數/右側PLN細胞數。
1.5.4淋巴細胞及早期活化指標分析 用解剖鑷分離、摘取腘窩淋巴結(PLN),常規制備單細胞懸液。用冷PBS洗滌細胞2次,細胞計數儀計數,調整細胞濃度為1×107·L-1。取上述各組淋巴細胞懸液100 μL(1×106個細胞)于流式管中,加入相應抗小鼠抗體0.5 μg,混勻后,室溫避光孵育30 min。然后經PBS洗滌2次(1400 r·min-1,r=18.5 cm,5 min),棄上清液,加 PBS溶液0.4 mL重懸,過濾后流式細胞儀分析。

2 結果
2.1豚鼠全身主動變態反應 結果顯示,供試品1~5組和氯化鈉注射液組均未出現明顯變態反應癥狀。
2.2小鼠局部淋巴結實驗
2.2.1PLN質量指數和PLN細胞指數測定 由表1可見,單次足趾部給予受試物后第7天,陽性對照組和供試品組2的PLN質量指數與陰性對照組比較有所升高,但差異無統計學意義;陽性對照組和供試品組1~5的PLN細胞指數與陰性對照組比較,均有升高,但差異無統計學意義,即WI和CI未達到陽性標準。
表1 受試物對PLN質量指數和細胞指數的影響
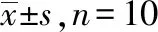
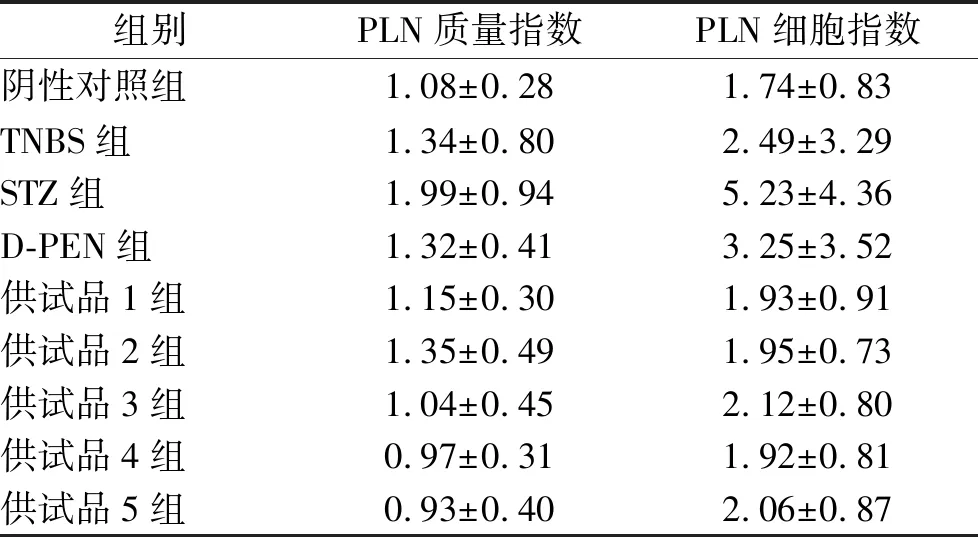
組別PLN質量指數PLN細胞指數陰性對照組1.08±0.281.74±0.83TNBS組1.34±0.802.49±3.29STZ組1.99±0.945.23±4.36D-PEN組1.32±0.413.25±3.52供試品1組1.15±0.301.93±0.91供試品2組1.35±0.491.95±0.73供試品3組1.04±0.452.12±0.80供試品4組0.97±0.311.92±0.81供試品5組0.93±0.402.06±0.87
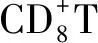
3 討論
中藥注射劑臨床應用廣泛,但近年來不良反應頻發,其中變態反應占75%,中藥注射劑中的某些成分、制劑輔料以及體內代謝產物可能為致敏原,引起I型超敏反應[10-12]。目前,大多數過敏實驗方法如ASA都是根據I型變態反應發病機制的設計建立的。本研究采用ASA法檢查5批中藥注射劑,結果均未出現明顯變態反應。但是,ASA的缺點是要采用較多動物,需要激發后進行觀察,主觀性較強,且給動物帶來了痛苦,不符合“3R原則”。

圖1 T、B細胞比例及其早期活化分子的流式分析圖
表2 陽性對照對T、B細胞比例及早期活化分子的影響
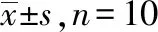

組別CD3CD3CD4CD3CD8B220CD3CD69CD4CD69CD8CD69B220CD69陰性對照組85.60±5.5047.30±4.1035.00±3.2016.60±4.102.13±0.302.68±0.460.02±0.040.11±0.07TNBS組80.20±11.5049.50±7.6027.90±6.40①21.90±12.002.83±0.82①3.20±0.830.02±0.020.15±0.04STZ組87.10±6.9048.40±3.5037.20±6.4015.20±6.501.58±0.491.81±0.43②0.02±0.020.05±0.04D-PEN組80.90±4.7043.80±4.7033.90±1.9019.50±5.001.44±0.24①2.00±0.280.03±0.040.16±0.07
①與陰性對照組比較,P<0.05;②與陰性對照組比較,P<0.01。
①Compared with negative control group,P<0.05;②Compared with negative control group,P<0.01.
表3 紅花注射液對T、B細胞比例及早期活化分子的影響
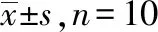
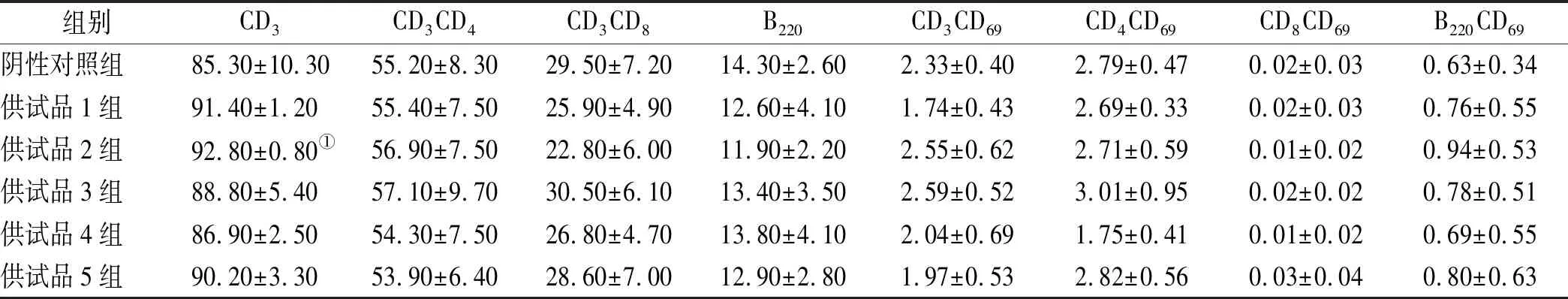
組別CD3CD3CD4CD3CD8B220CD3CD69CD4CD69CD8CD69B220CD69陰性對照組85.30±10.3055.20±8.3029.50±7.2014.30±2.602.33±0.402.79±0.470.02±0.030.63±0.34供試品1組91.40±1.2055.40±7.5025.90±4.9012.60±4.101.74±0.432.69±0.330.02±0.030.76±0.55供試品2組92.80±0.80①56.90±7.5022.80±6.0011.90±2.202.55±0.622.71±0.590.01±0.020.94±0.53供試品3組88.80±5.4057.10±9.7030.50±6.1013.40±3.502.59±0.523.01±0.950.02±0.020.78±0.51供試品4組86.90±2.5054.30±7.5026.80±4.7013.80±4.102.04±0.691.75±0.410.01±0.020.69±0.55供試品5組90.20±3.3053.90±6.4028.60±7.0012.90±2.801.97±0.532.82±0.560.03±0.040.80±0.63
①與陰性對照組比較,P<0.05。
①Compared with negative control group,P<0.05.

本研究通過已知的具有致敏性的幾種陽性藥對免疫細胞表面分子的表達影響的檢測,建立小鼠PLNA的檢測平臺。應用這些與陽性藥致敏性密切相關的指標來評價中藥注射劑的致敏性。PLNA結果顯示5批中藥注射劑中,僅有1批WI有增加的趨勢,且T淋巴細胞比例升高,提示這批樣品引起了淋巴結的增大和T淋巴細胞的增殖,具有一定的致敏潛在風險,而其他批次供試品指標的變化均差異無統計學意義,與ASA的結果基本一致,但PLNA的方法比傳統的ASA靈敏度更高。
小鼠PLNA可以更早期地對藥物致敏性給予預測和評價,該檢測手段不但靈敏度高,而且簡便、快速。通過致敏指標的檢測可以對致敏的原因和類型進行診斷,減少傳統過敏實驗中激發實驗給動物帶來的安全風險和痛苦。

