基于FDA疫苗不良事件報告系統數據的人乳頭狀瘤病毒四價疫苗不良反應信號監測*
王懿怡,陳力
(1.四川大學華西第二醫院藥學部,成都 610041;2.四川大學華西第二醫院循證藥學中心,成都 610041;3.出生缺陷與相關婦兒疾病教育部重點實驗室,成都 610041;4.南京醫科大學附屬無錫婦幼保健院藥學部,無錫 214002)
在全球,宮頸癌已成為僅次于乳腺癌的女性第二大致死癌癥[1]。臨床研究發現,宮頸癌是唯一病因和發病機制明確、可以通過早期篩查進行確認和防治的婦科癌癥。研究證實,高危型人乳頭狀瘤病毒(human papillomavirus,HPV)的持續感染是宮頸癌發生的最主要原因[2]。HPV四價疫苗(Gardasil)由美國 Merk制藥公司研發,2006 年 6 月 28 日獲得美國食品藥品管理局(FDA)批準上市,以病毒樣顆粒(virus-like particles,VLPs)為抗原的HPV 預防性四價疫苗[3],可以有效預防HPV 16型和18型引起的約70%宮頸癌,以及由HPV 6型和11型引起的90%生殖器疣病,并對大多數HPV引起的肛門、外陰、陰道和陰莖癌也有良好的預防作用,當前已在全球100多個國家和地區廣泛使用。HPV四價疫苗于2017年11月在國內上市。目前Gardasil說明書提及本品不良反應包括頭痛、頭暈、發熱、惡心和注射部位疼痛、腫脹、紅斑、瘙癢、瘀傷等。
HPV疫苗對預防宮頸癌前病變、HPV持續性感染、HPV相關外生殖器病變顯示了高效的保護效應和交叉保護效果[4],由于說明書上的不良反應的記載是根據使用中不斷發現、確認、更新、完善的過程,因此利用上市后真實世界的數據以及數據挖掘的方法,進一步揭示HPV 四價疫苗的潛在藥品不良反應信號十分必要。筆者通過對美國疫苗不良事件報告系統(Vaccine Adverse Event Reporting System,VAERS )收集的數據進行分析、整理和篩選,對HPV四價疫苗產生的可疑不良反應(adverse drug reaction,ADR)進行信號挖掘分析,為國內臨床安全合理使用HPV疫苗提供參考。
1 資料與方法
1.1資料來源 提取美國VAERS數據庫中2006年第一季度至2018年第四季度共52個季度的數據,原始數據為文本文件,將其導入數據庫中。 VAERS數據庫是一個疫苗上市后安全監測的自發呈報系統,是由疫苗接種者或衛生從業人員自發向不良反應數據庫報告的不良反應信息。由于報告系統的不良反應描述用語具有多樣性,為了便于后續工作,本文對收集到的報告按世界衛生組織不良反應術語集(world health organization adverse reaction terminology,WHOART)的首選術語(preferred term,PT)進行規范化編碼[5]。排除重復報告后,共得到報告1 496 105例。篩選出其中疫苗名稱為 HPV4(Gardasil)為首要懷疑疫苗的報告共120 674例。
1.2數據處理 目前國內外常用的藥品不良反應信號檢測方法主要采用比例失衡法(measure of disproportionality),又稱非均衡性測量法[6]。其基本原理是在1個包含所有報告的數據庫中,當某特定藥物事件組合明顯高于整個數據庫的背景頻率,并且達到一定標準,就認為產生了一個信號[7]。比例失衡法可分為頻數法和貝葉斯法,其中頻數法包括報告比值比法(reporting odds ratio,ROR)和比例報告比值法(proportional reporting ratio,PRR);貝葉斯法包括貝葉斯置信度遞進神經網絡法和伽馬泊松分布縮減法[8]。
采用ROR法和PRR法的特點為:可以估計相對危險度,減少由于對照組選擇所帶來的偏倚;計算簡單;計算結果一致性好[9]。
1.3篩選與計算 WHOART是一個精確度較高的用于編碼與藥物治療過程中的臨床信息的術語集[10]。為避免在后續進行統計時出現相同項目重復統計的錯誤,把表格中的 PT(后文 PT 代表HPV四價疫苗的不良反應)欄含義相同的報告整理為WHOART中的標準寫法。將不規范的習慣用語轉化成標準化信息數據,為相關數據挖掘提供研究基礎。并且 ROR 法要求報告數大于 3 例,如果相同含義的報告數量之和大于3例,而各自分開后報告數卻小于3例時,則會導致可能的信號被忽略。因此,篩選出報告數大于 3的 PT后,將數據整理成比例失衡法中各項所需的值,并計算相應 ROR 值、PRR 值和95%雙側置信區間(95%CI)下限。
2 結果
2.1疫苗不良反應信號 由于ROR法和PRR法兩種方法均靈敏度較高,因此較容易出現假陽性信號。為了避免此類情況發生且篩選出信號較強、較常出現的PT,通過以下方法處理。方法一:將2種方法同時使用。利用公式進行計算后,共得到HPV 四價疫苗不良反應信號3885個,ROR 法和 PRR 法所得的信號強度(ROR 值、PRR 值)有所不同,大多數信號重合。方法二:采取提高閾值[11],對有信號的 PT 進行二次篩選。其方法為:篩選出報告例數(a 值)前100位,并按95%下限降序將PT排序,ROR 95%CI下限和PRR 95%CI下限均應>1,提示生成一個信號,經過二次篩選后,得到PT信號數為 47個。按95%CI下限進行排序,排序情況見表1。
2.2不良反應信號累及系統 將二次篩選后的47個信號及其在WHOART中的累及系統相對應。信號數顯示較多的系統為:中樞及外周神經系統疾病12個信號,全身性損傷10個信號,皮膚及其附件類疾病7個信號,肌肉骨骼系統疾病6個信號。HPV四價疫苗新的不良反應信號與不良反應信號累及系統見表2。
3 討論
表1和表2顯示,經過二次篩選后,HPV四價疫苗得到PT信號數為47個,英文版說明書不良反應主要為頭痛,發熱,惡心,頭暈,注射部位反應(疼痛、腫脹、紅斑、瘙癢、瘀傷)和暈厥。HPV四價疫苗說明書總結中未出現過的不良反應信號有37個。主要涉及中樞及外周神經系統、全身性損傷、皮膚和肌肉骨骼系統疾病等方面,其中部分不良反應出現在說明書臨床應用文獻中。在數據處理過程中,利用ROR法和PRR法計算得出ROR值和PRR值。其數值越大,表明信號越強,則目標藥物和目標不良反應之間的統計學聯系越強。對于ROR和PRR的運用,如果95%CI的下限大于1,則認為檢測到信號。
如果僅從統計學角度考慮,HPV四價疫苗不良反應信號越強,對評估藥物與不良反應的相關性提示意義越大,但是否存在因果關系還需要進一步研究[12]。由于國內HPV四價疫苗2017年上市,時間較短,不良反應的監測數據和相關研究有待完善,因此,必須在使用過程中監測不良反應的發生并進行評估。
表1 HPV四價疫苗信號強度前47位的不良反應信號
Tab.1Top47adversereactionsignalsofHPVtetravalentvaccine

首選術語(PT)報告數(a)ROR95%CI下限(ROR)PRR95%CI下限(PRR)暈厥(syncope)406349.67846.29810.33510.185顱神經損傷(head 50324.59921.0638.4938.082 injury)意識喪失(loss of 175917.69216.4217.5957.372 consciousness)蒼白(pallor)132316.83615.4687.4327.178脫發(alopecia)29712.42810.5446.4735.982眼肌麻痹(gaze palsy)25811.6009.7546.2595.742偏頭痛(migraine)2989.6438.2655.6875.230跌倒發作(fall)8948.5337.8245.3205.061視覺異常(vision 3368.6477.5035.3534.937 blurred)流產(abortion 2538.3027.0605.2284.759 spontaneous)惡心(nausea)25685.4765.2234.0403.912震顫(tremor)6265.0004.5513.7843.544驚厥(convulsion)10714.8254.4913.6933.511運動障礙(dyskinesia)3704.6304.1033.5833.288頭暈(dizziness)39273.9093.7683.1793.093感覺異常(paraesthesia)8233.7833.4963.0922.914多汗(hyperhidrosis)6093.7803.4493.0902.884嘔吐(vomiting)15133.5463.3462.9462.818腹痛(abdominal pain)5632.8422.5912.4752.298肌無力(muscular 3922.7792.4882.4312.224 weakness)頭痛(headache)27032.5492.4442.2692.192焦慮(anxiety)2712.7672.4232.4222.176不適(malaise)7472.6102.4102.3112.165肌肉骨骼病3462.6092.3212.3102.100 (musculoskeletal stiffness)感覺遲鈍8772.4922.3162.2262.096 (hypoaesthesia)淋巴結病3782.4922.2292.2252.030 (lymphadenopathy)寒戰(cold sweat)2242.3822.0622.1431.902活動受限(activities of 4092.1451.9301.9641.797 daily living impaired)胸痛(chest pain)4062.1351.9201.9561.789疲勞(fatigue)13992.0281.9151.8741.785蕁麻疹(urticaria)13181.8311.7271.7161.632步態異常(gait 2351.9581.7051.8181.615 disturbance)肌痛(myalgia)6311.7811.6381.6761.558末梢水腫(oedema 5941.5411.4151.4771.369
續表1 HPV四價疫苗信號強度前47位的不良反應信號
Tab.1Top47adversereactionsignalsofHPVtetravalentvaccine
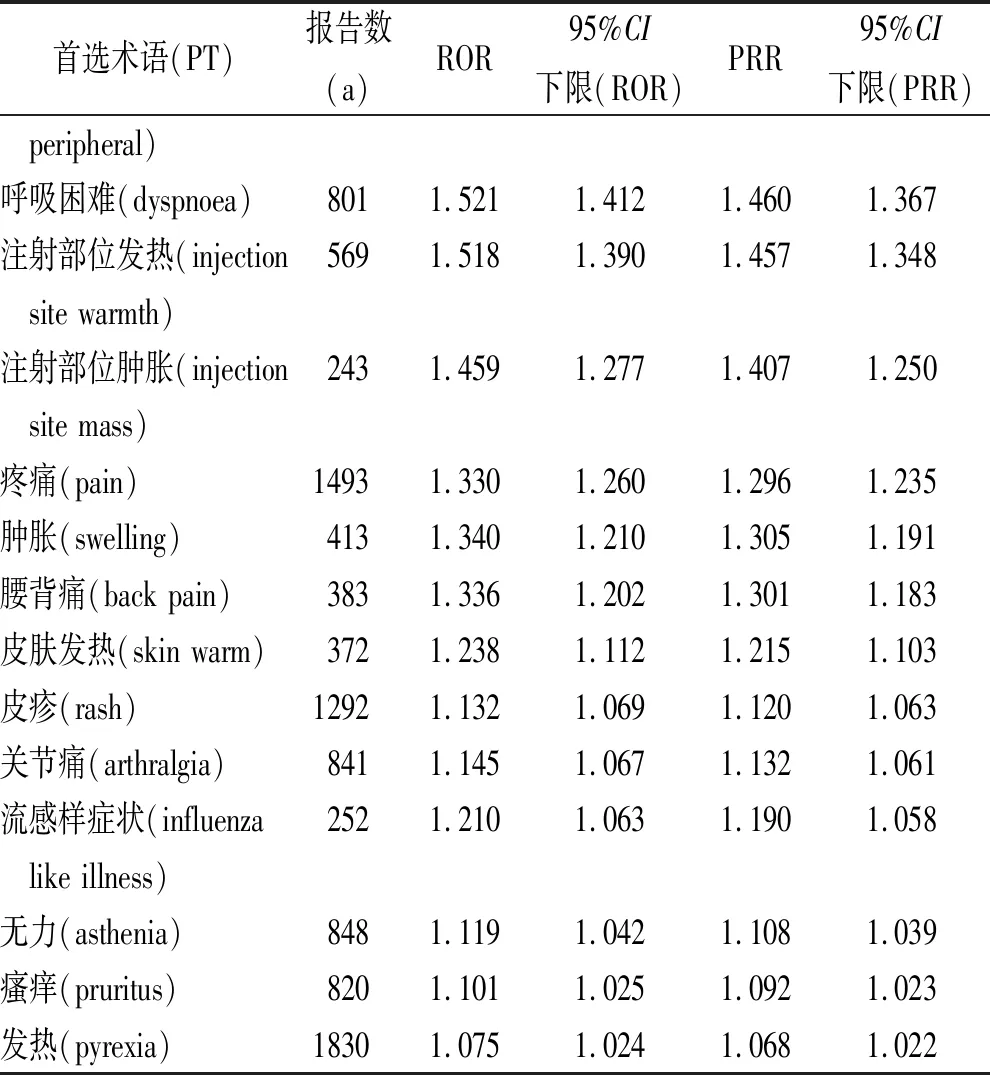
首選術語(PT)報告數(a)ROR95%CI下限(ROR)PRR95%CI下限(PRR) peripheral)呼吸困難(dyspnoea)8011.5211.4121.4601.367注射部位發熱(injection 5691.5181.3901.4571.348 site warmth)注射部位腫脹(injection 2431.4591.2771.4071.250 site mass)疼痛(pain)14931.3301.2601.2961.235腫脹(swelling)4131.3401.2101.3051.191腰背痛(back pain)3831.3361.2021.3011.183皮膚發熱(skin warm)3721.2381.1121.2151.103皮疹(rash)12921.1321.0691.1201.063關節痛(arthralgia)8411.1451.0671.1321.061流感樣癥狀(influenza 2521.2101.0631.1901.058 like illness)無力(asthenia)8481.1191.0421.1081.039瘙癢(pruritus)8201.1011.0251.0921.023發熱(pyrexia)18301.0751.0241.0681.022
表2顯示,將二次篩選后所得到的HPV四價疫苗不良反應信號與HPV四價疫苗說明書中的不良反應進行對比篩選,出現一些新的不良反應信號,其主要分布在神經系統、全身性損傷、皮膚及其附件和肌肉骨骼系統。通過該研究發現HPV四價疫苗說明書中記載的主要不良反應基本包括在所列的信號之內,并且信號數據強烈。47個PT信號:說明書總結不良反應10個,說明書記載相關文獻涉及的23個,未記載的14個。比較剔除用語不同但表達意思相同或相近的不良反應,挖掘出說明書未記載的14個不良反應信號有:皮膚及附件系統的脫發,多汗;肌肉骨骼系統的眼肌麻痹,肌無力;中樞神經和外周神經系統的意識喪失,驚厥,感覺異常,震顫;全身性損傷的胸痛,呼吸困難,末梢水腫;注射部位發熱;流產;焦慮。上述發掘出現的新的不良反應信號在使用過程中也需要關注,如暈厥、腦神經損傷、意識喪失、跌倒等統計信號強烈,說明發生率較高,更應該在HPV疫苗使用過程中加強監控和防范。
針對HPV四價疫苗說明書中出現的暈厥不良反應,在本次研究中發現其不良反應信號最為強烈,建議負責的接種機構配備應對突發急性不良反應的藥品及措施,接種者接種后應在原地休息0.5 h,1周內避免攝入易致過敏食物,如海鮮、雞蛋等,避免進行強烈的體育鍛煉[13]。此次研究的數據來自美國VAERS數據庫,利用 ROR 法和 PRR 法挖掘了HPV四價疫苗的47個不良反應信號。國外說明書中瘀傷,紅斑,注射部位疼痛、發熱、腫脹等有關描述與信號列表描述有所差異,可能與接種者個體體質或接種操作人員的操作有關,也可能國內外對癥狀的描述用語差異有關。
表2 HPV四價疫苗不良反應信號累及系統與說明書對比
Tab.2Comparisonofadversereactionsignalinvolved-systemandrelevantdescriptionintheinstructionsofHPVtetravalentvaccine

累及系統有信號的首選術語說明書中的不良反應皮膚及其附件類疾病蕁麻疹,皮疹,瘙癢,脫發,皮膚發熱,腫脹,多汗蕁麻疹,紅斑,銀屑病,硬皮病,皮膚變色,白斑肌肉骨骼系統疾病眼肌麻痹,關節痛,肌痛,肌無力,腰背痛,肌肉骨骼病肌痛,關節痛交感副交感神經系統疾病暈厥,嘔吐暈厥,嘔吐中樞及外周神經系統疾病頭暈,頭痛,意識喪失,驚厥,感覺遲鈍,感覺異常,震頭痛,頭暈,腦脊髓炎,運動障礙,麻痹,多發性硬化綜 顫,顱神經損傷,活動受限,偏頭痛,運動障礙,步態 合征,運動神經元疾病,癱瘓,癲 異常全身性損傷發熱,疲勞,疼痛,蒼白,跌倒發作,流感樣癥狀,不適,發熱,無力,死亡,不適,過敏樣反應,寒戰,流感樣癥狀 胸痛,寒戰,無力給藥部位反應注射部位腫脹,注射部位發熱注射部位疼痛,注射部位腫脹,注射部位紅斑,注射部 位瘙癢,注射部位瘀傷,注射部位血腫呼吸系統疾病呼吸困難支氣管痙攣,咳嗽,肺炎,哮喘胃腸系統疾病惡心,腹痛惡心,胰腺炎,腹痛,腹瀉,胃腸炎女性生殖系統疾病流產盆腔炎代謝及營養類疾病末梢水腫糖尿病視覺損傷視覺異常視神經炎神經紊亂焦慮失眠肝膽系統損傷淋巴結病淋巴結病紅細胞異常溶血性貧血心外血管損傷紫癜免疫功能絮亂免疫系統疾病泌尿系統損傷尿道感染,腎盂腎炎,蛋白尿內分泌紊亂甲狀腺炎,甲狀腺功能亢進,甲狀腺功能減退膠原組織損傷類風濕性關節炎,紅斑狼瘡綜合征心肌、心內膜、心包及瓣膜損傷心肌炎
本研究使用的FDA疫苗數據庫是基于自發呈報系統的數據,特點是樣本量大,表述用語和上報人群多樣化,覆蓋范圍廣,上報操作簡單。有些不良反應上報信息對病情和癥狀的描述與標準的醫學專業術語存在差異,相關數據可能存在一定的局限性和缺陷,在數據應用時應當加以注意。如不良反應的表述與專業詞匯具有差異,缺乏規范性;實際用藥人數量未知,無法計算出不良反應實際發生率,可能存在低報和漏報現象;可能存在由于患者身體原因以及服用其他藥物、食物等因素引起誤報。因此,加強疫苗上市后的監測,可以盡早發現潛在的疫苗不良反應問題信號,并提出早期警告[14],加以防范。
HPV四價疫苗在國內2017年才上市,目前九價疫苗正在推廣上市之中,中國疑似預防接種異常反應數據還無法獲得,筆者檢索相關文獻還沒有不同人種接種HPV四價疫苗不良事件的研究。本次研究基于FDA疫苗數據庫,結論主要反映歐美人種疫苗使用結果,亞洲人群和歐美人群可能會有種群差異,但可為亞洲人群提供參考依據。中國疾病預防控制中心已建立,相信將來中國的疫苗數據庫會更加完善,能夠為使用者安全使用疫苗和臨床療效確認提供大數據支持。

